Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Medica Herediana
Print version ISSN 1018-130XOn-line version ISSN 1729-214X
Rev Med Hered vol.18 no.2 Lima Apr./jun. 2007
Características clínico-epidemiológicas de 14 casos con aislamiento clínico de enterococo resistente a Vancomicina en el Hospital Nacional Edgardo Rebagliati Martins.
Clinical and epidemiological characteristics of 14 cases of vancomycin-resistant enterococci at the Hospital Nacional Edgardo Rebagliati Martins.
Flores Paredes Wilfredo Hernán1
1
Médico Residente de la especialidad de Patología Clínica, Hospital Nacional Edgardo Rebagliati Martins. Lima, Peru.
RESUMEN
Objetivo: Describir las características clínico-epidemiológicas de los casos con aislamiento clínico de enterococo resistente a la vancomicina (ERV). Material y métodos: Estudio descriptivo y retrospectivo que analiza todos los casos de ERV en un periodo de dos años (Set-2000 a Agost-2002). Se recolectó información de las historias clínicas de los pacientes y del sistema estadístico hospitalario. En la identificación y susceptibilidad antimicrobiana de las cepas ERV se utilizó el sistema MicroScan (Dade Behring). Resultados: El primer aislado ERV del hospital Rebagliati fue en setiembre-2000. En el periodo de dos años fueron 14 los pacientes a quienes se les aisló Enterococcus faecium resistente a la vancomicina. Los especímenes positivos fueron: sangre (7 aislados), orina (6 aislados), punta de catéter central (1 aislado) y líquido ascítico (1 aislado). Las características clínicas de los pacientes fueron: edad avanzada, hemodiálisis, cirugía abdominal complicada, postración crónica, y alta mortalidad intrahospitalaria (50%). La estancia hospitalaria fue prolongada (media 41 [1-90] días). Ocho (57%) pacientes se expusieron a una UCI y aquí su estancia también fue prolongada (media 34 [8-55] días). Nueve (64%) pacientes recibieron vancomicina, pero fueron 13 (93%) los pacientes que se expusieron a antibióticos relacionados a ERV (vancomicina, cefalosporinas de tercera generación y agentes antianaeróbicos). Se estableció alguna relación epidemiológica entre las cepas ERV con el seguimiento intrahospitalario de los pacientes y el fenotipo microbiológico de los aislados, se encontró al menos dos cadenas de transmisión que posiblemente tenían diseminación clonal. Se demuestra que hubo un brote nosocomial de ERV en una UCI entre Dic-2001 y Ene-2002. En el periodo de estudio no se realizaron estudio de tamizaje de colonización intestinal con ERV para conocer la verdadera magnitud del ERV en el hospital. Este estudio deja la hipótesis de que el ERV tiene una amplia diseminación en el hospital, teniendo como epicentro de esta propagación a las UCI; por ello que urge adherirse a los lineamientos para la prevención de la diseminación del ERV de los Centros para el Control y Prevención de Enfermedades (CDC).(Rev Med Hered 2007;18:68-75).
PALABRAS CLAVE: Enterococo resistente a vancomicina (ERV), infección nosocomial, aislados clínicos de ERV.
SUMMARY
Objectives: To determine the clinical and epidemiological characteristics of cases with clinical isolation of vancomycin-resistant enterococci (VRE). Material and methods: This is a descriptive and retrospective study. All cases of VRE isolated in the hospital during a 2 year-period from September 2000 to August 2002 was analyzed. Clinical information was taken from patients medical chart and from the hospitals statistical information system. The identification and the susceptibility of isolated strains were carried out using the MicroScan System (Dade Behring). Results: The first isolated of VRE at the hospital was in September 2000. Over a two-year period (Sept-2000 to August-2002) vancomicyn-resistant Enterococcus faecium was isolated in 14 patients from a clinical sample. The positive specimens were blood (7 isolates), urine (6 isolates), central catheter tip (1 isolate) and ascites (1 isolate). The most relevant clinical characteristics of the patients were older age, hemodialysis, complicated abdominal surgery, bed-bound state, and high in-hospital mortality (50%). Intra-hospitalary stay prior isolation was long (mean 41 [1-90] days). Eight (57%) patients were exposed to an ICU and their stay in that unit was also long (mean 34 [8-55] days). Nine (64%) patients received vancomycin. Thirteen (93%) patients were exposed to VRE-related antibiotics (vancomycin, third-generation cephalosporins and antianaerobic drugs). Establishing any epidemiological relationship between the isolates of VRE with the intrahospital follow-up of patients and the microbiologycal phenotype of the isolates, at least two chains of transmission with likely clonal dissemination were found. There was a nosocomial outbreak of VRE in an ICU during December 2001 and January 2002. To date no screening studies on VRE intestinal colonization have been conducted to know the real magnitude of VRE in the hospital. This study proposes the hypothesis that VRE is widely disseminated through the different hospital units, the ICU are being the epicenter of this dissemination; therefore, it is important to abide by the guidelines for preventing the spread of VRE established by the Centers for Disease Control and Prevention (CDC).(Rev Med Hered 2007;18:68-75).
KEY WORDS: Vancomycin-resistant enterococci (VRE), nosocomial infection, clinical isolation of VRE.
INTRODUCCIÓN
Durante los últimos 15 años, el enterococo resistente a vancomicina (ERV) ha emergido como una causa importante de infección nosocomial en todo el mundo. El primer reporte de ERV surgió en l986 en Europa, luego en l987 en Estados Unidos (1). De acuerdo al Sistema de Vigilancia Nacional de Infecciones Nosocomiales (NNISS) de los Centros para el Control y Prevención de Enfermedades (CDC), el porcentaje de aislados de enterococo que fueron resistentes a vancomicina en los Hospitales de E.U. se incrementó de 0,3% en l989 a 21,2% en l998 (2).
Las especies de ERV clínicamente importantes son el E. faecium y E. faecalis, estas especies adquieren genes de resistencia a vancomicina (vanA y vanB) a través de plásmidos y transposones, se diseminan rápidamente dentro de los hospitales y causan brotes nosocomiales. Las especies E. gallinarum y E. casseliflavus poseen genes (vanC1 y vanC2) con resistencia intrínseca a bajo nivel a la vancomicina, no son transferibles y no han sido asociadas con brotes. Es necesaria la identificación precisa de E. faecium y E. faecalis resistentes a la vancomicina para ser rápidamente distinguidos de E. gallinarum y E. casseliflavus, debido a las implicancias epidemiológicas y clínicas que esto conlleva. Los sistemas de detección automatizados comúnmente fallan en la precisión de diferenciar E. gallinarum y E. faecium. Una identificación más precisa de las especies ERV y de los genotipos de resistencia a los glicopéptidos (vanA y vanB) se puede lograr mediante la técnica de Reacción en Cadena de la Polimerasa (PCR) y con la prueba PFGE (Electroforesis en Campo de Pulsos), se puede determinar la distribución clonal de las cepas encontradas dentro de una institución (3).
Montecalvo y col. (4) en un estudio de vigilancia durante 8 meses a una unidad de oncología determinaron que la duración de la colonización con Enterococcus faecium resistente a vancomicina (EFRV) persistió al menos 7 semanas. También hallaron que la colonización con EFRV es 10 veces más prevalente que la infección. Los pacientes que desarrollan infecciones con ERV tienen con frecuencia colonización intestinal con estos organismos. Sin embargo, la transmisión del ERV de paciente a paciente también puede ocurrir tanto a través del contacto directo como por contacto indirecto vía las manos del personal sanitario, o por los equipos y materiales contaminados y las superficies ambientales (5). Los pacientes colonizados son sin duda el principal reservorio de ERV y juegan un papel importante en su diseminación dentro del hospital (1,3,6).
Las infecciones causadas por ERV frecuentemente involucran sitios intraabdominales, del tracto urinario, del torrente sanguíneo y de los catéteres vasculares (5). La infección o colonización con ERV ha sido asociado con severidad de la enfermedad, hospitalización prolongada, hospitalización en una unidad de cuidados intensivos (UCI), afecciones quirúrgicas concomitantes, falla renal crónica, y también el uso previo de vancomicina ha sido reportado repetidamente como factor de riesgo (1,3,6,7). El ERV representa una seria amenaza para los pacientes hospitalizados debido a que son resistentes a casi todos los antibióticos actualmente disponibles, pueden causar importarte brotes nosocomiales, incrementan la morbi-mortalidad y los costos de hospitalización (8,9).
Este estudio fue iniciado para determinar el perfil clínico de los pacientes con aislamiento clínico de ERV del hospital Rebagliati, con ello, intentar evaluar la situación actual de la diseminación del ERV dentro del hospital, teniendo como propósito posterior el diseñar una estrategia para limitar su propagación.
MATERIAL Y METODOS
Escenario de estudio
El Hospital Nacional Edgardo Rebagliati Martins, es un hospital docente de nivel IV, cuenta con 1492 camas distribuidas en servicios con casi todas las especialidades. El edificio del hospital tiene 13 pisos y cada piso se divide en 3 estaciones: A, B y C. Hay 2 UCI generales y 2 UCI especializadas.
Diseño del estudio
Estudio descriptivo que analiza retrospectivamente todos los casos de ERV aislados en el hospital en un periodo de dos años, de setiembre de 2000 a agosto de 2002.
Recopilación de datos
La información de los datos demográficos, clínicos, y los resultados de los estudios microbiológicos fueron tomados de las historias clínicas de los pacientes, del sistema de información estadística hospitalario y del sistema computarizado del servicio de microbiología. Se utilizó un único instrumento de recolección de datos individualizado para cada paciente. Para el seguimiento intrahospitalario se utilizó los libros de ingresos y egresos de los servicios por donde fueron transferidos los pacientes. Los datos de exposición a antibióticos, estancia hospitalaria, tiempo de hospitalización en UCI, se consideraron hasta el día de cultivo positivo para ERV.
Estudio microbiológico
todas las cepas de ERV aisladas fueron obtenidas de muestras clínicas. La identificación de los aislados se realizó utilizando el Sistema MicroScan (Dade Behring) version 22.26, con paneles convencionales Positive Breakpoint Combos 13 y 14. Para la interpretación de las susceptibilidades antimicrobianas se siguió las normas de la National Committee for Clinical Laboratory Standards (NCCLS) (10). Luego que las cepas ERV fueran aisladas por el sistema automatizado, se sometieron a tamizaje de resistencia a la vancomicina en agar BHI (Brain Heart Infusion) conteniendo 6 mg de vancomicina por mL como lo recomienda la NCCLS. Se utilizó como cepas de referencia a E. faecalis ATCC 29212 como susceptible y E. faecalis ATCC 51299 como resistente (10).
Definiciones
Antibióticos relacionados a ERV: es un listado de antibióticos específicos que se les ha relacionado como factores de riesgo para desarrollar infección/colonización con ERV basados en la mayor evidencia encontrada en las investigaciones relacionadas a ERV (7,11-19), y además estos antibióticos formaron parte del formulario terapéutico del hospital. Estos fueron: vancomicina, cefalosporinas de tercera generación (ceftriaxona, ceftazidima) y agentes antianaerobios (clindamicina, metronidazol, meropenem e imipenem).
Un día-antimicrobiano: es la recepción de un solo antibiótico por 1 día; por lo tanto, 10 días-antimicrobianos podría resultar de la recepción de un solo antibiótico por 10 días o de la recepción de dos antibióticos por un periodo de 5 días cada uno (19).
Servicios de alto riesgo: servicios donde gran parte de los reportes relacionados a ERV encontraron mayor la prevalencia de casos de ERV: UCI, unidades de transplante, servicios de onco-hematología, nefrología y unidades de diálisis (20-23).
RESULTADOS
El primer caso de enterococo resistente a vancomicina reportado en el hospital Rebagliati fue en setiembre del año 2000, dos años después, suman 14 los pacientes con aislamiento clínico positivo para ERV. Actualmente se observa que la frecuencia de aislamientos clínicos de ERV se viene incrementando. Así en el año 2000, hubo 1 solo caso; en el año 2001, 5 casos; y en los primeros 8 meses del 2002 se han presentado 8 casos.
Todos los aislados fueron Enterococcus faecium resistentes a vancomicina (EFRV), sumando en total 15 aislados (un paciente tuvo dos aislados). El espécimen positivo fue sangre en 7 (50%) pacientes; orina en 6 (43%) pacientes; punta de catéter, en 1 (7%) paciente; y líquido ascítico en 1 (7%) paciente.
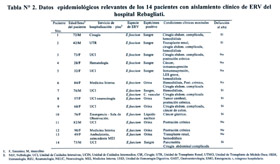
Las características clínicas más relevantes que tuvieron los pacientes (Tabla Nº1 y Tabla Nº2) fueron: la edad promedio de 64,4 años con un rango de 28 a 90 años; 9 (64%) fueron de sexo femenino. Siete de los pacientes se encontraban en una UCI en la fecha de aislamiento del EFRV, 2 pacientes en servicios de medicina interna, 1 paciente en la unidad de transplante renal, 1 paciente en hematología, 1 paciente en cirugía, y 1 paciente en la sala de observación de emergencia. En 12 casos (85,7%) el EFRV fue adquirido intrahospitalariamente. Las condiciones subyacentes más importantes fueron hemodiálisis, que estuvo presente en 6 (43%) pacientes; un número similar en pacientes con cirugía abdominal complicada; otros 6 pacientes tenían postración crónica; y 4 tenían cáncer como enfermedad subyacente. La mortalidad intrahospitalaria fue 50%.
La estancia hospitalaria prolongada fue la norma en casi todos los pacientes estudiados (excepto el paciente 10), con una media de 40,6 días y un rango de 1 a 90 días (Tabla Nº3). De los 8 pacientes que ingresaron a una UCI previo al aislamiento, también su estancia en esta unidad fue prolongada, media 33,8 días y rango de 8 a 55 días.
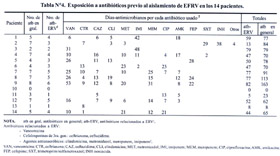
Respecto a la exposición a antibióticos; 9 (64%) pacientes recibieron vancomicina; esta cifra aumenta a 13 (93%) pacientes si se considera la exposición a antibióticos relacionados a ERV (Tabla Nº4). El promedio de días-antimicrobianos de exposición a antibióticos en general fue de 70,2 días (rango, 0-163), mientras que el promedio de días-antimicrobianos con antibióticos relacionados a ERV fue 45,7 días (rango, 0-82).
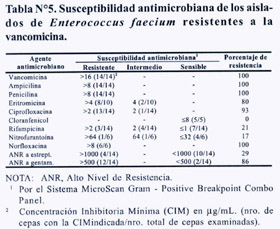
La susceptibilidad antimicrobiana de los E. faecium resistentes a la vancomicina se determinó tomando 1 solo aislado por cada uno de los 14 pacientes (Tabla Nº5). El paciente 7 tuvo dos aislados de idéntica susceptibilidad. De los 14 E. faecium aislados analizados, 14 (100%) fueron resistentes a la ampicilina, el 86% fueron resistentes de alto nivel a la gentamicina, 29% fueron resistentes de alto nivel a la estreptomicina, y 3 (21%) aislados fueron resistentes a ambos aminoglucósidos. La comparación conjunta de las susceptibilidades de los EFRV aislados del hospital nos hace sospechar de que se trataría de una población mezcla de varios tipos de clonas.
Para tratar de establecer alguna relación epidemiológica entre las cepas de EFRV aisladas en el hospital, se relacionó los datos del seguimiento intrahospitalario por tiempo y localización de los pacientes, con el fenotipo microbiológico de los aislados. Se encontró que en la 1ra semana de enero-2002, los pacientes 5, 7 y 8 coincidieron su estancia hospitalaria en la misma UCI. Las susceptibilidades antimicrobianas de los aislados de los 3 pacientes fueron muy similares.
En 10 de los 14 pacientes con EFRV se alcanzó la definición de infección nosocomial; dos aislados de orina se consideraron colonización, y dos aislados de sangre se consideraron bacteriemias transitorias. Ocho de los 10 pacientes con infección recibieron tratamiento antimicrobiano contra el ERV, a 6 de estos pacientes se les administró linezolid.
DISCUSION
En los últimos 15 años se viene observando la inexorable diseminación del ERV en todos los hospitales del mundo (14,26). En el hospital Rebagliati, desde la aparición del primer caso en setiembre del 2000 hasta 2 años después este microorganismo se ha diseminado por diferentes servicios hospitalarios hasta llegar a ser endémico en la institución.
Todos los ERV aislados fueron de la especie Enterococcus faecium, no se aisló ningún E. faecalis resistente a vancomicina, y los enterococos con resistencia intrínseca a la vancomicina como E. gallinarum y E. casseliflavus no fueron considerados en el estudio por su poca importancia epidemiológica (1,18,24,25).
Los rasgos generales de los 14 pacientes con ERV encontrados en este estudio, como edad avanzada, múltiples enfermedades subyacentes, hospitalización en servicios de alto riesgo, tiempo de hospitalización prolongado, con exposición significativa a antibióticos, y con alta mortalidad intrahospitalaria; constituyen un perfil característico frecuentemente hallado en la literatura pertinente a ERV (3,11,15,17,23,26).
La observación de 3 pacientes con aislamiento de ERV en el mismo periodo (1ra semana enero 2002), en la misma UCI y con susceptibilidad antibiótica similar, nos hace pensar que forman parte de una misma cadena de transmisión. Esto nos lleva a plantear que entre diciembre 2001 y enero 2002, hubo un brote nocosomial de de ERV en la referida UCI.
Otra posible cadena de transmisión se observó en junio 2002, en un servicio de Medicina Interna donde se aisló ERV en 2 pacientes que ocuparon la misma cama con diferecnia de 10 dias.
La genotipificación de cepas aisladas por métodos moleculares (PCR y PFGE) ayudaría a dilucidar las hipótesis mencionadas, y con esto a entender mejor el comportamiento epidemiológico del ERV dentro del hospital. Afortunadamente el servicio de microbiología conserva las cepas congeladas, lo que permitiría en un futuro la realización de análisis de biología molecular.
Muchos reportes reconocen como servicios de alto riesgo de infección/colonización con ERV a aquellos donde la prevalencia es mayor en comparación con el resto del hospital, y son las UCI, oncohematología, unidades de transplante, nefrología y unidades de diálisis (20-23). En la fecha de aislamiento ERV, 9 (64%) de los 14 pacientes estudiados estuvieron localizados en servicios de alto riesgo: 7 pacientes: en UCI, 1 paciente en la unidad de transplante renal, y 1 paciente en hematología.
Como se sabe, los sistemas automatizados no son fiables en la detección de ERV (3), por ello el número de aislados clínicos de ERV del hospital estaría subestimado. Se suma a esto, el hecho de que debió ser muy probable que todos los pacientes estudiados estuvieran colonizados con ERV (a nivel de piel o a nivel del tracto gastrointestinal principalmente), y por ende, expusieron a varios otros servicios hospitalarios a los que fueron transferidos tanto antes como posteriormente al aislamiento del ERV. Por último, los pacientes colonizados con ERV que estuvieron próximos a los casos identificados fueron en definitiva un número mayor y quizá estos pacientes jugaron un rol más importante en la diseminación del ERV. Estas razones vertidas hacen sospechar que el ERV tendría una amplia diseminación dentro del hospital.
Los pacientes que requieren hemodiálisis se descompensan con frecuencia y requieren de múltiples cursos de antibióticos y frecuentes hospitalizaciones, los cuales someten a esta población de pacientes a un mayor riesgo de infección o colonización con ERV (7,9,11). Una alta proporción (43%) de los pacientes-ERV del hospital Rebagliati requirieron hemodiálisis.
Dos casos de aislamiento de ERV no alcanzaron la definición de adquisición intrahospitalaria (27); el paciente 13, del cual se comentó más arriba, no estuvo hospitalizado cuando se le aisló ERV; y al paciente 10 se le aisló ERV de líquido ascítico en el primer día de ingreso al hospital, no tuvo el antecedente de anteriores hospitalizaciones, lo que nos indica que probablemente el ERV lo adquirió en la comunidad y que este sería un evento de ingreso de una nueva cepa al hospital.
En los estudios de ERV se considera la exposición a antibióticos sea en forma individual (e.g., vancomicina), por clases de antibióticos (e.g., cefalosporinas, quinolonas), o todos los antibióticos en general. Esta falta de uniformidad sería una de las causas de la gran heterogeneidad entre los resultados de los estudios. Así, algunos trabajos reportan a la vancomicina como factor de riesgo independiente para la infección/colonización con ERV (11,17,26), mientras que otros dan resultados controversiales (9,16,19,28).
Una explicación a esto sería que el efecto de competición a nivel intestinal para la multiplicación del ERV no la ejerza únicamente la vancomicina, sino que debe existir un efecto aditivo ejercida por los demás antibióticos recibidos (6,28). Pero tampoco todos los antibióticos en general ejercen presión de selección; en dos trabajos de Donskey y col. (12,13) se demuestra que no todos los agentes antianaeróbicos ejercen una presión antibiótica selectiva; antibióticos como quinolonas, cefepime y aztreonam entre otros, tendrían incluso un efecto protector contra el ERV.
Bajo este análisis teórico, creemos que la forma más óptima de estimar la variable exposición a antibióticos es mediante la selección de aquellos antibióticos que se ha demostrado que son un factor de riesgo para adquirir ERV a partir de la mayor evidencia encontrada en las investigaciones a cerca del ERV (e.g., vancomicina, cefalosporinas de tercera generación, varios agentes antianaeróbicos), y que además éstos deban formar parte del formulario terapéutico del hospital donde se realiza el estudio. A estos antibióticos los denominamos antibióticos relacionados a ERV. Tokars y col. (19) considerando la exposición a 6 antibióticos específicos (todos relacionados a ERV) obtuvieron que esta exposición conjunta fue un predictor independiente del status ERV. Esta nueva variable utilizada en estudios futuros podría permitir la comparar los resultados.
Los aislados clínicos de ERV estudiados podrían ser representativos de los tipos de cepas que estén circulando durante el periodo de estudio. Aunque el análisis de las cepas de pacientes con colonización intestinal podría proveer un panorama más completo. Por ende, la verdadera magnitud de la prevalencia del ERV se desconoce.
En el periodo de estudio no se realizó estudios de tamizaje de colonización intestinal con ERV en el hospital. Montecalvo y col. (4) en una unidad oncológica hallaron una relación de 10 pacientes con colonización intestinal por cada paciente infectado con E. faecium resistente a vancomicina. Kim y col. (29) señalan que los aislados clínicos de ERV sólo representarían la punta de un iceberg del total de la carga del hospital. La prevalencia de ERV en el hospital se obtendría de estudios de vigilancia de portadores de ERV como lo indican las normas del Consejo Consultivo de Prácticas de Control de Infecciones Hospitalarias (HICPAC) de los Centros para el Control y Prevención de Enfermedades (CDC) (5).
Las recomendaciones HICPAC incorporan cuatro enfoques en la prevención de la diseminación intrahospitalaria del ERV: vigilancia microbiológica, medidas adecuadas de control de infecciones, educación del personal sanitario, y el uso apropiado de la vancomicina (5). Las mayores evidencias sugieren que la emergencia y diseminación de estos patógenos son promovidas por las pobres técnicas de control de infecciones y por la presión antibiótica selectiva (6,8); esto también podría estar sucediendo en el hospital, tal es así, que el año 2002 se duplicó el uso de la vancomicina en relación al año 1999. Otra evidencia es que al presente se vienen incrementando los aislamientos de este germen a partir de muestras clínicas; así en enero-2003 hubo un nuevo brote de ERV en la Unidad de Transplante Renal, y en marzo-2003 por primera vez se aisló en un paciente pediátrico.
La identificación de los reservorios a través de cultivos de vigilancia y el aislamiento de los pacientes colonizados reduce significativamente el riesgo de propagación del ERV en el hospital. El documento HICPAC enfatiza la necesidad de estudios de cultivos periódicos de heces o hisopados rectales (5).
Una estrategia a seguir en el hospital sería el tamizaje de pacientes de alto riesgo de colonización/infección con ERV (pacientes de UCI, onco-hematología, unidades de transplante, nefrología, unidad de diálisis) en vez de un abordaje amplio de todo el hospital. Éste es un enfoque de varios estudios epidemiológicos (5,8,11,20-23), en el que se identifican poblaciones pequeñas en riesgo donde se hallan la mayor parte de pacientes con ERV, mejorando así su costo-efectividad, y además tienen la ventaja de poder ser aplicados en un tiempo muy corto.
REFERENCIAS BIBLIOGRÁFICAS
1. Murray BE. Vancomycin – Resistant Enterococcal Infections. N Engl J Med 2000;342(10):710-721. [ Links ]
2. Centers for Disease Control and Prevention. Summary of notificable diseases, United States, 1998. Morb Mortal Wkly Rep 1999;47:1-93. [ Links ]
3. Cetinkaya Y, Falk P, Mayhall CG. Vancomycin-resistant enterococci. Clin Microbiol Rev 2000;13(4):686-707. [ Links ]
4. Montecalvo MA, de Lencastre H, Carraher M, et al. Natural history of colonization with vancomycin-resistant Enterococcus faecium. Infect Control Hosp Epidemiol 1995;16(12):680-685. [ Links ]
5. Centers for Disease Control and Prevention. Recommendations for preventing the spread of vancomycin resistance. Recommendations of the Hospital Infection Control Practices Advisory Committee (HICPAC). MMWR Recomm Rep 1995;44(12):1-13. [ Links ]
6. Rice LB. Emergence of vancomycin-resistant enterococci. Emerg Infect Dis 2001;7(2):183-187. [ Links ]
7. Beltrami E, Singer D, Fish L, et al. Risk factors for acquisition of vancomycin-resistant enterococci among patients on a renal ward during a community hospital outbreak. Am J Infect Control 2000;28(4):282-285. [ Links ]
8. Hayden MK. Insights into the epidemiology and control of infection with vancomycin-resistant enterococci. Clin Infect Dis 2000;31(4):1058-1065. [ Links ]
9. Webb M, Riley LW, Roberts RB. Cost of hospitalization for and risk factors associated with vancomycin-resistant Enterococcus faecium infection and colonization. Clin Infect Dis 2001;33(4):445-452. [ Links ]
10. National Committee for Clinical Laboratory Standards. Performance Standards for Antimicrobial Susceptibility Testing (supplement). Villanova, Pennsylvania: National Committee for Clinical Laboratory Standards; 1999. [ Links ]
11. DAgata EM, Green WK, Schulman G, Li H, Tang YW, Schaffner W. Vancomycin-resistant enterococci among chronic hemodialysis patients: a prospective study of acquisition. Clin Infect Dis 2001;32(1):23-29. [ Links ]
12. Donskey CJ, Chowdhry TK, Hecker MT, et al. Effect of antibiotic therapy on the density of vancomycin-resistant enterococci in the stool of colonized patients. N Engl J Med 2000;343(26):1925-1932. [ Links ]
13. Donskey CJ, Hanrahan JA, Hutton RA, Rice LB. Effect of parenteral antibiotic administration on persistence of vancomycin-resistant Enterococcus faecium in the mouse gastrointestinal tract. J Infect Dis 1999;180:384-390. [ Links ]
14. Fridkin SK, Edwards JR, Courval JM, et al. The effect of vancomycin and third-generation cephalosporins on prevalence of vancomycin-resistant enterococci in 126 U.S. adult intensive care units. Ann Intern Med. 2001;135(3):175-183. [ Links ]
15. Loeb M, Salama S, Armstrong-Evans M, Capretta G, Olde J. A case-control study to detect modifiable risk factors for colonization with vancomycin-resistant enterococci Infect Control Hosp Epidemiol 1999;20:760-763. [ Links ]
16. MacIntyre CR, Empson M, Boardman C, Sindhusake D, Lokan J, Brown GV. Risk factors for colonization with vancomycin-resistant enterococci in a Melbourne hospital. Infect Control Hosp Epidemiol 2001;22(10):624-629. [ Links ]
17. Morris JG Jr, Shay DK, Hebden JN, et al. Enterococci resistant to multiple antimicrobial agents, including vancomycin. Establishment of endemicity in a university medical center. Ann Intern Med 1995;123(4):250-259. [ Links ]
18. Reid KC, Cockerill III FR, Patel R. Clinical and epidemiological features of Enterococcus casseliflavus/flavescens and Enterococcus gallinarum bacteremia: a report of 20 cases. Clin Infect Dis 2001;32(11):1540-1546. [ Links ]
19. Tokars JI, Satake S, Rimland D, et al. The prevalence of colonization with vancomycin-resistant Enterococcus at a Veterans Affairs institution. Infect Control Hosp Epidemiol 1999;20(3):171-175. [ Links ]
20. Coque TM, Tomayko JF, Ricke SC, Okhyusen PC, Murray BE. Vancomycin-resistant enterococci from nosocomial, community, and animal sources in the United States. Antimicrob Agents Chemother 1996;40(11):2605-2609. [ Links ]
21. Dan M, Poch F, Leibson L, Smetana S, Priel I. Rectal colonization with vancomycin-resistant enterococci among high-risk patients in an Israeli hospital. J Hosp Infect 1999;43(3):231-8. [ Links ]
22. Jordens JZ, Bates J, Griffiths DT. Faecal carriage and nosocomial spread of vancomycin-resistant Enterococcus faecium. J Antimicrob Chemother 1994;34(4):515-528. [ Links ]
23. Von Gottberg A, van Nierop W, Duse A, et al. Epidemiology of glycopeptide-resistant enterococci colonizing high-risk patients in hospitals in Johannesburg, Republic of South Africa. J Clin Microbiol 2000;38(2):905-909. [ Links ]
24. French GL. Entericocci and vancomycin resistance. Clin Infect Dis. 1998;27(Suppl 1):S75-83 [ Links ]
25. Sahm DF, Free L, Smith C, Eveland M, Mundy LM. Rapid characterization schemes for surveillance isolates of vancomycin-resistant enterococci. J Clin Microbiol 1997;35(8):2026-2030. [ Links ]
26. Gordts B, Van Landuyt H, Ieven M, Vandamme P, Goossens H. Vancomycin-resistant enterococci colonizing the intestinal tracts of hospitalized patients. J Clin Microbiol 1995;33(11):2842-2846 [ Links ]
27. Garner JS, Jarvis WR, Emori TG, Horan TC, Hughes JM. CDC definitions for nosocomial infections. Am J Infect Control 1988;16:128-140. [ Links ]
28. Carmeli Y, Samore MH, Huskins C. The association between antecedent vancomycin treatment and hospital-acquired vancomycin-resistant enterococci: a meta-analysis. Arch Intern Med. 1999;159(20):2461-2468. [ Links ]
29. Kim WJ, Weinstein RA, Hayden MK. The changing molecular epidemiology and establishment of endemicity of vancomycin resistance in enterococci at one hospital over a 6-year period. J Infect Dis. 1999;179(1):163-171. [ Links ]
Correspondencia:
Dr. Wilfredo Flores Paredes
Teléfono: 511-9985-0399.
Correo electrónico: wido2@hotmail.com