Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Medica Herediana
Print version ISSN 1018-130XOn-line version ISSN 1729-214X
Rev Med Hered vol.18 no.4 Lima Oct./dic. 2007
Efecto de la terapia antiretroviral de gran actividad (TARGA) en pacientes enrolados en un Hospital Público en Lima-Perú.
Effectiveness of highly active antiretroviral therapy (HAART) on HIV patients treated in a public hospital in Lima, Peru.
Echevarría Zárate Juan 1,2,3, López de Castilla Koster Diego1, Iglesias Quilca David1,3, Seas Ramos Carlos1,2,3, González Lagos Elsa1,2, Maldonado Costa Fernando1, Maguiña Vargas Ciro1,2,3, Verdonck Bosteels Kristien1,4, Gotuzzo Herencia Eduardo1,2,3.
1
Instituto de Medicina Tropical Alexander von Humboldt, Universidad Peruana Cayetano Heredia, Lima, Perú.2
Departamento de Enfermedades Infecciosas, Tropicales y Dermatológicas, Hospital Nacional Cayetano Heredia, Lima, Perú.3
Departamento de Medicina, Facultad de Medicina Alberto Hurtado, Universidad Peruana Cayetano Heredia. Lima, Perú.4
Virology Research Unit, Department of Microbiology, Institute of Tropical Medicine, Antwerp, Belgium.
RESUMEN.
Introducción: En mayo del 2004, el Ministerio de Salud (MINSA) en colaboración con el Fondo Global de lucha contra el SIDA, la tuberculosis y la malaria implementó el programa nacional (PN) para brindar terapia antiretroviral en forma gratuita a todos los pacientes infectados con el VIH con indicación de tratamiento de acuerdo a la guía del PN. Objetivos: Describir las características pre-tratamiento antiretroviral, respuesta a la terapia antiretroviral de gran actividad (TARGA), toxicidad y tasa de mortalidad de la población de pacientes que iniciaron TARGA a través del PN en un hospital general. Material y Métodos: Revisamos las historias clínicas, fichas médicas, resultados de laboratorio y tarjetas de TARGA de todos los pacientes enrolados en el PN en el Hospital Nacional Cayetano Heredia (HNCH) y describimos las características pre-tratamiento antiretroviral, respuesta a la TARGA, toxicidad y tasa de mortalidad. Los pacientes seleccionados para este estudio fueron sujetos infectados con el VIH que: (i) tenían 18 años o más; (ii) iniciaron TARGA en el PN entre mayo 2004 y abril 2006; y (iii) no habían recibido terapia antiretroviral anteriormente (naïve). Se consideró como éxito virológico a la presencia de por lo menos un valor de carga viral indetectable (VIH-1 ARN < 400 copias/mL) entre los 3-6 meses posteriores al inicio de la TARGA. Resultados: Se incluyeron en el estudio a 453 pacientes: 68% fueron varones, la edad promedio fue 35,7 ± 9,5 años y el peso fue 55,6 ± 10,8 Kg. El valor medio de CD4 pre-tratamiento fue 98 células/mm3 y el de carga viral fue 278 438 VIH-1 ARN copias/mL. Descontinuaron el tratamiento 84 pacientes (22 abandonaron, 59 fallecieron y 3 fueron transferidos a otra institución). Aquellos que continuaron fueron seguidos en promedio 337 días; el 38% (142/369) interrumpió temporalmente la TARGA, principalmente debido a toxicidad medicamentosa (82%). Se obtuvo éxito virológico en 85% de los pacientes. La mortalidad fue 13% y el 74% de las muertes ocurrió antes de los 3 meses de tratamiento. Conclusión: A pesar de una elevada frecuencia de interrupción del tratamiento, nuestros resultados muestran que la respuesta a las medicinas distribuidas por el PN es comparable a la reportada por programas de otros países. Es necesario realizar más estudios que evalúen la respuesta al tratamiento antiretroviral a largo plazo en el Perú. (Rev Med Hered 2007;18:184-191).
PALABRAS CLAVE: TARGA, antiretroviral, Fondo Global.
SUMMARY
In May 2004, the Peruvian Ministry of Health in collaboration with the Global Fund to fight AIDS, tuberculosis and malaria, implemented a national program (NP) to provide highly active antiretroviral therapy (HAART) free of charge to all HIV-infected patients who fulfilled the NPs guidelines. Objective: To evaluate the efficacy, safety and impact on mortality of HAART on HIV patients of a public hospital. Material and methods: We reviewed medical records, medical files, laboratory results and HAART charts of all patients enrolled within the NP at the Hospital Nacional Cayetano Heredia and described pre-treatment characteristics, response to HAART, toxicity and mortality rates. Study subjects were confirmed HIV-infected individuals who: (i) were > 18 years of age; (ii) started HAART under the NP between May 2004 and April 2006, and (iii) were naïve for antiretroviral treatment. Successful virological response was defined as at least one undetectable viral load (HIV-1 RNA < 400 copies/mL) determination 3 to 6 months after the initiation of HAART. Results: A total of 453 patients were included in the study: 68% were male; the mean age was 35.7 ±9.5 years and mean body weight was 55.6±10.8 Kg. Mean baseline CD4 cell count was 98 cells/mm3 and viral load was 278,438 copies/mL. Eighty-four patients discontinued HAART (22 abandoned treatment, 59 died and 3 were transferred to another institution). For those who continued HAART, the mean follow-up time was 337 days; 38% (142/369) temporarily interrupted HAART mainly due to drug toxicity (82%). Successful virological response was achieved in 85% of patients. Overall mortality was 13% and 74% of deaths occurred within the first 3 months of treatment. Conclusion: Despite of a high frequency of treatment interruption, our results show that the response to drugs provided by the NP is comparable to that reported by programs in other countries. Further studies should be performed to evaluate long-term outcome of HAART in Peru. (Rev Med Hered 2007;18:184-191).
KEYWORDS: Global Fund, HAART, antiretroviral treatment.
INTRODUCCIÓN
La epidemia del VIH/SIDA sigue en aumento en el Perú. A la fecha han sido reportados 28 624 casos de infección por VIH y 19 761 casos de SIDA(1). Hacia fines del 2003, más de 7 000 personas requerían terapia antiretroviral, pero sólo una pequeña proporción la recibió. El elevado costo de los medicamentos antiretrovirales y la ausencia de un programa nacional hacían el tratamiento únicamente accesible a personas que contaban con recursos económicos o con algún sistema de seguro de salud (EsSALUD, fuerzas armadas o policiales, o privado). Para el resto de personas el tratamiento sólo era posible a través de donaciones o programas de investigación, opción limitada a un reducido número de pacientes y difícil de sostener en el tiempo.
En los últimos años, la disminución de los precios y el apoyo de entidades internacionales ha permitido que los países con bajos recursos puedan implementar programas masivos de suministro de terapia antiretroviral. En mayo del 2004, la Estrategia Sanitaria del Ministerio de Salud del Perú con el apoyo del Fondo Global de las Naciones Unidas de lucha contra el SIDA, la tuberculosis y la malaria implementó el programa nacional (PN) que brinda gratuitamente terapia antiretroviral de gran actividad (TARGA) (2). El PN inició el suministro de medicamentos en 3 hospitales de la capital (Lima). Para el 2006 el PN se extendió en Lima a 17 hospitales, 3 organizaciones no gubernamentales (ONG) y el penal de Lurigancho y en provincias a 13 hospitales, todos los cuales brindan TARGA a través de sus programas locales de control de enfermedades de transmisión sexual y SIDA (PROCETSS). Para noviembre del 2006, 5892 pacientes habían iniciado tratamiento antiretroviral en todo el Perú (comunicación personal, Dr. José Luis Sebastián Mesones).
El Hospital Nacional Cayetano Heredia (HNCH), a través del Departamento de Enfermedades Infecciosas, Tropicales y Dermatológicas (DEITD) y el PROCETSS, es un centro de referencia de VIH/SIDA a nivel nacional. En él se diagnostica anualmente alrededor de 450 casos nuevos de infección por VIH y se realizan más de 5 000 consultas médicas ambulatorias de pacientes VIH positivos (3). Adicionalmente, el HNCH es responsable del 17% de los pacientes que reciben TARGA en el Perú. Para conocer el efecto de esta intervención, el Instituto de Medicina Tropical Alexander von Humboldt (IMTAvH), Universidad Peruana Cayetano Heredia (UPCH), y el DEITD, HNCH, iniciaron el presente estudio de seguimiento de todos los pacientes en TARGA atendidos en el PROCETSS del HNCH. El objetivo del estudio fue describir las características pre-tratamiento antiretroviral, respuesta a la TARGA, toxicidad y tasa de mortalidad de la población de pacientes que iniciaron TARGA a través del PN en el HNCH.
MATERIAL Y MÉTODOS
Pacientes y diseño
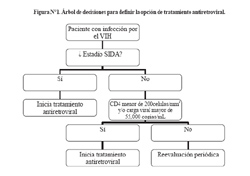
Para iniciar TARGA todo paciente debe contar con un resultado de ELISA positivo y una prueba confirmatoria positiva (Western Blot o inmunofluorescencia indirecta) (2). Los pacientes ingresan a un sistema de evaluación que consiste en un árbol de decisiones para definir la opción de tratamiento antiretroviral (Figura N°1 Figura N°1). Según la guía de tratamiento antiretroviral del PN (2), los pacientes con evidencia de procesos relacionados a inmunosupresión (estadío SIDA) son tributarios de tratamiento antiretroviral independientemente del valor de recuento de linfocitos T CD4 o de carga viral (VIH-1 ARN) de ese momento. Si el paciente es asintomático (sin evidencias de inmunosupresión) tiene indicación de TARGA si su recuento de CD4 está por debajo de 200 células/mm3 o si su carga viral es al menos 55 000 copias/mL. Los sujetos asintomáticos que no cumplen los requisitos de CD4 y carga viral son evaluados en forma periódica para identificar tempranamente la progresión de sus parámetros inmunológicos y virológicos o el desarrollo de procesos relacionados a inmunosupresión que definan el momento de inicio de TARGA. Para la selección del primer esquema de tratamiento antiretroviral, se considera como "paciente nunca tratado o naïve" a aquel sin experiencia previa con algún antiretroviral antes de ingresar al PN. Los pacientes seleccionados para este estudio fueron sujetos infectados con el VIH que: (i) tenían 18 años o más; (ii) iniciaron TARGA en el PN entre mayo 2004 y abril 2006; y (iii) no habían recibido terapia antiretroviral anteriormente (naïve). Se consideró como valor basal de CD4 y carga viral al valor más cercano al inicio de TARGA obtenido entre seis meses antes y dos semanas después del inicio. Se consideró como carga viral indetectable un valor VIH-1 ARN < 400 copias/mL.Toda la información se obtuvo directamente de los registros de los pacientes (historia clínica, ficha médica, resultados de laboratorio, tarjetas de tratamiento) por el personal del PROCETSS y el personal de investigación del IMTAvH.
Tratamientos
Para el tratamiento de pacientes naïve, el PN dispone de cuatro inhibidores nucleósidos de la transcriptasa reversa (NRTI siglas en inglés): estavudina (d4T), didanosina (ddI), zidovudina (AZT) y lamivudina (3TC); y de dos inhibidores no nucleósidos de la transcriptasa reversa (NNRTI siglas en inglés): efavirenz (EFV) y nevirapina (NVP). Adicionalmente, el PN cuenta con Duovir® que es una combinación de dosis fijas de 300mg de AZT + 150mg de 3TC, y Duovir-N® que añade a las anteriores dosis fijas de 200mg de NVP. El régimen estándar consiste en la combinación de dos NRTI y un NNRTI (2,4,5). En pacientes con anemia moderada o severa se substituye la AZT por ddI o d4T. En pacientes con elevación de enzimas hepáticas o exantema se substituye NVP por EFV o un inhibidor de proteasa (lopinavir/ritonavir). Para efectos de este estudio, suspensión de tratamiento fue definido como la interrupción (por una o más veces) del primer esquema de tratamiento de un paciente sin importar la duración, si el esquema fue reiniciado posteriormente o si fue motivo de cambio a un segundo esquema. éxito virológico se definió como la disminución de los valores de carga viral por debajo de niveles indetectables luego del tercer mes de tratamiento (considerando cualquiera de los resultados de las pruebas realizadas entre el tercer y sexto mes de tratamiento). Asimismo, se definió efectividad del primer esquema de TARGA como el porcentaje de pacientes que obtuvo éxito virológico.
Todos los pacientes fueron informados de los riesgos y beneficios de recibir tratamiento antiretroviral y firmaron el formulario de consentimiento informado voluntariamente, antes de iniciar la TARGA según lo requerido por el PN. El estudio de seguimiento de los pacientes fue registrado por el IMTAvH en la Dirección de Investigación de la UPCH y autorizado por el Comité institucional de ética de la UPCH y por el comité de ética del HNCH.
Análisis estadístico
Para la comparación de variables categóricas se utilizó la prueba chi-cuadrado y la prueba exacta de Fisher. Para las variables continuas se aplicó la prueba t de Student (variables paramétricas) y Mann-Whitney (variables no paramétricas).
RESULTADOS
Características iniciales de la población
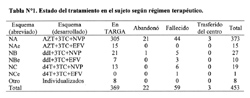
Cuatrocientos cincuenta y tres pacientes con diagnóstico de infección por el VIH fueron incluidos en el estudio. El 68% fueron hombres y la media de la edad fue 35,7 ± 9,5 años. El peso promedio fue 55,6 ± 10,8Kg, pero 136 (29,9%) sujetos pesaron menos de 50Kg. Las razones para iniciar la TARGA fueron: estadío SIDA 299/453 (66%), asintomáticos con valor de CD4 menor a 200 células/mm3 o carga viral mayor a 55 000 VIH-1 ARN copias/mL 154/453 (34%). Se contó con al menos un valor basal de CD4 en 415 pacientes (92%) y de carga viral en 298 (66%). De los pacientes que contaron con resultado de CD4 basal, el 62% (257/415) ingresó a la TARGA con valores de CD4 < 100 células/mm3, 23% (96/415) con valores entre 100 y 200 células/mm3 y 13% (62/415) con más de 200 células/mm3, siendo el promedio de CD4 de 98 ± 101 células/mm3. En cuanto a los resultados disponibles de carga viral basal, 64% (191/298) tuvo VIH-1 ARN > 100 000 copias/mL, 14% (42/298) entre 55 000 y 100 000 copias/mL y 22% (65/298) VIH-1 ARN < 55mil copias/mL, siendo el promedio 278,438 VIH-1 ARN copias/mL. La distribución de los pacientes según régimen de tratamiento se observa en la tabla N°1. El tratamiento asignado con mayor frecuencia fue AZT+3TC+ NVP (67%).
Seguimiento
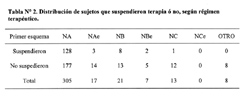
Del total de 453 pacientes estudiados, 84 pacientes descontinuaron la TARGA en el HNCH. Veintidós pacientes abandonaron el tratamiento por decisión propia, 59 fallecieron y 3 solicitaron transferencia a otros centros de salud. Los 369 pacientes restantes que continuaron en TARGA tuvieron un tiempo promedio de tratamiento de 337 días hasta la fecha de cierre del estudio; 71% (261/369) tuvo más de 6 meses de tratamiento; 13% (48/369) entre tres y seis meses y 16% (60/369) menos de tres meses de tratamiento. Treinta y ocho por ciento de los pacientes que continuaron en TARGA (142/369) suspendió el primer esquema de tratamiento (tabla N°2): 15% (22/142) por falla virológica, 3% (4/142) por decisión propia y 82% (116/142) por toxicidad asociada a la TARGA. De estos últimos, 68% (79/116) fue por toxicidad hematológica, 26% (30/116) por toxicidad dérmica, 4% (5/116) por toxicidad hepática y 2% (2/116) por toxicidad dérmica y hepática simultánea. El 92% (131/142) de las suspensiones ocurrió en los primeros seis meses de tratamiento. El 83% (118/142) de las suspensiones resultó en un cambio del esquema inicial por un segundo esquema de tratamiento; el resto de pacientes que suspendió la TARGA reinició el mismo esquema de inicio.
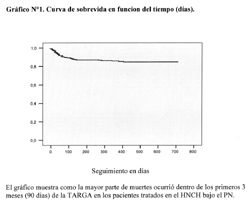
La mortalidad fue 13% (59/453). El 74% de las muertes ocurrió dentro de los primeros 3 meses (90 dias) de la TARGA (Gráfico N°2).
Trescientos veintidós pacientes recibieron AZT (300mg bid) dentro de su primer esquema de tratamiento. De ellos, 77 (24%) lo suspendieron por toxicidad hematológica: el 83% (64/77) cambió a un segundo esquema de tratamiento que no contenía AZT y el 17% (13/77) restante reinició la droga a dosis menores (AZT 200mg bid). De los 339 pacientes que recibieron NVP dentro de su primer esquema de tratamiento, 31 (9%) lo suspendieron por toxicidad dérmica (erupción cutánea); de éstos, el 90% (28/31) cambió a un segundo esquema sin NVP y el 10% (3/31) restante reinició NVP.
De los pacientes con CD4 basal, 86% (356/415) tuvo valores por debajo de 200 células/mm3. Luego de seis meses de terapia antiretroviral, de los 191 pacientes acudieron al control de CD4, 52% (99/191) tuvo valores por encima de 200 células/ mm3. Al cabo de un año de tratamiento, de los 119 pacientes que contaban con resultado de CD4, 64% (76/119) tuvo valores por encima de 200 células/ mm3. Ésto se vio reflejado en el incremento del promedio de CD4 de la población de pacientes. Por otro lado, de los 309 pacientes que cumplieron más de 3 meses de tratamiento, 81% (251/309) tuvo al menos un control de carga viral entre los tres y seis meses de tratamiento: de éstos, 85% (214/251) logró suprimir su carga viral a niveles indetectables (VIH-1 ARN < 400 copias/mL) mientras que 15% (37/251) presentó carga viral detectable. En este último grupo se documentó falla virológica en el 60% (22/37), lo que motivó un cambio de tratamiento a un esquema con un inhibidor de proteasa reforzado. Los 15 pacientes restantes continuaron el mismo régimen de terapia antiretroviral, observándose en ellos mejoría inmunológica y carga viral indetectable a los 9 ó 12 meses.
De los 453 sujetos que iniciaron tratamiento, 226 (50%) suspendieron el tratamiento inicial por alguna razón (muerte, abandono, transferencia, retiro voluntario, toxicidad o falla). Sin embargo, de los 116 pacientes que suspendieron debido a toxicidad, 24 reiniciaron el mismo esquema. Por tanto, la efectividad del primer esquema de TARGA durante el tiempo de observación en este grupo de pacientes fue de 251/453 (55%).
DISCUSIÓN
La introducción progresiva de la terapia antiretroviral TARGA en grandes comunidades ha demostrado ser una intervención costo-efectiva que ha cambiado el pronóstico clínico de la infección por VIH y mejorado la calidad de vida de estos pacientes al disminuir la mortalidad y la progresión a estadío SIDA, los costos de hospitalización y la transmisión del VIH (6,7). Actualmente, más de 40 millones de personas están infectadas con el VIH en todo el mundo, 95% de las cuales vive en países en vías de desarrollo. Organismos internacionales como ONUSIDA, la OMS y el Fondo Global de lucha contra el SIDA, la tuberculosis y la malaria han implementado programas de ayuda a países en vías de desarrollo para combatir esta epidemia, entre ellos la iniciativa "3 by 5" cuya meta fue proporcionar tratamiento antiretroviral a 3 millones de personas infectadas con el VIH para fines del 2005 (7). En el Perú, antes del 2004 el Ministerio de Salud no contaba con recursos para el tratamiento de pacientes viviendo con el VIH. Hacia el 2002 se iniciaron las gestiones para que a través de esta iniciativa global se implementara el tratamiento masivo, programa al cual se le denominó TARGA. En mayo del 2004, el HNCH fue sede del inicio de este programa y lugar en el que se dio tratamiento al primer paciente del PN. En el presente estudio describimos una serie de aspectos sobre la intervención con tratamiento antiretroviral masivo en la población peruana viviendo con VIH y los resultados observados durante esta intervención luego de 22 meses de implementado el programa TARGA en el HNCH.
La población de pacientes de este estudio estuvo fundamentalmente constituida por varones, con un rango de edad de 26-45 años, un promedio de peso de 55,6 Kg y una alta proporción de sujetos (30%) por debajo de 50Kg. El 63% de nuestros pacientes ingresó a la TARGA con valores de CD4 < 100 células/ mm3 y 66% de los sujetos con control de carga viral pre-TARGA tuvo un resultado por encima de 100 000 copias/mL. Nuestros resultados son semejantes a los observados por otros investigadores en países en desarrollo donde la mayoría de pacientes infectados con el VIH que acuden a los hospitales son varones jóvenes en estadíos avanzados de la enfermedad (6,8,9), ésto último un factor de riesgo conocido para toxicidad medicamentosa y para el síndrome de reconstitución inmune (2,10,11). Basados en la norma técnica (2), el 66% de nuestra población inició la TARGA por encontrarse sintomáticos y el tercio restante por valores de CD4 o carga viral. Es de esperar que a medida que el tratamiento antiretroviral cubra las necesidades de la población peruana, el "perfil" de los pacientes cambie hacia un sujeto diagnosticado en estadío temprano sin signos severos de inmunosupresión como ocurre actualmente en países desarrollados (10).
Los esquemas de tratamiento recomendados para iniciar la terapia antiretroviral están basados en un NRTI más NNRTI o inhibidores de proteasa. Según la guía del Departamento de Salud y Servicios Humanos de los Estados Unidos se recomienda el uso de EFV como primera línea de tratamiento si se emplea un esquema con NNRTI (4). El gobierno peruano decidió utilizar como droga de primera línea la NVP por su bajo costo y debido a que puede ser utilizado en gestantes según lo recomendado por la OMS (5). Por este motivo el PN no contó con EFV sino hasta después de 6 meses de la fecha de lanzamiento del programa. ésto se refleja en el hecho que un gran número de pacientes de la cohorte recibió esquemas con NVP (75%), siendo el esquema más utilizado el de AZT+3TC+NVP (67%). Sólo 8% de pacientes inició la TARGA con ddI o d4T en vez de AZT debido a que se encontraban con algún grado de anemia al momento de ingresar al PN. Un grupo de pacientes (25%) recibió EFV obtenido por gestiones individuales y posteriormente a través del PN de TARGA.
Durante los seis primeros meses de tratamiento, 85% de los sujetos en TARGA que contaban con un resultado control de carga viral alcanzaron valores indetectables lo que sugiere que aquellas personas que continúan la TARGA presentan una respuesta al tratamiento similar a la observada en países desarrollados incluso recibiendo fármacos genéricos (6,8).
Un elevado porcentaje de pacientes suspendió su primer esquema de tratamiento antiretroviral debido a toxicidad medicamentosa. La mayoría de estos pacientes desarrolló toxicidad hematológica la cual podría ser explicada en parte porque el régimen más utilizado contiene una dosis estándar de zidovudina de 600mg/día y por el bajo peso corporal de nuestros pacientes. Dado que los medicamentos genéricos empleados desde el inicio de la TARGA venían en dosis fijas, no se podía ajustar la dosis al peso, por lo que buena parte de los pacientes recibieron dosis por encima de las recomendadas para su peso. En Tailandia, estudios recientes sugieren que una dosis menor de zidovudina (200mg bid) podría reducir la toxicidad, manteniendo la misma efectividad en pacientes que pesan menos de 60Kg (12). Es importante resaltar que las dos drogas más utilizadas (Zidovudina y Nevirapina) están relacionadas con una alta frecuencia de los efectos adversos que condicionaron suspensión y cambio de tratamiento (13-16). El efecto de estas modificaciones en la generación de resistencia en nuestra población y su impacto en la sobrevida es algo que debe evaluarse a futuro.
La mortalidad (13%) en nuestra población fue comparable a otros estudios (6,8,17); sin embargo consideramos que fue relativamente elevada durante los primeros 3 meses de seguimiento. Todos los pacientes fallecidos estuvieron en estadío SIDA antes de ingresar al PN de TARGA, lo que indica claramente que se inició el tratamiento en forma tardía. Por ello, es muy importante reforzar aspectos educativos que faciliten el inicio de terapia en forma más precoz.
Las limitaciones de nuestra información fundamentalmente se derivadan del diseño, incluyendo, entre otras, datos incompletos principalmente en los resultados de CD4 y de carga viral (17). Por otro lado, decidimos incluir sólo pacientes nunca tratados o naïve debido a un potencial sesgo en el reporte de resultados referentes a la respuesta al tratamiento, como ha sido demostrado en otros estudios (18).
A pesar de que el número de pacientes en este estudio es pequeño, las enseñanzas de la iniciativa peruana son importantes. La corta duración de este estudio no nos permite comentar acerca del éxito a largo plazo de la terapia antiretroviral en nuestra población. Un seguimiento posterior nos permitirá determinar la importancia de la supresión virológica temprana (a los 6 meses) en eventos a largo plazo como sostenibilidad de la respuesta al tratamiento, tasa de infecciones oportunistas y muerte.
Con todas las limitaciones que tuvo el PN (pobre seguimiento de CD4 y cargas virales, dosis fijas de medicamentos, pocas alternativas de medicamentos y dificultades en la distribución de las medicinas) se obtuvo una respuesta virológica e inmunológica similar a la observada en otras series (6,8,10,17). Sin embargo, se observó una elevada tasa de toxicidad principalmente en los primeros meses de tratamiento que originó modificaciones en el esquema de tratamiento inicial. Por este motivo creemos que es fundamental tener acceso a combinaciones fijas de antiretrovirales a menores dosis en el Perú.
Agradecimientos
El presente estudio fue realizado con el apoyo financiero de la Directorate-General for Development Cooperation (DGDC) of the Belgian Government (Framework Agreement 1 and 2). Los autores agradecen al personal del PROCETSS del Hospital Nacional Cayetano Heredia por su dedicación al trabajo y al cuidado de los pacientes en TARGA y a los médicos residentes del DEITD del HNCH por su dedicada labor en el tratamiento de los pacientes que viven con VIH y el registro de información.
REFERENCIAS BIBLIOGRáFICAS
1. Oficina General de Epidemiología - Ministerio de Salud del Perú. Boletín TC/VIH/SIDA Abril 2007. Lima, Perú: Ministerio de Salud; 2007. [ Links ]
2. Ministerio de Salud del Perú. Norma técnica para el tratamiento antiretroviral de Gran Actividad - TARGA - en adultos infectados por el virus de la inmunodeficiencia humana NT N 2004-MINSA/DGSP-V.01. Lima, Perú: Ministerio de Salud; 2004. [ Links ]
3. Echevarria J, Lopez de Castilla D, Seas C, Verdonck K, Gotuzzo E. Scaling-up highly active antiretroviral therapy (HAART) in Peru: Problems on the horizon. J Acquir Immune Defic Syndr 2006; 43:625-626. [ Links ]
4. Department of Health and Human Services (DHHS) panel on antoretroviral guidelines for adults and adolescents - Office of AIDS research advisory council (OARAC). Guidelines for the use of antiretroviral agents in HIV-1- infected adults and adolescents - October 10, 2006. En: http://www.aidsinfo.nih.gov/ContentFiles/AdultandAdolescentGL.pdf (Fecha de acceso:15 de junio 2007). [ Links ]
5. World Health Organization. Antiretroviral therapy for HIV infection in adults and adolescents in resource-limited settings: Towards universal access. Recommendations for a public health approach. En: http://www.who.int/hiv/pub/guidelines/artadultguidelines.pdf . (Fecha de acceso: 15 de junio 2007). [ Links ]
6. Calmy A, Pinoges L, Szumilin E, Zachariah R, Ford N, Ferrandini L. Genetic fixed-dose combination antiretroviral treatment in resource-poor settings: multicentric observational cohort. AIDS 2006; 20:1163-1169. [ Links ]
7. Organizacion Mundial de la Salud. 3 Millones para 2005: Informe sobre los progresos realizados. ONUSIDA Diciembre. 2005. En: http://www.who.int/mediacentre/news/releases/2003/pr89/es/. (Fecha de acceso: 15 de junio 2007). [ Links ]
8. Sathapatayavongs B, Thakkinstian A, Promchanyakul K. Five-year experience on AIDS 1990–94: Ramathibodi Hospital, Thailand. J Infect Dis Antimicrob Agents 1999; 16: 69-72. [ Links ]
9. Braitstein P, Brinkhof MW, Dabis F, et al. Mortality of HIV-1-infected patients in the first year of antiretroviral therapy: comparison between low-income and high-income countries. Lancet 2006; 367: 817-824. [ Links ]
10. Matthews G, Sabin CA, Mandalia S, et al. Virological supression at 6 months is related to choice of inicial regimen in antiretroviral-naïve patients: a cohort study. AIDS 2002; 16: 53-61. [ Links ]
11. Lipman M, Breen R. Immune reconstitution inflammatory syndrome in HIV. Curr Opin Infect Dis 2004; 19:20-25. [ Links ]
12. Cressey TR, Leenasirimakul P, Jourdain G, Tawon Y, Sukrakanchana P, Lallemant M. Intensive pharmacokinetics of zidovudine 200mg twice daily in HIV-1-infected patients weighing less than 60 Kg receiving highly active antiretroviral therapy. J Acquir Immune Defic Syndr 2006;42:387-389. [ Links ]
13. Ssali F, Stöhr W, Munderi P, et al. Prevalence, incidence and predictors of severe anemia with zidovudine-containing regimens in Africans adults with HIV infection within the DART trial. Antiviral Therapy 2006; 11:741-749. [ Links ]
14. Kumarasamy N, Vallabhaneni S, Cecelia AJ, et al. Reasons for modification of generic highly active antiretroviral therapeutic regimens among patients in Southern India. J Acquir Immune Defic Syndr 2006; 41(1): 53-58. [ Links ]
15. Ananworanich J, Moor Z, Siangphoe U, et al. Incidence and risk factors for rash in Thai patients randomized to regimens with nevirapine, efavirenz or both drugs. AIDS 2005; 19(2):185-192. [ Links ]
16. van Leth F, Andrews S, Grinsztejn B, et al. The effect of baseline CD4 cell count and HIV-1 viral load on the efficacy and safety of nevirapine or efavirenz-based first-line HAART. AIDS 2005; 19(5):463-471. [ Links ]
17. van Leth F, Hassink E, Phanuphak P, et al. Results of the 2NN study: a randomized, comparative trial of firs-line antiretroviral therapy with regimens containing either nevirapine alone, efavirenz alone or both drugs combined, together with stavudine and lamivudine (Abstract 176). Boston, Massachusetts: 10th Conference on Retroviruses and Opportunistic Infections; February 10-14, 2003. [ Links ]
18. Severe P, Leger P, Charles M, et al. Antiretroviral therapy in a thousand patients with AIDS in Haiti. N Engl J Med 2005; 353:2325-2334. [ Links ]
Correspondencia:
Dr. Juan Echevarría Zárate
Dirección: Av. Honorio Delgado Nº430 Urb. Ingeniería, S.M.P. Lima, Perú.
Teléfono: (511) 482-3910; 482-3903; Fax: (511) 482-3404
Correo electrónico: chito@upch.edu.pe