Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Medica Herediana
Print version ISSN 1018-130XOn-line version ISSN 1729-214X
Rev Med Hered vol.21 no.3 Lima July 2010
Efecto in vitro del látex de Ficus insipida sobre la cascada de la coagulación sanguínea.
In vitro effect of the latex of Ficus insipida in the blood coagulation cascade.
Fernando Concha-Benavente 1
1Médico Cirujano miembro del Grupo de Investigación en Inmunología y Academia Peruana de Medicina Molecular. Facultad de Medicina de la Universidad Nacional de San Agustín. Arequipa, Perú.
RESUMEN
Es necesario investigar drogas naturales nuevas que aporten principios farmacológicos activos para ser utilizadas como una alternativa terapéutica. Por este motivo nos propusimos estudiar a Ficus insipida, cuyo látex ha sido usado como antihelmíntico durante muchos años en la amazonía, pero se investigó solo superficialmente su efecto anticoagulante in vitro. Objetivo: Comprobar el efecto anticoagulante in vitro y determinar la vía de la coagulación sobre la que actúa el látex de Ficus insípida. Material y métodos: Se obtuvo el látex de Ficus insipida y se prepararon diferentes concentraciones del mismo. Se obtuvieron muestras de sangre venosa periférica de 5 donantes voluntarios, anticoagulándolas con citrato de sodio. Luego, éstas se mezclaron con las diluciones del látex, se centrifugaron y se extrajo el plasma. Posteriormente, se obtuvo un pool de plasma para cada concentración del látex y se procedió a determinar el Tiempo de Protrombina (TP) y el Tiempo de Tromboplastina Parcial activada (TTPa), respectivamente. Resultados: Se encontró que el látex de Ficus insipida prolongó el TP a una concentración mayor o igual a 0,03125% (V/V), y ambos, el TP y TTPa a una concentración mayor o igual a 0,15% (V/V). Conclusiones: Los resultados obtenidos nos permiten afirmar que el látex de Ficus insipida posee un efecto anticoagulante in vitro dosis dependiente sobre la vía extrínseca de la coagulación sanguínea a una concentración igual o mayor a 0,03125% (V/V) y que a una concentración igual o mayor a 0,15% (V/V) posee un potente efecto anticoagulante sobre ambas vías de la coagulación.(Rev Med Hered 2010;21:146-152).
PALABRAS CLAVE: Factores de la coagulación sanguínea, tiempo de protrombina, tiempo parcial de tromboplastina, ficus, agentes anticoagulantes.
SUMMARY
We need to search for new natural drugs yielding pharmacological active principles to be used as an alternative to conventional therapies. For this reason, we proposed to study Ficus insipida, an amazonian plant that its latex has been used for years as an Antihelmintic agent but its anticoagulant effect has been only superficially studied. Objective: To corroborate the in vitro anticoagulant effect and to determine upon which of the coagulation pathways acts the latex of Ficus insipida. Material and methods: The latex of Ficus insipida was obtained and prepared at different concentrations. Then, samples of peripheral blood from 5 donors were taken using sodium citrate to avoid blood clotting; the samples were mixed with the latex dilutions and centrifuged, after that, the plasma was extracted to form a plasma pool from each latex concentration. Finally, the Prothrombin Time (PT) and the Partial Thromboplastin Time (PTT) were determined, respectively. Results: The results obtained demonstrated that the latex of Ficus insipida delays the PT at concentrations equal or higher than 0.03125% (V/V), and both the PT and PTT at concentrations equal or higher than 0.15% (V/V). Conclusions: This data allow us to affirm that the latex of Ficus insipida has a dose-dependent in vitro anticoagulant effect upon the extrinsic coagulation pathway at concentrations equal or higher than
0.03125% (V/V). Additionally, at concentrations equal or higher than 0.15% (V/V) it has a potent anticoagulant effect over both coagulation pathways.(Rev Med Hered 2010;21:146-152).
KEY WORDS: Blood coagulation factors, prothrombin time, partial thromboplastin time, ficus, anticoagulant agents.
INTRODUCCIÓN
El desarrollo de nuevos fármacos se logra a partir del estudio sistemático de sustancias químicas contenidas en plantas y hierbas. La enorme biodiversidad de plantas en el Perú nos da la oportunidad de identificar sus actividades biológicas y aplicarlas en la terapéutica de las enfermedades de nuestra población. Ficus insipida, conocida comúnmente con el nombre de Ojé, cuyo látex ha sido usado hace muchos años por habitantes de la Amazonia Peruana como antihelmíntico, es un claro ejemplo de una planta con efecto terapéutico exitoso (1-5). El látex de Ficus insipida posee un gran contenido de enzimas pertenecientes a la familia de las cisteino proteasas, entre las que destaca la Ficina como principal componente (4), ésta se encuentra estrechamente relacionada a otras cisteino proteasas de esta misma familia como son: Papaína y Bromelaína; ésta ultima siendo ampliamente conocida por su efecto antiinflamatorio e inmunomodulador (6-11), e incluso se le atribuye un efecto anticoagulante in vitro (12,13). Debido a la similitud entre estas proteínas surge el interrogante si la Ficina, siendo también una cisteino proteasa, podría tener alguna interacción con las proteínas que participan en la cascada de la coagulación sanguínea, clivándolas y así provocando alguna modificación en los parámetros de la misma.
La coagulación sanguínea es un complejo proceso de reacciones proteolíticas en cadena, denominado la "cascada de la coagulación sanguínea" (14,15). Gracias a experimentación in vitro se sabe que esta reacción enzimática en cadena posee dos vías distintas, las llamadas vía intrínseca y extrínseca, cada una con diferentes proteínas llamadas "factores de la coagulación". Además, se han desarrollado pruebas de laboratorio in vitro específicas para detectar la deficiencia de alguno de estos factores en cada una de ellas, conformando un importante avance en el diagnóstico, clasificación y tratamiento de las coagulopatías.
Investigaciones anteriores han demostrado un efecto anticoagulante in vitro en muchas plantas como es el caso de Ricinus communis (Higuereta) en Cuba (16) y de Chenopodium pertiolare HBK (Llipcha) (17), Chenopodium murale L. (Hierba del gallinazo) (18) y Chenopodium ambrosoides (Paico) (19), en nuestro país. Sin embargo, en el Perú no existen investigaciones publicadas sobre el efecto anticoagulante de Ficus insipida, excepto la realizada por Tutucayo M. (20); en dicha investigación se determinó sólo el efecto sobre la formación del coágulo sanguíneo, pero no se dilucidó qué vía de la coagulación era la afectada; por lo tanto, decidimos iniciar un nuevo trabajo de investigación trazándonos como objetivo, ésta vez, comprobar el efecto anticoagulante in vitro y determinar la vía de la coagulación sobre la que actúa el látex de Ficus insípida.
MATERIAL Y MÉTODOS
El estudio, por tratarse de una investigación in vitro, fue aprobado como un trabajo de riesgo mínimo por el comité de ética asesor de la secretaria académica de la Facultad de Medicina de la Universidad Nacional de San Agustín de Arequipa y fue realizado en el laboratorio de Microbiología e Inmunología de esa universidad. El látex de Ficus insipida fue obtenido en los jardines botánicos del Instituto Nacional de Investigación Agraria en Pucallpa. La variedad de la planta fue certificada por el Ing. Agrónomo Roberto Del Águila Lomas, representante del Ministerio de Agricultura de dicha ciudad.
Se extrajo el látex del tallo del árbol mediante incisiones en la corteza del árbol con bisturí y se colocó en un contenedor estéril sin aditivos y fue conservado hermético y refrigerado por 24 horas, para su posterior utilización. Las muestras de sangre venosa periférica fueron extraídas de sujetos voluntarios previo consentimiento informado, clínicamente sanos y sin tratamiento farmacológico alguno. Cinco donantes voluntarios cumplieron los criterios de inclusión y sus respectivas muestras se utilizaron en la investigación.
Se prepararon diferentes diluciones del látex en suero fisiológico a 37°C como se muestra en la tabla 1, del tubo 1 al 4 y del tubo A al G, se midieron los volúmenes directamente con micropipeta, a partir de la concentración de látex del tubo 5 se hicieron diluciones sucesivas al medio para obtener los volúmenes y concentraciones que se muestran en los tubos 5 al 11. A continuación se extrajeron las muestras de sangre venosa periférica según técnica estándar, utilizando para la anticoagulación tubos de 4,5 ml. (VacutainerÒ ) conteniendo 0,5 ml. de Citrato de Sodio al 3,2%, de éstos se extrajo 3 ml. de sangre para agregarlos al tubo Nº1 y 2,9 ml. al resto de los tubos, luego se centrifugaron para separar los elementos formes y el plasma, repitiéndose este procedimiento para todas las muestras de sangre venosa obtenidas. Seguidamente, se mezcló el plasma de tubos análogos (tubos con concentraciones similares del látex pero con muestras de sangre de los 5 diferentes donantes) obteniendo así un pool de plasma para cada concentración del látex. Acto seguido, se realizaron las mediciones del tiempo de protrombina (TP) y el tiempo de tromboplastina parcial activada (TTPa), haciendo 3 repeticiones para cada tubo en las diferentes concentraciones del látex. Se siguieron estrictamente las instrucciones del protocolo provisto por el fabricante.
Para la determinación del TP se utilizó el Kit de reactivos Neoplastine® Ci Plus 2 de Lote Nº 043381 (Diagnostica Stago, NJ, USA) y se procedió de la siguiente manera: Se incubó el reactivo (tromboplastina reconstituida) a 37ºC, luego se agregó 100 µl. del plasma de interés a un tubo de vidrio precalentado, se incubó a 37ºC durante 2 minutos y luego activando un cronómetro, se agregó 200 µl. del reactivo reconstituido; se mezcló por 3 segundos y se midió el tiempo de formación del coágulo. Para la determinación del TTPa se utilizó el Kit de reactivos C. K. PrestÒ 2 de Lote Nº 042333 (Diagonostica Stago, NJ, USA); se agregó 100 µl. del plasma de interés en un tubo de vidrio precalentado a 37ºC, luego se añadió 100 µl. del reactivo reconstituido (cefalina más buffer de caolín), se procedió a mezclar por 2 segundos y se incubó esta mezcla por 3 minutos. Luego, activando un cronómetro, se añadió 100 µl. de una solución de CaCl2 0,025 M, se mezcló por 3 segundos agitando el tubo y se determinó el tiempo de la formación del coágulo.
De acuerdo a los resultados obtenidos con las diferentes concentraciones en los tubos 3 a 11 (tabla 1), se decidió realizar nuevas diluciones del látex entre las concentraciones de 0,25% y 0,125% (tubos A al G), con el objetivo de determinar con mayor precisión hasta qué concentración del látex era cuantificable la prolongación del TP y del TTPa. El procedimiento para determinar los tiempos fue idéntico al utilizado para los tubos anteriores.
Para el análisis estadístico de los datos se utilizó la prueba de ANOVA y una prueba de especificidad de Tukey. Así mismo, se realizó regresión lineal simple para determinar la relación entre las diferentes concentraciones del látex y su respectivo efecto anticoagulante sobre el TP y TTPa. Para el procesamiento de los datos se utilizó el programa estadístico SPSS v.18.
RESULTADOS
Se hicieron 10 determinaciones del TP y TTPa con el pool de plasma del tubo 1 y según estos resultados se tomó como rango normal del TP 14,5 ± 0,71 segundos y del TTPa 43,1± 0,73 segundos. Como se observa en la tabla 1 en el tubo 1 (tubo control), el TP promedio fue de 15,17 segundos, y el TTPa promedio fue de 42,94 segundos. El tubo 2 fue el blanco para las diferentes diluciones del látex ya que en este tubo se mezcló la sangre con 100 µl. de suero fisiológico, siendo el máximo volumen de suero adicionado sin tener la sustancia problema, el TP fue de 15,17 segundos, similar al TP control (
Tabla 2). En cambio el TTPa fue de 44,07 segundos, mayor que el TTPa control (tabla 3).
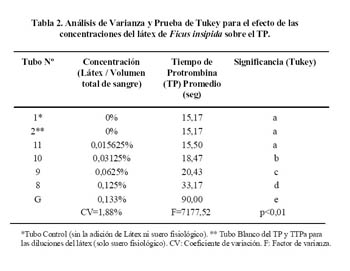
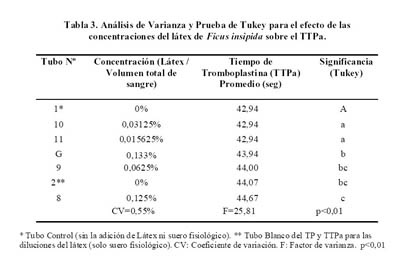
El análisis de varianza para el TP (Tabla 2), mostró que no había diferencia estadística significativa entre los valores de TP obtenidos en los tubos 1, 2 y 11, indicando que el suero fisiológico y el látex a una concentración de 0,015625% no tenían efecto inhibitorio sobre el TP. En cambio, se encontró diferencia significativa en el TP de los tubos 10, 9, 8 y G (p<0,01). Además, se encontró una relación positiva entre la concentración del látex y el TP(r=0,7869; p<0,05) (
Gráfico ).
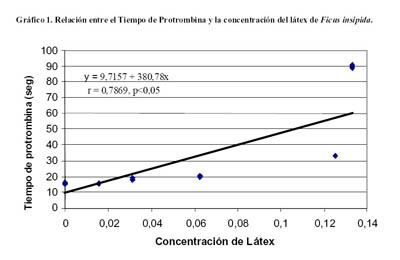
No se encontró diferencia estadística significativa entre los valores de TTPa del tubo control y aquellos con concentración de látex de 0,015625% y 0,03125% (tubos 11 y 10) (Tabla 3). Finalmente, a concentraciones de látex mayores a 0,15% el TP y TTPa fueron mayores de 24 horas (tubos 3 al F).
DISCUSIÓN
De acuerdo a los resultados, podemos afirmar que el látex de Ficus insipida ejerce efecto inhibitorio sobre la vía extrínseca de la coagulación sanguínea de manera dosis dependiente desde concentraciones muy pequeñas; contrariamente, dicho efecto no ocurre en la misma magnitud sobre la vía intrínseca. Sabemos que el Tiempo de Protrombina es una prueba de laboratorio para evaluar los factores II, V, VII y X, componentes de la vía extrínseca de la coagulación (21), por lo tanto el látex inhibiría dichos factores. El efecto inhibitorio cuantificable sobre esta vía, se produce hasta una concentración de 0,133%, ya que una concentración de 0,15%, es decir, con 0,5 µl. más del látex, prolonga ambos: el TP y el TTPa por un tiempo indefinido mayor de 24 horas; lo cual traduce la inhibición intensa de los factores de ambas vías de la coagulación sanguínea.
Éste efecto se explicaría de la siguiente manera: hasta una concentración de 0,133%, los componentes enzimáticos: cisteino proteasas, presentes en el látex de Ficus insipida provocarían el clivaje de los factores de la coagulación de la vía extrínseca, inactivándolos de una manera directamente proporcional a la concentración del látex; no actuando de la misma forma con los factores de la vía intrínseca de la coagulación, pues la poca variabilidad del TTPa nos indica que los factores de dicha vía no fueron afectados de la misma forma. Pero a una concentración de 0,15% la cantidad de cisteino proteasas presentes en el látex seria tal que sobrepasaría un umbral de actividad proteolítica y clivarían a los factores de ambas vías en su totalidad, impidiendo así la formación del coágulo de fibrina, efecto que se tradujo en la prolongación del TP y TTPa por más de 24 horas. Podemos añadir que el Coeficiente de Variación (CV<30%) 1,88% y 0,55% para TP y TTPa respectivamente (Tablas 2 y 3), nos indica que la variabilidad originada en el ensayo es propia del efecto de las concentraciones del látex y no es debido a errores en la heterogeneidad de la muestra o errores en la técnica de medición.
El látex de Ficus insipida fue estudiado anteriormente por numerosos investigadores lográndose determinar una exitosa actividad antihelmíntica. Se ha reportado efectos tóxicos tras su administración oral, tales como nauseas, vómitos, diarrea, calambres y edema cerebral entre otros; pero todos ellos fueron ocasionados tras ingerirlo en sobredosis mayores a 1,5 cm3/kg de peso; sin embargo, no se ha reportado un efecto anticoagulante tras su administración oral en las dosis recomendadas (22).
Muchos investigadores han estudiado el contenido enzimático de este látex, el cual recibió el nombre de Ficina (3,23-25). Ésta pertenece a la superfamilia de cisteino proteasas, compartiendo propiedades físico-químicas similares con la Bromelaina. Se ha reportado que la Bromelaina tiene un efecto anticoagulante producido por la reducción del factor X y factor II (protrombina) ambos componentes de la vía final común de la coagulación sanguínea, también provoca una reducción dosis dependiente del quininógeno de alto peso molecular y pre-calicreína, los cuales participan como aceleradores del inicio de la vía intrínseca de la coagulación (26). La Bromelaina en concentraciones altas prolonga marcadamente el TP y TTPa, y su efecto fibrinolítico se debe a que estimula la conversión del plasminógeno en plasmina (26). Debido al alto contenido de Ficina en el látex de Ficus insipida y que ésta posee propiedades similares con la Bromelaina, podríamos inferir que esta enzima seria la responsable del efecto anticoagulante in vitro.
Es difícil encontrar estudios que demuestren el efecto anticoagulante in vitro de látices derivados de plantas o árboles en el Perú. A nivel internacional, aunque la metodología no sea comparable ya que se usa el extracto alcohólico de las hojas de Ricinus communis, podemos mencionar el trabajo realizado en Cuba por Apechea M. et al (16) donde se demuestra que el mencionado extracto, prolongó el TP y TTPa. Con el mismo tenor, en nuestro medio se ha estudiado el extracto acuoso de hojas de Chenopodium pertiolare HBK (17), Chenopodium murale L. (18) y Chenopodium ambrosoides (19) demostrando un efecto anticoagulante in vitro según el método Lee White. El único estudio reportado donde se usó el látex de Ficus insipida (sinónimos F. glabrata, F. antihelmíntica) fue realizado por Tutucayo M, donde demuestra su efecto inhibitorio in vitro sobre la formación del coágulo sanguíneo (20), pero no se investigó qué vía de la coagulación era la afectada. Los resultados obtenidos en nuestra investigación nos permiten afirmar que el látex de Ficus insipida posee principios activos para inhibir in vitro la vía extrínseca de la coagulación sanguínea a una concentración igual o mayor a 0,03125% y que posee un potente efecto anticoagulante in vitro sobre ambas vías de la coagulación sanguínea a una concentración igual o mayor a 0,15%.
Finalmente, consideramos muy importante continuar investigando el látex de esta especie para determinar si su contenido de cisteino proteasas podría lisar también los enlaces peptidicos del polímero de fibrina una vez formado. También, realizar determinaciones específicas para determinar que factor en particular es el que inhibe dentro de las vías extrínseca e intrínseca. Adicionalmente, para afirmar categóricamente que el compuesto responsable de la anticoagulación es la Ficina, debemos aislar este complejo proteico del látex y realizar determinaciones in vitro sobre la coagulación sanguínea nuevamente. Así mismo, es necesario elaborar estudios in vivo en modelos animales para determinar su efecto tras la administración oral o parenteral y así establecer si este podría ser usado en la terapia farmacológica anticoagulante o fibrinolítica en el futuro.
Agradecimientos
Quiero expresar mi profundo agradecimiento al Dr. Jorge Ballón Echegaray por su invalorable orientación y tutoría en el desarrollo de la investigación, y al Dr. Alberto Cáceres Huambo por su ayuda en el procesamiento estadístico de los resultados.
REFERENCIAS BIBLIOGRÁFICAS
1. Oporto L. Efecto antihelmíntico del látex de Ficus glabrata. Tesis de Bachiller. Arequipa, Perú. Universidad Nacional de San Agustín, 1988. 65pp. [ Links ]
2. Amorin A, Borba J, Carauta J, Lope D, Kaplan M. Antihelmintic activity of the latex of Ficus species. J Ethnopharmacol 1999;64:255-58. [ Links ]
3. Cardenas W, Cabieses F. Algunas plantas antihelmínticas. Lima: Instituto de Medicina Tradicional; 1997.p.11-17. [ Links ]
4. Naquira C, Arroyo M, Hansson A. Preclinical and clinical studies with latex from Ficus glabrata HBK, a traditional intestinal antihelmintic in the Amazon area. J Ethnopharmacol 1986;17(2):105-138. [ Links ]
5. Stepek G, Behnke J, Buttle J, Duce R. Natural plant cysteine proteinases as anthelmintics? Trends Parasitol 2004;20(7):322-27. [ Links ]
6. Hale L. Proteolytic activity and immunogenicity of oral bromelain within the gastrointestinal tract of mice. Int Immunopharmacol 2004;4:255-64. [ Links ]
7. Manhart N, Akomeah R, Bergmeister H, Spittler A, Ploner M, Roth E. Administration of proteolityc enzymes bromelain and trypsin diminish the number of CD4+ cells and the interferon-ã response in Peyers patches and spleen in endotoxemic balb/c mice. Cell Immunol 2002;215:113-19. [ Links ]
8. Maurer H. Bromelain: Biochemistry, pharmacology and medical use. Cell Mol Life Sci 2001;58:1234-1245. [ Links ]
9. Hale L, Greer P, Sempowski G. Bromelain treatment alters leukocyte expression of cell surface molecules involved in cellular adhesion and activation. Clin Immunol 2002;104(2):183-90. [ Links ]
10. Gaspani L, Limiroli E, Ferrario P, Bianchi M. In vivo and in vitro effects of bromelain on PGE(2) and SP concentrations in the inflammatory exudates in rats. Pharmacology 2002; 65(2):83-6. [ Links ]
11. Desser L, Holomanova D, Zavadova E, Pavelka K, Mohr T, Herbacek I. Oral therapy with proteolytic enzymes decreases excessive TGF-beta levels in human blood. Cancer Chemother Pharmacol 2001;47:S10-5. [ Links ]
12. Metzig C, Grabowska E, Eckert K, Rehse K, Maurer H. Bromelain proteases reduce human platelet aggregation in vitro, adhesion to bovine endothelial cells and thrombus formation in rat vessels in vivo. In Vivo 1999;13(1):7-12. [ Links ]
13. Felton G. Fibrinolytic and antithrombotic action of bromelain may eliminate thrombosis in heart patients. Med Hypotheses 1980;6(11):1123-33. [ Links ]
14. Andreoli T, Carpenter Ch,Griggs R, Benjamin I. Andreoli and Carpenters Cecil Essentials of Medicine. 6th ed. Philadelphia: Elsevier Inc; 2004. p. 481-488. [ Links ]
15. Cotran R, Kumar V, Collins T. Robbins Pathologic basis of disease. 6th ed. Philadelphia: W.B. Saunders Company; 2000. p. 121-47. [ Links ]
16. Apechea M, Fano R, Garrido M. Efecto in vitro de un extracto acuoso de las hojas de Ricinus communis sobre la formación del coágulo sanguíneo. Rev Cubana Plant Med 1998;3(2):62-63. [ Links ]
17. Pierola R. Chenopodium pertiolare HBK (Hípica) como anticoagulante in vitro y su utilización en hemogramas. Tesis de Bachiller. Arequipa, Perú. Universidad Nacional de San Agustín, 1995. 65 pp. [ Links ]
18. Fernández M. Chenopodium murale L. como anticoagulante in vitro y su utilización en hemogramas. Tesis de Bachiller. Arequipa, Perú. Universidad Nacional de San Agustin, 1998. 69 pp. [ Links ]
19. Sanz J. Chenopodium ambrosoides (paico) como alternativa anticoagulante in vitro. Tesis de bachiller. Arequipa, Perú: Universidad Nacional de San Agustín, 1993. 74 pp. [ Links ]
20. Tutucayo M. Efecto in vitro del látex de Ficus antihelmíntica (Ojé) sobre la formación del coágulo sanguíneo. Tesis de Bachiller. Arequipa, Perú. Universidad Nacional de San Agustin, 2005. 68 pp. [ Links ]
21. Baglin T, Keeling D, Watson H. British Committee for Standards in Haematology. Guidelines on oral anticoagulation: third edition-2005 update. Br J Haematol 2006;132(3):277-85. [ Links ]
22. Hansson A, Zelada J, Noriega H. Reevaluation of risks with use of Ficus insipida latex as a traditional antihelmintic remedy in the Amazon. J Ethnopharmacol 2005;98(3):251-7. [ Links ]
23. Robbins B, Lamson P. Further studies on the proteolytic enzyme content of latex from the fig and related trees. J Biol Chem. 1934;106(2):725-27. [ Links ]
24. Jones I, Glazer A. Comparative studies of four Sulfhydryl Endopeptidases ("Ficins") of Ficus glabrata Latex. J Biol Chem 1970; 245(11):2765-72. [ Links ]
25. Williams D, Whitaker J. Multiple molecular forms of Ficus glabrata Ficin. Their separation and Relative Physical, Chemical, and Enzymatic Properties. Plant Physiol 1969;44:1574-83. [ Links ]
26. Kelly G. Bromelain: A literature review and discussion of its therapeutic applications. Altern Med Rev 1996;1(4):243-57. [ Links ]
Correspondencia:
Fernando Concha-Benavente
Urbanización San Rafael II Etapa G5 – Yanahuara.
Arequipa, Perú.
Correo electrónico: fernandoboris.cb@gmail.com
Teléfono: 054 959349032