RESUMEN
Se describe el caso de una mujer de 57 años de edad, con diagnóstico de síndrome de Wolf Parkinson White, en tratamiento con amiodarona 200 mg/día; que acudió por presentar palpitaciones, fatiga y aumento de sueño. Al examen físico no se encontró bocio, pero los reflejos osteotendinosos estaban prolongados. Los exámenes auxiliares mostraron TSH elevado, T4 libre disminuido y anticuerpos antiperoxidasa tiroidea negativos. Se suspendió la amiodarona y se inició levotiroxina. Después de dos meses; los niveles de TSH y T4 libre eran normales y la paciente no presentaba molestias. La amiodarona está asociada a diversos efectos adversos que pueden limitar su uso. Entre estos efectos adversos, se describe el hipotiroidismo inducido, que se caracteriza por TSH elevado, T4 libre disminuido y síntomas inespecíficos como fatiga, intolerancia al frío y piel seca. El tratamiento de elección es la levotiroxina.
PALABRAS CLAVE: Amiodarona, hipotiroidismo, tiroiditis. (Fuente: DeCS, BIREME)
SUMMARY
We report a case of a Wolf Parkinson White syndrome in a 57-yearl-old woman receiving amiodarone (200 mg/ day) who presented with tachycardia, fatigue and somnolence. The physical examination did not reveal goiter, but the osteotendinous reflexes were brisk. Laboratory examinations revealed high TSH level, low T4 free level and negative antiperoxidase antibodies. Amiodarone was stopped and levotiroxine was started. Two months after, TSH and T4 free levels were normal and the patient was asymptomatic. Amiodarone is associated with several side effects that can preclude its indication; one of these side effects is hypothiroidism, characterized by high TSH levels, low T4 free levels and unspecific symptoms such as fatigue, cool intolerance and dry skin. The treatment of choice is levotiroxine.
KEYWORDS: Amiodarone, hypothyroidism, thyroiditis. (Source: Mesh, NLM)
INTRODUCCIÓN
La amiodarona (AM) es un antiarrítmico de clase III con alto contenido de yodo que puede alterar la función tiroidea (1,2). La mayoría de pacientes permanece eutiroideo durante el tratamiento; sin embargo, algunos pueden presentar tirotoxicosis o hipotiroidismo, dependiendo del antecedente de enfermedad tiroidea y de la procedencia del paciente (3, 4).
La molécula de AM es similar al de las hormonas tiroideas, y ejerce efectos tóxicos directos en los folículos tiroideos y en los tejidos periféricos (5). Es un derivado benzofurano que contiene dos átomos de yodo por molécula; es decir, el 37% de su peso molecular (6). Actualmente, a las dosis usuales de 100-600mg/día, suministra a los pacientes entre 3-21 mg/día de yodo inorgánico, lo que representa entre 35-140 veces la dosis diaria recomendada de ingesta de yodo (150 μg/día) (7).
En los tejidos periféricos, la AM inhibe a la deiodinasa tipo I, incrementando los niveles circulantes de T4 y T3 reversa y disminuyendo los niveles de T3 (8); mientras que, en la tiroides ejerce efectos citotóxicos directos relacionados a su alto contenido de yodo. No existe relación entre el uso de AM y la inducción de autoinmunidad (9).
La incidencia global de disfunción tiroidea asociada al uso de AM oscila entre 14-18% (7,9). El hipotiroidismo inducido por AM (HIA) es más frecuente en zonas yodo-suficientes, en mujeres y en personas con anticuerpos antiperoxidasa tiroidea (antiTPO) positivos (10).
En nuestro país no existen reportes del tipo o frecuencia de disfunción tiroidea asociada al uso de AM. En este reporte, describimos el caso de una mujer, sin antecedente de patología tiroidea, que presentó hipotiroidismo asociado al uso de AM.
Caso clínico
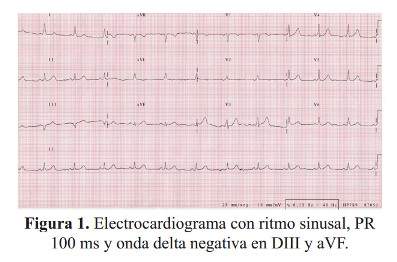
Mujer de 57 años, natural y procedente de Lima, sin antecedente personal o familiar de enfermedad tiroidea, que acudió con un tiempo de enfermedad de cuatro semanas, caracterizado por palpitaciones, fatiga, caída del cabello y aumento del sueño. La paciente estaba recibiendo amiodarona 200 mg/día desde tres meses antes de la consulta, por un diagnóstico de Síndrome de Wolf Parkinson White ( Figura 1).
Al examen físico se encontró PA: 120/80 mm Hg, FC: 88 latidos/min, y peso de 62,6 Kg; piel seca y reflejos osteotendinosos prolongados. No se encontró bocio.
Los análisis de laboratorio mostraron TSH 144 mUI/dL (VN: 0,3-5) y T4 libre 0,46 μg/dL (VN: 0,8-2). Con estos resultados se hizo el diagnóstico de hipotiroidismo inducido por amiodarona.
Se suspendió la amiodarona y se inició levotiroxina 150 μg por día. Dos meses después, la paciente acudió a control sin presentar molestias y la TSH fue 0,9 mUI/dL y T4 libre 1,64 μg/dL. Los anticuerpos antiTPO fueron negativos y continuó el tratamiento a largo plazo con levotiroxina 75 μg por día.
En la evaluación electrocardiográfica se encontró un patrón de preexcitación caracterizado por PR corto y la presencia de ondas delta, sin embargo la paciente no había presentado taquicardia sostenida ni síncope. La paciente permaneció sin arritmias incluso luego de suspender la amiodarona. Después de un año la evolución fue favorable sin uso de antiarrítmicos y no es candidata para ablación.
DISCUSIÓN
Entre 10-20% de los pacientes tratados con AM pueden presentar HIA (6), variando de acuerdo al status de yodo suficiencia. Así por ejemplo, en áreas de ingesta alta, media y baja de yodo, la incidencia de HIA es de 13,2%, 5,7% y 6,4%, respectivamente (9). En general, el HIA es más frecuente en zonas yodo-suficientes, con una incidencia mujer/hombre de 1,5/1 (6-11) y se presenta generalmente antes de los 12 meses de iniciado el tratamiento (10).
La presencia de anticuerpos antitiroideos aumenta la posibilidad de desarrollar HIA (6). De hecho, el riesgo relativo de HIA asociado a la presencia de antiTPO y sexo femenino es de 7,9 y 7,3, respectivamente; sin embargo, el riesgo se incrementa a 13,5 si ambos factores están presentes (7,9). Por otro lado, el antecedente de tiroiditis de Hashimoto (TH) es un factor de riesgo para desarrollar HIA (6-8). En el caso de nuestra paciente, ella procedía de una zona yodo-suficiente, no existía el antecedente de TH y los anticuerpos antiTPO fueron negativos.
En la glándula tiroides, el alto contenido de yodo de la AM inhibe directamente la síntesis de hormonas tiroideas (efecto Wolff-Chaikoff) (7,8). Este efecto es mayor en glándulas con daño previo, como es el caso de los pacientes con TH (6-8).
En el HIA, los síntomas son inespecíficos e incluyen fatiga, piel seca, intolerancia al frío y bradipsiquia (6-11). En los pacientes que ya están recibiendo levotiroxina, se debe aumentar la dosis por el efecto inhibitorio de la conversión periférica de T4 a T3 inducido por AM (7, 8). El bocio es raro, y el coma mixedematoso es muy infrecuente (9).
Los exámenes de laboratorio muestran TSH elevado y T4 libre disminuido (6-11). En algunos casos la tiroglobulina se puede incrementar, pero este fenómeno está relacionado a la elevación del TSH (7,10).
El tratamiento de elección es la levotiroxina. La AM puede ser suspendida según el criterio del cardiólogo y el tipo de arritmia cardíaca subyacente (6,10). Si la AM es descontinuada, el HIA remite en 2-4 meses en el 60% de los pacientes (9), especialmente en los pacientes sin antecedente de TH (7). En general, se recomienda continuar con la AM e iniciar levotiroxina. El nivel de TSH se debe mantener en el nivel normal superior, y debe ser monitoreado de manera regular (7-8,11).
En nuestra paciente, se suspendió la AM y se inició tratamiento con levotiroxina. La evolución clínica fue favorable, sin necesidad de utilizar otros antiarrítmicos.
En algunos pacientes la amiodarona puede inducir tirotoxicosis (TIA) (12). La TIA es más frecuente en zonas yodo-deficientes, en hombres, impredecible y se puede presentar de manera abrupta y en cualquier momento del tratamiento; inclusive después de haber suspendido la AM (6-9). Los síntomas clásicos de tirotoxicosis suelen estar ausentes. La TIA suele estar precedida por empeoramiento de la arritmia cardíaca o insuficiencia cardíaca (8-10,12). El diagnóstico se realiza con TSH suprimido y T3 elevado (10-12).
En general, se recomienda una evaluación inicial de la glándula tiroides y la determinación basal de TSH, T4 libre, T3 total y antiTPO (7-9). En algunos casos es necesaria una ecografía de tiroides (7). El TSH se debe repetir cada 6 meses (7-9).
REFERENCIAS BIBLIOGRÁFICAS
1.Barbesino G. Drugs affecting thyroid function.Thyroid. 2010; 20:763-70. [ Links ]
2.Basaria S, Cooper DS. Amiodarone and the thyroid. Am J Med. 2005; 118:706-14. [ Links ]
3.Padmanabhan H. Amiodarone and thyroid dysfunction. South Med J. 2010; 103:922-30. [ Links ]
4.Paz-Ibarra JL. Disfunción tiroidea inducida por amiodarona en la práctica clínica. An Fac Med. 2011; 72:69-78. [ Links ]
5.Ursella S, Testa A, Mazzone M, Gentiloni Silveri N. Amiodarone-induced thyroid dysfunction in clinical practice. Eur Rev Med Pharmacol Sci. 2006; 10:269-78. [ Links ]
6.Cohen-Lehman J, Dahl P, Danzi S, Klein I. Effects of amiodarone therapy on thyroid function. Nat Rev Endocrinol. 2010; 6:34-41. [ Links ]
7.Martino E, Bartalena L, Bogazzi F, Braverman LE. The effects of amiodarone on the thyroid. Endocr Rev. 2001; 22:240-54. [ Links ]
8.Bogazzi F, Bartalena L, Gasperi M, Braverman LE, Martino E. The various effects of amiodarone on thyroid function. Thyroid. 2001; 11:511-19. [ Links ]
9.Eskes SA, Wiersinga WM. Amiodarone and thyroid. Best Pract Res Clin Endocrinol Metab. 2009; 23:735-51. [ Links ]
10.Han TS, Williams GR, Vanderpump MP. Benzofuran derivatives and the thyroid. Clin Endocrinol (Oxf). 2009; 70:2-13. [ Links ]
11.Loh KC. Amiodarone-induced thyroid disorders: a clinical review. Postgrad Med J. 2000; 76:133-40. [ Links ]
12.Alyan O, Arda K, Ozdemir O, Açu B, Soylu M, Demirkan D. Differential diagnosis and clinical course of amiodarone-induced thyroid dysfunction. Med Sci Monit. 2003; 9:117-22. [ Links ]
Correspondencia:
Miguel Pinto Valdivia
Servicio de Endocrinología, Hospital Nacional Cayetano Heredia
Avenida Honorio Delgado 262, Lima 31, Perú
Teléfono: 511 4370201
Fax: 511 4814177
E-mail:
miguelpinto72@yahoo.comRecibido: 13/10/11
Aceptado para publicación: 17/02/12