INTRODUCCIÓN
En la actualidad, el cáncer de mama es el más común en mujeres a nivel mundial, siendo la primera causa de muerte en mujeres en países en desarrollo 1, y el segundo cáncer más frecuente en mujeres en Perú 2. Se espera que la incidencia y la mortalidad por este cáncer aumenten en los países en vías de desarrollo 3. En Perú, cerca del 50% de los casos de cáncer de mama son detectados en estadios avanzados 4.
El sistema ideal de clasificación de cáncer de mama debería tener relación con el pronóstico y el tratamiento, siendo el análisis de expresión genética mediante plataformas moleculares el método más aceptado. Sin embargo, debido a su alto costo este no se encuentra ampliamente disponible 5. Por ello, se utiliza como alternativa el análisis inmunohistoquímico de biomarcadores por su fácil aplicación en el contexto clínico y adecuada relación costo-beneficio 6. Estas pruebas no solo dan información adicional más allá de los clásicos factores clínicos e histológicos 7, sino que también permiten tomar decisiones terapéuticas 8.
Los marcadores inmunohistoquímicos utilizados rutinariamente para la tipificación del cáncer de mama son los siguientes: receptores de estrógeno, receptores de progesterona, HER2/neu, y Ki67 9. Según la expresión de estos marcadores, el cáncer de mama puede clasificarse en cuatro tipos, cada uno con tratamiento y pronóstico diferentes 6. El método de clasificación basado en marcadores inmunohistoquímicos es más accesible económicamente en comparación con el análisis genético y tiene una adecuada reproducibilidad, característica importante en países donde los recursos económicos son limitados, pero donde se requiere obtener la mayor información de la enfermedad y su pronóstico 10,11.
Existen pocos reportes en la literatura nacional sobre las características inmunohistoquímicas del cáncer de mama y la mayoría han sido realizados en un centro especializado 12,13. Los institutos especializados representan el último escalón del sistema de salud peruano para el tratamiento de una patología, por ello estudios en estos centros sobrerrepresentan a los casos de peor pronóstico que son referidos provenientes de niveles previos de atención 14 . En comparación, los hospitales generales son los primeros establecimientos donde se realiza el diagnóstico de esta enfermedad 10, y creemos que podrían proveer una oportunidad para brindar información más cercana a la generalidad de los casos de cáncer de mama. Y debido a que estas características guían el tratamiento en esta enfermedad, un mayor conocimiento podrá brindar mayor información en la toma de decisiones para la adquisición y financiamiento de nuevos tratamientos que surjan en el futuro. Por ello, el objetivo del trabajo fue describir el perfil inmunohistoquímico de cáncer de mama en pacientes atendidos en un hospital general de Lima, Perú.
MATERIAL Y MÉTODOS
Estudio descriptivo, transversal y retrospectivo. La población de estudio estuvo conformada por pacientes cuyas biopsias o piezas operatorias de mama fueron estudiadas en el Departamento de Anatomía Patológica del Hospital Nacional Arzobispo Loayza (Lima, Perú), durante el periodo comprendido entre el 01 de mayo de 2015 al 30 de abril de 2017.
Se incluyó en el estudio a todos los pacientes mayores de 18 años que fueran atendidos en el Hospital Nacional Arzobispo Loayza que tuvieran una muestra de biopsia o pieza operatoria de glándulas mamarias, con estudio inmunohistoquímico completo y cuyo diagnóstico final fue carcinoma infiltrante de mama en el informe anatomopatológico. Se excluyeron casos con información demográfica incompleta. En aquellos casos que contaron con más de un informe anatomopatológico solo se incluyó la información del reporte más antiguo. Esto se debe a que el reporte inicial usualmente corresponde a la biopsia diagnóstica del paciente previo a cualquier tratamiento. Mientras que en los reportes posteriores el paciente usualmente ha recibido tratamiento con fármacos o radioterapia, lo que puede conllevar a una modificación del perfil inmunohistoquímico en algunos casos de cáncer de mama 15, que no es el objetivo de este estudio.
El procedimiento de los estudios anatomo- patológicos de mama se realizó mediante un protocolo estandarizado del servicio de anatomía patológica del hospital, basado en las recomendaciones dadas por Lester et al. 16. En cada caso se seleccionó la lámina más representativa del tumor y su respectivo bloque de parafina para el estudio de inmunohistoquímica mediante receptores de estrógenos, receptores de progesterona, Her2/neu, y Ki-67. Los procedimientos para el estudio de inmunohistoquímica se realizaron de acuerdo con protocolos y recomendaciones internacionales 17-19, mientras que el reporte de los resultados fueron realizados de acuerdo al protocolo vigente del College of American Pathologists20.
Variables de estudio
Se estudiaron las siguientes variables de los informes de anatomía patológica: edad, tipo histológico y lateralidad de la lesión. Para una mayor uniformidad, en el tipo histológico se consideró la clasificación de la OMS 21, dividiéndose solamente en tres categorías: Carcinoma invasivo sin tipo especial, carcinoma invasivo lobular y otros (que incluyó a los demás subtipos).
Para el grado histológico se utilizó el score de Nottingham, basado en puntajes de la diferenciación tubular, pleomorfismo nuclear e índice mitótico, clasificando a la neoplasia en tres grados: Grado I, Grado II y Grado III, siendo este último el de menor diferenciación.
Los receptores de estrógeno y progesterona se consideraron positivos si más del 1% de células estaban teñidas. Her2/neu se consideró positiva si en más del 10% de las células tumorales se teñían de forma completa e intensa, e “indeterminado” si más del 10% de las células tumorales se tiñeron de forma incompleta y débil o si menos del 10% se tiñeron de forma completa e intensa. En los casos “indeterminados”, se realizó la prueba por CISH (Chromogenic in situ hybridization), que determinó si era positivo o negativo. El Ki67 se expresó como el porcentaje de células teñidas, considerándose el valor como alto si se expresaba en más del 14% de las células.
De acuerdo a los resultados de inmunohistoquímica, se clasificaron los casos en cuatro categorías: Luminal A, Luminal B, Triple negativo, HER2/neu positivo no luminal (Tabla 1) 22.
Análisis de datos
Para el análisis de los datos se utilizó el programa estadístico Stata v.13 (StataCorp LP, College Station, TX, USA). Se utilizó estadística descriptiva de las variables categóricas, determinándose frecuencias absolutas y relativas; en el caso de las variables numéricas se utilizó la media y desviación estándar o la mediana y el rango intercuartil, previa evaluación del supuesto de normalidad mediante la prueba de Shapiro- Wilk. Para la evaluación de asociación entre variables se utilizó la prueba de chi cuadrado, considerándose un valor p<0,05 como estadísticamente significativo.
Aspectos éticos
Para asegurar la confidencialidad de los datos de los pacientes, solo los investigadores tuvieron acceso a la información. Solo se utilizó algunos datos personales de los pacientes durante la fase de recolección de datos. Al finalizar la recolección de los datos, estos fueron procesados de forma anónima para lo cual fueron codificados mediante un código alfanumérico generado por el autor principal quien fue el único que conocía los códigos. Los datos codificados fueron almacenados de forma virtual en la computadora del autor principal.
RESULTADOS
En el periodo del estudio, en el hospital se emitieron 330 informes de cáncer de mama, de los cuales se excluyeron 71 casos, 38 por ser duplicados y 33 por tener información incompleta. Al final se consideraron en el estudio 259 casos.
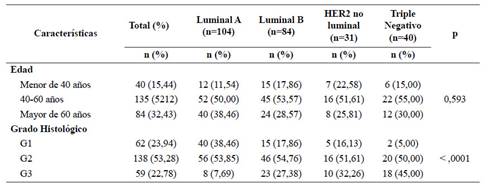
Todos los casos fueron de género femenino, con una media de edad de 54,64 ± 14,07 años. La mayor parte de casos ocurrieron en la mama derecha (53,28%), el tipo histológico predominante fue el carcinoma invasivo ductal sin subtipo histológico (88,03%) y el grado histológico más frecuente fue el intermedio (53,28%) (Tabla 2).
En más de la mitad de los casos se observó la expresión de receptores de estrógenos y receptores de progesterona, mientras que HER2/neu fue positivo en la cuarta parte del total de casos. Por otro lado, se observó que la mediana de la expresión de Ki67 fue 15% (IQR: 10-40%).
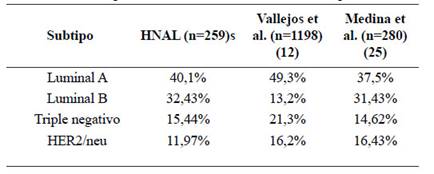
El subtipo molecular principal fue el Luminal A (40,15%), Luminal B (32.43%), HER2 positivo no luminal (11,97%) y triple negativo (15,44%) (Tabla 3). El análisis combinado de las variables mostró que el subtipo molecular no estuvo asociado a la edad (p=0,593), pero está asociado al grado histológico (p<0,0001).
DISCUSIÓN
El cáncer de mama es un problema de salud pública importante en el Perú, siendo el cáncer más frecuente en mujeres después del cáncer de cérvix 1. La heterogeneidad de esta enfermedad plantea un importante reto para su clasificación y manejo 23.
En nuestros resultados, por clasificación histológica, el tipo predominante fue el carcinoma invasivo ductal sin subtipo especial, lo que concuerda con la literatura existente 23. Se acepta que los subtipos histológicos no influyen en la sobrevida del paciente 24,25, por lo que a pesar de ser descrito de forma rutinaria en los informes patológicos, su valor pronóstico es ínfimo. Esta clasificación está siendo desplazada por la inmunohistoquímica, que brinda información importante sobre el pronóstico del paciente.
Por otro lado, se encontró que Her2/neu fue positivo en el 25,87% de casos evaluados, resultado mucho que es mayor al de otros países 7,27. Debido a que hasta un cuarto del total de pacientes con cáncer de mama expresan Her2/neu, recomendamos la evaluación constante de los nuevos medicamentos en desarrollo que bloquean este protooncogen para su posible uso y financiamiento en los hospitales públicos. Un ejemplo es Trastuzumab, un anticuerpo monoclonal anti-Her2/ neu que ha mejorado el pronóstico de estos pacientes 28, y que actualmente es financiado por el seguro integral de salud en el Perú 28.
De forma similar, la proporción del subtipo triple negativo-el subtipo de peor pronóstico- fue mayor que los encontrados en estudios internacionales (7.4%-12%) 7,30,31. Esta diferencia con estudios internacionales podría ser explicada por la etnicidad de nuestra población de estudio, pues la raza hispánica se considera un factor de riesgo para el subtipo triple negativo en estudios realizados fuera de Latinoamérica 7,27.
Finalmente, es importante comentar que las proporciones de factores de mal pronóstico inmunohistoquímicos (HER2/neu positivo y subtipo triple negativo) encontradas en el este estudio, son similares a las encontradas en otro hospital general peruano 25 pero menores a las encontradas en estudios nacionales realizados en institutos especializados (12). Esto podría ser por un sesgo de referencia, que incrementa los casos de mal pronóstico mientras mayor sea el nivel de complejidad del establecimiento de salud 14.
Este estudio tiene importantes limitaciones que deben ser tomadas en cuenta antes de interpretar los resultados. Primero, en este estudio no se evaluaron variables clínicas ni el estadiaje de las neoplasias, por no ser parte del objetivo del estudio. Ello imposibilitó la evaluación del pronóstico de los subtipos de cáncer de mama según inmunohistoquímica y establecer una asociación entre el perfil inmunohistoquímico y la presentación clínica de la enfermedad al momento en que la paciente entró en contacto con nuestra institución.
Por otro lado, toda la población estuvo constituida por pacientes atendidos en un solo hospital y la población de estudio comprendió un periodo de solo dos años, por lo que las características presentadas en este estudio podrían estar sujetas a sesgos de selección (ya que no se realizó un muestreo probabilístico) y no sería posible generalizarlas a todo el país o a otros hospitales.
En conclusión, en nuestro estudio uno de cada cuatro casos de cáncer de mama presentó una inmunohistoquímica de Her2/neu positivo. También encontramos que, al igual que en reportes previos, Luminal A predomina como el subtipo inmunohistoquímico más común de carcinoma de mama invasivo, y que el grado histológico se asocia al subtipo inmunohistoquímico.