INTRODUCCIÓN
La erosión dental es una condición multifactorial que describe la pérdida química de la superficie de esmalte y dentina por exposición a ácidos no derivados de bacterias orales 1,2. La prevalencia global de erosión dental en todo el mundo es de 30% a 50% en niños, 30 % en adolescentes y de 20% a 45% en adultos 3,4.
Los ácidos responsables de la erosión provienen de fuentes extrínsecas (dieta, hábitos de higiene, consumo de medicamentos, actividad física, ocupación) y fuentes intrínsecas (reflujo gastroesofágico, trastornos de la alimentación) 3-5. En los últimos años los hábitos dietéticos han cambiado, se ha incrementado el consumo de jugos y frutas naturales por su alto nivel de antioxidantes, fibras y vitaminas, sin embargo también han sido asociados a mayor prevalencia de erosión dental 2,3,6. La ingesta de cítricos, el consumo de frutas más de dos veces al día, consumo diario de refrescos y consumo semanal de vinagre o bebidas deportivas puede aumentar significativamente el riesgo de erosión dental 5,7. Asimismo, la mayor pérdida de minerales en los dientes se produce a un pH menor a 4,5 de tal forma que los jugos de frutas (pH 2,78-4,60), bebidas carbonatadas (pH 2,5-3,46), bebidas alcohólicas (pH 2,8-4,4), vinagre (pH 3,2), suplementos deportivos (pH 3,17-3,87) presentan un pH bajo 8-10.
Ciertas frutas y bebidas industrializadas contienen diferentes tipos de ácidos débiles que les confieren el potencial erosivo de las estructuras dentales, cuyas características dependen de factores químicos acidez titulable (AT), tipo de ácido, pH, adhesión del producto a la superficie, presencia y concentración de calcio, fosfato, fluoruro; factores de comportamiento: forma de ingerir la bebida, consumo excesivo de alimentos o bebidas ácidas, exposición nocturna a bebidas ácidas, prácticas de higiene bucal y factores biológicos los que son aspectos inherentes al individuo: capacidad buffer, rango de flujo salival, formación de película adquirida, composición y estructura de los dientes, anatomía y oclusión, movimientos fisiológicos de los tejidos blandos 5,8,10,11.
En la amazonía peruana existen frutas que son consumidas frecuentemente por sus propiedades antioxidantes y alto contenido de vitamina C. Veras en Brasil y Ruilova en Perú encontraron que el camu camu presenta un pH de 2,80 y 2,90 respectivamente, produciendo disminución de la microdureza superficial del esmalte in vitro 12,13, sin embargo los resultados no se pueden replicar en el entorno oral con todas las variaciones biológicas que influyen en la erosión 14, mientras que un esquema de investigación in situ permite la posibilidad de controlar el desafío erosivo, permitiendo contacto directo con la saliva dando lugar a la formación de la película adquirida, siendo este último, un factor relevante en el desarrollo y progresión de las lesiones erosivas 14,15. Por otro lado, no existe una evidencia conclusiva del potencial erosivo de los jugos de fruta 7.
El objetivo del presente estudio fue evaluar in situ el potencial erosivo de frutas amazónicas Physalis Peruviana (aguaymanto), Averrhoa Carambola (carambola), Myrciaria Dubia (camu camu) sobre el esmalte dental mediante microdureza superficial Vickers (MSV).
MATERIAL Y MÉTODOS
Diseño experimental
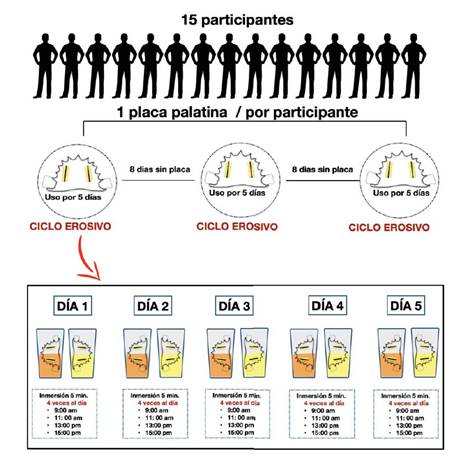
El presente estudio doble ciego, randomizado e in situ presentó 3 fases de 5 días con un intervalo de 8 días entre ellos. El protocolo fue aprobado por el Comité Institucional de Ética de la Universidad Peruana Cayetano Heredia (Nº 477-20-18). Se incluyeron quince voluntarios entre 18 - 30 años (3 hombres y 12 mujeres) con buen estado general, flujo salival estimulado mayor a 1 ml/min y no estimulado mayor a 0,1 ml/min. Se excluyeron de este estudio voluntarios con lesiones de caries activa, enfermedad periodontal, aparatología ortodóncica, fumadores, uso de medicamentos en los últimos 2 meses (antidepresivos, narcóticos, diuréticos, antihistamínicos, antimicrobianos), enfermedades sistémicas autoinmunes, xerostomía, diabetes tipo 1, malnutrición, problemas gastroesofágicos y regurgitación o vómito 16-21. Antes de la participación los voluntarios firmaron un consentimiento informado.
Para la evaluación del flujo salival estimulado y no estimulado se recolectó saliva 2 horas después de la última comida. Para la saliva estimulada, los voluntarios masticaron un pedazo de parafina (Parafilm® M, Illinois, Estados Unidos) durante un minuto, luego escupieron por 5 minutos en tubos cónicos de polipropileno de 17 x 120 mm 17,18,22. El tamaño de muestra fue calculado en base a un estudio piloto con 3 voluntarios. Se estimó un tamaño de muestra de 15 voluntarios basados un nivel de confianza del 95%, poder estadístico de 85%, considerando una deserción del 20% lo que corresponde a lo reportado en la literatura (14,16- 18,21).
Preparación de los especímenes
Se utilizaron 225 especímenes de esmalte (4 x 4 x 2 mm) obtenido de premolares humanos sanos, sin signos de erosión, sin manchas, ni deformaciones, sin restauraciones ni grietas 16. Los dientes fueron seccionados con un disco diamantado biactivo (KG Sorensen®, São Paulo, Brasil) bajo refrigeración constante, para obtener especímenes de 4 x 4 x 2 mm. El pulido de la superficie de esmalte se realizó con lija de agua (Asalite, Lima, Perú) de grano 600, 800, 1000, 1500 y 2000 durante 2 min con irrigación constante con cada lija, para lograr una superficie uniforme. Finalmente, los especímenes fueron expuestos a ultrasonido durante 10 minutos para eliminar los residuos. Todos los especímenes se almacenaron en agua destilada desionizada bajo refrigeración a una temperatura de 4°C hasta que se iniciaron los ciclos erosivos 19. Todas estas muestras fueron esterilizadas en óxido de etileno (16- 18). Se prepararon 45 especímenes para cada bebida evaluada.
Confección de los dispositivos intraorales
Se fabricó una placa palatina intraoral removible de resina acrílica autopolimerizable, por participante. Los especímenes fueron distribuidos aleatoriamente para cada sujeto y para cada fase del estudio para lo cual se realizaron 6 cavidades (4x4x2 mm), 3 de cada lado. Los especímenes fueron fijados a las cavidades con cera pegajosa en bastón (Asfer, São Paulo, Brasil). Adicionalmente, se colocaron dos alambres ortodónticos adheridos al dispositivo sobre las cavidades de la placa, sin contacto con el esmalte, para garantizar la ausencia de abrasión por la lengua 22. Todos los especímenes fueron colocados a nivel de la placa palatina y fueron reemplazados en cada fase experimental.
Preparación de las bebidas
Se emplearon las siguientes bebidas: Physalis Peruviana (aguaymanto), Averrhoa Carambola (carambola), Myrciaria Dubia (camu camu), Coca cola® (control positivo) y agua destilada (control negativo). Para la preparación de los jugos de frutas se seleccionaron frutas maduras y en buen estado. Se lavaron en agua corriente y luego se secaron a temperatura ambiente. Para la preparación de los jugos se utilizaron 100 ml de pulpa de fruta con 200 ml de agua destilada desionizada, en una proporción 1:2 dando un total de 300 ml de jugo 23. Las bebidas se mantuvieron a temperatura ambiente y se utilizaron el mismo día 13.
Ciclo erosivo
Se entregó una placa palatina a los voluntarios junto a una lista de indicaciones diarias, agua destilada desionizada, cepillo dental Colgate 360º (Colgate Palmolive S.A), pasta dental Colgate Máxima Protección (Colgate Palmolive S.A), recipiente plástico para almacenar las placas acrílicas y gasa. Los voluntarios realizaron su higiene dental normalmente, sin cepillar el dispositivo. También se informó a los voluntarios de no utilizar ningún producto fluorado o alimentos ricos en flúor durante el desarrollo del estudio.
Todos los voluntarios elegibles fueron identificados por un número único de estudio. Se les asignó al azar un orden de tratamiento de secuencia de acuerdo con el orden de entrada en el estudio. La asignación al azar se determinó a partir de una tabla de asignación estándar al azar. Los especímenes fueron distribuidos aleatoriamente a los diferentes grupos experimentales y codificados. La placa palatina fue instalada la noche anterior al inicio de la fase experimental, después de la última higiene y antes de dormir para propiciar la formación de película adquirida. El segundo día las placas acrílicas fueron expuestas a las bebidas, 4 veces al día en horarios predeterminados (9:00 am, 11: 00 am, 13:00 pm y 15:00 pm) de la siguiente forma: El dispositivo se retiró del paladar y fue colocado dentro de un recipiente que contenía una bebida durante 5 minutos, se procedió a lavar con agua destilada desionizada y se sumergió el otro lado del dispositivo en otra bebida durante 5 minutos, luego se procedió a lavar con agua destilada e inmediatamente fueron recolocados en la boca. Estos dispositivos fueron usados diariamente, inclusive para dormir, excepto durante los horarios de alimentación (desayuno, almuerzo y cena). Después de cada fase experimental hubo un periodo de washout de 8 días para evitar cualquier efecto cruzado entre las bebidas y de descanso para los voluntarios. Seguidamente cada grupo fue expuesto a diferentes bebidas siguiendo los mismos procedimientos y tiempos 17 (Figura 1).
Microdureza Los especímenes fueron llevados a un microdurómetro de Vickers HV 1000 (Liangong Group, Shandong, China). La MSV se midió antes y después de la exposición a las bebidas. El equipo fue calibrado en 50 g de presión durante 5 segundos 2. Se registraron tres medidas de microdureza por cada espécimen. Se calculó la diferencia de dureza superficial. Para el cálculo del porcentaje de pérdida de dureza se utilizó la siguiente fórmula (% PPD = [(Dureza final- dureza inicial) / dureza inicial] * 100) 12.
Los datos obtenidos fueron analizados en el programa SPSS versión 19 (IBM, Nueva York, Estados Unidos). Se realizó una análisis univariado (media y desviación estándar). Para el análisis bivariado se empleó el test ANOVA/Tukey (a=0,05).
RESULTADOS
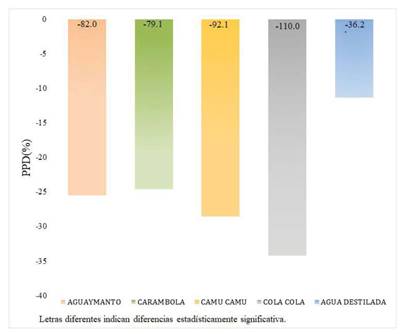
Los valores de microdureza superficial del esmalte inicial y final de acuerdo a los jugos utilizados se observan en la Tabla 1. Los cuatro grupos experimentales disminuyeron significativamente la microdureza superficial del esmalte (p<0,05), sin diferencias significativas entre ellos (Gráfico 1).
Tabla 1 Media y desviacion estandar de los valores de microdureza (kg/mm2) de esmalte antes y después de la exposición a las bebidas
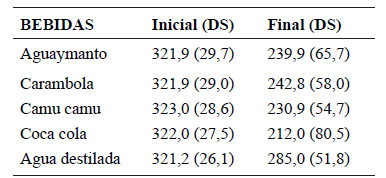
Unidad de medición kg/mm2
DISCUSIÓN
El objetivo de este trabajo fue evaluar in situ el potencial erosivo de frutas amazónicas Physalis Peruviana (aguaymanto), Averrhoa Carambola (carambola), Myrciaria Dubia (camu camu) sobre el esmalte dental. Se encontró que todas las bebidas evaluadas produjeron una disminución de la microdureza superficial en el esmalte, similar a la Coca cola.
Se ha reportado que frutas tropicales como araçá boi, camu camu, cupuaçu, taperebá y umbu tienen el potencial erosivo en el esmalte evidenciando valores de pérdida de microdureza de 77,9 % (araçá boi), 65,3% (camu camu), 53,8% (cupuaçu), 74,8% (taperebá) y 77,3% (umbu) en un modelo in vitro 12.
El potencial erosivo de una bebida está relacionado al pH y la AT de la misma. El pH se refiere a la concentración de iones de hidrógeno (H+) en una solución y nos indica si una solución es ácida, neutra o básica. La AT corresponde a la cantidad de hidróxido de sodio (NaOH) requerida para llevar a una solución a pH neutro 5,11. Los jugos estudiados presentaban un pH ácido: aguaymanto (pH 3,7/AT 1,6-2,0), carambola (pH 1,98-2,16/AT 0,72-0,78) y camu camu (pH 2,8-2,9/AT 1,08) presentando potencial erosivo 12,13,24-26.
La exposición repetida a bebidas con un pH menor a 4,5 por cortos períodos de tiempo para el esmalte dental es un factor de riesgo para erosión, a diferencia de la lesión cariosa que implica la interacción con ácidos bacterianos de la placa durante periodos prolongados de tiempo generalmente a un pH superior a 5,5 27.
Nirmala et al. compararon el pH y los oligoelementos de diferentes jugos de frutas y su relación con la erosión de esmalte, encontrando potencial erosivo de los jugos de piña (pH 3,30), uva (pH 3), caña de azúcar (pH 4,20), naranja (pH 3,26), limón dulce (pH 3,50), mango (pH 4,20), granada (pH 3,06), manzana (pH 5,25), zapote (pH 4,80) y sandía (pH 3,80) todos con un pH bajo; además los jugos de uva, piña y caña carecian de calcio en su composición por lo que no protegen la matriz del esmalte ante el ataque de bebidas ácidas 28.
La AT es otro factor físico-químico a considerar en el potencial erosivo. Enam et al. determinaron el potencial erosivo de gaseosas, bebidas energéticas, jugos de fruta (pH 2,4-3,9). La AT fue alta para las bebidas energéticas, moderado para gaseosas o jugos de frutas y bajo para agua. Cabe resaltar que la concentración de calcio fue mayor para los jugos de frutas 29. Benjakul y Chuenarrom encontraron que las bebidas de carabao y de guayaba presentaban un pH idéntico de 3,71, sin embargo la AT del carabao fue de 5,4 y de la guayaba 1,7. El carabao tuvo un mayor potencial erosivo que el jugo de guayaba con una pérdida de minerales del esmalte de 10,1% para la bebida de carabao y 6,9% para el jugo de guayaba 11. Así, cuanto mayor sea la cantidad de solución de NaOH añadida para alcanzar un valor de pH neutro, mayor será el efecto erosivo 30.
Los jugos evaluados en la presente investigación presentan ácido ascórbico. Se ha demostrado que diferentes ácidos presentan diferente potencial erosivo. Los ácidos maleico, tartárico y cítrico son los ácidos menos erosivos, mientras que los ácidos fosfórico, ascórbico y láctico son los más erosivos 30.
En relación al camu camu, Veras encontró que la pérdida de microdureza superficial del esmalte fue de 63,5% 12 y Ruilova de 77,58% 13 en modelos in vitro, sin embargo, en este estudio in situ se obtuvo una pérdida de 28,5%. Se ha reportado que la Coca cola ocasionó una pérdida de microdureza superficial del esmalte de 77,27% (pH 2.5/AT 0.1) que difiere de nuestro estudio con una pérdida de 34,2% 31. Las diferencias se pueden explicar a los diferentes diseños metodológicos empleados para estudiar erosión dentaria, in vitro e in situ.
Los estudios in vitro se ejecutan en un periodo de tiempo corto, son más económicos, y proporcionan información al investigador antes de realizar estudios en el entorno clínico, sin embargo, sobreestiman la pérdida de tejido superficial por la falta de remineralización de la saliva artificial, carece de proteínas, pérdida de su capacidad protectora contra la degradación ácida, reducción de grado de amortiguación y descomposición de proteínas 17,32-34.
Los estudios in situ tienen muchas ventajas como un número reducido de voluntarios, cambios medibles en escala de tiempo más corto, posibilidad de controlar el desafío erosivo porque la desmineralización se produce fuera del medio bucal evitando daños perjudiciales a los tejidos de los voluntarios 34,35 y el almacenamiento de los especímenes al medio bucal, donde la saliva puede diluir, neutralizar y amortiguar los ácidos. Además, la saliva transporta los iones calcio, fosfato y fluoruro al esmalte dental y desempeña un papel importante en la formación de la película adquirida 36, que actúa como una barrera semipermeable entre la superficie del diente y la cavidad oral, modulando los procesos de mineralización/desmineralización 15.
A pesar de las ventajas de los estudios in situ se han propuesto ciclos erosivos variados. Considerando que las lesiones erosivas iniciales se generan en tiempos cortos los especímenes han sido sumergidos durante 30 o 120 segundos, 4 veces al día durante 5 o 7 días 15,20,21. También se han empleado exposiciones a bebidas erosivas de 5 minutos a 10 minutos, 4 veces al día durante 5-7 días 20,36,37. En nuestro estudio se expuso el esmalte por 5 minutos, 4 veces al día (20 minutos/ día) lo cual nos permite simular la ingesta regular de individuos de alto riesgo de erosión dental 36.
El intervalo entre cada desafío erosivo se estableció en dos horas para garantizar el efecto protector contra la erosión y la acción de remineralización 19,20. Por otro lado, se optó por el uso de placas palatinas y no linguales debido a la mayor evidencia de erosión en especímenes de placas palatinas y por la mayor comodidad de los participantes 15,21. El uso de alambres de ortodoncia sobre los especímenes para inhibir el contacto con la lengua es importante ya que se ha demostrado que la pérdida de esmalte se incrementa por la combinación del consumo de bebidas ácidas y los efectos abrasivos de la lengua 22.
Los jugos de frutas estudiados se consideran saludables y se recomienda su consumo debido a su alto contenido de vitamina C, vitamina A, propiedades antioxidantes, antiinflamatorios y antimicrobiales, además son una alternativa para el tratamiento de diabetes, obesidad y enfermedades cardiovasculares 38,39. Sin embargo, el consumo excesivo puede tener efectos perjudiciales en los tejidos dentales. Se ha detectado la aparición temprana de lesiones erosivas en jóvenes de 12 años de 6 comunidades con una correlación positiva entre la frecuencia de erosión dental y la proximidad de las plantaciones de cítricos, que presumiblemente se relacionó con el alcance del consumo diario de naranja 40. Por otro lado, existe una controversia respecto al consumo de jugos de frutas al 100% ya que los resultados combinan datos de jugos de frutas naturales y envasadas con aditivos de azúcar. Sin embargo, la evidencia existente sobre el consumo de fruta al 100% y erosión dental en estudios de asociación con factores de riesgo no es concluyente 6.
Es importante reconocer que para personas que incluyen en su alimentación frutos o bebidas a base de frutas con potencial erosivo deben tener controles periódicos para identificar lesiones erosivas iniciales. La intervención temprana puede ayudar a crear conciencia en pacientes y profesionales de la salud sobre los riesgos potenciales. También es importante combinar estrategias de prevención como el consumo de productos ricos en minerales de calcio y fosfato, estimulación salival, uso de productos a base de flúor, CPP-ACP, té verde y mejorar la higiene bucal 5,13,27.
En conclusión, este estudio in situ demostró que los jugos a base de camu camu, aguaymanto y carambola son potencialmente erosivos.