INTRODUCCIÓN
El recubrimiento pulpar directo (RPD) busca reducir el riesgo de infección y daño adicional a la pulpa con un material biocompatible y antibacteriano, mientras proporciona un sello biológico y previene la filtración bacteriana. De tal manera, el éxito en este tipo de terapia con cementos a base de silicato de calcio (CSC) es contrastante en comparación al uso del hidróxido de calcio convencional 1,2.
El hidróxido de calcio se ha utilizado tradicionalmente como el material de recubrimiento pulpar de elección para las exposiciones pulpares en dientes permanentes; sin embargo, su alta solubilidad que conduce a la desaparición del material y la formación de defectos en la dentina reparadora no proporcionan un sello permanente contra la invasión bacteriana 3; a diferencia de los CSC que presentan alta bioactividad, biocompatibilidad, capacidad de sellado y propiedades mecánicas; razón por la que lo han desplazado en su uso 2.
El cemento agregado de trióxido mineral (MTA) es considerado el primer CSC introducido y tiene propiedades favorables para el RPD que incluyen reducción de la inflamación pulpar e inducción de formación de puente dentinario de calidad 1,4; pero dadas algunas desventajas que presenta su formulación original se ha desarrollado una mayor variedad de CSC como el White MTA, MTA Angelus, Biodentine, TheraCal LC, entre otros, que buscan mejorar las propiedades de biocompatibilidad y regeneración, disminuir el tiempo de fraguado, capacidad de sellado y resistencia 1,3-8. La presente revisión analiza las variedades de CSC, su mecanismo de acción, desventajas, factores relacionados y tasas de éxito clínico en su aplicación en casos de RPD.
Cementos a base de silicato de calcio
Los CSC se han desarrollado hace veintiocho años. El MTA fue la primera formulación más conocida y utilizada. Fueron propuestos inicialmente como materiales de reparación y obturación retrógrada, pero su uso clínico se expandió también a otros procedimientos como el recubrimiento pulpar. Por las desventajas asociadas al MTA, como el largo tiempo de fraguado, la difícil manipulación, el alto costo y la decoloración de los dientes y tejidos blandos, se desarrollaron nuevas formulaciones con mejores propiedades físico mecánicas y de manipulación por lo que nuevas marcas han sido introducidas al mercado. Debido a que, en el tratamiento de RPD, estos materiales están en contacto directo con la pulpa vital, también deben tener propiedades biológicas adecuadas, que son importantes de conocer para su utilización 5. Se detallarán los CSC más empleados en los estudios para su uso en RPD.
Cementos a base de silicato de calcio utilizados para recubrimiento pulpar directo MTA (agregado de trióxido mineral)
El MTA es considerado el primer CSC y fue introducido en 1993 por Torabinejad como material de reparación y obturación radicular. El polvo del MTA es una mezcla de silicato dicálcico, silicato tricálcico, aluminato tricálcico, sulfato cálcico, aluminoferrita tetracálcica y óxido de bismuto, que se mezcla con agua destilada durante la manipulación. Las propiedades favorables del MTA para su uso en RPD incluyen la reducción de la inflamación pulpar e inducción de formación de puente dentinario de calidad, por lo que se ha convertido en un sustituto superior al hidróxido de calcio. Sin embargo, el MTA es difícil de usar debido a su largo tiempo de fraguado, sus malas propiedades de manipulación, su alto costo y la potencial decoloración de los dientes y tejidos blandos 4,6. MTA gris o GMTA (ProRoot MTA, Dentsply, Tulsa, EE.UU.) fue la formulación original que se introdujo, y el MTA blanco se desarrolló posteriormente ya que esta versión mejoraría la estética 7.
Las nuevas generaciones de MTA disponibles comercialmente incluyen al White ProRoot MTA o WMTA, MTA Angelus, Retro MTA, MTA Plus, entre otros, a quienes se les ha modificado o añadido ingredientes para superar las desventajas del ProRoot MTA original. Por ejemplo, el MTA Angelus ofrece la ventaja de un tiempo de fraguado final entre 24-83 min y el Retro MTA tiene un tiempo de fraguado final de 12 min; tiempos menores comparados con los 228-261 min del ProRoot MTA 3.
Otros generaciones más recientes como el MTA Plus de la marca Bio MTA+ (Cerkamed, Polonia) contiene partículas nanocerámicas (2%) e ingredientes de hidroxiapatita (2%); también presenta una disminución del tamaño de los granos con partículas tres veces más pequeñas que del MTA convencional, que le confieren la propiedad de penetración de iones de calcio en el tejido desmineralizado, aumenta el proceso de sellado, fuerza y homogeneidad, al mismo tiempo que reduce el tiempo de fraguado a 15 minutos 1.
Neo MTA Plus (Avalon Biomed Inc., Houston, TX, EE. UU.) y la familia de productos iRoot (Innovative BioCeramix Inc., Vancouver, BC, Canadá) son materiales que también se pueden usar en tratamiento pulpar vital, pero aún hay pocos estudios que evalúan su uso en la práctica clínica. Neo MTA Plus fue desarrollado para ser utilizado en pulpotomías sin riesgo de decoloración debido al reemplazo del óxido de bismuto por óxido de tantalio, tiene mayor bioactividad, pero se ha demostrado que tiene un fraguado final en 315 ± 5 min. Los productos iRoot están disponibles en tres consistencias, lo que podría ofrecer la ventaja de elegir uno adecuado para cada aplicación clínica: iRoot BP IBC, Burnaby, Canadá) tiene presentación de jeringa precargada, mientras que iRoot BP Plus está disponible en frasco y con una consistencia más espesa, y iRoot FS se desarrolló especialmente para fraguar más rápido con un tiempo de fraguado final de 57 ± 2,7 min. Se ha demostrado que iRoot BP e iRoot BP Plus son materiales biocompatibles que mejoran la proliferación, migración, mineralización y formación de puentes dentinarios de las células de la pulpa dental humana en los procedimientos de recubrimiento pulpar 3.
Biodentine
Biodentine (Septodont, Saint-Maur-des-Fossés, Francia) fue introducido el 2009 y es un material de dos componentes: un polvo y un líquido. El polvo tiene presentación de cápsula predosificada de 0,7 g y contiene principalmente silicato tricálcico, silicato dicálcico, carbonato cálcico, y óxido de circonio como radio opacificador. El líquido consiste en cloruro de calcio como acelerador de fraguado y agente reductor de agua. La mezcla se hace con los 0,7 g de polvo y cinco gotas de líquido mediante el uso de un amalgamador durante 30 s a 4000-4200 rpm, lo que permite obtener un material con propiedades óptimas. El tiempo de fraguado inicial según el fabricante es de unos 12 min 3,8. Biodentine fue
diseñado como un sustituto de dentina permanente y biocompatible para aplicarse directamente en una sesión, con la técnica de sándwich, para la restauración final con resina, o en todo el volumen de la cavidad durante un período de observación antes de la restauración final. Existe amplia evidencia de los efectos positivos de Biodentine en las células pulpares vitales, para estimular la formación de dentina terciaria y la formación temprana de dentina reparadora 7. Biodentine, en comparación con el HC, es mecánicamente más fuerte, menos soluble y produce un sellado más hermético, por lo que se usa para recubrimiento pulpar 3.
Theracal LC
TheraCal LC (Bisco, Schaumburg, IL, EE.UU.) se introdujo en 2011 y es un silicato tricálcico modificado con resina fotopolimerizable de pasta única para su uso como agente de recubrimiento pulpar y como revestimiento protector para su uso con materiales de restauración, cemento u otros materiales base. Es un material híbrido: la patente original indicaba que consta de cemento Portland tipo III (45%), sílice como agente espesante (7%), resina (43%), óxido de bismuto (3%) y sulfato de bario (3%) como radio opacificadores. No requiere ningún acondicionamiento de la superficie de la dentina; se puede unir con diferentes tipos de adhesivos directamente después de la aplicación y su reacción de fraguado se activa por el componente polimerizable, lo que facilita la colocación de la restauración final sin retraso. El fabricante recomienda colocarlo en capas de 1 mm y curarlo durante 20 segundos. El material sella el sitio de recubrimiento pulpar a pesar del contacto con los fluidos dentinarios o pulpares ya que su solubilidad es menor. A pesar de que ha mostrado bioactividad suficiente, propiedades de manipulación superiores y calidad de unión con la restauración final, se recomiendan más estudios para su utilización en RPD 3,5.
Mecanismo de acción de los cementos a base de silicato de calcio
En la actualidad, el hidróxido de calcio está siendo desplazado por materiales como los CSC, los cuales presentan alta biocompatibilidad, actividad osteoconductora intrínseca y capacidad para inducir respuestas regenerativas en el cuerpo humano.
En el caso de RPD, el uso de estos materiales es fundamental porque ayudan a crear puentes dentinarios de mejor calidad en cuanto a grosor y volumen, siendo estos de suma importancia debido a que consiste en la formación de tejido mineralizado o dentina reparativa en el sitio de la exposición y, consecuentemente, preservación de la vitalidad pulpar. Asimismo, se obtiene un mejor sellado del sitio de recubrimiento pulpar, evitando cualquier filtración de microorganismos o sustancias irritantes a la pulpa dental 3.
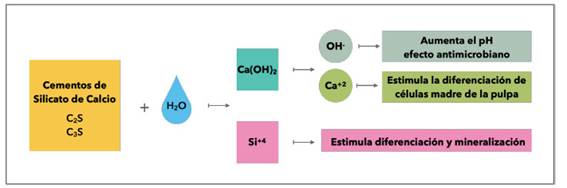
Para el recubrimiento pulpar directo, se tienen los siguientes materiales comercialmente disponibles: ProRoot MTA, MTA Angelus, RetroMTA, Biodentine y TheraCal LC, los cuales, debido a que están compuestos por silicato de calcio, tienen una reacción de fraguado común que es la hidratación. Como subproductos de esta reacción química se obtienen OH−, Ca2+ y Si4+ (Figura 1) 5.
Los iones hidroxilos (OH−) liberados tras la hidratación aumentarán el pH en el tejido subyacente, dando lugar a una fina capa necrótica entre el tejido vital restante y el cemento de silicato de calcio, esta capa necrótica protege a las células pulpares vitales subyacentes del pH alcalino del material y permite que estas lleven a cabo las funciones de regeneración. La posterior calcificación de esta capa necrótica superficial, seguida de la formación de dentina terciaria a partir de células madre de la pulpa dental estimuladas y diferenciadas, da lugar a un puente dentinario protector. Asimismo, el pH alcalino también garantiza la actividad antimicrobiana. De igual manera, los iones de calcio (Ca2+) contribuyen a la formación de este puente dentinario protector, ya que estimulan la diferenciación de las células madre de la pulpa dental. Finalmente, la liberación de los iones de silicio (Si4+) estimula la diferenciación en células odontoblastoides y la mineralización 9.
Desventajas de los cementos a base de silicato de calcio
Actualmente, los cementos dentales basados en silicato de calcio son reconocidos por su biocompatibilidad y por ser inductores de tejidos mineralizados. Sin embargo, estos cementos también presentan desventajas. Por ejemplo, el MTA tiene algunos inconvenientes como el potencial de decoloración, el tiempo de fraguado prolongado y malas propiedades de manipulación. La causa de la decoloración gris aún es discutible; sin embargo, la interacción del óxido de bismuto con el colágeno presente en la matriz dentinaria se ha indicado como el principal factor causante de la decoloración inducida por el ProRoot MTA 4.
Por otro lado, el Theracal LC (Bisco, Schaumburg, EE.UU.), un cemento a base de silicato de calcio modificado con resina, tiene como mayor desventaja la citotoxicidad, por incluir en su composición monómeros de metacrilato como el BIS-GMA. La presencia de resina que puede permanecer sin polimerizar a menudo se asocia con reacciones pulpares adversas que conducen a toxicidad e inflamación de la pulpa. También se le asocia a la formación de puente dentinario de menor grosor, que puede atribuirse a las propiedades de hidratación de TheraCal LC. Además, a pesar de que la fotopolimerización de TheraCal LC se asocia con una baja generación de calor, podría inducir efectos pulpares adversos cuando se utiliza en procedimientos de recubrimiento pulpar 3.
Sobre el Theracal LC, el fabricante también señala que, en contacto prolongado o repetido con la piel, tejidos blandos orales y ojos, podría producir irritación y posible daño en la córnea. En personas sensibles, podría producirse sarpullido cutáneo, irritación de la mucosa oral u otras reacciones alérgicas como la dermatitis alérgica de contacto.
Los materiales a base de silicato tricálcico como el Biodentine (Septodont, Saint-Maur-des- Fossés, Francia) no incluyen óxido de bismuto en su composición, que se ha atribuido como factor causante de la decoloración en cementos con este componente, sino que contiene un radio opacificador diferente que es el óxido de zirconio. Es por ello que en casos tratados con Biodentine no se vería la pigmentación y/o alteración en su coloración 4; sin embargo, hace que su radiopacidad sea significativamente menor que MTA Angelus, por ejemplo, y disminuya gradualmente con el tiempo, lo que causa dificultades en las observaciones radiográficas a largo plazo 3. Otro inconveniente del Biodentine, a pesar de la posibilidad de colocación inmediata de la restauración después del fraguado inicial, es su maduración intrínseca deficiente que puede tardar más de dos semanas y tiene valores más bajos de fuerza de unión al cizallamiento con la resina, que el ionómero de vidrio y el MTA, es decir, presenta una unión deficiente. Es importante dejar que, tanto Biodentine como MTA, maduren antes de la aplicación de la restauración suprayacente para obtener mejores resultados clínicos. Si la elección es una restauración en una cita es importante esperar de 12 a 15 minutos después de la colocación de estos cementos a base de Silicato de calcio. Otra opción es el manejo del caso en 2 citas; dejar que culmine el cristalizado completo que tarda en obtener el máximo endurecimiento hasta 28 días 3.
Factores que intervienen en el éxito del recubrimiento pulpar directo
De los diversos factores y/o condiciones que van a desempeñar un rol fundamental en el éxito del recubrimiento pulpar directo (RPD), los más relevantes son:
Edad
Debido al envejecimiento fisiológico propio de la edad, la pulpa dentaria experimenta cambios morfológicos, dimensionales y estructurales. Los cuales influyen en la posibilidad de éxito del recubrimiento pulpar directo, esto es debido a que con la edad se observa aumento del tejido calcificado sobre las paredes de la dentina y/o dentro del tejido pulpar, lo cual reduce el volumen original de la cavidad pulpar y conlleva a la disminución de la densidad celular, dando como resultado la disminución gradual de la irrigación e inervación, lo cual afecta a la capacidad de defensa y recuperación. Estudios como el de Harms et al. evaluaron los resultados clínicos del recubrimiento pulpar directo con cemento de silicato de calcio (Biodentine), describiendo, en relación con la edad, que la tasa de éxito más alta se encontró en los pacientes de edad más joven (10 a 20 años), y la tasa de éxito disminuyó con la edad 10. Asimismo, la evidencia científica basada en estudios clínicos, como el realizado por Lipski et al. determinan que el éxito del tratamiento depende de la edad y que fue estadísticamente significativo en pacientes menores de 40 años con un 90,9% y un 73,8% en pacientes de 40 años a más, mencionan que la edad del paciente influyó claramente en el resultado del recubrimiento pulpar directo con resultados menos favorables en pacientes mayores de 40 años 8.
Tipo de diente y ubicación
Otro de los factores evaluados en estudios asociados al éxito de recubrimiento pulpar directo, es el tipo y ubicación de la pieza dentaria. Lipski et al., al evaluar los factores que afectan los resultados del RPD con Biodentine, en el cual mencionan que el tipo de diente (anterior o posterior) y la ubicación (mandíbula o maxilar) no muestran diferencias significativas en la tasa de supervivencia con relación al éxito del procedimiento 8.
Diagnóstico
El diagnóstico constituye una pieza clave. En base a él podremos realizar el tratamiento adecuado, es por ello la importancia de realizar un examen y evaluación minuciosa, se considera que la conservación de la estructura dentaria y el mantenimiento de la vitalidad pulpar son los objetivos de la odontología actual.
El recubrimiento pulpar directo es el procedimiento en el cual la pulpa expuesta accidentalmente, durante la preparación cavitaria o por traumatismo, es cubierta con un material protector de injurias adicionales, material que simultáneamente estimula la formación de una barrera o puente de dentina reparadora. Las piezas dentarias deben cumplir las siguientes indicaciones: dientes permanentes inmaduros, dientes permanentes maduros con pulpa joven, traumatismos con exposición (antes de 24 horas), exposición accidental sobre dentina sana, pulpa sana e hiperemia pulpar (estado pre inflamatorio reaccional); y está contraindicada en estados inflamatorios irreversibles y cambios regresivos pulpares (atrofia o cálculos pulpares).
De igual manera, al examen clínico y radiográfico, debemos observar las siguientes consideraciones: Diagnóstico pulpar de pulpitis reversible, naturaleza del dolor condicionada a estímulos, la coloración del tejido pulpar debe ser normal, rojo intenso o brilloso. A la inspección y exploración evaluar: presencia de fractura coronaria con compromiso pulpar o exposición pulpar por exposición cavitaria, sin cambios de coloración de la pieza o la encía, sin presencia de edema ni fístula mucosa, la intensidad de la hemorragia post exposición no debe ser abundante y debe ser controlada en un máximo de 5 a 10 minutos para ser considerada favorable, las pruebas térmicas de respuesta normal, la prueba eléctrica de respuesta positiva normal. Radiográficamente observar fractura coronaria o preparación cavitaria con compromiso de cámara pulpar y espacio de ligamento periodontal normal con hueso alveolar sin rarefacción y sin lesión periapical 1,4,8,10.
Localización de la lesión
La localización del trauma o de la lesión cariosa que genera la exposición pulpar, puede alterar el pronóstico con relación al éxito del procedimiento. Las exposiciones pulpares con caries radiculares o cavidades clase V, constituyen una desventaja ante el procedimiento conservador. Jang et al. observaron que dos tercios de los fracasos del tratamiento involucraron restauraciones de dientes con caries de clase V causadas por caries radiculares; la tasa de fracaso fue del 50%, que fue la tasa más alta, en comparación con los grupos con cavidades de clase I, II o III 11.
Tiempo de exposición de la pulpa
El tratamiento en exposición pulpar debe ser tratado inmediatamente o en el periodo más corto posible con el fin de reducir el proceso de contaminación y preservar el complejo dentino pulpar, contribuyendo así al éxito del RPD, a menor tiempo transcurrido de la exposición pulpar traumática o mecánica, el pronóstico es más favorable porque disminuye las posibilidades de contaminación microbiana.
DISCUSIÓN
El uso de CSC para el RPD ha ganado popularidad en los últimos años debido a que es un método que preserva la vitalidad pulpar. Dado que existen CSC con distinta formulación, que les otorga propiedades de manipulación y tiempo de fraguado variados, es de suma importancia conocer sus efectos en el complejo dentino pulpar, como la formación del puente dentinario y la resultante ausencia de reacciones inflamatorias a largo plazo, que denotan el éxito clínico en un RPD; lo que es posible gracias a la biocompatibilidad del material e inexistencia de bacterias en el medio ambiente.
Existe una diferencia en la biocompatibilidad de los materiales basados en silicato de calcio en contacto con las células de la pulpa dental 12, la cual está directamente relacionada con la formación de puentes dentinarios. Diferentes estudios tomográficos e histológicos muestran que existe una mayor formación del puente dentinario en grosor y volumen al utilizar MTA y Biodentine 13,14 ya que estos materiales estimulan más a las células madre de la pulpa dental comparado con materiales como el hidróxido de calcio. De igual modo, esto concuerda con revisiones sistemáticas que confirman la predecible formación de esta barrera dentinaria con los materiales anteriormente mencionados 7,15. Asimismo, los CSC modificados con resina (Theracal LC) fueron evaluados in vitro e in vivo y se observaron puentes dentinarios completos solo en el 33% de los especímenes 16, así como una inflamación crónica leve, reducción del grosor de los puentes dentinarios y capacidad reparadora inferior a otros CSC como Biodentine, probablemente como consecuencia de monómeros sin polimerizar o de su reacción de hidratación incompleta 17.
Se puede evaluar la calidad, cantidad, grosor, continuidad y volumen del puente dentinario. Bakhtiar et al. en un estudio comparativo, hallaron que todos los especímenes que utilizaron Biodentine mostraron una formación completa continua delpuente dentinario evaluado histológicamente, mientras que las tasas fueron del 11% y 56% para TheraCal y ProRoot MTA, respectivamente. Tanto en el grupo ProRoot MTA como en el grupo Biodentine, se formó un puente dentinario completo por células parecidas a odontoblastos diferenciadas, mientras que más de la mitad de las muestras del grupo TheraCal presentaron uno incompleto. Además, el puente dentinario observado con Biodentine fue más grueso que con MTA 18.
Respecto al éxito clínico y radiográfico, han sido evaluados en estudios donde se comparan los tipos de CSC en el tiempo. La evaluación clínica se basa en la aparición o ausencia de signos y síntomas tales como dolor a estímulos térmicos, dolor a la masticación, dolor espontáneo, dolor a la percusión, movilidad o cambio de coloración de la corona. La evaluación radiográfica se basa en la formación ausente, parcial o total del puente dentinario medida en milímetros, cambios en el periodonto o formación de caries secundaria 1,2,4,8,10,19.
Entre los estudios que evaluaron el éxito clínico y radiográfico, hay estudios que comparan a la formulación original del MTA o ProRoot MTA con Biodentine. Parinyaprom et al. encontraron en un seguimiento de 18,9 ± 12,9 meses, tasas de éxito de 92,6% con ProRoot MTA y de 96,4% con Biodentine 4; similar a Linu et al., quienes encontraron tasas de éxito del 84,6% y 92,3% para el ProRoot MTA y Biodentine respectivamente luego de un seguimiento de 18 meses, esta ligera diferencia podría deberse a que la edad de los pacientes del primer estudio fue menor, de 6 a 18 años, y en el segundo fue de 15 a 30 años; evidenciando la influencia de la edad en el éxito del RPD. Por otro lado, en ambos estudios se observó cambio de coloración de la corona del diente con el ProRoot MTA 6.
A partir de la aparición del WMTA se tenía la expectativa de que no generaría cambio de color dental; sin embargo, Hedge et al., en un seguimiento de 6 meses donde compararon WhiteProRoot MTA (WMTA) y Biodentine, encontraron altas tasas de éxito del 91,7% y el 83,3% respectivamente; pero el WMTA produjo cambio de color del diente. Se cree que el componente de óxido de bismuto en el WMTA, el NaOCl utilizado para la hemostasia o la luz de curado utilizada para la restauración pueden ser responsables de esta decoloración. La alta tasa de éxito del MTA se atribuye a su capacidad para estimular la formación del puente dentinario, la propiedad antibacteriana y la excelente capacidad de sellado, que son fundamentales para el éxito del procedimiento RPD. Biodentine produce una respuesta pulpar similar, pero con las ventajas de mayor grosor del puente dentinario formado y un tiempo de fraguado más corto. La similitud de la respuesta tisular con estos materiales puede deberse a su composición química similar (silicato tricálcico), el subproducto liberado durante la reacción de fraguado y sus propiedades físicas 19.
Las altas tasas de éxito de Biodentine también han sido reportadas en otros estudios. Lipski et al., encontraron una tasa de éxito de 82,6% al cabo de 1 a 1,5 años 8, y Harms et al., hallaron tasas de 86% en un periodo de 2,3 años y 83,4% en 7,4 años (10), en estos estudios también se resalta la importancia de la elección del caso con el diagnóstico de pulpitis reversible y un procedimiento minucioso que incluye una restauración final de calidad para obtener el éxito del tratamiento 8,10.
El hidróxido de calcio (HC), como material usado tradicionalmente para RPD, también ha sido empleado en estudios comparativo con los CSC. Brizuela et al. hallaron que Biodentine y WMTA son adecuados para reemplazar al HC; Biodentine con un éxito de 100% tuvo ventajas como el tiempo de fraguado y la no decoloración del diente, mientras que HC en polvo (Hertz Pharmaceutical, Santiago, Chile) y WMTA (Dentsply Maillefer) tuvieron un fracaso de 13,64% al cabo de un año 2. Kundzina et al. demostraron que el WMTA se comportó mejor que el HC en pasta (Dycal, Dentsply) como material de RPD en molares con exposición pulpar cariosa en pacientes adultos, con tasas de éxito a los 36 meses de 85% y 52% respectivamente 20.
También se han evaluado nuevos materiales de CSC. El Bio MTA (Cerkamed, Polonia) fue evaluado por Peskerjoy et al., donde encontraron que luego de 36 meses el MTA Plus (Bio MTA) con 86,3% y Biodentine con 79,4% obtuvieron las mejores tasas de éxito clínico y radiográfico comparadas con las de Theracal LC con 72,1% y de Dycal con 69,4% 1.
Los factores que parecen tener influencia significativa en el resultado del éxito del procedimiento del RPD son: edad, diagnóstico y localización de la pieza dentaria; mientras que los factores como tipo de pieza dentaria y ubicación no presentan efectos significativos en el éxito del procedimiento. Con respecto al factor tiempo de exposición no se encontró evidencia experimental, la evidencia conceptual menciona que el éxito está relacionado con la rapidez con que se realice la técnica de RPD posterior a un daño, injuria y/o trauma 8. Asimismo, la elección del material que proporciona el efecto inductivo en las células pulpares y la calidad de sellado, que incluyen una restauración final adecuada, constituyen también factores determinantes en el éxito del RPD.
Los estudios muestran que los CSC tienen mayores tasas de éxito que el hidróxido de calcio usado tradicionalmente para RPD. Los CSC más recientes, como Biodentine y Theracal, tienen mayores ventajas que los CSC a base de MTA como alta biocompatibilidad, menor costo, tiempo de fraguado reducido, no producen cambio de color del diente y muestran un buen rendimiento terapéutico; sin embargo, al Theracal se le atribuyen un efecto citotóxico y la formación de puente dentinario de menor grosor. El Biodentine parece ser superior para su uso en casos de RPD por sus propiedades y ventajas, pero se requiere de más estudios clínicos a largo plazo para una recomendación definitiva.
CONCLUSIONES
El éxito del RPD se basa en la preservación de la vitalidad pulpar mediante la formación de un puente dentinario producto de la biocompatibilidad del material utilizado con las células pulpares, la ausencia de sintomatología dolorosa y la consideración de factores que pueden tener influencia en el resultado del procedimiento.
Actualmente existe una gran variedad de cementos a base de silicato de calcio que, a pesar de presentar algunas desventajas, la mayoría tiene tasas de éxito bastante altas en su uso para RPD, siendo una excelente alternativa para este tipo de tratamiento.