Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.25 n.3 Lima jul./set. 2005
ARTÍCULOS ORIGINALES
Seroprevalencia del Virus de Hepatitis C (VHC) en pacientes del Laboratorio Regional de Referencia Virológica (Maracaibo, Venezuela)
César Cuadra-Sánchez1; Reyna Moronta-Piñango1; Evelyn Córdova-Villanueva2; Raimy Mindiola-Morles3; Mary Araujo-Soto3; Diana Callejas-Monsalve4; Leticia Porto-Espinoza1
1 Lic. en Biología, M.Sc. en Microbiología. Laboratorio Regional de Referencia Virológica, Facultad de Medicina, La Universidad del Zulia, Maracaibo, Venezuela.
2 Lic. en Economía, Diplomada en Estadística para Investigadores, M.Sc. en Planificación de Ciencia y Tecnología. Facultad de Ciencias Económicas y Sociales, La Universidad del Zulia, Maracaibo, Venezuela.
3 Lic. en Bioanálisis. Laboratorio Regional de Referencia Virológica, Facultad de Medicina, La Universidad del Zulia, Maracaibo, Venezuela.
4 Lic. en Biología, M.Sc. en Inmunología. Laboratorio Regional de Referencia Virológica, Facultad de Medicina, La Universidad del Zulia, Maracaibo, Venezuela.
RESUMEN
OBJETIVO. Recolectar y analizar información referente a la seroprevalencia del VHC en una población de 722 pacientes que acudió al Laboratorio Regional de Referencia Virológico (Maracaibo, Venezuela) durante los años 2000-2003. MATERIAL Y MÉTODOS. Se utilizó el análisis inmunoenzimático Innotest HCV Ab IV de Innogenetics para evaluar la presencia de anticuerpos tipo IgG contra el Virus de Hepatitis C en los sueros de los pacientes estudiados. Los resultados obtenidos de seroprevalencia y otras variables epidemiológicas se organizaron y analizaron utilizando el software SPSS ® 10.0 (Chicago, USA) y Origin Pro ® 7.5 (Northampton, USA). RESULTADOS. Se encontró una seroprevalencia de 2,63% (19/722), la cual es superior a la reportada en Venezuela para la población general (0,9%) y otros grupos. La infección fue más frecuente en hombres que en mujeres. Los síntomas más comunes en los pacientes infectados fueron ictericia y cefalea (31,58%). CONCLUSIÓN. Los datos reportados actualizarán investigaciones previas en la zona y fundamentan la necesidad de desarrollar control epidemiológico para VHC en el Estado de Zulia.
PALABRAS CLAVE: Epidemiología de la Hepatitis C, Venezuela, Seroprevalencia.
SUMMARY
PURPOSE: Collect and analyze information regarding seroprevalence of Hepatitis C Virus (HCV) in a population of 722 patients that visited the Regional Viral Reference Laboratory (Maracaibo, Venezuela) during the years 2000-2003.
MATERIAL AND METHODS: An immunoenzymatic test INNOTEST HCV Ab IV of Innogenetics was used to evaluate the presence of IgG type antibodies against the Hepatitis C Virus (HCV) in the serum of the patients studied. Results obtained with respect to seroprevalence and other epidemiological variables, were organized and analyzed using SPSS ® 10.0 (Chicago, USA) and Origin Pro ® 7.5 (Northampton, USA) software.
RESULTS: A seroprevalence of 2.63% (19/722) was found, higher than that reported in Venezuela for the general population (0.9%) and other groups. The infection was more frequent in men than in women. The most common symptoms in the infected patients were jaundice and cephalagia (31.58%).
CONCLUSION: The data reported shall update previous research in the zone and indicates the need to develop epidemiological control for Hepatitis C Virus (HCV) in the State of Zulia.
KEY WORDS: Hepatitis C virus (HCV) epidemiology, Venezuela, Seroprevalence.
INTRODUCCIÓN
Actualmente, la hepatitis C es una de las enfermedades virales más frecuentes e importantes a nivel mundial.(1) Su agente etiológico es un flavivirus, el virus de la hepatitis C (VHC), el cual se transmite fundamentalmente por exposición parenteral a productos sanguíneos contaminados. (2, 3)
El principal problema con esta enfermedad reside en que una gran cantidad de los infectados (>85%) desarrolla una infección crónica,(2) la cual genera con frecuencia, a largo plazo, patologías hepáticas de consideración como cirrosis y carcinoma hepatocelular, que pueden hacer necesario un transplante de hígado.(4)
Esa es la razón por la que últimamente esta infección ha llamado la atención de las autoridades de salud y epidemiólogos, los cuales se han trazado como meta encontrar cuanto antes a los pacientes infectados (la mayoría asintomáticos) y ofrecerles tratamiento antiviral, para evitar así una crisis futura por la imposibilidad de abastecer la gran cantidad de transplantes de hígado que serán necesarios si no se frena la diseminación del virus en los próximos años.(5)
En este sentido, es lógico que los estudios de epidemiología y despistaje del VHC cobren cada vez mayor relevancia por colaborar con el propósito anteriormente planteado.
Las investigaciones epidemiológicas referentes al VHC realizadas hasta el momento en Venezuela, así como en muchos países de América Latina, son relativamente escasas (6-9) y además no se ha escrutado la totalidad de los grupos de personas con riesgo de la infección. De allí el interés en realizar el presente trabajo, el cual tuvo como objetivo principal determinar la seroprevalencia del VHC en un grupo de personas de relativo alto riesgo para la infección; específicamente, determinar dicho parámetro epidemiológico en los pacientes que asistieron al Laboratorio Regional de Referencia Virológica (LRRV) de la ciudad de Maracaibo, en Venezuela, entre los años 2000 y 2003, muchos de los cuales presentaron síntomas compatibles con la presencia de hepatitis viral aguda.
El LRRV es un laboratorio especializado donde se realizan pruebas para detectar infecciones por una variedad de virus humanos. A éste acuden pacientes remitidos de diversos centros hospitalarios del estado Zulia, así como personas sin síntomas que requieren el despistaje de estos agentes virales para diversos fines, principalmente laborales.
Se espera que el estudio de las características epidemiológicas de los pacientes infectados por el VHC aquí encontrados constituya una valiosa contribución al entendimiento de la diseminación del VHC en la región, ya que los trabajos anteriores han estudiado poblaciones muy diferentes a la aquí estudiada (como pacientes hemofílicos, hemodializados y donantes entre otros), además de ser necesaria una actualización de la información disponible hasta el momento acerca del tema.(6-9)
MATERIAL Y MÉTODOS
La población de estudio estuvo comprendida por todos los pacientes que acudieron al LRRV (N=722) durante el período comprendido entre el 1 de enero de 2000 y el 31 de diciembre de 2003, con el fin de realizarse pruebas de despistaje para el VHC, independientemente de si presentaban síntomas y signos de hepatitis.
Todos los pacientes fueron entrevistados con el fin de recolectar información epidemiológica como datos personales, síntomas y antecedentes de salud. Todos dieron su consentimiento por escrito para la toma de las muestras sanguíneas.
A cada paciente se le extrajo 5 ml de sangre venosa, en tubos sin anticoagulante. Luego se centrifugó la muestra para obtener el suero, y éste se refrigeró a -20°C hasta su procesamiento.
A cada muestra se le realizó la prueba para la detección de anticuerpos tipo IgG anti VHC, utilizando el análisis inmunoenzimático de cuarta generación Innotest HCV Ab IV de la casa Innogenetics (Gent, Bélgica), siguiendo las instrucciones del fabricante.
A las muestras que resultaron reactivas para el VHC con el Kit Innotest, se les realizó la prueba confirmatoria INNO-LIA HCV Ab III, también de Innogenetics (Gent, Bélgica).
Sólo se reportan como positivas para anticuerpos contra el VHC aquellas muestras que resultaron positivas según los parámetros indicados en el Kit INNO-LIA HCV Ab III.
El análisis estadístico de los datos fue realizado con el Software SPSS Versión 10.0 (Chicago, USA) y el Origin Pro Versión 7.5 (Northampton, USA)
Los resultados se organizaron en tablas de frecuencias y las variables se expresaron en números y porcentajes.
Para las variables cuantitativas se determinaron la media aritmética y la desviación estándar. Para comparar los promedios de edad por sexo, se utilizó la prueba T de igualdad para medias de muestras independientes. Fue considerado como significativo todo valor de probabilidad menor de 0,05.
Por último, se declara que todo el desarrollo de la presente investigación estuvo regido por las normas del código de Bioética y Bioseguridad del Fondo Nacional de Ciencia y Tecnología de la República Bolivariana de Venezuela.(10)
RESULTADOS
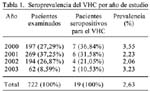
De los 722 pacientes examinados, 19 resultaron positivos según la secuencia de pruebas Innotest HCV Ab IV e INNO-LIA HCV Ab III. La seroprevalencia calculada para el período de estudio fue de 2,63% (19/722). La tabla 1 presenta con detalle la información relativa a la seroprevalencia del VHC por cada año de estudio.
Con respecto a los valores encontrados para otras variables epidemiológicas en el grupo de pacientes seropositivos, se obtuvo que la edad promedio de éstos fue de 48,28 ± 17,86 años, con una edad mínima de 13 años y una máxima de 79 años. En cuanto al género, 11 pacientes fueron hombres (57,89%) y 8 fueron mujeres (42,11%). Al comparar la edad promedio de los hombres seropositivos (38,9 ± 17,23 años) con el promedio de edad de las mujeres seropositivas (60,00 ± 10,50 años) se encontró que los varones presentaron una edad media significativamente menor (P=0,008<0,05). La tabla 2 representa la distribución de los pacientes seropositivos por grupo etario encontrada en la presente investigación.
Por otra parte, los individuos que resultaron positivos para VHC, registraron un promedio de 2,11 ± 3,04 síntomas. Específicamente, la frecuencia de los síntomas en este grupo de pacientes se resume en la tabla 3.
Con respecto a los antecedentes de salud y factores de riesgo para hepatitis viral, a los que declararon haber estado expuestos los individuos seropositivos, se consignó que todos reportaron por lo menos uno de estos antecedentes, estableciéndose un promedio de 1,42 ± 1,31 antecedentes en este grupo de personas, lo cual se muestra en la tabla 4.
Ningún paciente declaró haber usado drogas intravenosas, haberse realizado tatuajes, sufrido accidentes con material médico-quirúrgico contaminado, ni prácticas sexuales homosexuales, los cuales son factores de riesgos importantes y frecuentes vías de transmisión del VHC.(3)
DISCUSIÓN
La seroprevalencia de la infección por el VHC en Sudamérica es baja (<1.9%). (6, 11) Sin embargo, los valores de prevalencia obtenidos en la presente investigación (2,63%), son mayores que los señalados en Venezuela para la población general, (0,9%),(6) y otros grupos de individuos como: Amerindios (2,1%) (6) y Prostitutas (0,5%).(8) También este valor de prevalencia es superior al reportado para la población general y donantes de sangre en varios países de latinoamerica como Colombia (0,97%),(12) Brasil (0,9%), (13) México (1,47%), (14) Cuba (0,9%) (15) y Perú (0,60%).(16)
Este hallazgo reportado inicialmente, podría ser explicado por el hecho de que, apróximadamente, el 60% de las personas que acuden al LRRV solicitando la realización de exámenes de despistaje para hepatitis viral, presentan síntomas compatibles con dicha patología, por lo cual se espera una seroprevalencia mayor del VHC que en la población general y donantes.
Por lo anteriormente señalado, era posible esperar en este trabajo una seroprevalencia similar a los de ciertos grupos de personas con riesgo, tales como hemofílicos, consumidores de drogas intravenosas, y politransfundidos (seroprevalencia >10%). Sin embargo, los valores fueron considerablemente menores.
Al comparar los valores de seroprevalencia por año (ver tabla 1), se observa una tendencia a la disminución por cada año de estudio, debido, quizás, a las mejoras en la implementación de los despistajes contra los virus de hepatitis y otros agentes infecciosos en los bancos de sangre de la ciudad. Recientemente han surgido datos que indican dicha posibilidad.(9)
No obstante, durante el año 2003 se observa un incremento importante de 1,17%, hasta casi igualar la prevalencia del año 2000. No fue posible precisar el origen de dicho aumento. Sin embargo, tomando en cuenta que el número de pacientes examinados en el año 2003 (62 pacientes) declinó sustancialmente (68,04%) con respecto al año anterior, podríamos inferir que el valor de seroprevalencia de ese año pudiese variar si se hubiese examinado una muestra más grande, acercándose posiblemente a los valores de años anteriores.
Todos estos valores de prevalencia obtenidos y su dinámica a lo largo del periodo considerado en esta investigación, son indicativos indirectos de una baja tasa de infección por el VHC en la región. A pesar de que en la población estudiada el 60% de sus integrantes presentaban algún síntoma de hepatitis, i.e. ictericia, dolor abdominal, etc., en ningún caso los valores de seroprevalencia llegaron al 4% y presentaron una marcada tendencia a bajar con la edad (ver tabla 2).
El VHC se presentó con mayor frecuencia en pacientes del sexo masculino, al igual que en USA,(17) Perú (18) y Cuba. (19) También se observó que los pacientes masculinos registraron una edad promedio menor que las mujeres infectadas. Esto podría estar relacionado con el hecho de que la enfermedad hepática posterior a la infección se desarrolla con mayor celeridad en hombres que en mujeres;(20) los síntomas de deterioro progresivo del hígado aparecen primero en este grupo, motivándolos a recurrir al médico y por ende, a detectársele la infección, a una edad más temprana.
De igual manera, el grupo etario que presentó mayor prevalencia fue el correspondiente a 40-49 años, seguido por el grupo inmediato superior (50-59 años). La literatura refiere que el VHC a nivel mundial infecta principalmente a personas sobre los 30 años.(21) Sin embargo, se pueden observar algunas variaciones al respecto según la zona geográfica. En USA, por ejemplo, el grupo etario con mayor prevalencia es el de 30-39 años de edad;(17) en Bélgica, es el de 50-57 años (22) y en Australia es el de 20-29 años.(23)
Es interesante observar que ningún paciente seropositivo se encontró en el grupo de edad de 20-29 años, quizás ocasionado por la baja prevalencia en el uso de drogas intravenosas en latinoamerica,(12) ya que en otras zonas geográficas los principales consumidores de este tipo de droga pertenecen a este grupo etario.
La frecuencia de los síntomas en los pacientes seropositivos se resume en la tabla 3. Como se puede apreciar, menos del 33% de los pacientes presentó los sintomas clásicos de Hepatitis (Ictericia, Decaimiento, Náuseas, Dolor abdominal). La ausencia de síntomas a corto y mediano plazo después de la primoinfección es una característica típica de la infección por el VHC.(4, 24)
Es dificil diagnosticar una hepatitis aguda antes de la aparición de ictericia, por lo que no es de extrañar que éste sea el síntoma de mayor frecuencia reportado en este estudio. Sin embargo, la presencia de ictericia, no es un marcador inequívoco de infección aguda por el VHC, (25) sólo la demostración de seroconversión puede corroborar una etapa aguda en un paciente. (25, 26)
Debido a que ninguno de los pacientes infectados que refirieron ictericia tenían una muestra de suero anterior que demostrase su seronegatividad, no se puede concluir que presentaban una infección aguda por VHC.
Recientemente, se han desarrollados técnicas basadas en la avidez de los anticuerpos tipo IgG contra el VHC, que pueden determinar, con buena aproximación, la antigüedad de la infección por este virus,(25, 26) por lo que sería recomendable su aplicación para precisar este dato en los pacientes con aparente infección aguda.
Hay que recalcar que sólo dos pacientes se realizaron los exámenes para determinación de los niveles de bilirrubina y aminotransferasas, y en ambos resultaron elevados. Muy probablemente en los restantes 17 se hubiesen encontrado valores por encima de los normal en estos dos rubros, si se hubiesen llevado a cabo las pruebas respectivas.
Con respecto a los factores de riesgo a los que declararon haber estados expuestos los individuos seropositivos (ver tabla 4), es notoria la alta frecuencia de transfusiones (57,89%), las cuales, al constituir el medio principal de transmisión del VHC en Venezuela,(6) pudiese ser la vía mas probable por la cual se infectaron estos pacientes.
Todos los pacientes que manifestaron haber sido sometidos a tratamiento con acupuntura también declararon haber sido transfundidos, lo que dificultó la identificación de la vía de contagio del VHC. Esto sirve de alerta sobre posibles riesgos epidemiológicos en la región zuliana por la transmisión de este virus a través de estas prácticas médicas.
Se puede concluir que a pesar de la alta seroprevalencia registrada en el presente estudio (2,63%) en relación con la reportada recientemente para Venezuela (0,9%),(6) los valores del resto de los indicadores epidemiológicos estudiados, tales como edad, sexo, síntomas y factores de riesgo de la personas infectadas, se corresponden con lo señalado en la literatura internacional. Además, por haberse estudiado aquí una población con características distintas a las ya examinadas en otros trabajos, la presente investigación será de utilidad para completar el estudio de la epidemiología del VHC en todos los grupos de personas con riesgo de infección en Venezuela.
Es difícil encontrar un estudio parecido al presente, por lo menos en la región latinoamericana. Las poblaciones analizadas en diferentes investigaciones de la región son generalmente donantes de sangre, población general o grupos de personas de alto riesgo, cuyos valores de seroprevalencia distan mucho de los aquí presentados.(6-9) Se recomienda la realización de más investigaciones en laboratorios de referencia ó clínicos, a donde acudan gran cantidad de personas con alguna sintomatología compatible con hepatitis, para determinar la participación del VHC en este grupo de personas.
REFERENCIAS BIBLIOGRÁFICAS
1. TERRÉS-SPEZIALE AM. Hepatitis C. Historia natural y estado actual de su manejo. Rev Mex Patol Clin. 2003;50(4):179-189. [ Links ]
2. LAUER GM, WALKER BD. Hepatitis C virus infection. N Engl J Med. 2001;345(1):41-52. [ Links ]
3. BONKOVSKY HL, MEHTA S. Hepatitis C: a review and update. J Am Acad Dermatol. 2001;44(2):159-82. [ Links ]
4. MANDELL GL, DOUGLAS RG, BENNETT JE, DOLIN R. MANDELL. DOUGLAS, and BENNETTS principles and practice of infectious diseases. 5th edition [ CD-ROM ]. Philadelphia: Churchill Livingstone; 2000.
5. STEPHENSON P. Hepatitis C carriers must be found and treated to avert crisis. BMJ 2004; 328: 1031. [ Links ]
6. AGUILAR MS, COSSON C, LOUREIRO CL et al. Prevalence of infection with hepatitis C virus in Venezuela, as assessed with an immuno-assay based on synthetic peptides. Ann Trop Med Parasitol. 2001;95(2):187-95. [ Links ]
7. ARTEAGA-VIZCAINO M, BLITZ-DORFMAN L, ECHEVERRIA JM et al. Hepatitis C in hemophiliac patients in Maracaibo, Venezuela. Invest Clin. 1993;34(3):113-8. [ Links ]
8. CAMEJO MI, MATA G, DIAZ M. Prevalence of hepatitis B, hepatitis C and syphilis in female sex workers in Venezuela. Rev Saude Publica. 2003;37(3):339-44. [ Links ]
9. MONSALVE-CASTILLO F, GOMEZ-GAMBOA L. Hepatitis C virus. Iatrogenic and nosocomial transmition?. Invest Clin. 2004;45(3):193-5. [ Links ]
10. Fondo Nacional de Ciencia y Tecnología. Código de Bioética y Bioseguridad. 2002 [ cited 25/11/2004 ] ; 2da edición Available from: http://www.conicit.gov.ve /bioetica.htm [ Links ]
11. World Health Organization. Global distribution of hepatitis A, B and C 2001. Weekly Epidemiological Record. 2002;77(6):45-47. [ Links ]
12. HOYOS A, VANEGAS N, PÁEZ E. Epidemiología de la hepatitis C en Colombia. Acta Med Colomb. 2002;27(4):209-217. [ Links ]
13. PALTANIN LF, REICHE EM. Seroprevalence of anti-hepatitis C virus antibodies among blood donors, Brazil. Rev Saude Publica. 2002;36(4):393-9. [ Links ]
14. URIBE M, MENDEZ-SANCHEZ N. Hepatitis C in Mexico. Rev Gastroenterol Mex. 2002;67 Suppl 2:S7-8. [ Links ]
15. SABINA M, GARCÍA F, ASCONEGUI A, MARTINEZ O. Características epidemiológicas de la hepatitis C en donantes de sangre. Rev Cubana Hig Epidemiol. 2002;40(3):279-293 [ Links ]
16. FARFAN G, CABEZAS C. Prevalence of viral hepatitis type C in blood donors in Peru. Rev Gastroenterol Perú 2003;23(3):171-6. [ Links ]
17. ALTER MJ. Hepatitis C virus infection in the United States. J Hepatol. 1999; 31 Suppl 1:88-91. [ Links ]
18. PINTO VALDIVIA JL, VIDAL ESCUDERO J, BUSSALLEU A et al. Hepatitis C virus infection in blood bank donors at the Hospital Nacional Cayetano Heredia (1998 - 2002). Rev Gastroenterol Perú 2003; 23(1): 22-8. [ Links ]
19. VILAR E, GRÁ B, LLANIO R, ARÚS E. Influencia de factores epidemiológicos en la progresión de la fibrosis en la hepatitis crónica C. Rev Cubana Med. 2003 42(5):0-0 [ Links ]
20. RAMOS-GÓMEZ M. Natural history of chronic hepatitis C. Rev Gastroenterol Mex. 2002;67 Suppl 2:S17-20. [ Links ]
21. World Health Organization. Hepatitis C Fact sheet. 2000 [ cited 26/11/2004 ] Fact sheet N°164: Available from: http://www.who.int/mediacentre/factsheets /fs164/en/print.html [ Links ]
22. BEUTELS M, VAN DAMME P, AELVOET W et al. Prevalence of hepatitis A, B and C in the Flemish population. Eur J Epidemiol. 1997;13(3):275-80. [ Links ]
23. CROFT N, THOMPSON S, KALDOR J. Epidemiology of the hepatitis C virus. 1st edition. Canberra: Communicable Diseases Network Australia and New Zealand; 1999. [ Links ]
24. FELDMAN M, FRIEDMAN LS, SLEISENGER MH. SLEISENGER & FORDTRANS gastrointestinal and liver disease: pathophysiology, diagnosis, management. 7th edition [ CD-ROM ] Philadelphia: Saunders; 2002. [ Links ]
25. LEÓN P, LOPEZ JA, DE ORY F et al. Detection of low- avidity IgG antibodies in the diagnosis of primary acute infection by hepatitis C virus. Enferm Infecc Microbiol Clin 1997;15(1):14-8. [ Links ]
26. KANNO A, KAZUYAMA Y. Immunoglobulin G antibody avidity assay for serodiagnosis of hepatitis C virus infection. J Med Virol 2002;68(2):229-33. [ Links ]