Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.25 n.4 Lima oct./dic. 2005
TRABAJOS ORIGINALES
Ciclosporosis: una parasitosis emergente (I). Aspectos clínicos y epidemiológicos
Sonia Burstein Alva1
1 Profesor Principal de la Facultad de Medicina de la Universidad Nacional Mayor de San Marcos. Lima, Perú.
RESUMEN Objetivo: Determinar la prevalencia de Cyclospora cayetanensis en pacientes sintomáticos que acudieron a la consulta médica y en pobladores que habitan en asentamientos que rodean a la ciudad de Lima, Perú.
Material y métodos: La población completa estuvo compuesta por 3,259 personas: 2,968 entre 1 mes y 87 años de edad, que acudieron a un laboratorio de atención privada por presentar trastornos digestivos, principalmente diarreas y el segundo por 291 pobladores de áreas periféricas, denominadas conos, de 5 meses a 75 años, aparentemente sanos. Se investigó la presencia de Cyclospora mediante técnicas microscópicas «en fresco» con solución salina y lugol y se empleó una nueva técnica de coloración descrita en otra publicación. Se hizo una ficha consignando los datos clínicos y epidemiológicos, que se evaluaron estadísticamente.
Resultados: En el primer grupo la incidencia de Cyclospora fue de 7.3% y en el segundo 41.6% observándose con más frecuencia en adultos jóvenes y mayores, hasta los 60 años. No se encontró mayor incidencia estacional. Las manifestaciones clínicas de los pacientes que acudieron al laboratorio fueron mayormente diarrea y dolor abdominal, mientras que las personas que provenían de los conos, presentaron principalmente gases, dolor abdominal, diarreas ocasionales y síntomas generales, como cansancio y adelgazamiento.
Conclusiones: La Cyclospora mostró una elevada incidencia, especialmente en los conos. Se encontraron dos tipos de manifestaciones clínicas: una aguda, muy severa que puede llevar a la deshidratación, otra crónica con diversas manifestaciones digestivas, principalmente gases y dolor abdominal. Los pacientes que acuden a la consulta médica presentan cuadros agudos y crónicos, mientras que los que habitan en los conos, sí presentan patología ésta es de tipo crónico. Aparentemente los pacientes que presentan cuadros agudos están inmunológicamente expuestos al parásito, pero no se inmunizan posteriormente a pesar de recibir tratamiento ya que pueden reinfectarse una y otra vez. En cambio, los que presentan cuadros crónicos, parece que mantuvieran un equilibrio huésped-parásito, al estar en contacto permanente con él. Aparentemente la fuente de contaminación es el agua, por tanto se deben tomar las medidas epidemiológicas necesarias para evitar que este problema alcance mayores proporciones.
PALABRAS CLAVE: Cyclospora cayetanensis; prevalencia; aspectos clínicos; epidemiología; Lima,Perú.
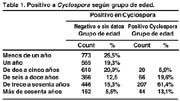
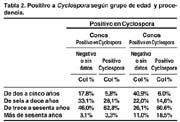
SUMMARY Purpose: Determine the prevalence of Cyclospora cayetanensis in asymptomatic patients consulting a physician, or dwellers of marginal urban settlements surrounding Lima, Peru. INTRODUCCIÓN La Cyclospora es un parásito emergente, que puede producir trastornos digestivos agudos o crónicos. Puede encontrarse tanto en pacientes inmunocompetentes nativos o viajeros como en inmunodeprimidos (VIH), en los que el proceso es más severo y prolongado. La elevada frecuencia con que se encuentra últimamente y la diversidad de cuadros clínicos que produce, nos obliga a hacer un diagnóstico de laboratorio rápido y preciso para poder indicar el tratamiento adecuado. El síntoma más importante es la diarrea, que tiene carácter explosivo. Puede ser líquida o pastosa y en número de 4 a 6 al día, pudiendo llevar a la deshidratación. Se acompaña de distensión abdominal, gases, náuseas, vómitos, dolor tipo cólico, y eventualmente febrícula y mialgias. Se puede presentar decaimiento marcado, anorexia y disminución de peso. En algunos pacientes inmunocompetentes, el cuadro puede autolimitarse después de algunos días o semanas, pero en otros, así como en los inmunodeprimidos, se presentan molestias digestivas persistentes, con períodos de diarrea o estreñimiento, cefalea y flatulencia, pudiendo confundirse con otras parasitosis, con colon irritable u otros trastornos funcionales. En 1979, este cuadro fue catalogado como una nueva parasitosis por Ashford (1), un parasitólogo inglés, que detectó en 3 casos de diarrea en pacientes de Papua-Guinea, unas formas esféricas que no había observado anteriormente. Fue el primero en relacionarlo con un coccidio, «no descrito». Posteriormente entre 1983 y 1986, Soave, en Haiti, descubrió en las heces de pacientes con VIH un organismo ácido-resistente cuyo tamaño era intermedio entre el Cryptosporidium y la Isospora belli, denominándolo Crypto-gigante (2). En nuestro medio, desde 1985, el Dr. Jorge Naranjo del laboratorio de parasitología de la Universidad Peruana Cayetano Heredia, había observado estos microorganismos y los describía como objetos similares al Cryptococcus muris, (3). Muy pocas referencias aparecen durante este período, hasta 1990 en que Long, después de haberlo observado en diarrea del viajero y personas con VIH, lo catalogó como «cyanobacterium-like» o «coccidian-like body» (CLB) (4,5), nombre con el que fue designado por varios investigadores (6,7). Así mismo Hoge, en un estudio epidemiológico en Nepal, lo describió como un microorganismo similar a un coccidio, (8). Finalmente en l993, Ortega y colaboradores estudiando cepas remitidas del Perú, lograron clasificar al nuevo parásito como un coccidio del género Cyclospora (9) y debido a que en la Universidad Peruana Cayetano Heredia, se efectuaron los estudios pertinentes, este nuevo coccidio recibió la denominación de Cyclospora cayetanensis (10). Durante la década de los 90, aparecen una serie de publicaciones sobre la incidencia y epidemiología de este parásito. Se demuestra que afecta a niños y a adultos tanto inmunocompetentes como inmunodeprimidos (11). Su distribución es mundial pero existen países donde es endémico, como Nepal (12), Haití (13) y Perú (14). En otros lugares aparece en forma aislada, generalmente en sujetos que han viajado a zonas endémicas y en muy raras ocasiones, como formas nativas. En l997 reportan un caso en Chile (15). En 2002, en Costa Rica (16) se menciona el hallazgo de 2 casos y en Cuba, reportan una incidencia de 0.2% de pacientes con ciclosporosis, en un período de 21 meses (17). En Turquía, el 2003 se reporta el primer paciente de ciclosporosis autóctona (18), y en el 2004, los australianos describen su primer caso en un paciente que había viajado a Bali (19). En los países desarrollados como Estados Unidos y Canadá, la ciclosporosis se presenta como episodios epidémicos bien definidos. El primer brote reportado por Huang en 1995 (20) en un hospital de Chicago, comprometió a personal médico y auxiliar y se relacionó con agua estancada en un tanque que había sufrido una avería en el sistema de bombeo. Posteriormente se han descrito más de 10 brotes epidémicos en eventos científicos o sociales que fueron relacionados con la ingesta de alimentos frescos, frutas como fresas o frambuesas, o distintos tipos de vegetales verdes como lechugas o albahaca, que se consumen crudos y que fueron importados de Guatemala, Perú u otros lugares endémicos (21-22). En los últimos años se siguen reportando casos aislados o brotes epidémicos en diferentes partes del mundo. Inclusive preocupa a los europeos la escasa incidencia que encuentran, cuestionándose en un Eurosurveillance Report, si ellos están investigando adecuadamente la presencia de Cyclospora. La infestación de los pacientes se debe a la ingesta de agua o alimentos contaminados con heces portadoras de ooquistes de cyclospora (23). Se ha podido demostrar mediante técnicas microscópicas y moleculares, la existencia de ooquistes en el agua que se utiliza para consumo humano o en el regadío de vegetales y frutas (24). Aparentemente el hombre es el único reservorio de los ooquistes, que hasta el momento no han podido ser inoculados en animales de laboratorio. No existe evidencia de infección en animales domésticos o salvajes (25). Sin embargo Zerpa (26) en un estudio realizado en el Perú, identificó el microorganismo en 3 pacientes con diarrea y en las heces de un animal doméstico que convivía con ellos. El diagnóstico de cyclospora se efectúa mediante la observación microscópica de las heces por exámenes «en fresco» y coloraciones especiales. El tratamiento indicado es el empleo de trimetoprim-sulfametoxazole (160 mg – 800 mg), 2 veces al día, durante 7 días. En casos de recidiva, se repite otra serie de 7 días y si se comprueba que el paciente sigue eliminando ooquistes en las heces, especialmente en el caso de pacientes inmunodeprimidos que presentan los cuadros más severos y rebeldes, se indica un tratamiento de mantenimiento de 3 días a la semana por 3 a 4 meses (27). A pesar que se considera esta asociación quimioterápica como el único tratamiento adecuado, actualmente se está utilizando ciprofloxacina (500 mg), 2 veces al día y por el mismo período de tiempo, como una droga alternativa en pacientes intolerantes al cotrimoxazol (28). El objetivo del presente trabajo es determinar la prevalencia de cyclospora en dos grupos humanos: el primero conformado por pacientes que fueron estudiados en un laboratorio de atención particular y el segundo por pobladores de asentamientos humanos periféricos. Asimismo, evaluar las manifestaciones clínicas en ambos grupos y las implicancias epidemiológicas. MATERIAL Y MÉTODOS Se investigó la presencia de Cyclospora cayetanensis en las heces de una población compuesta por 3,259 personas que se clasificaron en seis grupos de edad, el más numeroso de los cuales fue el de menores de un año y el menor, el de mayores de sesenta años. El estudio se efectuó en dos grupos humanos: el primero estuvo constituido por 2,968 pacientes cuyas edades fluctuaron entre 1 mes y 87 años de edad. Estos pacientes fueron remitidos por el clínico tratante por presentar síntomas digestivos diversos, principalmente diarrea. El segundo grupo estuvo constituido por 291 pobladores de tres asentamientos humanos ubicados en Tablada de Lurín (cono Sur), Ventanilla (cono Norte) y Flor de Amancaes (Rímac), cuyas edades fluctuaron entre 5 meses y 75 años. Fueron elegidos al azar, encontrándose aparentemente sanos. A todos se les practicó examen copro-parasitológico completo y se les hizo una ficha clínica donde se consignaron los datos personales, las manifestaciones clínicas generales y los trastornos digestivos específicos. Las muestras fueron estudiadas en la ciudad de Lima, Perú, en un laboratorio de microbiología de atención privada, entre enero de 2002 y diciembre de 2004. Para la investigación de la Cyclospora se emplearon las técnicas microscópicas en fresco y una nueva coloración que se describe en la segunda parte de esta comunicación. Debemos señalar que muchas veces es necesario hacer un muestreo seriado para poder hacer el hallazgo del parásito. En la evaluación estadística se emplearon los siguientes procedimientos: - Estadística descriptiva para determinar la incidencia de Cyclospora por grupo de pacientes y edad. - Análisis de tablas cruzadas (crosstaps) y pruebas chi-cuadrado para determinar la independencia entre variables. - Medidas de correlación no paramétricas para determinar la asociación entre las variables de estudio. - Análisis de varianza para comprobar la incidencia diversa de cyclospora por grupos de edad. - Análisis factorial de los síntomas para determinar su estructura interna general y según procedencia. - Análisis discriminante para comparar las diferencias del perfil de síntomas en las poblaciones. RESULTADOS De los 2968 pacientes que se atendieron en el laboratorio durante 3 años, la prevalencia de ciclosporosis fue del 7.3% mientras que en los 291 pobladores escogidos aleatoriamente durante los últimos 6 meses en tres asentamientos humanos de los llamados conos que rodean a la ciudad de Lima, la incidencia fue de 41.6%. La distribución por edades, se aprecia en las Tablas 1 y 2. En la primera se presentan los casos positivos a Cyclospora en la población total. La Tabla 1 permite apreciar que no hay presencia de análisis positivos en los grupos de un año y menos de un año, por lo que los siguientes análisis estadísticos se realizaron excluyendo dichos segmentos. La Tabla 2, permite apreciar que la distribución por edades de los casos positivos de los conos y del laboratorio, sigue un patrón marcadamente creciente hasta los sesenta años en ambos grupos, para decrecer luego de dicha edad (el descenso es más fuerte en el caso de los pacientes de los conos). Los grupos de edades de los pacientes con resultado negativo, no siguen el mismo patrón. Para analizar si la presencia de Cyclospora está asociada a la edad, se aplicó el test Chi-cuadrado, que indicó que ambas variables se encuentran asociadas con significatividad estadística. Los análisis para mostrar la dirección de la asociación muestran que esta es positiva, es decir que la incidencia tiende a aumentar conforme aumenta la edad de las personas. Los coeficientes de asociación se pueden considerar moderados (pese a que alcanzan significatividad estadística), lo que puede deberse a la disminución porcentual de los pacientes positivos a Cyclospora en el grupo de mayor edad. (Recordar que este análisis no incluye a los dos grupos de menor edad porque en ellos no hay casos positivos. Sin embargo esto abonaría todavía más a favor de la hipótesis). Los exámenes efectuados para verificar la relación entre la edad y la presencia de Cyclospora según el grupo de procedencia, muestra que ésta está más fuertemente asociada en el caso del laboratorio que en el de la población general y en los conos, donde se distribuye más uniformemente entre los diferentes grupos de edad. Como una forma de control, se dirigió un análisis adicional para determinar si hay relación entre el sexo del paciente y la presencia de Cyclospora. Los resultados negativo tanto para la población completa como para cada uno de los pobladores de los conos y cada uno de los grupos de edad. Tal como se indicó antes, la incidencia de Cyclospora fue significativamente mayor en los conos que en el laboratorio. En cuanto a la frecuencia de ciclosporosis de acuerdo a los meses del año, no existe una mayor incidencia estacional. Hemos encontrado el parásito en todos los meses del año, con variaciones que no revisten mayor significación. En la Figura 1, analizamos los síntomas de tipo digestivo y las manifestaciones clínicas generales de los pacientes con Cyclospora. La molestia digestiva más importante fue la diarrea que se presentó en el 69.9% de pacientes que acudieron a solicitar atención especializada. En cambio los pacientes de los asentamientos humanos sólo manifestaron diarreas esporádicas en el 35.5% de los casos. La mayor parte de estos pacientes manifestó presencia de gases (65.3%)), dolor abdominal (59.5%) y síntomas generales como astenia (52.1%), cefalea (40.5%), anorexia (24%) y adelgazamiento (30.6%). Los síntomas fueron estadísticamente sometidos a un análisis factorial que se presentan en las Figuras 2 y 3, donde se aprecia que ambos muestran variaciones de una población a otra. Por ejemplo en el caso del laboratorio podemos apreciar que la diarrea se asocia más a los vómitos y a la fiebre, mientras que en los conos no se une a un grupo determinado. Finalmente se dirigió un análisis discriminante para determinar si los síntomas registrados entre los casos positivos, permiten afirmar que hay perfiles distintos en los conos y en el laboratorio. Los resultados muestran que el análisis es positivo: los pacientes de cada procedencia forman grupos naturales con características muy diferenciadas entre sí. La función discriminante hallada fue suficiente para calificar correctamente al 66% de los pacientes procedentes de los conos, así como a más del 94% de los pacientes procedentes del laboratorio. Esta diferencia significa que un grupo de pacientes de los conos puede tener síntomas parecidos a los pacientes del laboratorio. Los conos se asocian más a las variables: cansancio, gases, dolor abdominal, cefalea y adelgazamiento. DISCUSIÓN Esta comunicación tiene como objetivo demostrar la elevada prevalencia de Cyclospora cayetanensis que se presenta en nuestro medio. Llama la atención que a pesar que este parásito se ha descrito hace ya más de una década y que fue inicialmente investigado en una universidad de Lima, motivo por el cual lleva su nombre, rara vez es reportado en los laboratorios microbiológicos particulares o del sector salud. La explicación de esta deficiencia puede ser atribuida a la escasa información de su existencia, ya sea por falta de conocimiento por parte de los clínicos como de los laboratoristas, que al hacer el examen microscópico, no reparan en su existencia o lo confunden con otros parásitos. La literatura sin embargo, es extensa y a pesar que el Perú es considerado como un país donde la ciclosporosis es endémica, los reportes locales son escasos y están mayormente vinculados con investigaciones publicadas en el extranjero y muy poco difundidas en nuestro medio. Tres factores que contribuyen a diagnosticar erróneamente esta parasitosis son: en primer lugar la tendencia del proceso a autolimitarse lo cual hace que el paciente no solicite atención médica hasta que el cuadro clínico recidive o pase a la cronicidad; en segundo lugar, la costumbre tan arraigada de administrar terapia tentativa, especialmente en los casos agudos que simulan cuadros bacterianos; y en tercer lugar, el hábito tan difundido de los pacientes de recurrir a las farmacias a buscar ayuda terapéutica empírica. Generalmente se les prescribe cotrimoxazol o quinolonas que administradas adecuadamente podrían ser efectivas contra un proceso cuya etiología se desconoce, pero en el caso de la ciclosporosis, si el tratamiento es insuficiente, el paciente presentará un cuadro recurrente de tipo crónico y difícil de catalogar. El hallazgo frecuente de Cyclospora cayetanensis nos llevó a investigar la prevalencia de este parásito en diversos grupos humanos. El primer grupo estudiado en nuestro laboratorio en el lapso de 3 años, incluyó 2,968 pacientes de diferentes edades y arrojó una incidencia de ciclosporosis del 7.3%. En el laboratorio, recibimos muchas muestras de niños, especialmente lactantes. A pesar que algunos informes reportan casos de esta parasitosis en niños muy pequeños, no hemos observado ninguno por debajo de 1 año (Tabla1), así es que para tener una cifra más real, hemos excluido a estos pacientes obteniendo así, una incidencia de 9.87%. Este porcentaje tan alto, es similar al obtenido en Nepal en viajeros o residentes extranjeros (8) y en Haití, en pacientes con VIH (13). Inicialmente el parásito sólo se observó en adultos y niños mayores, pero posteriormente también se hizo el hallazgo en niños menores. Estudios realizados hace varios años en poblados rurales cerca a Lima, (10,14), muestran una incidencia de Cyclospora muy diferente a la nuestra, respecto a la edad. Ellos estudiaron poblaciones de niños de 0 meses a 4 años, encontrando una incidencia relativamente elevada en esa población y ninguna en niños hasta los 15 años, o en adultos. La explicación podría estar en cambios epidemiológicos que podrían haber ocurrido en este período de tiempo. Al laboratorio llega una población de clase media y alta, que generalmente procede de zonas céntricas de Lima y urbanizaciones con un nivel socio-económico más elevado, lo cual presupone buenas condiciones sanitarias. Este hecho nos llevó a investigar qué pasa en los conos, o sea los asentamientos humanos que rodean a la ciudad de Lima, ya que los primeros trabajos que sirvieron para estudiar este parásito, fueron realizados en uno de estos centros poblados (14,29). Así, pudimos investigar la presencia de Cyclospora en 291 personas de diferentes edades, elegidas aleatoriamente. La incidencia fue muy elevada: 41.6%, llegando en uno de ellos hasta el 50%. No hemos podido apreciar mayor diferencia estacional como se describe en otros países donde la ciclosporosis es endémica; se ha observado en todos los meses del año, lo cual se explicaría porque nuestro clima no sufre modificaciones significativas en las diferentes estaciones La prevalencia por grupos de edad y procedencia demostró tanto en los pacientes que acudieron al laboratorio como en los que provenían de los conos, que la ciclosporosis es más frecuente entre los 12 y 50 años (Tablas 1 y 2), lo cual indicaría una mayor posibilidad de contaminarse con el parásito, en dicho período. Es muy interesante estudiar las manifestaciones clínicas en ambos grupos. La mayor parte de los pacientes que acudieron al laboratorio, tenían una elevada incidencia de diarrea líquida y explosiva, problema que indudablemente los había llevado a la consulta (Figura 1). Otros presentaron cuadros larvados, con manifestaciones esporádicas de diarrea, presencia de balonamiento abdominal y gases. En cambio los pacientes procedentes de los conos manifestaron tener diarreas eventuales y lo que más primaba en ellos fueron trastornos digestivos funcionales de tipo crónico, gases y dolor abdominal. Asimismo presencia de síntomas generales: astenia, cefalea, anorexia y pérdida de peso. Muchos refirieron ausencia total de síntomas, pero con antecedentes de diarrea que había cedido espontáneamente. Si estudiamos las diferentes manifestaciones clínicas que presentan los pacientes con ciclosporosis, podemos afirmar, refrendados por los estudios estadísticos (Figuras 2 y 3), que en realidad no hay mucha diferencia en los síntomas que presentan los pacientes que acuden al laboratorio y los pobladores de los conos. En general podemos decir que estamos frente a dos tipos de manifestaciones: un cuadro agudo, que se caracteriza principalmente por diarreas líquidas y otro crónico donde priman manifestaciones digestivas diversas y síntomas generales. Los pacientes que acuden al consultorio, presentan cuadros agudos y crónicos, en cambio los que vemos en los conos tienen en su mayoría cuadros crónicos y también están enfermos. Estas últimas manifestaciones generalmente se presentan cuando el paciente ha tenido un cuadro agudo que se autolimitó o recibió un tratamiento insuficiente. Hemos tenido la oportunidad de controlar 74 pacientes después de un primer episodio de ciclosporosis, que fue tratado. De ellos, 59 procedían del consultorio y 15 de los conos. Los pacientes del consultorio tuvieron un comportamiento variable: 39 tuvieron controles negativos después del tratamiento, en períodos que variaron de 1 a 6 meses, en cambio 20 presentaron recurrencias. De ellos en 8 casos hubo alternancia de controles positivos y negativos, en períodos que oscilaron entre 3 meses y un año y en 12, todos los controles fueron positivos, a pesar de recibir tratamiento en cada episodio. Este último comportamiento fue similar al de los 15 pobladores de los conos, que tuvieron controles persistentemente positivos a cyclospora, a pesar de la terapia que fue administrada por nosotros en un plan piloto. Cuando analizamos los síntomas de estos pacientes, podemos observar que la mayor parte que tuvieron cuadros agudos, no recurrieron, en cambio es probable que los pacientes que tuvieron alternancia de positivos y negativos, se hayan reinfectado. El grupo que permaneció persistentemente infectado, al igual que en los conos, podría estar en contacto permanente con el parásito y recidivar constantemente. Podríamos decir que los pacientes que hacen cuadros agudos y severos, están inmunológicamente expuestos a la acción patógena del parásito al no estar en contacto permanente con él. Sin embargo después de sufrir ese episodio no adquieren inmunidad, ya que al recibir tratamiento y dejar de eliminar parásitos en sus heces, pueden reinfectarse posteriormente una y otra vez, siempre con síntomas agudos. En cambio los pacientes que son asintomáticos o tienen cuadros crónicos o larvados, están en un aparente estado de equilibrio paciente-parásito o adquieren cierta inmunidad al estar en contacto permanente con éste, lo cual explica su elevada incidencia en los conos. Estos pacientes se comportan como portadores y aunque eventualmente pueden hacer cuadros agudos, generalmente presentan sintomatología discreta o ausente. Esta situación también ha sido observada en Haití (30) y Venezuela (31), donde se describe que a pesar que la incidencia de Cyclospora es elevada, los cuadros agudos de diarrea y malestar general son poco frecuentes. Se sabe que la Cyclospora es un coccidio que puede permanecer en forma quística durante mucho tiempo en el medio ambiente. Para adquirir rol patógeno debe madurar o sea pasar por un proceso de esporulación y exquistación. Una vez ingerida y atacada por el ácido gástrico del estómago, se liberan dos esporoquistes y dos esporozoítos, elementos infectantes que penetran en las células epiteliales del intestino delgado, multiplicándose asexualmente y posteriormente por reproducción sexual, producen quistes inmaduros que se eliminan por las heces y que aparentemente no tienen rol patógeno hasta que vuelven a esporular (32,33). Mientras parasitan el intestino delgado producen lesión de la mucosa y se originan diarreas líquidas profusas que no se acompañan de reacción inflamatoria. Como ya se ha descrito los ooquistes inmaduros, después de ser eliminados por las heces permanecen en el medio ambiente, principalmente en el agua hasta su esporulación, pudiendo contaminar los vegetales y frutas cuando se utiliza como agua de regadío o para diluir los insecticidas que se aplican a las plantas (24). La fuente de contaminación en nuestro medio es aparentemente el agua, lo cual explica por qué los niños menores de un año, no la adquieren. A pesar que todos los asentamientos humanos que hemos estudiado cuentan con agua potable, está demostrado que la Cyclospora es muy resistente, tolera la clorinación del agua y el lavado simple de verduras y frutas que se consumen crudas, causando brotes epidémicos si estos productos son exportados a países desarrollados, o consumidos por nativos expuestos. Aparentemente el agua en Lima, ciudad, no se encuentra contaminada, sin embargo un alto porcentaje de pacientes hace cuadros agudos de ciclosporosis, cuyas causas se desconocen. Todavía no está bien determinado el tiempo de incubación. A pesar que se sostiene que los ooquistes demoran entre 7 y 14 días para esporular, muchos pacientes relacionan su cuadro con la ingesta reciente de mariscos o pescado, e inicialmente nosotros lo vinculábamos a la época de veraneo en las playas atribuyéndolo a la contaminación del mar con aguas servidas, pero ahora el problema no sólo se da en el verano sino en cualquier época del año. Podríamos elucubrar que los habitantes de los conos o asentamientos humanos que rodean Lima como un cinturón, podrían comportarse como fuente de contaminación, ya que muchos de ellos trabajan o expenden sus productos en la capital. No existen todavía modelos experimentales que permitan determinar la susceptibilidad del huésped ni las características biológicas del parásito que expliquen su virulencia y su supervivencia. Inclusive en un trabajo piloto presentado en Abril del 2004 (Emerging Infection Diseases), se trató de infectar a 7 voluntarios controlados clínica y microbiológicamente, con esporozoitos extraídos experimentalmente en el laboratorio y ninguno hizo manifestaciones clínicas ni fue posible recuperar ooquistes de sus heces durante las 16 semanas que estuvieron en control.En cuanto al tratamiento, hemos observado que los pacientes con cuadros agudos de diarrea y malestar general, se alivian rápidamente con el tratamiento específico. Los pacientes con cuadros crónicos también se benefician con la terapia, pero pueden recurrir si están en contacto permanente con el parásito. Estamos pues frente a un parásito enigmático que es necesario tomar en cuenta, no sólo desde el punto de vista clínico sino epidemiológico. Si bien es cierto que no produce mortalidad, aunque en los casos agudos puede llevar a una deshidratación severa, causa muchas molestias que pueden ser manejadas desde el punto de vista terapéutico. Por ello insistimos que la investigación de Cyclospora cayetanensis, sea incluida rutinariamente en los exámenes de heces empleando las técnicas presentadas por nosotros, que como volvemos a insistir son simples, rápidas y económicas, pudiendo implementarse en cualquier laboratorio de rutina. Por otro lado invocamos a los centros de Epidemiología y Salud Pública, que tomen las medidas necesarias para investigar la prevalencia de este parásito en otros departamentos del país ya que varios pacientes procedían de otras localidades, especialmente de la sierra, e incentivar a la población afectada para que tome las precauciones necesarias: hirviendo el agua y pelando o cocinando las frutas y verduras, para evitar que este problema alcance mayores proporciones, porque a pesar que sabemos que estamos en un país donde la ciclosporosis es endémica, nunca imaginamos su verdadera magnitud. AGRADECIMIENTOS: Al Dr. César Náquira Velarde, Director del Instituto Nacional de Salud (INS), por la revisión del trabajo y por sus valiosas sugerencias. Al Profesor José Agustín Ortiz Elías, de la Universidad Peruana de Ciencias Aplicadas (UPC), por los análisis estadísticos realizados con toda minuciosidad y gran profesionalismo. Al personal del laboratorio por su entrega y dedicación, especialmente a la Sra. Patricia Hurtado por su valiosa colaboración técnica y logística y al Sr. Ever Paredes, por su ayuda en la recolección de las muestras en los conos. BIBLIOGRAFÍA 1. ASHFORD RW. Occurrence of an undescribed coccidian in man in Papua New Guinea. Ann Trop of Med Parasitol 1979;73:497-500. [ Links ] 2. SOAVE R, DUBEY JP, RAMOS LJ, TUMMINGS M. A new intestinal pathogen? (Abstract) Clin Res 1986; 34:533A. [ Links ] 3. NARANJO J, STERLING CR, GILMAN RH. et al. Cryptosporidium muris-like objects from fecal samples of Peruvians (abstract 324). In: Program and abstracts of the 38th Annual Meeting of the American Society of Tropical Medicine and Hygiene (Honolulu) December 10-14, 1989:243. [ Links ] 4. LONG EG, EBRAHIMZADEH A, WHITE EH, SWISHER B, CALLAWAY CS. Alga associated with diarrhea in patients with adquired inmunodeficiency syndrome and in travelers. J Clin Microbiol 1990; 28:1101-4 [ Links ] 5. LONG EG, WHITE EH, CARMICHAEL. WW et.al. Morphologic and staining characteristics of a cyanobacterium-like organism associated with diarrhea. J Infect Dis 1991; 164:199-02. [ Links ] 6. BENDALL RP, LUCAS S, MOODY A, TOVEY G, CHIODINI PL. Diarrhoeae associated with cyanobacterium-like bodies: a new coccidian enteritis of man. Lancet 1993; 341:590-2. [ Links ] 7. CONNOR BA, SHLIM DR, SHOLES JV, RAYBURN JL, REIDY J, RAJAH R. Pathologic changes in the small bowel in nine patients with diarrhea associated with a coccidia-like body. Ann Int Med 1993; 119:377-82. [ Links ] 8. HOGE CW, SHLIM DR, RAJAH R, TRIPLETT J, SHEAR M, RABOLD JG, ECHEVERRÍA P. Epidemiology of diarrhoeal illness associated with coccidian-like organism among travellers and foreign residents in Nepal. Lancet 1993 May 8; 341 (8854):1175-9. [ Links ] 9. ORTEGA YR, STERLING CR, GILMAN RH, CAMA VA, DÍAZ F. Cyclospora species. A new protozoan pathogen of humans. N England J Med 1993; 328(18):1308-12. [ Links ] 10. ORTEGA YR, GILMAN RH, STERLING CR. A new coccidian parasite (Apicomplexa: Eimeriidae) from humans. J Parasitol 1994; 80(4):625-9. [ Links ] 11. WURTZ R. Cyclospora: a newly identified intestinal pathogen of humans. Clin Infect Dis 1994 Apr; 18(4):620-3. [ Links ] 12. SHLIM DR, COHEN MT, EATON M, RAJAH R, LONG EG, UNGAR BLP. An alga-like organism associated with an outbreak of prolonged diarrhea among foreigners in Nepal. Am J Trop Med Hyg 1991; 45:383-9. [ Links ] 13. PAPE JW, VERDIER RI, BONCY M, BONCY J, JOHNSON WD. Cyclospora infection in adults infected with HIV. Clinical manifestations, treatment, and prophylaxis. Ann Intern Med 1994; 121(9):654-7. [ Links ] 14. MADICO G, MCDONALD J, GILMAN RH, CABRERA L, STERLING CR. Epidemiology and treatment of Cyclospora cayetanensis infection in peruvian children. Clin Infect Dis 1997; 24:977-81. [ Links ] 15. RIVERA N, TORREJÓN E, MADRID M. Primer hallazgo de Cyclospora cayetanensis en Concepción, Chile 1997. Parasitología al Día 1997 Jul; 21(3-4):129-32. [ Links ] 16. CEDEÑO-CASCANTE T. Cyclospora cayetanensis: descripción del primer caso en el Hospital San Rafael de Alajuela. Acta Méd Costarric 2002 Jun; 44(2):79-81. [ Links ] 17. MARTÍNEZ I, AYLLON L, BENÍTEZ X. Cyclospora cayetanensis. Presentación de 20 casos. Revista Cubana de Pediatría 2002 Abr-Jun; 74(2):178-81. [ Links ] 18. TÜRK M, TÜRKER M, AK M, KARAAYAK B, KAYA T. Cyclosporiasis associated with diarrhoea in an inmunocompetent patient in Turkey. J Med Microbiol 2004; 53: 255-7. [ Links ] 19. PINGÉ-SUTTOR V, DOUGLAS C, WETTSTEIN A. Cyclospora infection masquerading as coeliac disease. MJA 2004; 180(6):295-6. [ Links ] 20. HUANG PH, WEBER JT, SOSIN DM, GRIFFIN PM, LONG EG, MURPHY JJ, KOCKA F, PETERS C, KALLICK C. The first reported outbreak of diarrheal illness associated with Cyclospora in the United States. Ann Intern Med 1995 Sept; 123(6):409-14. [ Links ] 21. HERWALDT BL. Cyclospora cayetanensis: a review, focusing on the outbreaks of Cyclosporiasis in the 1990s. Clin Infect Dis 2000; 31:1040-57. [ Links ] 22. FLEMING C, CARON D, GUNN JE, BARRY A. A foodborne outbreak of Cyclospora cayetanensis at a wedding. Arch Intern Med 1998, 158:1121-5. [ Links ] 23. STURBAUM GD, ORTEGA YR, GILMAN RH, STERLING CR, CABRERA L, KLEIN DA. Detection of Cyclospora cayetanensis in Wastewater. Applied and Environmental Microbiology 1998 Jun; 64(6):2284-6. [ Links ] 24. ORTEGA YR, ROXAS CR, GILMAN RH, MILLER NJ, CABRERA L, TAQUIRI C, STERLING CR. Isolation of Cryptosporidium parvum and Cyclospora cayetanensis from vegetables collected in markets of an endemic region in Peru. Am J Trop Med Hyg 1997; 57(6):683-6. [ Links ] 25. EBERHARD ML, NACE EK, FREEMAN AR. Survey for Cyclospora cayetanensis in domestic animals in an endemic area in Haiti. J. Parasitol 1999; 85:562-3. [ Links ] 26. ZERPA R, UCHIMA N, HUICHO L. Cyclospora cayetanensis associated with watery diarrhoea in peruvian patients. J Trop Med Hyg 1995; 98:325-9. [ Links ] 27. HOGE CW, SHLIM DR, GHIMIRE M, et al. Placebo-controlled trial of cotrimoxazole for Cyclospora infections among travellers and foreign residents in Nepal. Lancet 1995; 345:691-3. [ Links ] 28. VERDIER RI, FITZGERALD DW, JOHNSON WD, PAPE JW. Trimethoprim-Sulfamethoxazole compared with ciprofloxacin for treatment and prophylaxis of Isospora belli and Cyclospora cayetanensis infection in HIV-infected patients. Ann Internal Med 2000 Jun; 132(11):885-8. [ Links ] 29. BERN C, ORTEGA YR, CHECKLEY W, ROBERTS JM, LESCANO AG, CABRERA L, VERÁSTEGUI M, BLACK RE, STERLING C, GILMAN RH. Epidemiologic differences between Cyclosporiasis and Cryptosporidiosis in peruvian children. Emerging Infectious Diseases Jun 2002; 8(6):581-5. [ Links ] 30. EBERHARD ML, NACE EK, FREEMAN AR, STREIT TG, DA SILVA AJ, LAMMIE PJ. Cyclospora cayetanensis infections in Haiti: a common occurrence in the absence of watery diarrhea. Am J Trop Med Hyg 1999; 60(4):584-6. [ Links ] 31. CHACIN-BONILLA L, MEJÍA DE YOUNG M, ESTÉVEZ J. Prevalence and pathogenic role of Cyclospora cayetannensis in a venezuelan community. Am J Trop Med Hyg 2003; 68(3):304-6. [ Links ] 32. SUN T, ILARDI CF, ASNIS D, BRESCIANI AR, GOLDENBERG S, ROBERTS B, TELCHBERG S. Light and electron microscopic identification of Cyclopora species in the small intestine. Evidence of the presence of asexual life cycle in human host. Am J Clin Pathol 1996; 105:216-20. [ Links ] 33. ORTEGA YR, NAGLE R, GILMAN RH. Pathologic and clinical findings in patients with cyclosporiasis and a description of intracellular parasite life cycle stages. J Infect Dis 1997; 176:1584-9.
Materials and Methods: The population was composed of 3,259 individuals: 2,968 individuals between 1 month and 87 years of age, who consulted a private physician because of digestive disorders, particularly diarrhea, and 291 individuals between 5 months and 75 years of age from marginal areas, all apparently healthy. The presence of Cyclospora was investigated through fresh microscopic techniques using a saline solution and Lugol`s solution. A new staining technique described in other publication was used. A record was created containing all clinical and epidemiological data, which were assessed statistically.
Results: Cycloscopora incidence was 7.3% in the first group, and 41.6% in the second group. A higher rate was observed in young and elder adults up to 60-year-old. No major seasonal incidence was found. Clinical signs/symptoms for individuals consulting a private physician were mainly diarrhea and abdominal pain while individuals from marginal urban areas mainly showed meteorism, abdominal plain, occasional diarrhea and general symptoms such as fatigue and weight loss. Conclusions: Cyclospora showed a high incidence, particularly in marginal urban areas. Two types of clinical signs/symptoms were found: an acute and very severe condition that can cause dehydration, and a chronic condition with several digestive signs/symptoms, particularly meteorism and abdominal pain. Individuals consulting a private physician show acute and chronic episodes while individuals from marginal urban areas do show a chronic condition. Apparently individuals showing acute episodes are immunologically exposed to the parasite, but they do not acquire immunity later in spite of the treatment because they may become re-infected from time to time. However, individuals showing chronic episodes apparently keep a host-parasite balance due to a permanent contact with the parasite. The contamination source appears to be the water. Therefore all required epidemiological actions shall be taken to prevent this problem from reaching higher dimensions.
Keywords: Cyclospora cayetanensis; prevalence; clinical aspects; epidemiology; Lima, Peru.