Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.29 n.3 Lima jul./set. 2009
REPORTE DE CASOS
Disección submucosa endoscópica (DSE) para el tratamiento curativo del cáncer gástrico precoz: experiencia inicial en Costa Rica
Endoscopic submucosal dissection (esd) for the curative treatment of early gastric cancer: initial experience in Costa Rica
Sergio A. Con1
; Gil R. Con-Chin2 ; Gustavo Kishimoto3 ; Reinaldo Con-Wong41 Cirujano Digestivo y Endoscopista; Divisiones de Cirugía y Endoscopia Digestiva del Centro Digestivo Doctores Con-Mediplaza, San José, Costa Rica.
2 Cirujano Digestivo y Endoscopista; Divisiones de Cirugía y Endoscopia Digestiva del Centro Digestivo Doctores Con-Mediplaza, San José, Costa Rica.
3 Médico-cirujano; División de Endoscopia del Hospital del Centro Nacional de Cáncer en Tokio, Japón. Dirección de Investigación Científica – Clínica Centenario Peruano Japonesa, Perú.
4 Gastroenterólogo Quirúrgico y Endoscopista; Divisiones de Cirugía y Endoscopia Digestiva del Centro Digestivo Doctores Con-Mediplaza, San José, Costa Rica.
RESUMEN
OBJETIVO. Reportar el primer caso de disección submucosa endoscópica (DSE) en Costa Rica y analizar el futuro impacto de esta técnica en el abordaje del cáncer gástrico precoz en este país.
PACIENTES Y MÉTODOS. Presentamos el caso de una paciente de 67 años, quien tras una endoscopia digestiva alta por leve epigastralgia, se le encuentra una lesión elevada sésil no ulcerada (0-IIa) de aproximadamente 12 milímetros localizada en el antro hacia la curvatura mayor. Posterior al resultado histopatológico de adenocarcinoma bien diferenciado limitado a mucosa, la paciente fue sometida a una disección submucosa en una pieza (en-bloc) de la lesión por vía endoscópica.
RESULTADOS. La DSE fue realizada sin ninguna complicación, como sangrado o perforación, intra o postoperatoria. El tiempo operatorio fue de 65 minutos. Con el análisis histopatológico del especimen en-bloc se confirmó el diagnóstico de adenocarcinoma intramucoso con márgenes negativos.
CONCLUSIÓN. La DSE promete ser una excelente alternativa para el tratamiento curativo del cáncer gástrico precoz, siendo un método más costo-efectivo, y menos invasivo, ofreciendo una mejor calidad de vida al paciente con iguales resultados a largo plazo que la cirugía convencional a cielo abierto.
PALABRAS CLAVE. Disección submucosa endoscópica, DSE, cáncer gástrico, Costa Rica.
ABSTRACT
OBJECTIVES. To report the first case of endoscopic submucosal dissection (ESD) in Costa Rica and to analyze the future impact of this technique for the treatment of early gastric cancer in this country.
PATIENTS AND METHODS. We present the case of a 67-year-old woman who underwent an upper endoscopy for mild epigastralgia, resulting in a 12 mm non-ulcerated sessile lesion (0-IIa) located in the antrum at the greater curvature. After biopsy confirmation of a well-differentiated adenocarcinoma limited to the mucosa, the patient underwent an endoscopic submucosal dissection for the en-bloc resection of the lesion.
CONCLUSION. ESD is novel alternative for the curative treatment of early gastric cancer, due to its cost-effectiveness, less invasiveness, which provides a better quality of life for the patient than that of conventional open surgery with same long-term results.
KEYWORDS: Endoscopic submucosal dissection, ESD, gastric cancer, Costa Rica.
INTRODUCCIÓN
El cáncer gástrico es la segunda causa de muerte por neoplasias a nivel mundial.(1) Un total de 700.000 muertes por cáncer gástrico fueron reportadas en el 2002, de las cuales dos terceras partes acaecieron en Latinoamérica(2) Esta enfermedad se ha convertido en un problema de salud pública, especialmente en países como Costa Rica, dónde se registró la mayor tasa de mortalidad por cáncer gástrico en hombres y mujeres durante 1983-1997 entre 30 países, incluyendo a Japón y Chile.(3) La falta de reconocimiento de lesiones en etapas tempranas, así como la ausencia de programas nacionales de detección masiva de cáncer gástrico serían las causas principales de su alta mortalidad, debido a que la gran mayoría de los casos son diagnosticados ya en etapas tardías de la enfermedad. La implementación de estos programas permitiría la aplicación de un tratamiento oportuno con alto grado de curabilidad. (4,5)
La disección submucosa endoscópica (DSE) es una novedosa técnica aplicada en casos de cáncer gástrico precoz, difundida principalmente en el sureste asiático. (6-10) Ésta, al igual que la conocida mucosectomía o resección mucosa endoscópica (RME), posibilita un tratamiento curativo endoscópico, evitando la cirugía convencional a cielo abierto y las posibles complicaciones postoperatorias, resultando en una mejor calidad de vida para el paciente. Sin embargo, a diferencia de la RME, la DSE permite la remoción segura y curativa en "una pieza" (en-bloc) de lesiones de mayor tamaño y profundidad, permitiendo un estudio histopatológico completo del espécimen. Esta característica ha contribuido a reducir la tasa de recurrencia local post tratamiento endoscópico. (11) El presente reporte describe el primer caso en Costa Rica tratado con la técnica DSE y el futuro impacto de esta alternativa terapéutica para el abordaje del cáncer gástrico precoz en este país.
REPORTE DEL CASO
Una paciente de 67 años de edad, con antecedentes de hipertensión arterial por 28 años en tratamiento con losartán y amlodipina, y diabetes mellitus tipo 2 por cinco años en tratamiento con metformina, acude a nuestro centro para someterse a una endoscopia digestiva alta de rutina debido a una leve epigastralgia.
Evaluación endoscópica e histopatológica:
Endoscopia 24.04.2009: Gastritis crónica atrófi ca antral con erosiones múltiples. Lesión elevada sésil no ulcerada (0IIa) de aproximadamente 12 milímetros localizada en el antro hacia la curvatura mayor (Figura 1). Resultado de biopsia: adenocarcinoma bien diferenciado limitado a mucosa.
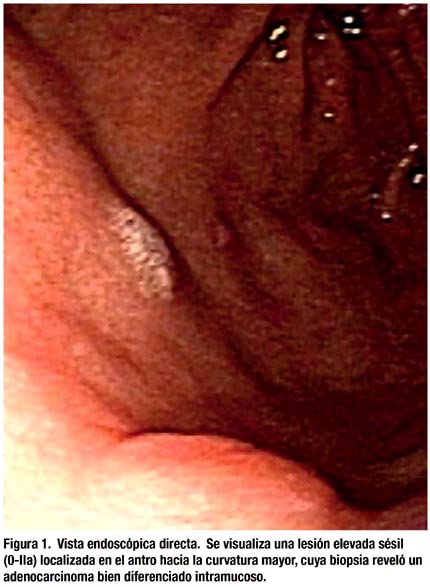
Exámenes auxiliares:
Hemoglobina 13,9 g/dL, hematocrito 43,0%, leucocitos 9,600/mm3, plaquetas 344.000/mm3, glucosa 110mg/ dL, urea 38 mg/dL, creatinina 1,1 mg/dL, tiempo de protrombina 13,0 seg, tiempo parcial de tromboplastina 32,0 seg, TGO (AST) 20 UI/L, TGP (ALT) 24 UI/L, fosfatasa alcalina 62 U/L.
Descripción del procedimiento:
DSE 13.05.2009: Bajo sedoanalgesia asistida por un anestesiólogo y luego de la confirmación cromoendoscópica con índigo-carmín (IC), se demarcaron los bordes libres de la lesión utilizando un bisturí endoscópico aguja (Needle knife) (Olympus Medical Systems Corp., Tokio, Japón) con el sistema electroquirúrgico ERBE (VIO 200S, Tuebingen, Alemania) en modo FORCED COAGULATION a 20 vatios (Figura 2). Posterior a la inyección submucosa de solución salina con IC y epinefrina, se realizó la incisión inicial (pre-cut) con el Needle knife en modo ENDO-CUT efecto 3 a 80 vatios. Luego se insertó la punta de un bisturí endoscópico con bola de cerámica (insulation-tipped (IT) knife-2) (Olympus Medical Systems Corp.) dentro de la incisión inicial y se procedió a cortar la mucosa circunferencialmente por fuera de la demarcación previa (Figura 3). El IT knife-2 también fue utilizado para la disección de la submucosa, alternándose con un coagrasper (Olympus Medical Systems Corp.) para el control de hemostasia de los vasos visibles. La lesión fue removida en-bloc en aproximadamente 65 minutos, sin ninguna complicación por sangrado o perforación, provocando una úlcera artificial (Figura 4). La paciente fue hospitalizada con control hemodinámico permaneciendo nada vía oral por 24 horas sin presentar trastornos abdominales. Al segundo día posoperatorio (PO), posterior a la confirmación de ausencia de aire subdiafragmático a través de una radiografía simple de abdomen, se prosiguió con dieta líquida. La paciente fue dada de alta al tercer día PO, sin ninguna complicación, con tratamiento de inhibidores de bomba de protones y sucralfato. Después de 15 días se controló a la paciente por consultorio externo, quién refirió encontrarse asintomática y en buen estado general.
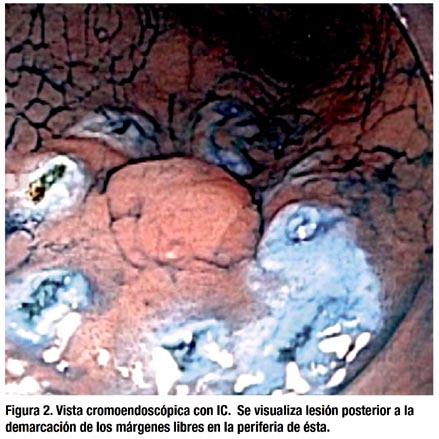
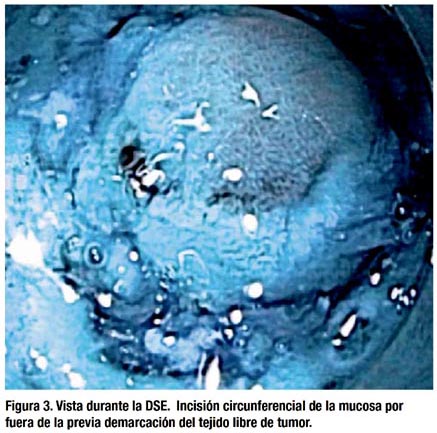
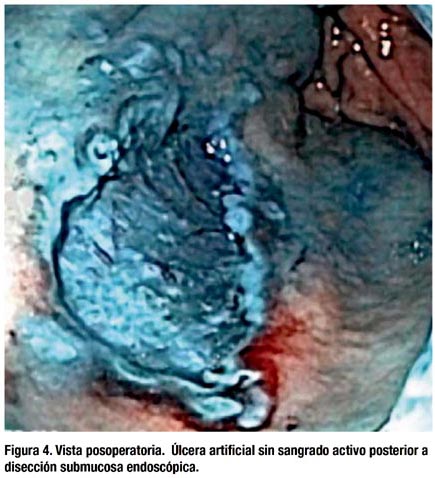
DISCUSIÓN
El cáncer gástrico precoz se define como aquel cuya profundidad de invasión es confinada a la mucosa o submucosa indiferentemente de la presencia de metástasis de ganglios linfáticos regionales.(12) La cirugía radical con disección ganglionar tipo D2 es el tratamiento de elección para pacientes en esta etapa del cáncer,(13,14) con sobrevida a cinco años mayor al 90%.(15-17) Recientemente se ha difundido el tratamiento endoscópico para el cáncer gástrico precoz, en especial las técnicas de RME y DSE, las cuales ofrecen una mejor calidad de vida para el paciente con iguales resultados a largo plazo que la cirugía convencional a cielo abierto.(18,19)
Gracias a la técnica japonesa aprendida en el Hospital del Centro Nacional de Cáncer en Tokio, se logró por primera vez en Costa Rica aplicar la técnica de DSE para el tratamiento curativo de un carcinoma gástrico intramucoso.
Posterior a la identificación directa de la lesión, se realizó la confirmación cromoendoscópica con IC. Este importante paso proporciona una mejor visualización de los bordes de la lesión tumoral. La inyección submucosa con la solución de IC y epinefrina diluida en suero fi siológico permite un procedimiento más sencillo y seguro, ya que el engrosamiento de la submucosa da un margen de seguridad para disminuir el riesgo de perforación, y el teñido de azul ayuda a distinguir claramente la capa submucosa de la muscular. Las características del IT knife-2 permiten un corte más tiempo-efectivo que otros bisturíes endoscópicos, debido a que proporciona una incrementada capacidad de corte vertical y lateral, y una gran facilidad para enganche del tejido antes de su corte.(20) Es importante advertir a los médicos con poca o sin experiencia en el uso de este instrumento, que en este paso también se han reportado perforaciones gástricas(21) y que se debe tener mayor cuidado en la manipulación de este nuevo bisturí, en comparación con el IT-knife original, pues no necesita mucho torque para realizar el corte.
En este caso se optó por la técnica de DSE sobre la RME debido a que la profundidad del tumor no pudo ser delimitada por medio de ultrasonido endoscópico. Además, la lesión sobrepasó el tamaño de hasta 10 mm, que es el ideal para la aplicación de la RME.(22) Debido a estas razones se decidió remover más allá de la capa mucosa y prevenir una posible invasión del tumor a la capa submucosa. Con el posterior análisis histopatológico del espécimen en una pieza se mostró la presencia de bordes libres, y se confirmó el diagnóstico de adenocarcinoma bien diferenciado limitado a mucosa.
A diferencia de otros países del istmo centroamericano, el cáncer es la segunda causa de muerte en Costa Rica. Lo más preocupante es que el sistema de salud nacional dedica menos del 7% del gasto anual al tratamiento de cáncer y únicamente el 0.4% para la prevención, que en su mayoría consiste en prevención del cáncer cervical. Se ha reportado que en Costa Rica la incidencia de cáncer gástrico precoz es de 6.7%(23), siendo extremadamente baja en comparación con países como Japón (40-60%). (24) Por esta razón, es esencial desarrollar programas de detección precoz de cáncer gástrico a nivel nacional. Un intento inicial se puso en práctica a nivel piloto posterior a un estudio que reportó una asociación significativa entre niveles séricos bajos de pepsinógenos (PG) y lesiones precursoras del cáncer gástrico como atrofia gástrica y metaplasia intestinal en una población costarricense, donde casos con bajos niveles séricos de PG fueron sometidos a gastrocopia con toma de biopsias.(25) Varios estudios han demostrado que valores bajos de la relación PGI/PGII se asocian a alto riesgo de atrofi a gástrica y cáncer gástrico, por lo cual, la determinación de estos niveles podría ser utilizada como un método de tamizaje.(26-30) Hasta la fecha en este programa piloto no se ha hallado casos de cáncer gástrico precoz, sin embargo se detectó un caso de carcinoma avanzado que fue sometido a cirugía radical y dos casos de displasia gástrica de bajo grado los cuales están siendo vigilados periódicamente.En conclusión, la técnica DSE promete ser una excelente alternativa para el tratamiento curativo del cáncer gástrico precoz, siendo un método más costo-efectivo, y menos invasivo, ofreciendo una mejor calidad de vida al paciente.
Agradecimientos
Los autores agradecen a Olympus America Inc., Latin Ame-rica Group y a Eurociencia Costa Rica S.A. por su apoyo con el programa de detección temprana del cáncer gastrointestinal en Costa Rica y por su aporte de equipo endoscópico.
REFERENCIAS
1. PLUMIER M, FRANCESCHI S, MUÑOZ N. Epidemiology of gastric cancer. IARC Sci Publ. 2004 (157): 311-326.
2. PARKIN DM, BRAY F, FERLAY J, PISANI P. Global cancer statistics, 2002. CA Cancer J Clin 2005; 55: 74-108.
3. KUROISHI T, HIROSE K, TAKESAKI T, et al. Cancer mortality statistics in 30 countries (1953-1997). In: Tajima K, Kuroishi T, Oshima A, editors. Cancer mortality and morbidity statistics Japan and the world-2004. 1st ed. Tokyo: Japan Scientifi c Societies Press; 2004. p. 165-229.
4. HISAMICHI S, SUGAWARA N, FUKAO A. Effectiveness of gastric mass screening in Japan. Cancer Detect Prev 1988;11: 323-329.
5. FUKAO A, TSUBONOY, TSUJI I. The evaluation of screening of gastric cancer in Miyagi Prefecture, Japan: a population-base-control study. Int J Cancer 1995; 60: 45-48.
6. ONOZATO Y, ISHIHARA H, IIZUKA Z, et al. Endoscopic submucosal dissection for early gastric cancers and large flat adenomas. Endoscopy 2006; 38: 980-986.
7. LEE IL, LIN PY, TUNG SY, et al. Endoscopic submucosal dissection for the treatment of intraluminal gastric subepithelial tumors originating from the muscularis propria layer. Endoscopy 2006; 38 (10): 1024-1028.
8. GOTODA T, YAMAMOTO H, SOETIKNO R. Endoscopic submucosal dissection of early gastric cancer. J Gastroenterol 2006; 41: 929-942.
9. YAHAGI N, FUJISHIRO M, KAKUSHIMA N, et al. Endoscopic submucosal dissection for early gastric cancer using the tip of an electrosurgical snare (thin type). Dig Endosc 2004; 16: 34-38.
10. ODA I, GOTODA T, HAMANAKA I, et al. Endoscopic submucosal dissection for early gastric cancer: technical feasibility, operation time and complications
from a large consecutive series. Dig Endosc 2005; 17: 54-58.11. GOTODA T. Endoscopic resection of early gastric cancer. Gastric cancer 2007; 10: 1-11.
12. JAPANESE GASTRIC CANCER ASSOCIATION, Japanese Classification of gastric carcinoma, 2nd English edition, Gastric Cancer 1: 10-24, 1998.
13. MARUYAMA K, OKABAYASHI K, KINOSHITA T. Progress in gastric cancer surgery in Japan and its limits of radicality. World J Surg 1987; 11: 418-425.
14. TAKESHITA K, TANI M, INOUE H. A new method of endoscopic mucosal resection of neoplastic lesions in the stomach: its technical features and results. Hepato-Gastroenterology 1997; 44: 1602-1611.
15. SANO T, SASAKO M, KINOSHITA T, et al. Recurrence of early gastric cancer: follow-up of 1475 patients and review of Japanese literature. Cancer 1993; 72: 3174-3178.
16. SUE-LING HM, MARTIN IG, GRIFFITH J, et al. Early gastric cancer: 46 cases treated in one surgical department. Gut 1992; 33: 1318-1322.
17. SASAKO M, KINOSHITA T, MARUYAMA K. Prognosis of early gastric cancer (abstract in English). Stomach and intestine 1993; 28: 139-146.
18. TAKESHITA T, TANI M, INOUE H, et al. Endoscopic treatment of early esophageal or gastric cancer. Gut 1997; 40: 123-127.
19. MORITA Y, AOYAMA N, SHIRASAKA D, et al. Prospect of endoscopic mucosal resection for early gastric cancer: our devices in insulated-tip electrosurgical knife method. Dig Endosc 2003; 15: S12-S14.
20. ONO H, HASUIKE N, INUI T, et al. Usefulness of a novel electrosurgical knife, the insulation-tipped diathermic knife-2, for endoscopic submucosal dissection of early gastric cancer. Gastric Cancer 2008; 11: 47-52.
21. CON SA, ODA I, SUZUKI H, et al. Risk of perforation during endoscopic submucosal dissection using latest insulation-tipped diathermic knife (IT knife-2). Endoscopy 2009; 41: E69-E70.
22. NAKAMURA K, UEYAMA T, YAO T, et al. Pathology and prognosis of gastric carcinoma: fi ndings in 10,000 patients who underwent primary gastrectomy. Cancer 1992; 70: 1030-1037.
23. SIGARÁN M, CHAVES CERVANTES M, QUESADA A, y col. Incidencia de cáncer gástrico temprano en Costa Rica. Resultados de un quinquenio en hospitales del área metropolitana. Acta Méd Costarric 1995; 37: 1-8.
24. SHIMIZU S, TADA M, KAWAI K. Early gastric cancer: its surveillance and natural course. Endoscopy 1995;
27: 27-31.
25. CON SA, CON-WONG R, CON-CHIN GR et al. Serum pepsinogen levels, Helicobacter pylori CagA status, and cytokine gene polymorphisms associated with gastric premalignant lesions in Costa Rica. Cancer Epidemiol Biomarkers Prev 2007; 16: 2631-2636.
26. MIKI K, ICHINOSE M, ISHIKAWA K et al. Clinical application of serum pepsinogen I and II levels for mass screening to detect gastric cancer. Jpn J Cancer Res 1993; 84: 1086-1090.
27. KODOI A, YOSHIHARA M, SUMII K et al. Serum pepsinogen in screening for gastric cancer. J Gastroenterol 1995; 30: 452-460.
28. AOKI K, MISUMI J, KIMURA T et al. Evaluation of cuttof levels for screening of gastric cancer using serum pepsinogen and distributions of levels of serum pepsinogen I, II and PGI/PGII ratios in a gastric cancer case-control study. J Epidemiol 1997; 7: 143151.
29. YOSHIHARA M, SUMII K, HARUMA K et al. Correlation of ratio of serum pepsinogen I and II with prevalence of gastric cancer and adenoma in Japanese subjects. Am J Gastroenterol 1998; 93: 1090-1096.
30. KITAHARA F, KOBAYASHI K, SATO T et al. Accuracy of screening for gastric cancer using serum pepsinogen concentrations. Gut 1999; 44: 693-697.
Correspondencia:
Centro Digestivo Doctores Con-Mediplaza, San José, Costa Rica
Divisiones de Cirugía y Endoscopia Digestiva
Tel.: (506) 2201-7028
Fax: (506) 2201-7033
Correo electrónico: scon@gastrocolon.com













