Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.31 n.1 Lima ene./mar. 2011
ARTÍCULOS ORIGINALES
Estudio Piloto: terapia secuencial en la erradicación del Helicobacter Pylori en el Hospital Cayetano Heredia
Pilot study: sequential therapy in erradicating Helicobacter pylori in the Cayetano Heredia Hospital
Arturo Zegarra Chang1 ; Eduar Bravo Paredes1 ; Ricardo Prochazka Zárate2 ; Alejandro Piscoya Rivera2 ; Raúl De los Ríos Senmache2 ; José Luis Pinto Valdivia2 ; Jorge Huerta-Mercado Tenorio2
1. Médico Residente Hospital Cayetano Heredia.
2. Médico Asistente Hospital Cayetano Heredia.
RESUMEN
INTRODUCCIÓN: La terapia secuencial nace como una alternativa a la creciente resistencia antibiótica del Helicobacter pylori (HP) a la terapia triple (estándar). A pesar de los resultados satisfactorios que ha tenido en Europa, en nuestro medio no tenemos referencia de un estudio al respecto.
OBJETIVOS: Evaluar la tasa de erradicación del Helicobacter pylori empleando la terapia secuencial y evidenciar sus efectos adversos.
METODOLOGÍA: Se realiza un estudio prospectivo, observacional, descriptivo, abierto. Se evaluaron 31 pacientes que recibieron tratamiento con terapia secuencial de la siguiente forma, los 5 primeros días omeprazol 20 mg y amoxicilina de 1 g cada 12 horas y los 5 días siguientes omeprazol 20 mg, claritromicina 500 mg y tinidazol de 500 mg cada 12 horas. A las 4 semanas de terminado el tratamiento se le realizó a cada paciente una prueba de aliento con carbono 13 para comprobar la erradicación del HP.
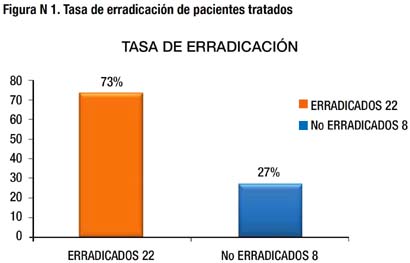
RESULTADOS: Se incluyeron a 31 pacientes, un paciente fue excluido del protocolo por presentar RAM a la amoxicilina. De los 30 pacientes restantes que completaron el tratamiento, 22 (73%) resultaron negativos en la prueba del aliento y 8 (27%) resultaron positivos. De los pacientes que completaron el tratamiento, 10 presentaron eventos adversos menores al tratamiento, principalmente epigastralgia y náuseas.
CONCLUSIONES: La terapia secuencial tuvo una tasa de erradicación del 73% la cual es mucho menor a la reportada en los estudios europeos. Sin embargo, es una terapia de fácil acceso, de menor costo y con menores efectos colaterales.
PALABRAS CLAVE: Terapia secuencial, Helicobacter pylori, prueba del aliento.
ABSTRACT
BACKGROUND: Sequential therapy is used as an alternative to growing antibiotic resistance of Helicobacter pylori to the standard triple therapy. Despite the success it had in Europe, we have no information regarding this therapy in our region.
OBJECTIVES: To evaluate the eradication rate of Helicobacter pylori using sequential therapy and show its adverse effects.
METHODS: We performed a prospective, observational, open descriptive study. 31 patients were evaluated who were treated with sequential therapy in the following way: the first 5 days omeprazole 20 mg and amoxicillin 1 g every 12 hours and following 5 days omeprazole 20 mg, clarithromycin 500 mg and tinidazole 500 mg every 12 hours. After four weeks of treatment, each patient had a C13 urea breath test to check for eradication.
RESULTS: 31 patients were included, one patient was excluded from the protocol due to adverse drug react to amoxicillin. Of the remaining 30 patients who completed treatment, 22 (73%) were negative to breath test and 8 (27%) were positive. Of the patients who completed treatment, 10 had minor adverse events to treatment, the main symptoms were epigastralgia and nausea.
CONCLUSIONS: Sequential therapy had an eradication rate of 73% which is much lower than that reported in European studies. However, therapy is easily accesible with lower cost and fewer side effects tan standard therapy.
KEYWORDS: sequential therapy, Helicobacter pylori, breath test.
INTRODUCCIÓN
La infección por Helicobacter pylori tiene una alta prevalencia a nivel mundial; se estima que más del 50% de la población en todo el mundo presenta la infección (1,2). Se ha demostrado que el Helicobacter pylori juega un rol importante en la patogénesis de distintas enfermedades como la gastritis crónica, la enfermedad úlcera péptica, el linfoma MALT y el adenocarcinoma gástrico (3). También se sabe que la prevalencia es distinta en cada región, la cual se ve influenciada por una serie de factores como la edad, etnicidad, estatus socioeconómico y el área geográfica.
En el consenso de Maastricht III, se reconoce a la terapia triple (omeprazol, amoxicilina, claritromicina) como la terapia de primera línea para la erradicación del Helicobacter pylori (4-6).
Cuando se inició la terapia triple en los 90s, los primeros estudios mostraron una tasa de erradicación por encima de 90%. Sin embargo, estas cifras han disminuido con el tiempo, es así que estudios recientes muestran tasas de erradicación entre 75 a 80%. (7, 8)
Las tasas de erradicación son variables de acuerdo a cada región. En nuestro hospital tenemos una tasa de erradicación de alrededor del 80% (9). Esta variabilidad en algunas poblaciones se debe a la tasa de resistencia a los macrólidos. (10-15). Recientes estudios en USA muestran una tasa de resistencia a claritromicina de 10 a 13%. (12)
En nuestro medio el régimen terapéutico utilizado como primera línea para la erradicación del Helicobacter pylori es la terapia triple. Existen estudios pilotos utilizando pantoprazol con levofloxacina + amoxicilina y lanzoprazol con tinidazol + claritromicina obteniendo tasas de erradicación de 41.2% y 68.4% respectivamente (16).
Un estudio reciente de terapia secuencial, con 10 días de tratamiento (17,18), los primeros 5 días con un inhibidor de bomba y un antibiótico (amoxicilina) seguido de 5 días de tratamiento con inhibidor de bomba y 2 antibióticos (claritromicina, tinidazol) fue realizado por Vaira et al en 300 pacientes con dispepsia funcional o enfermedad úlcero-péptica, mostrando una tasa de erradicación de 89% versus 77% con terapia estándar (diferencial 12%, 95% CI 3-20%). (19)
La racionalidad de este esquema radica en que la amoxicilina podría actuar debilitando la pared bacteriana en la primera fase del tratamiento, bloqueando los canales de salida de la bacteria, lo cual permitiría a la claritromicina actuar a nivel de los ribosomas en la segunda fase de tratamiento, mejorando su eficacia y evitando así la resistencia a este antibiótico. (20, 21).
A la fecha se han publicado varios estudios y dos meta-análisis con respecto al uso de terapia secuencial vs terapia triple, encontrándose tasas de erradicación de 93,4% en la terapia secuencial y de 76,9% con la terapia triple (22, 23).
En nuestro medio aún no se han reportado estudios empleando la terapia secuencial en la erradicación del Helicobacter pylori.
MATERIALES Y MÉTODOS
Objetivos
Nuestros objetivos fueron evaluar la tasa de erradicación del Helicobacter pylori empleando la terapia secuencial y observar los efectos adversos así como la tolerancia de los pacientes a esta terapia.
Población de estudio
La población en estudio la conformaron 31 pacientes con dispepsia no ulcerosa que acudieron a la consulta externa del Servicio de Gastroenterología del Hospital Cayetano Heredia, y que tuvieron diagnóstico de novo de infección por HP en la biopsia gástrica. Todos los pacientes incluidos en el estudio dieron su consentimiento para participar estudio realizado.
Los criterios de inclusión fueron tener entre 18 y 75 años con evidencia de infección por HP, registrada mediante estudio histopatólogico. Los criterios de exclusión fueron tener cirugía gástrica previa, presencia de neoplasia gástrica, alergia conocida a uno de los fármacos usados en el estudio, uso de inhibidores de la bomba de protones, anti H2, antibióticos y bismutol en las 4 semanas previas al ingreso al estudio, presencia de úlcera gástrica o duodenal, tratamiento anti HP previo en los últimos 12 meses, presencia de comorbilidad descompensada: cirrosis, insuficiencia renal, enfermedad coronária, embarazo , lactancia, alcoholismo.
Diseño del estudio
Se realizó un estudio prospectivo, abierto, observacional, descriptivo en un solo centro.
Metodología
Todos los pacientes incluidos en el estudio tuvieron diagnóstico de infección por Helicobacter pylori mediante la biopsia gástrica empleando tinción de hematoxilina y eosina.
A todos los pacientes se les brindó tratamiento para erradicar HP usando la terapia secuencial la cual consistió en:
Los primeros 5 días (primera fase):
Omeprazol 20 mg, Amoxicilina 1 g (2 tabletas de 500 mg) cada 12 horas
Los siguientes 5 días (segunda fase):
Omeprazol 20 mg, Claritromicina 500 mg y Tinidazol 500 mg (1/2 tableta de 1gr) cada 12 horas.
A las 4 semanas de finalizado el tratamiento, cada paciente fue sometido a una prueba del aliento con Carbono 13 para determinar la erradicación del HP. Se considera como erradicación, cuando la prueba del aliento resulta negativa; es decir un valor menor de 50 desintegraciones por minuto (DPM), positiva si tiene un valor mayor de 200 DPM e intermedio cuando está entre 50 a 200 DPM.
El protocolo fue aprobado por el comité de ética de la Universidad Peruana Cayetano Heredia.
Seguimiento de los pacientes
Cada paciente luego de recibir la medicación, fue seguido telefónicamente a los 5 días de terminada la primera fase y luego de terminada la segunda fase de tratamiento, para determinar el cumplimiento del mismo y evaluar posibles efectos adversos.
Análisis de Resultados
Para el procesamiento de los resultados y la construcción de tablas se empleó la base de datos del programa Microsoft Office Excel 2007.
RESULTADOS
Para nuestro estudio se incluyeron 31 pacientes de los cuales 1 paciente abandonó el estudio por presentar reacción alérgica a la amoxicilina.
De los 30 pacientes que completaron la terapia secuencial, 7 fueron varones y 23 fueron mujeres. El promedio de edad fue de 40,7 años (rango 19-70 años).
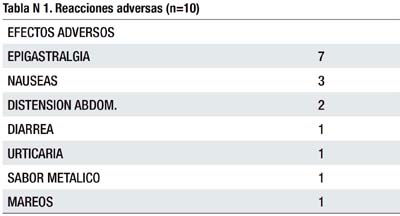
A las 4 semanas de finalizada la terapia secuencial se encontró que 8 (26,6%) pacientes resultaron positivos y 22 (73,3%) negativos en la prueba del aliento. (Figura 1). La tasa de erradicación de la terapia secuencial por intención a tratar fue de 70,96%. De los pacientes tratados, 10 (33,3%) tuvieron reacciones adversas leves durante la medicación, los síntomas principales fueron epigastralgia y náuseas. (Tabla 1). Sólo un paciente presentó una reacción alérgica a la amoxicilina por lo cual se suspendió la medicación y fue excluida del protocolo.
DISCUSIÓN
La terapia secuencial aparece como una posible solución ante la creciente resistencia bacteriana del HP a los diversos esquemas terapéuticos. Así lo han demostrado diversos estudios y meta-análisis. Sin embargo, la mayoría de estos estudios se han desarrollado en Italia y Grecia con resultados alentadores como los de Zullo et al en Italia usando la terapia secuencial, en donde se evidenció tasas de erradicación de 93,5% (18, 20). Muchos expertos coinciden en que cada población tiene una tasa de erradicación variable debido a la creciente resistencia bacteriana de las diversas cepas de Helicobacter pylori, por ejemplo en Korea y Turquía Se encontraron tasas de erradicación de 77,9 y 50% respectivamente, menores a la de los estudios italianos. (24,25)
En nuestro medio no existen estudios previos publicados empleando terapia secuencial. La tasa de erradicación obtenida en nuestro estudio fue de 73% y resulta mucho menor a la obtenida en estudios previos empleando al terapia triple donde se encontró una tasa de erradicación de 80% (9).
El presente trabajo es un estudio piloto con un grupo reducido de pacientes. La tasa de erradicación encontrada podría estar en relación a que probablemente la resistencia antibiótica sólo a claritromicina no sea tan alta como en otras regiones (19), y por el contrario tengamos cepas resistentes a otro antibiótico (tinidazol, un imidazólico de la familia del metronidazol).
Desafortunadamente en nuestro medio contamos con pocos estudios en donde se incluya cultivos con sensibilidad antibiótica. Entre estos, el estudio de Soto et al. (26) e encontró cepas resistentes al metronidazol 52%, a claritromicina 27% y a amoxicilina en 7%. En este sentido, el trabajo realizado por Viara et al. (19) encontró que los pacientes con cepas de Helicobacter pylori resistentes a claritromicina y metronidazol, fracasaron a la terapia secuencial.
Con respecto a los efectos adversos, en términos generales la terapia secuencial fue bien tolerada, sólo un paciente presentó una reacción alérgica a la amoxicilina por lo que se tuvo que suspender la medicación, los demás pacientes toleraron la medicación y sólo un 30 % (10 pacientes) presentaron efectos adversos leves que no impidieron continuar con la terapia. Una de las desventajas de la terapia secuencial y de la terapia triple es que ambas incluyen en sus esquemas amoxicilina, lo cual contraindicaría su uso a pacientes alérgicos a la penicilina. La ventaja de la terapia secuencial es el menor costo, por el menor tiempo de uso de la claritromicina (el fármaco de mayor costo), en la terapia secuencial que en la terapia triple.
Dentro de las limitaciones que presenta nuestro estudio, está el número reducido de pacientes que se incluyeron, además de la falta de un brazo control (terapia triple) con el que se pudiera comparar las tasas de erradicación. Idealmente para establecer si una terapia es superior a la otra se hubiera requerido hacer un ensayo clínico, lo cual es difícil por la gran cantidad de recursos (económicos y humanos) que ello implica. A pesar de todo, este primer estudio piloto del uso de la terapia secuencial en nuestro medio, plantea algunas interrogantes y abre las puertas para futuros estudios.
En conclusión, en nuestro estudio, el uso de la terapia secuencial mostró una tasa de erradicación del 73%, la cual difiere de otros estudios en donde las tasas de erradicación son cercanas al 90%; pero similar a la que se encuentra en el estudio koreano (24). Esto se debe a la probable resistencia al tinidazol. Finalmente, es importante reconocer la buena tolerancia de los pacientes a la terapia secuencial, así como la importancia tener menor costo para el paciente.
REFERENCIAS
1. CAVE DR .Transmission and epidemiology of Helicobacter pylori. Am J Med 1996 May 20;100(5A):12S-17S
2. POUNDER RE, et al. The prevalence of Helicobacter pylori infection in different countries. Aliment Pharmacol Ther 1995;9 Suppl 2:33-9.
3. SUERBAUM S, MICHETTI P. Helicobacter pylori infection.
N Engl J Med 2002; 347:1175-86.4. MALFERTHEINER P, MEGRAUD F, O´MORAIN C, et al. Current concepts in the management of Helicobacter pylori infection: The Maastricht III Consensus Report. Gut. 2007;56:772-781
5. LAM SK, TALLEY NJ. Reporto f the 1997 Asia Pasific Consensus. Conference on the managemente of Helicobacter pylori infection. J. Gastroenterol Hepatol. 1998;13:1-12
6. BOURKE B, CEPONIS P, CHIBA N, et al. for the Canadian Helicobacter Study Group. Canadian Helicobacter Study Group Consensus Conference: Update on the approach to Helicobacter pylori infection in children and adolescents an evidence-based evaluation. Can J. Gastroenterol. 2005;19:399-408.
7. O´CONNOR A. GISBERT J. O´MORAIN C. Treatment of Helicobacter pylori infection. Helicobacter, 2009;14 (Suppl 1): 46-51.
8. JASSEN MJ, VAN OIJEN AH, VERBEEK AL, et al. A systematic compariion of triple therapies for treatment of Helicobacter pylori infection with proton pump inhibitor/ ranitidine bismuth citrate plus clarithromycin and either amoxicillin or nitroimidazole. Aliment Pharmacol Ther 2001; 15:613-624.
9. DE LOS RÍOS R, PINTO JL, ZEGARRA A, GARCÍA C, PISCOYA A, HUERTA-MERCADO J. Esomeprazol versus omeprazol en la terapia triple para la erradicación del Helicobacter pylori en pacientes dispépticos no ulcerosos. Rev Gastroenterol Peru. 2009 JulSep;29(3):234-8.
10. UYGUN A, ATES Y, ERDIL A, et al. Efficay of Omeprazol plus two antimicrobials for the erradication of Helicobacter pylori in a Turkish population. Clin Ther. 1999;21:1539-1548.
11. NERI M, MILANO A, LATERZA F, et al. Role of antibiotic sensitivity testing before first line Helicobacter pylori erradication treatmentes. Aliment Pharmacol. Ther. 2003; 18: 821-827.
12. WERMEILLE J, CUNNINGHAM M, DEDERDING JP, et al. Failure of Helicobacter pylori erradication; Is poor compliance the main cause? Gastroenterol Clin Biol. 2002;26:207-209.
13. CALVET X, DUCONS J, BUJANDA L, et al. For the Asociación Española de Gastroenterología. Seven versus tem days of rabeprazole triple therapy for Helicobacter pylori erradication. A multicenter randomized Trial. Am J Gastroenterol. 2005;100:1696-1701.
14. SIVRI B, SIMSEK I, HULAGU S, et al. The efficay, safety and tolerbility of pantoprazole-based on one-week triple therapy in H pylori erradication and duodenal ulcer healing. Curr Med Resp Opin. 2004;20:1301-1307.
15. UYGUN A, KADAYIFCI A, YESILOVA Z, et al. Recent success of pantoprazole- or lanzoprazole-based clarithromycin plus amoxicillin treatment in the erradication of Helicobacter pylori. Turk J Gastroenterol.2004;15:219-224.
16. BUSSALLEU A, PINTO JL, HUERTA-MERCADO J, CEDRÓN H, DE LOS RÍOS R, PISCOYA A, COK J, MENDOZA G. Evaluación de dos nuevos esquemas de terapia triple para el tratamiento de la infección por Helicobacter pylori en el Hospital Nacional Cayetano Heredia. Libro de Resúmenes del XX Congreso Peruano de Enfermedades Digestivas, Noviembre del 2006, Lima-Perú.
17. MOAYYEDI P. Sequential regimens for Helicobacter pylori eradication. Lancet 2007;370:1010-2.
18. ZULLO A, DE FRANCESCO V, HASSAN C, MORINI S, VAIRA D. The sequential therapy regime for Helicobacter pylori erradication: a pooled data analysis. Gut. 2007;56:1353-7.
19. VIARA D, ZULLO A, VAKIL N, et al.
Sequential therapy versus standard triple-drug therapy for Helicobacter pylori eradication: a randomized trial. Ann Intern Med 2007;146:556-6320. DE FRANCESCO, MARGIOTTA M, ZULLO A, HASSAN C, TROIANI L, BURATTINI O, et al.
Clarithromycin-resistant genotypes and eradication of Helicobacter pylori. Ann Intern Med. 2006;144:94-100.21. MURAKAMI K, FUJIOKA T, OKIMOTO T, et al. Drug combination with amoxicillin reduce selection of clarithromycin resistance during Helicobacter pylori eradication therapy. Int J Antimicrob Agents. 2002;19:67-70.
22. NADIM S. JAFRI, CARLTON A. HORNUNG, COLLIN W. HOWDEN. Meta-analysis: Sequential Therapy Appears Superior to Standard Therapy for Helicobacter pylori Infection in Patients Naive to Treatment. Annals of Internal Medicine 2008, 148: 1-10.
23. TONG JL, RAN ZH, SHEN J, XIAO SD. Sequential therapy vs standard triple therapy for Helicobacter pylori infection: a meta-analysis. Journal of Clinical Pharmacy and Therapeutics (2009) 34, 41-53.
24. CHOI WH, PARK DI, OH SJ et al. Effectiveness of 10 day-sequential therapy for Helicobacter pylori eradication in Korea. Korean J Gastroenterol 2008;51:280-4.
25. SEZGIN O, ALTINTA E, NAYIR E, UÇBILEK E. A pilot study evaluating sequential administration of a PPI-Amoxicillin followed by PPI-Metronidazole-Tetracycline in Turkey. Helicobacter. 2007 Dec;12(6):629-32.
26. SOTO G, BAUTISTA CT, Roth DE, Gilman RH et al. Helicobacter pylori reinfection is common in Peruvian adults after antibiotic eradication therapy. J Infec Dis 2003; 188(9):1263-75.













