Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.31 n.3 Lima jul./set. 2011
ARTÍCULOS ORIGINALES
Uso de Cianoacrilato en la Terapia Endoscópica de Várices Gástricas: Experiencia en el Hospital Nacional Edgardo Rebagliati Martins del 2006 al 2010
Use of cyanoacrylate in the endoscopic therapy of gastric varices: experience in the National Hospital Edgardo Rebagliati Martins from 2006 to 2010
Ofelia Castillo1
; Fernando Palacios2 ; Max Yoza2 ; Carlos Contardo3 y César Soriano41 Médico residente del Departamento de Aparato Digestivo del Hospital Edgardo Rebagliati Martins. ESSALUD – Lima, Perú.
2 Médico asistente del Departamento de Aparato Digestivo del Hospital Edgardo Rebagliati Martins. ESSALUD – Lima, Perú.
3 Médico asistente del Departamento de Aparato Digestivo del Hospital Edgardo Rebagliati Martins. ESSALUD – Lima, Perú; y médico asistente de la Clínica "El Golf" – Lima, Perú.
4 Médico jefe del Dpto. del Aparato Digestivo del Hospital Nacional Edgardo Rebagliati Martins, EsSALUD, Lima, Perú.
RESUMEN
OBJETIVO: Evaluar el éxito terapéutico de la inyección de N-butil-2-cianoacrilato en el tratamiento de las várices gástricas. MATERIALES Y MÉTODOS: Estudio transversal que incluyó 33 pacientes con várices gástricas que sólo recibieron terapia endoscópica con cianoacrilato entre el 2006 al 2010. El cianoacrilato fue inyectado intravaricealmente en una dilución 1:1 con lipiodol hasta obtener la obturación de las várices. La situación terapéutica fue: Hemorragia activa, várices con estigmas de sangrado reciente y profilaxis secundaria. El éxito del tratamiento se evaluó según la hemostasia, recurrencia de sangrado y obturación. RESULTADOS: De los 33 pacientes, 3 (9.1%) fueron por hemorragia activa, 20 (60.6%) con estigmas de sangrado reciente y 10 (30.3%) como profilaxis secundaria. Las várices fueron GOV2, 17 (51.5%); IGV1, 14 (42.4%) y GOV1, 2 (6.1%). Se logró hemostasia total en 21 (91.3%) pacientes con sangrado agudo o reciente y en 2 (66.7%) de 3 sujetos con sangrado activo. En 5 (15.6%) pacientes hubo recurrencia de sangrado y 2 de ellos recibieron cianoacrilato con éxito de hemostasia. Se logró obturación en 25 (75.8%) del total de pacientes. Cuatro pacientes fallecieron, uno por fracaso del control de sangrado. La mayor severidad de clasificación Child-Pugh se relacionó con falla terapéutica (p=0.034). La complicación principal fue el sangrado post-inyección del cianoacrilato. CONCLUSIONES: Nuestros resultados favorecen el uso de cianoacrilato en el tratamiento de várices gástricas, con raras complicaciones mayores.
PALABRAS CLAVES: Várices gástricas; N-butil-2-cianoacrilato; terapia endoscópica.
ABSTRACT
OBJECTIVE: To evaluate the therapeutic success of the injection of N-butyl-2-cyanoacrylate in the treatment of gastric varices. METHODS: Cross-sectional study included 33 patients with gastric varices who only received cyanoacrylate endoscopic therapy between 2006 and 2010. Intravariceally, cyanoacrylate was injected in a 1:1 dilution with lipiodol until the obliteration of varices. The therapeutic situation was: active bleeding, varices with stigmata of recent bleeding and secondary prophylaxis. Treatment success was evaluated according to hemostasis, recurrent bleeding and obliteration. RESULTS: Of the 33 patients, 3 (9.1%) were for active bleeding, 20 (60.6%) with stigmata of recent bleeding and 10 (30.3%) as secondary prophylaxis. Gastric varices were GOV2, 17 (51.5%); IGV1, 14 (42.4%); GOV1, 2 (6.1%). Hemostasis was achieved in 21 (91.3%) and in 2 (66.7%) of 3 patients with active bleeding. Five (15.6%) patients had recurrent bleeding and 2 of them used cyanoacrylate with successful hemostasis. Obliteration was achieved in 25 (75.8%). Four patients died and one for failure of control bleeding. A high severity of Child-Pugh classification was related to treatment endoscopic failure (p=0.034). The main complication was bleeding after the injection of cyanoacrylate. CONCLUSIONS: Our results support the use of cyanoacrylate in the treatment of gastric varices with few major complications.
KEYWORDS: Gastric varices, N-butyl-2-cyanoacrylate, endoscopic therapy.
INTRODUCCIÓN
Las várices gástricas son una complicación de la hipertensión portal y se presentan aproximadamente en el 20% de los pacientes (1). El conocimiento es incompleto acerca de su historia natural y fisiopatología que es diferente al de las várices esofágicas. Además, la heterogeneidad anatómica de las várices gástricas determina diferencias en las opciones terapéuticas. La clasificación de Sarin (2) luego recomendada por los consensos de Baveno III, IV y V, recoge estos diferentes tipos que permiten un manejo terapéutico diferenciado. La recomendación actual es tratar las várices gástricas fúndicas (IGV1 o GOV2, de la clasificación de Sarín) con el adhesivo tisular N-butil-2 -cianoacrilato (3) que se considera la terapia de elección tanto para el sangrado agudo como para la prevención secundaria de la hemorragia por várices gástricas, (Grado de recomendación 1b: A).
A pesar del amplio uso y excelentes resultados de la inyección de cianoacrilato en el sangrado de várices gástricas, existen diferencias en la literatura en relación a la técnica, seguridad y resultados a largo plazo. La mayoría de los estudios se han realizado en Asia y es necesaria la validación de esta intervención terapéutica en el Perú. Por ello, el objetivo fue evaluar el éxito de la terapia endoscópica de várices gástricas con cianoacrilato en el Hospital Nacional Edgardo Rebagliati Martins e identificar las complicaciones luego del tratamiento durante el período 2006 al 2010.
MATERIAL Y MÉTODOS
El tipo de estudio fue observacional, transversal y analítico.
Población: Pacientes con diagnóstico de várices gástricas que recibieron terapia endoscópica con N-butil-2-cianoacrilato en la Unidad de Hemorragia Digestiva (UHD) del Hospital Nacional Edgardo Rebagliati Martins (HNERM) desde el 01 de enero del 2006 hasta el 31 de diciembre del 2010.
Criterios de inclusión:
-
Pacientes mayores de 18 años.
-
Tratamiento endoscópico de várices gástricas con cianoacrilato en situación de hemorragia activa y/o estigmas de sangrado reciente, así como tratamiento electivo de profilaxis secundaria.
Criterios de exclusión:
-
Ausencia del informe endoscópico sobre el tratamiento aplicado o descripción del tipo de várices gástricas según la clasificación de Sarin.
-
Incongruencia sobre el tipo de várices gástricas por dos endoscopistas con experiencia en manejo de várices gástricas.
-
Uso de agentes esclerosantes sobre várices gástricas.
-
Falta de controles endoscópicos y/o seguimiento por consultorio externo.
Se recolectaron las características clínicas, endoscópicas y resultados de la terapia endoscópica. La etiología de la hipertensión portal fue establecida por parámetros clínicos, bioquímicos y radiológicos. La función hepática en pacientes con cirrosis fue clasificada según la puntuación Child-Pugh Turcotte. También se registró el tratamiento de várices esofágicas anterior o posterior a la terapia de várices gástricas.
Clasificación de várices gástricas: Según Sarín (2): (a) Várices Esófago-Gástricas (GOV): Prolongación de las várices esofágicas hacia el estómago por la curvatura menor (GOV1) o por la curvatura mayor hacia el fondo gástrico (GOV2); y (b) Várices Gástricas Aisladas (IGV): En ausencia de várices esofágicas y ubicadas en el fondo gástrico (IGV1) o ectópicas (IGV2).
Según el tamaño (4): Tortuosa, menores de 10 mm; Nodular, entre 10 y 20 mm; y Pseudotumoral, mayores de 20 mm; las várices difusas fueron referidas a cordones varicosos pequeños (menores de 5 mm), recorriendo el fondo gástrico y no circunscritas.
Situación terapéutica: (1) Hemorragia activa: Sangrado "a chorro" o "rezumante" visualizado endoscópicamente; (2) Várices gástricas con estigmas de sangrado reciente: Presencia de hematemesis o melena, con o sin caída del hematocrito, pero con signos endoscópicos de sangrado reciente como tapón de fibrina (signo del "pezón blanco"), coágulo adherido o erosión; y (3) Tratamiento electivo: Profilaxis secundaria luego de un episodio de sangrado.
Éxito de la terapia endoscópica con cianoacrilato: Se evaluó en términos de hemostasia, recurrencia de sangrado y obturación de las várices gástricas.
Se consideró hemostasia a la ausencia de sangrado clínica y/o endoscópicamente detectable luego de la inyección de cianoacrilato en pacientes con hemorragia activa o con estigmas de sangrado reciente, en estos últimos se empleó el término de "hemostasia tardía". En episodios de recurrencia de sangrado, también se evaluó el éxito de hemostasia con retratamiento de cianoacrilato.
Según el consenso de Baveno V (3), la recurrencia de sangrado fue definida como sangrado activo o estigmas de sangrado endoscópico proveniente de la várice inyectada o várices contiguas, luego del quinto día de un episodio de hemorragia tratada con cianoacrilato. La recurrencia fue temprana si se produjo en los primeros 30 días y tardía, posterior al mes del tratamiento.
La obturación de várices gástricas fue definida como várices firmes no colapsables al tacto con el uso del inyector o pinza de biopsia cerrada y la erradicación se refiere a la no visualización de várices gástricas patentes.
Se consideró éxito del tratamiento cuando se logró hemostasia y no hubo recurrencia del sangrado o éste fue confirmado en una localización diferente a la várice obturada, y con controles endoscópicos que confirmen obturación o erradicación de várices gástricas. En pacientes que recibieron profilaxis secundaria y no presentaron recurrencia de sangrado, también se calificó como éxito terapéutico.
La falla del tratamiento fue definida de acuerdo al consenso de Baveno V (6) como fracaso en el control del sangrado, cuando no se consigue hemostasia definitiva en un período de cinco días con necesidad de cambiar la terapia; y fracaso de la profi laxis secundaria, en presencia de recurrencia de sangrado con hematemesis, caída del hematocrito mayor a 9% o desarrollo de shock hipovolémico. Algunos pacientes reciben TIPS (shunt portosistémico intrahepático transyugular) y otros a pesar de esto fallecen, esto último es mortalidad por falla de tratamiento.
Terapia endoscópica:
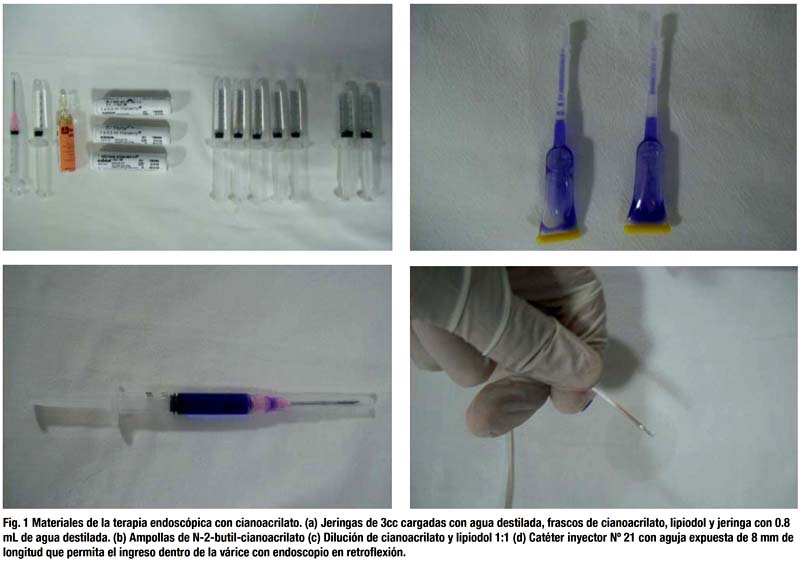
Materiales y equipo (Fig. 1):
-
N-butil-2 cianocrilato (Histoacryl®) en ampollas de 0.5 mL que contienen 0.5g de embucrilato (Laboratorio B| Braun Sharing Expertise; Distribuidora Química Suiza, Lima – Perú). Es un monómero en forma líquida que en contacto con iones hidroxilo de agua o sangre se polimeriza formando un acrílico que produce obturación inmediata de la várice esófago-gástrica.
-
Lipiodol ® ultrafluído como medio de contraste en ampollas de 10 mL, que contiene aceite de adormidera yodado al 40% (Laboratoire Guerbet, Francia; Distribuidora Cardio Perfusión, Lima - Perú). Demora el tiempo de polimerización del cianoacrilato hasta 20 seg. y permite el control radiológico.
-
Aguja y catéter de escleroterapia Nº 21.
-
Jeringas de 3 mL (diez), agua destilada, silicona.
-
Video endoscopio de visión frontal con canal terapéutico estándar.
-
Camilla de paciente en posición estándar y trendelemburg invertido.
-
Gafas, mascarilla, guantes quirúrgicos e indumentaria endoscópica.
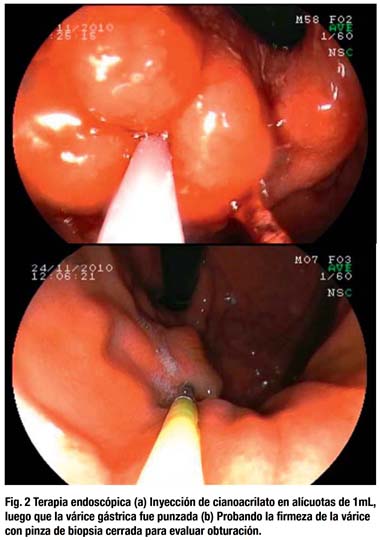
Técnica endoscópica (Fig. 2): El canal de trabajo y la punta del endoscopio fueron lubricados con silicona o lipiodol. Antes del procedimiento, se midió el espacio muerto del catéter de inyección (± 0.8 – 1.5 mL, según el tipo de catéter), luego fue cebado con agua destilada y no se cargó con cianoacrilato hasta que la várice gástrica fuera punzada. La dilución de Histoacryl® con lipiodol fue en proporción 1:1, con 0.5 mL de cada componente, en una jeringa de 3 mL, en algunos casos se empleó más de una ampolla de cianoacrilato. A juicio del endoscopista, se seleccionaba la várice y se inyectaba 1 a 4 mL de la dilución de acuerdo al tamaño de la várice, en alícuotas de 1 mL, seguidas inmediatamente de 0.8 - 1.5 mL de agua destilada para liberar todo el adhesivo desde el catéter hacia la várice gástrica. La aguja fue luego retraída, seguida de la instilación de agua para mantenerla patente. La inyección intravariceal se realizó en la proximidad del punto de sangrado y se terminaba cuando las várices se tornaban "hinchadas". La obturación fue evaluada probando la firmeza de la várice con el catéter con la aguja inyectora retraída. Si las várices permanecían "blandas", entonces se repetía la inyección hasta lograr la obturación. Hubo pocas variaciones en la técnica endoscópica entre los gastroenterólogos.
Estadística:
Se utilizó el paquete estadístico STATA® versión 11.1 (Copyright 2009, StataCorp LP, USA 2009). Se empleo análisis descriptivo calculando medidas de tendencia central y de dispersión. Las proporciones de los resultados del tratamiento endoscópico fueron descritas con intervalo de confianza al 95%. Para el análisis bivariado se realizo una Prueba exacta de Fisher (X2) para variables categóricas y una prueba de T de Student para las variables continuas (p<0.05).
Aspectos éticos:
El estudio fue conducido de acuerdo a los principios éticos de la Declaración de Helsinski en el marco del respeto de la confidencialidad de información.
RESULTADOS
En la UHD del hospital se registraron 239 casos de sangrado digestivo por várices gástricas entre el 01 de enero del 2006 al 31 de diciembre del 2010, que constituyeron el 5.7% de los ingresos por hemorragia digestiva alta. Sesenta pacientes recibieron tratamiento endoscópico de várices gástricas con cianoacrilato, pero se encontraron historias clínicas con informes endoscópicos completos de 53 sujetos, 12 fueron referidos de provincia, y se excluyeron 20 pacientes por recibir escleroterapia en algunos episodios de sangrado. Se realizaron 48 procedimientos de inyección del cianoacrilato en 33 pacientes y la mayoría por tres endoscopistas del hospital.
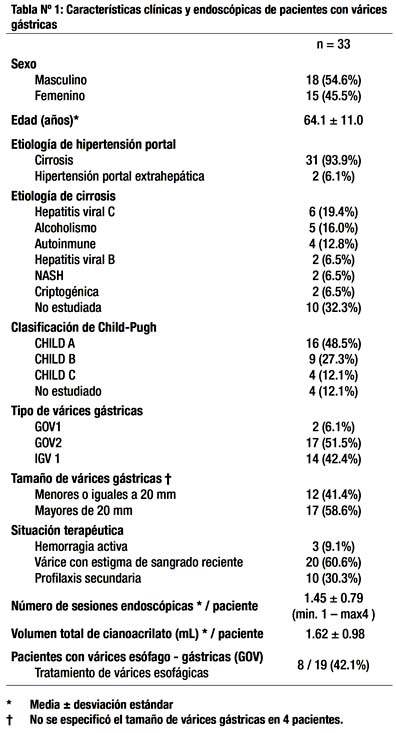
Las características clínicas y endoscópicas de los pacientes se muestran en la tabla Nº 1. De los 33 pacientes, 18 (54.6%) fueron varones y 15 (45.5%) mujeres, con edad promedio de 64.1 ± 11.0 (DS) años. La etiología más común de hipertensión portal fue cirrosis en 31 (93.9%). La distribución según el tipo de várices gástricas fue: Várices esófago-gástricas en 19 (57.6%) pacientes, la mayoría GOV2 en 17 (51.5%); y várices gástricas aisladas (todas del tipo IGV1) fueron 14 (42.4%). La principal indicación terapéutica fue por várices con estigmas de sangrado reciente en 20 (60.6%) pacientes, y luego como profilaxis secundaria en 10 (30.3%). Sólo hubieron 3 (9.1%) sujetos con hemorragia activa que recibieron tratamiento con cianoacrilato.
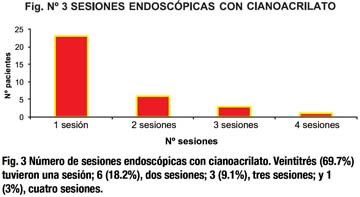
Diecisiete (58.6%) pacientes presentaron várices gástricas pseudotumorales y el volumen total de cianoacrilato inyectado por cada paciente fue 1.62 ± 0.98 (DS) mL (aproximadamente 3 ampollas). La mayoría (69.7%) tuvo una sesión endoscópica (Fig.3). De 19 pacientes con várices esófago – gástricas (GOV), 8 (42.1%) recibieron tratamiento endoscópico de várices esofágicas (escleroterapia y/o endoligadura), y en 4 de ellos antes de la terapia de várices gástricas. El antecedente de tratamiento endoscópico de várices esofágicas previo a las gástricas, realizado en el hospital de origen, fue observado en 2 pacientes con várices tipo IGV1.
Los resultados del tratamiento de várices gástricas con cianoacrilato se resumen en la Tabla Nº 2. Se logró hemostasia total en 21 pacientes (91.3%), aunque fue menor en sangrado activo (2 de 3 pacientes). La recurrencia de sangrado se observó en 5 (15.6%) y fue tratada con cianoacrilato en 2 de ellos con éxito de hemostasia. Una paciente con recurrencia de sangrado por várices gástricas IGV1 difusas recibió TIPS y los otros dos pacientes no fueron referidos oportunamente al hospital. Cuatro (80%) pacientes tuvieron un episodio de recurrencia de sangrado, y un sujeto presentó dos episodios que fueron manejados en su hospital de origen. Sólo hubo un episodio de recurrencia temprana que se presentó a los 21 días.
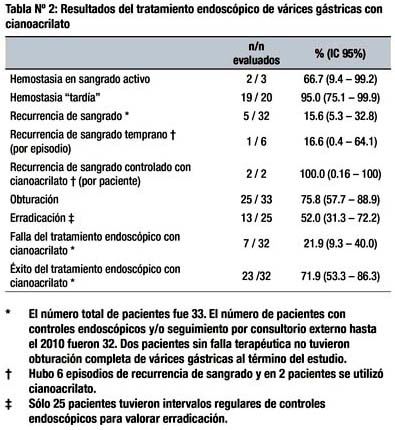
La obturación con cianoacrilato se alcanzó en el 75.8% de los sujetos. El éxito del tratamiento con cianoacrilato se obtuvo en 23 (71.9%) y se excluyó un paciente que sólo tuvo controles endoscópicos hasta el 2008. Hubo 7 pacientes con falla del tratamiento, siendo 2 (28.6%) por fracaso del control del sangrado y el restante por falla en la profilaxis secundaria.
En el análisis bivariado no se observó relación de trombosis de vena porta, hepatocarcinoma, situación terapéutica y tipo de várices gástricas con recurrencia de sangrado o falla de tratamiento (p > 0.05), pero no se realizó ecografía doppler portal en 9 pacientes. La distribución de Child-Pugh en aquéllos con falla de tratamiento fue: A, 1 (14.3%); B, 2 (28.6%); C, 3 (48.9%) y no estudiado en 1 (14.3%); mientras que, en los pacientes que no presentaron falla luego de la terapia con cianoacrilato fue: A, 14 (56%); B, 7 (28%); C, 1 (4%) y no estudiado en 3 (12%) (p=0.034). El antecedente de várices esofágicas no se relacionó con recurrencia de sangrado (p=0.261) o fracaso del tratamiento con cianoacrilato (p=0.218). Dos pacientes con episodios de recurrencia por várices gástricas habían recibido terapia endoscópica de várices esofágicas antes del uso de cianoacrilato en las gástricas.
Las complicaciones se presentaron en 9 pacientes y fueron principalmente sangrado post-inyección de cianoacrilato que cedieron inmediatamente, en un paciente se presentó hemorragia significativa que requirió cirugía (Tabla Nº 3). El promedio de unidades de paquete globular transfundidas fue 1.94 ± 2.37 (DS) y se necesitó hasta 10 unidades en hemorragia activa.

Durante el período de estudio fallecieron 4 pacientes y la mortalidad estuvo relacionada a falla de tratamiento con cianoacrilato en tres sujetos, uno debido a fracaso del control del sangrado. Se registró fallecimiento en el contacto telefónico realizado para el control endoscópico en tres pacientes.
DISCUSIÓN
El Hospital Nacional Edgardo Rebagliati Martins es un centro de referencia de tercer nivel que provee atención médica y quirúrgica a millones de habitantes de Lima y ciudades cercanas con diversas procedencias geográficas y étnicas. En el período del 2006 al 2010, el 5.7% de sangrado digestivo alto fue por várices gástricas y el 21.5% fue debido a várices esofágicas La hemorragia por ruptura de várices gástricas es menos frecuente que las várices esofágicas, y aunque sólo el 25% de las várices gástricas sangran antes de su diagnóstico o durante el seguimiento (2), generalmente es más grave y con mayor tendencia a la recurrencia.
La mayoría de los trabajos publicados, con excepción de tres estudios americanos (5, 6,7), han examinado cohortes del sureste de Asia e India y señalan que las várices gástricas son más frecuentes en pacientes con hipertensión portal extrahepática (2). Según Sarín (2) el tipo GOV1 son las más frecuentes (74%), mientras GOV2, IGV1 e IGV2 constituyen el 18%, 8% y 2% respectivamente. Nosotros hallamos a la cirrosis como principal causa de hipertensión portal en pacientes con várices gástricas que recibieron cianoacrilato y la mayoría fueron Child-Pugh A o B (75.8%). Debido a la selección de los pacientes, ya que sólo fueron incluidos aquéllos tratados con cianoacrilato, las várices GOV2 e IGV1 representaron el 93.9% y la baja prevalencia de várices GOV1 se atribuye a que generalmente no reciben terapia con adhesivo tisular, excepto si persiste el sangrado a pesar del tratamiento (escleroterapia o endoligadura) de várices esofágicas-gástricas.
También es necesario distinguir las várices gástricas primarias y secundarias; estas últimas aparecen después de escleroterapia o ligadura de várices esofágicas. Entre 10% y 20% de los pacientes desarrollan várices gástricas evidentes luego de la erradicación de várices esofágicas (8,9). Se reportaron seis pacientes con várices gástricas (dos tipo IGV1) que tuvieron antecedente de terapia endoscópica de várices esofágicas; sin embargo, por ser un estudio retrospectivo, no se puede atribuir al tratamiento previo como etiología de várices gástricas secundarias.
La inyección intravariceal de cianoacrilato que se solidifica dentro de la variz formando un molde que interrumpe el flujo y promueve la trombosis, se denomina "obturación de várice gástrica" (OVG). Este molde es expulsado al lumen gástrico luego de semanas o meses de la inyección, originando una ulceración tardía y fibrosis de la zona (10). Dos ensayos randomizados han demostrado que es superior a la escleroterapia (EVG) (10,11) y la ligadura endoscópica (ELVG) en el control inicial de la hemorragia (90% OVG vs. 62% EVG y 40% ELVG) (12). Múltiples series no controladas muestran una tasa de hemostasia inicial que supera el 90% con cianoacrilato (1,13,14) y la tasa de recurrencia temprana varía entre 0 y 30%, al igual que la erradicación de las várices gástricas entre 50 y 75% (15,16,17). Actualmente la terapia endoscópica con N-butil-2 cianoacrilato es recomendada para hemorragia activa y profi laxis secundaria por várices IGV1 y GOV2 (1b: A) (3); sin embargo, existen variaciones en la técnica y en las definiciones de hemostasia y recurrencia de sangrado en los diferentes estudios.
Nosotros consideramos los criterios según el consenso de Baveno V y encontramos una hemostasia total de 91.3% similar a lo reportado. En sangrado activo fue 66.7%, debido a que el procedimiento representa un desafío para los endoscopistas que tienen un limitado campo visual endoscópico y pobre colaboración del paciente. La recurrencia de sangrado (15.6%) se encontró dentro del límite estimado y los episodios de recurrencia temprana fueron 16.6%. La tasa de recurrencia temprana varía entre 0 – 15% (15), debido a que el cianoacrilato permanece dentro de la várice hasta por un año con mínima ulceración, pero cuando se produce la extrusión (salida del acrílico) puede haber sangrado tardío. También se relaciona con la falta de obturación del 100%, ya que al tercer día la necrosis de la mucosa descubre las várices gástricas remanentes (10). En Brasil (18) en un reporte de 23 casos de profi laxis secundaria de várices gástricas con cianoacrilato se obtuvo 87% de obturación con 4.3% de recurrencia de sangrado.
La eficacia del cianoacrilato también depende del patrón hemodinámico, vasos aferentes y eferentes, flujo sanguíneo y dirección (19,20). La obturación de várices gástricas difusas generalmente es incompleta por su compleja estructura vascular (19). Por ello ante la presencia de sangrado por várices gástricas difusas recomendamos la posibilidad de colocación de TIPS.
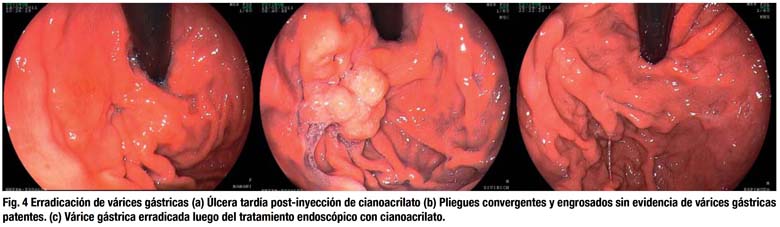
Es difícil estimar la erradicación de las várices gástricas porque el cianoacrilato generalmente permanece por semanas, luego se produce la extrusión con la formación de una úlcera y en algunos pacientes disminuye de tamaño sin ulceración o se forman pliegues convergentes (Fig.4). Las tasas de erradicación y obturación de várices gástricas fueron semejantes a lo publicado (1,13).
La mortalidad por fracaso del control de sangrado en un paciente con várices GOV1 fue debido a difi cultad técnica para afrontar con equipo en retroversión por la localización yuxtacardial de las várices.
Los factores de riesgo relacionados con el sangrado son: tamaño mayor de 5 mm, tipo de várices gástricas, presencia de signos rojos y CHILD C (21). Nosotros hallamos que la mayor severidad de Child-Pugh se relacionó con falla del tratamiento. Sin embargo, el tamaño muestral y diseño metodológico no permiten establecer asociaciones definitivas.
Los resultados del tratamiento endoscópico de várices esofágicas sobre las várices gástricas han sido poco explorados y contradictorios. En presencia de GOV1/2, se ha recomendado erradicar primero las várices esofágicas y, luego de 6 meses, evaluar la indicación de tratar las várices gástricas persistentes (1). Otra alternativa es tratar tanto las várices esofágicas como las gástricas desde el comienzo. Esto deberá evaluarse en futuros estudios prospectivos.
Seewald y col (15) describen una técnica estandarizada de inyección del cianoacrilato con dilución de 0.5 / 0.8 e inyección intravariceal en alícuotas de 1 mL, consiguiendo menor recurrencia de sangrado al obturar las tributarias de las várices gástricas. Nosotros empleamos la dilución de 0.5 mL de cianoacrilato con 0.5 mL de lipiodol ó de 1/1; esta última en várices pseudotumorales que tienen mayor frecuencia de shunts portosistémicos espontáneos y mayor riesgo de embolización si uno retarda la solidificación del cianoacrilato con mayor dilución.
Las complicaciones asociadas a la inyección de cianoacrilato son infrecuentes pero potencialmente graves e incluyen fiebre, trombosis e infarto esplénico, absceso retroperitoneal y embolia portal o sistémica en 3 – 4.3% (22,23). El riesgo de embolización no depende del volumen total de cianoacrilato por sesión sino por alícuota y de la velocidad de la inyección. La embolización es mayor en pacientes con shunt o síndrome hepatopulmonar. Algunos autores postulan que el uso de cianoacrilato sin dilución en lipiodol se asocia a menos tasa de embolizaciones como una técnica segura y efectiva en el manejo de sangrado (24).
Las complicaciones menores pueden estar poco documentadas y eso explica la ausencia de fiebre y tos. La bacteremia está reducida en la era de uso rutinario de profi laxis antibiótica en pacientes con sangrado de várices esófago-gástricas. La complicación más frecuente fue el sangrado post-inyección que cedía con aplicación de cianoacrilato y la embolización sintomática no fue reportada; sin embargo, no se realizaron radiografías sistemáticas. Para evitar el sangrado por úlcera tardía post-cianoacrilato, los pacientes recibieron inhibidores de bomba de protones (omeprazol) o antagonistas de receptores de Histamina 2 (ranitidina) (10).
Todos los pacientes que se presentaron con hemorragia de várices gástricas recibieron resucitación con fluídos, profilaxis antibiótica con cefalosporina de tercera generación o quinolona (ciprofl oxacino) endovenosa y un agente vasoactivo como octreótide o terlipresina antes del procedimiento terapéutico. Además, los pacientes recibieron transfusión sanguínea en su hospital de origen lo que explicaría la evolución favorable de la mayoría.
Serpa H. (25) reportó los primeros 10 casos de várices gástricas tratados en el Perú, en una clínica privada, durante 1997 y 1998, usando una técnica "combinada" (26) de cianoacrilato y esclerosante con resultados similares a la literatura mundial. En el Hospital Nacional Edgardo Rebagliati Martins se comenzó a realizar la obturación de várices gástricas con cianoacrilato en el 2000; sin embargo la técnica se estandarizó desde el 2005. Este estudio preliminar ha analizado desde el año 2006 con el objetivo de homogenizar los criterios de clasificación de várices gástricas y el desarrollo de la curva de aprendizaje de la técnica endoscópica por los gastroenterólogos del hospital.
La principal limitación es el diseño transversal con una muestra pequeña. Además, el estudio retrospectivo incluye interpretación de los informes endoscópicos y diferencias interobservador (entre endoscopistas). Sin embargo, el período de estudio es suficiente para detectar complicaciones mayores y recurrencia de sangrado. Se recomienda en futuros estudios prospectivos valorar el éxito terapéutico con el uso de guías de manejo de várices gástricas. En pacientes con sangrado activo se observó menor hemostasia, por ello se recomienda vigilancia endoscópica estrecha.
A pesar de la restricción por el pequeño número de pacientes, nuestros resultados favorecen el uso de cianoacrilato en el sangrado y profilaxis secundaria de várices gástricas con raras complicaciones inmediatas y tardías. Con apropiada experiencia es posible adoptar esta terapia endoscópica como primera elección en el tratamiento de várices gástricas en el Perú.
REFERENCIAS
1. RYAN B, STOCKBRUGGER R, RYAN J. A pathophysiologic, gastroenterologic, and radiologic approach to the management of gastric varices. Gastroenterology 2004; 126: 1175-89.
2. SARIN S K, LAHOTI D, SAXENA S P, MURTHY S, MAKWANA U K. Prevalence, classification and natural history of gastric varices: a long-term follow-up study in 568 portal hypertension patients. Hepatology 1992; 16: 1343-9.
3. DE FRANCHIS R. Revising consensus in portal hypertension: Report of the Baveno V consensus workshopon methodology of diagnosis and therapy in portal hypertension. Journal of Hepatology 2010; 30(60): 1-7.
4. HASHIZUME M, KITANO S, YAMAGA H et al. Endoscopic classification of gastric varices. Gastrointest. Endosc. 1990; 36: 276–80.
5. GREENWALD BD, CALDWELL SH, HESPENHEIDE EE, et al. N-2-butylcyanoacrylate for bleeding gastric varices: A United States pilot study and cost analysis. Am J Gastroenterol 2003;98:1982-8.
6. CALDWELL SH, HESPENHEIDE EE, GREENWALD BD, NORTHUP PG, PATRIE JT. Enbucrilate for gastric varices: extended experience in 92 patients. Aliment Pharmacol Ther 2007;26:49-59.
7. RENGSTORFF DS, BINMOELLER KF. A pilot study of 2-octyl cyanoacrylate injection for treatment of gastric fundal varices in humans. Gastrointest Endosc 2004;59: 553-8.
8. DE BK, GHOSHAL UC, DAS AS, NANDI S, MAZUMDER DN. Portal hypertensive gastropathy and gastric varices before esophageal variceal sclerotherapy and after obliteration. Indian J Gastroenterol 1998;17:10–12.
9. SARIN SK, JAIN AK, LAMBA GS, GUPTA R, CHOWDHARY A. Isolated gastric varices: prevalence, clinical relevance and natural history. Dig Surg 2003; 20: 42–47.
10. WANG YM, CHENG LF, LI N, WU K, ZHAI JS, WANG YW. Study of glue extrusion after endoscopic N-butyl-2- cyanoacrylate injection on gastric variceal bleeding. World J Gastroenterol 2009; 15(39): 4945-4951.
11. MALUF-FILHO F, SAKAI P, ISHIOKA S, et al. Endoscopic sclerosis versus cyanoacrylate endoscopic injection for the first episode of variceal bleeding: a prospective, controlled and randomized study in Child-Pugh class C patients. Endoscopy 2001;33:421-7.
12. LO GH, LAI KH, CHENG JS, et al. A prospective, randomized trial of butyl cyanoacrylate injection versus band ligation in the management of bleeding gastric varices. Hepatology 2001;33: 1060-4.
13. IRANI S, KOWDLEY K, AND KOZAREK R. Gastric varices: An updated review of management. WGO Review article. J Clin Gastroenterol 2011; 45:133–148.
14. HASHIZUME M, AKAHOSHI T AND TOMIKAWA M. Management of gastric varices. Journal of Gastroenterology and Hepatology 2011; 26 (Suppl. 1): 102–108.
15. SEEWALD S, LEONG T, IMAZU H, NAGA M, OMAR S, GROTH S, SEITZ U, ZHONG Y, THONKE F, SOEHENDRA N. Standardized injection technique and regimen ensures success and safety of N-butyl-2-cyanoacrylate injection for the treatment of gastric fundal varices (with videos). Gastrointest Endosc 2008; 68: 447-54.
16. HUANG YH, YEH HZ, CHEN GH, et al. Endoscopic treatment for bleeding gastric varices by N-butyl2-cyanoacrylate (Histoacryl) injection: longterm effi cacy and safety. Gastrointest Endosc 2000;52:160-7.
17. MUMTAZ K, MAJID S, SHAH HA, et al. Prevalence of gastric varices and results of sclerotherapy with N-butyl 2 cyanoacrylate for controlling acute gastric variceal bleeding. World J Gastroenterol 2007;13: 1247-51.
18. PRATA F; PEREIRA E; ANDRADE G; SHIGUEO F; CELSO J; PAULO A. Endoscopic follow-up of cyanoacrylate obliteration of gastric varices. Arq. Gastroenterol. 2009; 46(1):81-4.
19. IWASE H, MAEDA O, SHIMADA M, TSUZUKI T, PEEK R, NISHIO Y et al. Endoscopic ablation with cyanoacrylate glue for isolated gastric variceal bleeding. Gastrointest Endosc 2001;53:585-92.
20. ZHAO L, HE W, JI M, LIU P, LI P. 64-row multidetector computed tomography portal venography of gastric variceal collateral circulation World J Gastroenterol 2010; 16 (8): 1003-1007.
21. KIM T, SHIJO H, KOKAWA H et al. Risk factors for hemorrhage from gastric fundal varices. Hepatology 1997; 25: 307–12.
22. TAN YM, GOH KL, KAMARULZAMAN A, et al. Multiple systemic embolisms with septicemia after gastric variceal obliteration with cyanoacrylate. Gastrointest Endosc 2002; 55:276-8.
23. KOK K, BOND RP, DUNCAN IC, et al. Distal embolization and local vessel wall ulceration after gastric variceal obliteration with N-butyl-2-cyanoacrylate: a case report and review of the literature. Endoscopy 2004; 36:442-6.
24. KUMAR A, SINGH S, MADAN K, KUMAR P , KUMAR S. Undiluted N-butyl cyanoacrylate is safe and effective for gastric variceal bleeding. Gastrointest Endosc 2010; 72: 721-7.
25. SERPA H, FIGUEROA R. Manejo del Sangrado agudo por várices esófago-gástricas. Resúmenes de comunicaciones libres al XVI Congreso Peruano de Enfermedades Digestivas. Revista de Gastroenterología del Perú 1998; 18 (Suplemento Nº 1): 63.
26. THAKEB F, SALAMA Z, SALAMA H et al. The value of combined use of N-butyl-2- cyanoacrylate and ethanolamine oleato in the management of bleeding esophagogastric varices. Endoscopy 1995; 358-364.
Correspondencia
Dra. Ofelia Castillo.
E-mail: brisaida2@yahoo.es













