Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.32 n.4 Lima oct./dic. 2012
REPORTE DE CASOS
Rebrote virológico en el tratamiento de hepatitis B con entecavir ¿resistencia?
Virological breakthrough in treating hepatitis B with entecavir. It means resistance?
Javier Díaz Ferrer(1), Ronald Arcana(2), Danni Quinte(1),Carla Bustios(1), Rossana Román(1), Milagros Dávalos(1), Eduardo Zumaeta(1)
1. Médico Asistente. Servicio de Hepatología. HNERM
2. Médico Residente. Servicio de Hepatología. HNERM
RESUMEN
Paciente varón de 45 años natural de Lima, casado con antecedentes de , múltiples parejas sexuales y operado de fimosis, que debuta con eritema nodoso y diagnosticado de hepatitis B crónica en Agosto del 2008, en controles por consultorio se realiza diagnóstico de cirrosis hepática child A y hepatocarcinoma. Inicia tratamiento para la hepatitis B con Entecavir 0,5mg y luego se realiza hepatectomía del segmento V, En Febrero 2009 en controles de imágenes se evidencia recidiva de hepatocarcinoma en el segmento VI (lesión de 14mm) con AFP de 68 ng/dl, se realiza etanolización, con evolución final favorable. Durante el seguimiento no se observa evidencia de recidiva de HCC, continua con Entecavir 0,5 mg /d y en abril 2010, luego de 72 semanas de tratamiento con adecuada adherencia al tratamiento presenta rebrote virológico (carga viral positiva de 646 UI/dl), y se decide agregar a la terapia Tenofovir. Actualmente paciente con buena evolución con última carga viral de Abril del 2012 negativa recibiendo terapia doble para VHB. Reportamos el caso por ser uno de los primeros en nuestro país de resistencia probable a Entecavir y donde se pone de manifiesto la necesidad de examenes complementarios que confirmen dicha sospecha.
PALABRAS CLAVE: hepatitis viral B, terapia antiviral, resistencia, Entecavir, rebrote virológico.
ABSTRACT
A 45 year- old – married man, with several sexual partners, initiated symptoms with nodosum erythema and in August 2008, is diagnosed of chronic hepatitis due to hepatitis B virus (HBV). Later he was diagnosed of Child A cirrhosis and hepatocarcinoma. He began HBV treatment with Entecavir 0,5 mg; then he underwent a V segment hepatectomy. In February 2009 he presented a relapse with a tumor of 14 mm on VI segment with AFP values of 68 ng/dl, so he underwent an ethanolization with good evolution. During the follow up, he has not presented evidence of relapse of hepatocarcinoma and continued with Entecavir 0,5 mg/d. In April 2010, after 72 weeks of therapy with good compliance, the patient presented a virological breakthrough (viral load 646 UI/dl) and Tenofovir was added to his therapy. Nowadays the patient is receiving double therapy for HBV and his last viral load, April 2012, was negative. This could be the first case in our country of a probable resistance to Entecavir; complementary tests are needed in order to rule out this suspicion.
KEY WORDS: Hepatitis B, Entecavir, Virological Breakthrough, resistance.
INTRODUCCIÓN
Aproximadamente un tercio de la población mundial tiene evidencia serológica de infección pasada o actual de hepatitis B y 350 millones de personas están crónicamente infectadas por el virus de hepatitis B. La morbilidad y mortalidad de esta enfermedad está asociada cercanamente a la replicación viral persistente y el consecuente desarrollo de cirrosis y hepatocarcinoma. Por tal motivo el tratamiento y la negativización de la replicación viral son objetivos primordiales en esta enfermedad. El tratamiento de la hepatitis B crónica ha mejorado significativamente en la ultimas décadas, debido principalmente a la disponibilidad de los nuevos análogos núcleos(t)idos, estos agentes son bien tolerados y suprimen adecuadamente la replicación viral, lamentablemente esta replicación continua cuando se suprime el tratamiento, por tal razón este debe ser administrado por un largo tiempo sino indefinidamente y desafortunadamente la terapia por largo tiempo con estas drogas genera el desarrollo de resistencia. La resistencia antiviral se debe al alto porcentaje de mutaciones que pueden ocurrir durante la replicación viral y a la selección de estos mutantes debido a la persistencia de replicación en presencia del agente antiviral (1,2). Los fármacos disponibles para su tratamiento son diversos, su mecanismo de acción es dispar y su eficacia no es absoluta, lo que conlleva a limitaciones notables. Por todo ello, decidir qué pacientes pueden beneficiarse del tratamiento, qué fármacos se deben utilizar y cuando se debe iniciar, cambiar o interrumpir el tratamiento es una decisión que puede ser difícil y debe basarse en los conocimientos actuales que tenemos de este virus y su tratamiento. Actualmente las drogas aprobadas para el tratamiento de la hepatitis B son: Interferon alfa-2b, Lamivudina, Adefovir, Peg Interferon alfa-2a, Entecavir, Telbivudina y Tenofovir, siendo los fármacos considerados de primera línea: El peginterferon alfa-2a, Entecavir, y Tenofovir, dado que estos agentes han demostrado superior eficacia tolerabilidad y un adecuado perfil de resistencia tanto en HBeAg-positivo y HB eAg-negativo. (3,6)
El mejor predictor de la respuesta sostenida a Lamivudina, Adefovir y Telbivudina es la respuesta virológica a las 24 y 48 semanas (No detectable por PCR en tiempo real), sin embargo la relación entre respuesta Virológica temprana, Entecavir y Tenofovir es menos clara y los reporte de resistencia son extremadamente raros en el corto plazo, reportandose resistencia al Entecavir < 1 % después de 2 años de tratamiento.(5). Para identificar resistencia es de suma importancia conocer la definición de respuestas en la terapia con análogos Nucleos(t)idos.
-
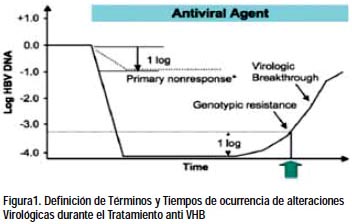
Respuesta virológica: es definida como HBV DNA in-detectable por PCR en tiempo real a la semana 48 del tratamiento.
-
No respuesta primaria. Se define por la caída del DNAVHB menor de 1 log10 UI/ml tras 6 meses de tratamiento.
-
Respuesta virológica parcial. Se define por la caída de DNA-VHB mayor de 1
log10 con persistencia de DNA-VHB detectable a las 24 semanas de tratamiento con lamivudina o telbivudina o bien a las 48 semanas de tratamiento con adefovir, entecavir o tenofovir. -
Rebrote virológico. Se define por un ascenso del DNAVHB superior a 1 log10 respecto al valor más bajo observado durante el tratamiento (nadir) (3,4,6).
El rebrote virológico puede ser debido a un mal cumplimiento terapéutico o a la aparición de mutaciones que confi eren resistencia al fármaco utilizado. El manejo de esta situación es variable en función del fármaco utilizado y del tipo de mutación emergente. Siendo el rebrote virológico una señal precoz de posible resistencia, es que reportamos el caso a fin de promover su revisión y sus consideraciones para el adecuado monitoreo y manejo.
CASO CLÍNICO
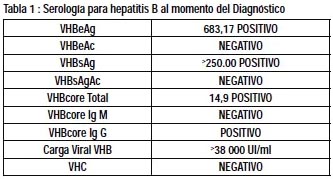
Reportamos el caso de un paciente varón de 45 años natural de Lima, casado con antecedentes de fi ebre tifoidea hace 20 años, sinusitis crónica desde hace 3 años, múltiples parejas sexuales y operado de fimosis 6 años antes de su ingreso, que debuta con eritema nodoso y es diagnosticado de hepatitis viral B crónica en agosto del 2008 y en controles por consultorio se le realiza el diagnóstico complementario de cirrosis hepática Child A (6 ptos) Meld 5 puntos. Al examen físico: lucido y orientado, Buen estado general, índice de masa corporal (IMC) de 29, pálido, telengiectasias en rostro y tronco, eritema palmar, en extremidades inferiores eritema en placas en ambas piernas, en los exámenes de laboratorio: grupo sanguíneo O positivo, hemoglobina 14,6 gr/dl plaquetas 130,000/mm, Leucocitos 3 930/mm TP 13,4 segundos INR 1,12 fibrinógeno 241 mg% proteínas totales 8,12 gr%.albúmina 3,48 g/dl globulina 4,6g/dl Bilirrubina total 0,78 mg% TGO/TGP 122/115 U/l fosfatasa alcalina 182 U/ml ,glucosa 94 mg% urea 22 mg% creatinina 0,76 mg% Na 138 mEq/L, alfa feto proteína (AFP) 41,8 ng/ml (valor normal de 0-10,9) Endoscopia digestiva Alta: no varices esofágicas, gastritis leve. Serología para hepatitis B en tabla 1
En noviembre 2008 inicia tratamiento para la hepatitis B con entecavir 0,5mg antiviral de amplia barrera genética y baja resistencia con una carga viral de >38 000 UI/ml, además por vigilancia de hepatocarcinoma se le encuentra AFP de 41,8 ng/ml y por ecografía y tomografía se observa nódulo de 18mm en segmento V hepático sin características típicas de hepatocarcinoma (HCC) por lo que se decide realizar biopsia hepática en la que se confirma el diagnóstico de hepatocarcinoma y cirrosis. Como opción terapéutica se decide por hepatectomia del segmento V, En febrero 2009 en controles de imágenes se evidencia recidiva de HCC, lesión de 14mm en el segmento VI con AFP de 68 ng/dl, por lo que se decide realizar etanolización en cinco sesiones, presentado adecuada evolución post etanolización. Se realiza evaluación pre trasplante, en otro nosocomio considerandolo no tributario de trasplante, después de valorar el compromiso microvascular en la pieza operatoria extraida.
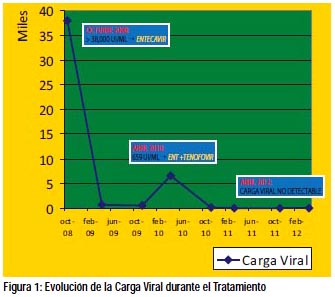
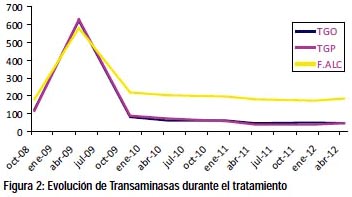
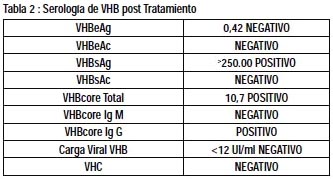
En controles posteriores por consultorio no se evidencia recidiva de HCC, continua tomando entecavir por VHB y en abril 2010, luego de 18 meses de tratamiento (72 semanas) con entecavir 0,5mg por día presenta carga viral de 646 UI/ml, después de haber tenido cargas virales de 66 UI/mly 60 UI/ml en los controles previos, siendo diagnosticado como rebrote virológico con alta probabilidad de resistencia a Entecavir y teniendo las opciones de rotar de antiviral o agregar otro, se decide agregar a la terapia Tenofovir 300mg/d medicación que continua tomando hasta la actualidad. Actualmente paciente estable con buena evolución clínica con ultima carga viral de Abril del 2012 negativa (<12 UI/ml limite inferior PCR tiempo real) y seroconversión del antígeno E (VHB AgE negativo) recibiendo terapia doble para VHB y con control de AFP de 4,2ng/dl sin recidiva de HCC. Reportamos el caso por ser uno de los primeros en nuestro país de Rebrote Viro-lógico con probable resistencia naive a entecavir en una etapa temprana del tratamiento
DISCUSIÓN
Un problema mayor en el tratamiento con AN (análogos Nucleos(t)idos) es la selección de mutaciones antiviralesresistentes, el porcentaje de mutaciones está relacionado al nivel sérico de DNA HBV, la rapidez de la supresión viral, la duración del tratamiento y la exposición previa a la droga (5,7-9).
La incidencia de resistencia genotípica tambien podría variar de acuerdo a la sensibilidad del método usado para su detección. De las terapias aprobadas con AN para hepatitis B, en pacientes nunca tratados, Lamivudina es la droga asociada con mayor tasa de resistencia en el mediano y largo plazo mientras que Entecavir y Tenofovir son las drogas con menores tasas de resistencia (10,11).
La primera manifestación de resistencia antiviral es el rebrote virológico(RV), más del 30 % de rebrotes viro-lógicos observados se deben principalmente a la falta de adherencia al tratamiento(4) y se ha podido demostrar que hasta 26% de los pacientes naive tratados con AN pueden presentar un episodio de RV durante los primeros años del tratamiento . El RV es usualmente seguido de un rebrote bioquímico, el cual es definido como una elevación de ALT durante el tratamiento en un paciente con respuesta bioquímica inicial. La aparición de resistencia antiviral conlleva a una alteración de la respuesta clínica inicial, en algunos casos reactivación de la hepatitis (flares) y descompensación hepática o muerte. Las mutaciones virales que confieren resistencia pueden ser detectadas meses y en algunos casos años antes de la reactivación o rebrote bioquímico, por ello es muy importante su identificación y la intervención oportuna que puede incluso evitar la generación de futuras resistencias cruzadas con otros antivirales.
En nuestro caso, El RV de nuestro paciente en una etapa relativamente temprana del tratamiento con un antiviral de alta barrera genética como el Entecavir, nos obliga a pensar en primer lugar que este podría deberse a falta de adherencia al tratamiento expresado en descontinuación o irregularidades en la toma del medicamento y esta posibilidad fue investigada con minuciosidad, negando el paciente en todo momento dichas sospechas, aunque debemos hacer mención, que el paciente recibió en todo momento Entecavir de 1mg, que el paciente partía para conseguir la dosis indicada de 0,5 mg/d (lo que podría llevar hipotéticamente a perdida de componente activo durante la partición). De tal modo que el plan siguiente a la investigación de la toma de la medicación, debiera ser evaluar e investigar resistencia antiviral.
En la práctica clínica no es necesario realizar un examen para evaluar resistencia de modo basal y sólo debería ser solicitado ante respuestas antivirales sub optimas antes de cambiar la terapia en pacientes con rebrote virológico o bioquímico, como en el caso de nuestro paciente.
Las guías y las opiniones de expertos coinciden en que se debe monitorear la aparición de resistencia a través de la valoración del DNA VHB sérico usando pruebas sensibles. Vigilancia de la resistencia con evaluación genotípica, no se recomienda de rutina por los altos costos y pobre disponibilidad, como hemos mencionado, pero debería ser solicitada ante la sospecha primaria de resistencia. Un monitoreo razonable sería la valoración de DNA VHB sérica de base y c/3 meses hasta que se haga indetectable y luego c/3-6 meses durante el mantenimiento del tratamiento, en nuestro medio a pesar de su baja sensibilidad ALT debería también ser monitoreada para identificar el rebrote bioquímico(3,4,6).
En nuestro caso debido a la falta de disponibilidad de pruebas que confirmen o descarten la resistencia y ante la sospecha clínica por ser un paciente que cumplía aparentemente con la medicación indicada y debido a la persistencia de viremia después de 48 semanas de tratamiento además de su condición de paciente cirrótico, se optó por adicionar inmediatamente una segunda droga de alta barrera genética como el Tenofovir, que no genere resistencias cruzadas, (3,6,12,13) Si bien es cierto que uno debería solicitar una nueva carga viral que confirmara el rebrote virológico, muchas veces esta posibilidad se ve diluida por problemas logísticos en nuestros hospitales que retardarán el tratamiento en algunos meses inclusive, en desmedro de posibles descompensaciones de la enfermedad hepática de fondo, particularmente si es cirrótico, que podría terminar en la muerte del paciente.
Decidimos reportar el caso a fin de poner en evidencia el problema que enfrentamos y enfrentaremos, con el advenimiento de nuevas drogas y su uso en el tratamiento de hepatitis B, a fin de tener en cuenta la necesidad no sólo de estas drogas, sino de exámenes de laboratorio complejos, como cargas virales y pruebas que valoren resistencia genotípica a fin de evitar el incremento significativo de resistencia por un mal uso de estos medicamentos.
REFERENCIAS
1. RICHMAN DD. The impact of drug resistance on the effectiveness of chemotherapy for chronic hepatitis B. Hepatology 2000;32:866-867.
2. MURRAY JM, PURCELL RH, WIELAND SF. The halflife of hepatitis B virions. Hepatology 2006;44:11171121.
3. LOK AS, MCMAHON BJ. Chronic hepatitis B: update 2009 (AASLD practice guidelines). Hepatology 2009;50:1-36.
4. HONGTHANAKORN CH, Chotiyaputta W, Oberhelman K, Fontana R J, Marrero J, Licari T, and Lok AS .Virological Breakthrough and Resistance in Patients with Chronic Hepatitis B Receiving Nucleos(t) ide Analogues in Clinical Practice. Hepatology 2011;53:1854-1863.
5. LOK AS, ZOULIM F, LOCARNINI S, BARTHOLOMEUSZ A, GHANY MG, PAWLOTSKY JM, et al. Antiviral drug-resistant HBV: standardization of nomenclature and assays and recommendations for management. Hepatology 2007;46:254-265.
6. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Management of chronic hepatitis B virus infection. Journal of Hepatology 2012 vol. 57. 167–185.
7. GHANY M AND DOO E. Antiviral Resistance and Hepatitis B Therapy. Hepatology 2009;49:S174-184.
8. PETERSEN J, RATZIU V, BUTI M, JANSSEN H, BROWN CH, LAMPERTICO P. Entecavir plus tenofovir combination as rescue therapy in pre-treated chronic hepatitis B patients: An international multicenter cohort study. Journal of Hepatology 2012 vol. 56 j 520–526.
9. YOSHIYASU KARINO ; JOJI TOYOTA ; HIROMITSU KUMADA ; YOSHIAKI KATANO ; NAMIKI IZUMI ; HARUHIKO KOBASHI ; MICHIO SATA ; MITSUHIKO MORIYAMA Efficacy and resistance of entecavir following 3 years of treatment of Japanese patients with lamivudine-refractory chronic hepatitis B. Hepatol Int (2010) 4:414–422
10. ZOULIM F. Antiviral therapy of chronic hepatitis B. Antiviral Res 2006;71: 206-15.
11.
ZOUTENDIJK R, REIJNDERS J, BROWN A, ZOULIM F, MUTIMER D, KATJA DETERDING, PETERSEN J. Entecavir Treatment for Chronic Hepatitis B: Adaptation Is Not Needed for the Majority of Naıve Patients with a Partial Virological Response. Hepatology 2011;54:443-45112. HOON AHN S; CHAN H ; PEI-JER CHEN ; JUN CHENG ; MAHESH K. GOENKA JINLIN HOU ; SENG GEE LIM ; MASAO OMATA. Chronic hepatitis B: whom to treat and for how long? Propositions, challenges, and future directions. Hepatol Int (2010) 4:386–395
13. LOCARNINI S, HATZAKIS A, HEATHCOTE J, KEEFFE EB, LIANG TJ, MUTIMER D, et al. Management of antiviral resistance in patients with chronic hepatitis B. Antivir Ther 2004;9:679-693.













