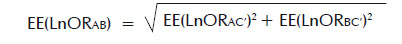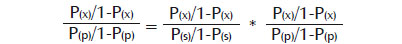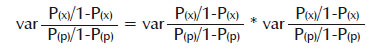Print version ISSN 1022-5129
Rev. gastroenterol. Perú vol.34 no.2 Lima Apr. 2014
Artículo de revisión
Introducción al meta-análisis indirecto
Introduction to the indirect meta-analyses
Rafael Bolaños Díaz1,2, María Calderón Cahua3
1 Unidad de Análisis y Generación de Evidencias en Salud Pública (UNAGESP), Instituto Nacional de Salud (INS). Lima, Perú.
2 Organización Médica para el Desarrollo de la Salud (ODDS PERU). Lima, Perú.
3 Universidad Peruana Cayetano Heredia. Lima, Perú.
RESUMEN Los meta-análisis son estudios que tienen la finalidad de compilar toda la información disponible, agrupándola según un tema específico y evaluándola a través de herramientas de calidad metodológica. Cuando existen comparaciones de dos tratamientos específicos basados en ensayos clínicos aleatorizados los meta-análisis tradicionales son la mejor opción, pero existen escenarios en donde no se dispone de suficientes estudios comparativos directos. En estos casos una opción a tomar en consideración son las comparaciones indirectas o meta-análisis indirectos. El objetivo de la presente revisión es comprender el fundamento conceptual, la necesidad, las aplicaciones y limitaciones de las comparaciones indirectas para el posterior entendimiento de los meta-análisis en red o network meta-análisis.
Palabras clave: Metanálisis; Ensayos clínicos aleatorios; Metodología (fuente: DeCS BIREME).
ABSTRACT Meta-analyses are studies that aim to compile all available information, grouping them according to an specific theme and evaluating it through methodological quality tools. When there are two specific comparisons of treatments based on randomized clinical trials, standard meta-analyses are the best option, but there are scenarios in which there is no available literature for those direct comparisons. In these cases, an alternative method to consider is indirect comparison or indirect meta-analyses. The aim of this review is to understand the conceptual foundations, the need, applications and limitations of indirect comparisons for further understanding of network meta-analyses.
Key words: Meta-analysis; Randomized controlled trials; Methodology (source: MeSH NLM).
INTRODUCCIÓN
Actualmente las revisiones sistemáticas (RS) con o sin meta-análisis (MA) se consideran las mejores fuentes de evidencia (1-3). Cuando se quiere responder una pregunta científica es ideal encontrar estudios que comparen exactamente los dos tratamientos o intervenciones que se quiere analizar. Sin embargo, lo que sucede en la práctica real es que muchas veces, especialmente al evaluar nuevos fármacos, es muy difícil encontrar ensayos clínicos aleatorizados (ECAs) que se hayan ejecutado específicamente para la comparación de interés. Esta situación conlleva a que el profesional de salud tenga que sustentar sus decisiones en ausencia de estudios con una comparación directa del desenlace de interés.
Cuando se realiza una búsqueda bibliográfica con el objetivo de encontrar información sobre dos tratamientos o intervenciones, es común encontrar ECAs que no comparan directamente las intervenciones que queremos evaluar, pero sí comparan en forma directa una de ellas frente a otro comparador, por ejemplo placebo (4).
Por lo antes descrito, en 1997 Bucher y cols. (5) propusieron un método para realizar comparaciones indirectas, en las que se podía hacer un análisis compilatorio. Este artículo fue central para el desarrollo de los MA indirectos de ECAs, que a su vez es el fundamento principal que sustenta la metodología del network meta-analysis o MA de comparación múltiple.
Es por esta razón que la presente revisión tiene como objetivo comprender el fundamento conceptual, la necesidad y limitaciones de las comparaciones indirectas.
Tipos de comparaciones indirectas
Las comparaciones directas se realizan cuando los ECAs encontrados analizan la misma comparación de interés (el análisis de éstos ya fue explicado en el apartado de Introducción al Meta-análisis Tradicional presentado en el número anterior de la revista), y para hacer más fácil el entendimiento de las comparaciones directas mostramos una representación gráfica en la Figura 1.

La figura muestra la comparación entre un tratamiento A y un tratamiento B. En este caso, los estudios que analizan esta comparación están disponibles y en caso se quisiera estimar el tamaño de efecto entre estos dos tratamientos se realizaría un MA tradicional.
Por otro lado, una comparación indirecta hace referencia a una comparación de dos tratamientos de interés pero a partir de estudios primarios que no hacen la comparación específica que buscamos (comparación directa) sino que comparan dichos tratamientos de manera independiente con un mismo tratamiento de control (que muchas veces es el placebo). Estas comparaciones pueden ser no-ajustadas o naive y ajustadas (6).
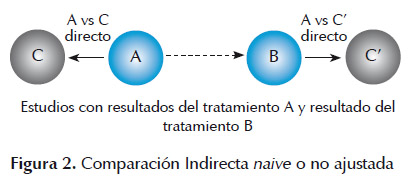
Las comparaciones indirectas naive o no-ajustadas comparan directamente los resultados de los brazos individuales de diferentes estudios como si se tratara de brazos de un mismo estudio, sin considerar la variabilidad del grupo control en los estudios directos individuales. Por ejemplo, si nosotros queremos saber cuál es la diferencia entre el tratamiento A y el tratamiento B para una enfermedad dada, asumiendo que sólo se dispone de ECAs de ambos tratamientos de manera independiente y frente a un mismo comparador C (que pudiera ser el placebo) y que no existen ECAs primarios que comparen directamente la eficacia de ambos tratamientos, se seguiría una comparación naive o no-ajustada si se analizaran directamente los resultados de A versus B sin considerar que a pesar de ser el mismo comparador C los sujetos y las condiciones de investigación de C en uno y otro estudio son distintas (a lo que diferenciamos como C). Una forma gráfica de representar este escenario se encuentra en la Figura 2. Aunque esta metodología ha sido descrita se sabe que no debería utilizarse porque conlleva a severos riesgos que amenazarían significativamente la calidad del análisis y las conclusiones (7).
Dado lo anteriormente descrito, Bucher y cols.(5) desarrollaron una metodología para realizar comparaciones indirectas ajustadas. En este tipo de comparación se toman los resultados de diferentes tratamientos ajustados de acuerdo a los resultados de una comparación directa con un control común, que en la mayoría de los casos, es el placebo. Siguiendo con el ejemplo anterior, tenemos el tratamiento A y el tratamiento B y queremos saber cuál de los dos es mejor para cierta enfermedad y no encontramos ECAs que evalúen la comparación directa. Sin embargo, como se observa en la Figura 3, encontramos estudios que comparan el tratamiento A contra el tratamiento C así como también estudios que comparan el tratamiento B contra el tratamiento C. En este caso, el MA directo en cada brazo puede hallar un efecto relativo entre A y C y también entre B y C, y estas medidas sí podrían compararse para tener un resultado indirecto entre el tratamiento A y el tratamiento B siempre que se ajuste la variabilidad de la eficacia de C para cada brazo independiente (es decir, C y C). Este tipo de comparación indirecta ajustada (o MA indirecto) tiene evidencia suficiente y consistente para tomarla como herramienta alternativa cuando no se dispone de ECAs directos entre los tratamientos de interés.
Asunciones
Es importante recalcar que para realizar un MA indirecto basado en comparaciones directas ajustadas a un comparador común, se requiere asunciones que se presentan a continuación:
1.
Similitud clínica y metodológica: Es ideal que el tipo de paciente, tratamiento, duración del seguimiento y en especial la medición de los resultados sean similares en cada estudio directo. Además, se debe tomar en cuenta que las covariables que puedan modificar el efecto relativo también sean similares en los estudios combinados. Los estudios que se combinan deben ser los adecuados y es por ello que hay que seguir los parámetros descritos para el MA tradicional, realizando una búsqueda apropiada, considerando posibles sesgos como el de publicación (8). 2. Consistencia: Si existen resultados de comparaciones directas y de comparaciones indirectas, estas deben tener la misma dirección, los resultados no pueden ser divergentes. En el caso exista inconsistencia se debe investigar el motivo ya sea falta de validez interna de los estudios, heterogeneidad elevada o sesgos de confusión (8).
3. Homogeneidad/Heterogeneidad: Como se describió en la revisión anterior del MA tradicional la heterogeneidad es la variabilidad entre los resultados de los estudios que componen un MA o en los brazos que conforman la comparación indirecta. Es decir, es la variabilidad del resultado medido en cada estudio con respecto al resultado global promedio (variabilidad estadística y no clínica). Se podría cuantificar a partir del Test de I2 .
Análisis
Una vez seleccionados los estudios que se van a comparar de modo indirecto es necesario combinar sus resultados. Como antes fue mencionado, el comparar medidas de resumen como Odds Ratio (OR) por separado es una práctica errónea (comparación indirecta naive o no-ajustada). Para hacer comparaciones indirectas ajustadas en donde la incertidumbre se encuentra en la comparación de los tratamientos A y B como se muestra en la Figura 2 se utilizará el método de Bucher (5).
En caso de querer hallar el OR de la comparación del tratamiento A y B. Se toma el logaritmo de las razones de los odds, es decir
ORAB = ORAC/ORBC
Al obtener el logaritmo natural se obtiene que,
Ln ORAB = Ln ORAC – Ln ORBC
Por lo tanto, la varianza indirecta será:
var (LnORAB) = var (LnORAC) + var (LnORBC)
o
EE(LnORAB)2 = EE(LnORAC)2 + EE(LnORBC)2
Y el Error Estandar (EE) será:
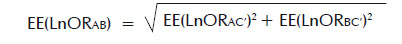
De esta forma se puede hallar el intervalo de confianza de la estimación puntual del OR para la comparación del tratamiento A frente al tratamiento B.
Una fortaleza importante de este análisis es que el método de comparación indirecta ajustada utiliza la magnitud del efecto informado en los ensayos controlados y aleatorizados que compararon por separado cada uno de los dos tratamientos frente a un comparador común. Cuando se hace una comparación indirecta ajustada, la fuerza de la aleatorización se mantiene parcialmente y las diferencias entre los tratamientos comparados indirectamente (debido a las diferencias de los pacientes en el tratamiento comparador común) es menos probable (9, 10). Más aún, la combinación de evidencia directa e indirecta en la evaluación de dos intervenciones puede brindar estimaciones más precisas al estrechar los intervalos de confianza en comparación con las estimaciones basadas únicamente en evidencia directa (10).
Hasselblad y cols. (11) describieron la estimación de la eficacia de un tratamiento experimental frente al placebo a partir de su comparación directa frente al tratamiento estándar, considerando que no todos los tratamientos experimentales pueden compararse directamente con el placebo por razones éticas (Figura 4). No obstante, la descripción metodológica de Hasselblad sirve de base para estimaciones indirectas distintas al OR.
De acuerdo a Hasselblad, el beneficio absoluto de una terapia experimental frente a una estándar puede fundamentarse mediante la Diferencia Absoluta (DA) estimada entre la tasa de eventos de la intervención experimental y la tasa de eventos de la intervención estándar, simbolizado de la siguiente manera:
P(x) – P(s)
(1)
Donde:
P(x): tasa de eventos con el tratamiento experimental
P(s): tasa de eventos con el tratamiento estándar
De igual modo, el beneficio absoluto de la intervención estándar frente al placebo estaría dado por:
P(s) – P(p)
. (2)
Donde:
P(s): tasa de eventos del tratamiento estándar
P(p): tasa de eventos del tratamiento placebo
Es importante observar que P(s) y P(s) corresponden al tratamiento estándar pero con efectos potencialmente distintos (indicándose esta diferencia por el apóstrofe) debido a que se trata del efecto del tratamiento estándar en dos estudios diferentes, bajo condiciones seguramente distintas entre uno y otro estudio.
Por tanto, la eficacia del tratamiento experimental sobre el tratamiento placebo estará dada por:
P(x) – P(p)
Y este efecto puede estimarse sumando las estimaciones (1) y (2):
P(x) – P(p) = [P(x) – P(s)] + [P(s) – P(p)]
Debido a que el tratamiento estándar es un estudio independiente, la varianza de la comparación indirecta x versus p es simplemente la suma de las varianzas de las estimaciones de x vs s y de s vs p (considerando que los tratamientos s y s se refieren al estándar pero en dos estudios diferentes).
var[P(x)-P(p)] = var[P(x)-P(s)] + var[P(s)-P(p)]
Las estimaciones indirectas basadas en Riesgo Relativo (RR) se sustentan en las siguientes ecuaciones para el caso de querer estimar la comparación P(x) vs P(p):
P(x)/P(p) = P(x)/P(s) * P(s)/P(p)
Observando además que:
Ln [P(x)/P(p)] = Ln[P(x)/P(s)] + Ln[P(s)/P(p)]
De modo que:
var (Ln [P(x)/P(p)]) = var (Ln[P(x)/P(s)]) + var (Ln[P(s)/P(p)])
De manera similar, para el cálculo del OR indirecto según la derivación de Hasselblad, se tienen las siguientes ecuaciones:
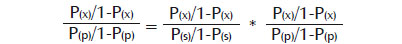
Y para la estimación de la varianza (var):
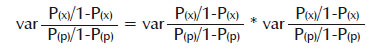
A partir de las ecuaciones de Hasselblad se obtienen las aproximaciones de Bucher (ver más arriba) y se pueden derivar algebraicamente las fórmulas para la estimación indirecta de la eficacia de los tratamientos experimental y estándar a partir de sus comparaciones directas con un mismo comparador (placebo o control). Así, para el escenario descrito en la Figura 3 la estimación del RR indirecto entre los tratamientos A y B sería como sigue:
RRAB = RRAC * RRCB
Ln(RRAB) = Ln(RRAC * RRCB)
Ln(RRAB) = Ln(RRAC) + Ln(RRCB)
var[Ln(RRAB)] = var [Ln(RRAC)] + var [Ln(RRCB)]
Y para el caso de una Diferencia de Riesgos (DR):
DRAB = DRAC + DRCB
var(DRAB) = var(DRAC) + var(DRCB)
Limitaciones de las comparaciones indirectas
El modelo desarrollado por Bucher y cols. presenta limitaciones descritas en la literatura. A continuación presentaremos las más importantes.
El modelo para comparaciones indirectas sólo puede ser aplicado para datos generados a partir de dos brazos, es decir, exactamente como está descrito en nuestro ejemplo, tratamientos A vs C y tratamientos B vs C (7,12).
Casi siempre las asunciones con respecto a la similitud de los estudios que se van a comparar no son verificables y esto constituye una limitación seria que disminuye el poder de la comparación (6).
Si hay sospecha de sesgo, es válido utilizar las herramientas descritas para el MA tradicional como corrección por análisis de subgrupos o meta-regresión sin la necesidad de descartar el análisis por completo.
CONCLUSIÓN
La comparación indirecta ha probado ser útil cuando no existen estudios directos tipo head-to-head y su metodología ha sido revisada en distintas publicaciones. Sin embargo, tiene limitaciones debido a que requiere la extrapolación de resultados definidos hacia un escenario donde el estudio directo aún no ha sido ejecutado. Los estudios de dos intervenciones independientes frente a un mismo comparador (placebo por lo común) pueden tener diferencias suficientes en los sujetos participantes y dicha heterogeneidad podría acarrear tamaños de efecto muy diferentes. Sin embargo, el uso razonable de esta metodología es útil para los decisores que enfrentan situaciones donde la evidencia directa es escasa o ausente.
BIBLIOGRAFÍA
1. Evidence-Based Medicine Working Group. Evidence-based medicine . A new approach to teaching the practice of medicine. JAMA. 1992 Nov 4;268(17):2420-5. [ Links ]
2. Guyatt GH, Oxman AD, Kunz R, Vist GE, Falck-Ytter Y, Schunemann HJ, et al. What is quality of evidence and why is it important to clinicians? BMJ. 2008 May 3;336(7651):995-8. doi: 10.1136/bmj.39490.551019.BE. [ Links ]
3. Hedges LV, Olkin I, Statistiker M, Olkin I, Olkin I. Statistical methods for meta-analysis. New York: Academic Press; 1985.
4. Caldwell DM, Ades AE, Higgins JP. Sim ultaneous comparison of multiple treatments: combining direct and indirect evidence. BMJ. 2005 Oct 15;331(7521):897-900. [ Links ]
5. Bucher HC, Guyatt GH, Griffith LE, Walter SD. The results of direct and indirect treatment comparisons in meta-analysis of randomized controlled trials. J Clin Epidemiol. 1997 Jun;50(6):683-91. [ Links ]
6. Gartlehner G, Moore CG. Direct versus indirect comparisons: a summary of the evidence. Int J Technol Assess Health Care. 2008 Spring;24(2):170-7. doi: 10.1017/S0266462308080240. [ Links ]
7. Signorovitch JE, Sikirica V, Erder MH, Xie J, Lu M, Hodgkins PS, et al. Matching-adjusted indirect comparisons: a new tool for timely comparative effectiveness research. Value Health. 2012 Sep-Oct;15(6):940-7. doi: 10.1016/j.jval.2012.05.004. [ Links ]
8. Glenny AM, Altman DG, Song F, Sakarovitch C, Deeks JJ, DAmico R, et al. Indirect comparisons of competing interventions. Health Technol Assess. 2005 Jul;9(26):1-134, iii-iv. [ Links ]
9. Edwards SJ, Clarke MJ, Wordsworth S, Borrill J. Indirect comparisons of treatments based on systematic reviews of randomised controlled trials. Int J Clin Pract. 2009 Jun;63(6):841-54. doi: 10.1111/j.1742-1241.2009.02072.x. [ Links ]
10. Wells GA, Sultan SA, Chen L, Khan M, Coyle D. Indirect Evidence: Indirect Treatment Comparisons in Meta-Analysis. Ottawa: Canadian Agency for Drugs and Technologies in Health; 2009. [ Links ]
11. Hasselblad V, Kong DF. Statistical methods for comparison to placebo in active-control trials. Therapeutic Innovation & Regulatory Science. 2001;35(2):435-49. [ Links ]
12. Song F, Loke YK, Walsh T, Glenny AM, Eastwood AJ, Altman DG. Methodological problems in the use of indirect comparisons for evaluating healthcare interventions: survey of published systematic reviews. BMJ. 2009 Apr 3;338:b1147. doi: 10.1136/bmj .b1147. [ Links ]
 Cited by SciELO
Cited by SciELO  Similars in
SciELO
Similars in
SciELO