Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú vol.36 no.2 Lima abr./jun. 2016
ARTÍCULOS ORIGINALES
Lesiones mucosas gastroduodenales por aspirina. Administrando los riesgos
Gastroduodenal mucosal injuries by aspirine. Management of the risks
Julián David Martínez M.1,2, Juan Carlos Molano V.2, Sandra Consuelo Henao R.1
1 Facultad de Medicina, Universidad Nacional de Colombia, Bogotá D.C., Colombia
2 Centro médico Endocentrolimitada. Bogotá D.C, Colombia.
RESUMEN
Introducción: La aspirina es uno de los medicamentos más utilizados en el mundo, con una amplia variedad de indicaciones terapéuticas. Desde sus indicaciones originales como analgésico y antiinflamatorio, son sus propiedades como antiagregante plaquetario la que la han convertido en el medicamento más empleado para prevenir enfermedades cardiovasculares. Sin embargo, es un medicamento con efectos adversos y toxicidad especialmente gastrointestinal. Objetivos: El objetivo de identificar los motivos de uso de aspirina, los hallazgos endoscópicos de gastropatía por aspirina y los riesgos relativos de presentar lesiones mucosas gastroduodenales, en una muestra de pacientes adultos en una institución de referencia particular. Materiales y métodos: Estudio de casos y controles, entre enero 1 y junio 31 de 2014, con pacientes con endoscopias digestivas altas en el centro médico Endocentro Bogotá D.C. se seleccionaron personas con consumo de aspirina a dosis de 500 mg/ día o menores, por más de seis meses previos al examen endoscópico. Resultados: Se enrolaron 602 pacientes, 534 (88%) mujeres y 168 (12%) hombres, con un rango de edad 17 a 92 años y con edad promedio de 51,8 años. Los usuarios de aspirina lo formaron 107 pacientes, 59 (55%) mujeres y 48 (45%) hombres con rango de edad de 23 a 85 años y edad promedio de 58 años. Se encontraron los siguientes riesgos relativos, para erosiones gastroduodenales RR= 4,0 (95%IC 3,87-8,37), úlcera gástrica RR=2,4 (95%I 1,3-9,0), úlcera duodenal RR=2,8 (95%IC 1,3-7,0), cualquier tipo de lesión gastroduodenal RR=5,5 (95%IC 4,1-7,2), usuarios de aspirina sin indicación alguna el riesgo de presentar alguna lesión mucosa RR=2,0 (95%IC 1,4-3,0). Conclusiones: El estudio mostró una importante proporción (18%) de adultos remitidos para endoscopia digestiva consumen aspirina, que el 13,8% de estos tienen una clara indicación para su uso, un considerable porcentaje (13%) no pueden informar ninguna indicación médica para usar aspirina; el uso de aspirina por más de seis meses a dosis inferiores de 500 mg/día aumenta la prevalencia de lesiones mucosas gastroduodenales (58%) ylos riesgos relativos de padecer estas lesiones son altos.
Palabras clave: Aspirina; Gastropatías; Heridas y lesiones; Úlcera (fuente: DeCS BIREME).
ABSTRACT
Background: Aspirin is one of the most used drugs around the Word, it has wide therapeutic indications. From its original indications, as analgesic and anti-inflammatory and due to its platelet antiaggregate properties, this drug has become in the most employed medicine to prevent cardiovascular disease. Never the less, it is a drug with adverse effects and gastrointestinal toxicity indeed. Objectives: To identify the reasons of using aspirin, endoscopic findings on gastropathy caused by ASA and the relative risk of developing mucosal lesions. This based on a sample of adult patients in a chosen particular institution. Materials and methods: Prospective study of cases and controls, from January 1 to June 31, 2014, with patients with high digestive endoscopy. In the medical center Endocentro Bogotá D.C. it was selected the people with aspirin consumption on 500 mg per day dose or less taken for more than six months prior the endoscopy. Results: We selected 602 patients, 534 (88%) were women and 168 (12%) were men, with an age range from 17 to 92 years and with an average of 51.8 years. 107 patients were the aspirin users, 59 (55%) were women and 48 (45%) were men, with an range from 23 to 85 years and with an average of 58 years. The follow relative risks were found: gastroduodenal erosions RR=4.9 (95%IC 3.87-8.37), gastric ulcer RR=2.4 (95%IC 1.3-9.0), duodenal ulcer RR=2.8 (95%IC 1.3-7.0) any kind of gastrointestinal injury RR=5.5 (95%IC 4.1-7.2) aspirin users without any indication to the risk of develop any mucosa injury RR=2.0 (95%IC 1.4-3.0). Conclusions: This study showed an important proportion (18%) of dispatched aspirin users adults to digestive endoscopy, the 13.8% of them have a clear indication to use it, a substantial percent (13%) cannot inform any medical reason; the aspirin usage for more than six months in doses lower than 500 mg per day increases the mucosal gastroduodenal injury prevalence (58%) and relative risk of suffering these injuries are high.
Key words: Aspirin; Stomach diseases; Wounds and injuries; Ulcer (source: MeSH NLM).
INTRODUCCIÓN
Más de 50 000 años han pasado desde que los médicos asirios, sumerios, egipcios y griegos prescribieran el extracto de la corteza de sauce (género Salix, familia Salicacedae) contra el dolor de origen muscular. En 1897 el químico alemán Felix Hoffman sintetizó el ácido acetil salicílico (ASA o aspirina) el primer antiinflamatorio no esteroideo conocido (AINES) (1).
En la actualidad los AINES son los medicamentos más usados en el mundo por sus propiedades analgésicas, antiinflamatorias y antipiréticas. En USA cerca de 30 millones de personas los emplean a diario y más del 60% de ellos los adquieren sin prescripción médica. Como muchos otros medicamentos, el uso de AINES se ha asociado a un amplio rango de efectos adversos y tóxicos, que incluyen complicaciones gastrointestinales, nefro-toxicidad, aumento de la presión arterial sistémica y deterioro de la clase funcional en pacientes con insuficiencia cardiaca congestiva y en los cirróticos (2,3).
La aspirina (ASA) es en la actualidad uno de los medicamentos más utilizados en el mundo, con una amplia variedad de indicaciones terapéuticas, además de ser un medicamento de venta libre y muy publicitado en los medios de comunicación masivos (TV, radio, prensa)(2).
Desde sus indicaciones originales como analgésico y antiinflamatorio, son sus propiedades como antiagregante plaquetario la que la han convertido en el medicamento más empleado para prevenir enfermedades cardiovasculares. La ASA a dosis de 500 mg a 1000 mg tres veces por día se recomienda para el control del dolor y la inflamación; dosis menores, entre 75 mg a 325 mg/día usualmente se prescriben para la prevención primaria y secundaria de eventos coronarios y cerebro vasculares(4,5).
Todos los medicamentos con acción antitrombótica aumentan el riesgo de hemorragias, la ASA en especial, aumenta en 60% el riesgo de hemorragias y es el sistema digestivo el sitio que presenta complicaciones con más frecuencia. Estas van desde manifestaciones leves como dispepsia, moderadas, como erosiones gastroduodenales, hasta eventos graves como úlceras gástricas o duodenales y hemorragias digestivas altas (5). Un estudio colombiano con 285 pacientes con hemorragia digestiva alta atendidos en un hospital universitario, mostró que el 33% de estos sangró desde una úlcera gástrica o duodenal y que 55% de los pacientes informaron consumo previo de aspirina o AINES(6).
El uso prolongado de aspirina también se asocia a sangrado digestivo bajo en cerca del SOo/o de sus consumidores, lo que muestra que la toxicidad por ASA no se limita a las vías digestivas altas. En las últimas tresEl uso prolongado de aspirina también se asocia a sangrado digestivo bajo en cerca del 50% de sus consumidores, lo que muestra que la toxicidad por ASA no se limita a las vías digestivas altas. En las últimas tres décadas, además de la infección por Helicobacter pylori (H.pylori) el empleo de ASA es considerado una de las principales causas de sangrado por úlceras pépticas y su uso prolongado aumenta significativamente el riesgo de estas complicaciones(5).
El objetivo de este trabajo es identificar el motivo de uso de aspirina, los hallazgos endoscópicos sugestivos de gastropatía por ASA y los riesgos relativos de presentar esas lesiones mucosas, en una muestra de pacientes atendidos de manera ambulatoria en una institución de referencia particular.
MATERIALES Y MÉTODOS
Se realizó un estudio prospectivo de casos y controles, entre 1 de enero y 31 de junio de 2014, con pacientes remitidos para la realización de endoscopias digestivas al centro médico Endocentro limitada, de Bogotá D.C. Antes del procedimiento endoscópico, se entrevistaron los pacientes y se diligenció el formulario diseñado para el estudio y se obtuvo su consentimiento. El grupo de pacientes que usaban aspirina a dosis de 500 mg o menos, se definió como personas que la tomaban a diario en los seis meses previos a la endoscopia y por cualquier causa, se excluyeron las personas que informaron uso de ranitidina, medicamentos inhibidores de la bomba de protones, antibióticos, corticoesteroides, anticoagulantes, otros antiagregantes de las plaquetas, otros AINES y alcohol seis meses antes del examen endoscópico. El grupo control fueron personas que no tomaban aspirina, tampoco otros medicamentos lesivos o gastro protectores para la mucosa gastrointestinal como los ya mencionados. Se realizaron endoscopias con equipos marca Olympus Exera CV-160 (Japón), se definieron como lesiones significativas la presencia de erosiones gástricas y/o duodenales, las úlceras gástricas y duodenales, a todos los pacientes se les tomaron biopsias gástricas de la incisura angularis con pinzas Boston Scientific referencia 1330 (USA), las cuales fueron interpretadas según la clasificación de Sydney.
La estadística descriptiva empleó un programa Excel para Windows 2010, el cálculo de los riesgos relativos y sus intervalos de confianza se realizó mediante el programa MediCalc, se definió un error del 5%; el estudio contó con el permiso de comité de investigación de la institución.
RESULTADOS
Se enrolaron 602 pacientes, 534 (88%) mujeres y 168 (12%) hombres, con un rango de edad 17 a 92 años y con edad promedio de 51,8 años. El grupo de usuarios de aspirina lo formaron 107 pacientes, 59 (55%) mujeres y 48 (45%) hombres con rango de edad de 23 a 85 años y edad promedio de 58 años. El grupo control con 495 personas, 375 (76%) mujeres y 120 (24%) hombres, rango de edad de 17 a 92 años y edad promedio de 47,5 años.
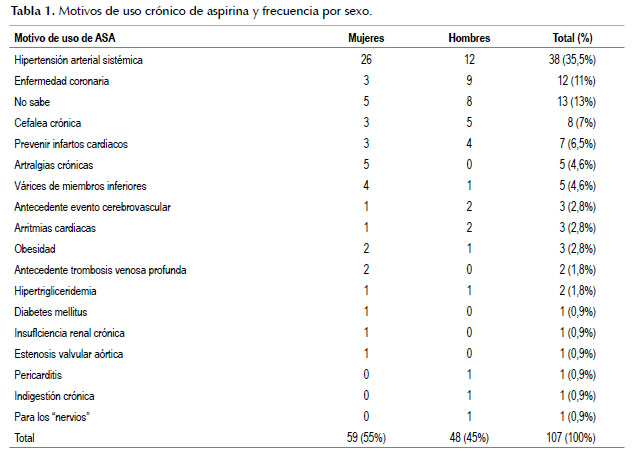
Se resalta que solamente el 11% (enfermedad coronaria) y el 2,8% (antecedente de evento cerebro vascular) tenían indicación médica precisa para el uso del medicamento, el 13% de los usuarios no sabían una causa clara para usarla y que se encontró una amplia variedad de “indicaciones”, desde la hipertensión arterial hasta la indigestión crónica. Tabla 1.
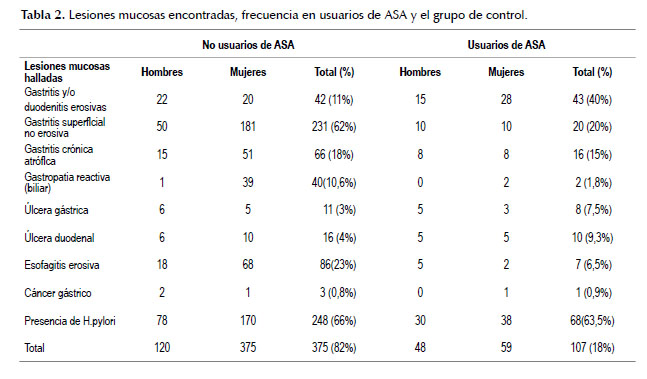
Las lesiones mucosas más frecuentemente halladas en los usuarios de ASA fueron las erosiones gastroduodenales (40%), la gastritis superficial no erosiva (20%) y la gastritis crónica atrófica (15%), las úlceras gástricas (7,5%) y las úlceras duodenales (9,3%). Tabla 2.
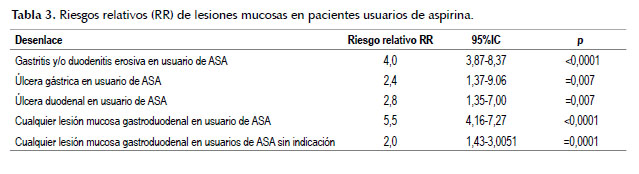
Los resultados de los cálculos de los riesgos relativos (RR) para cada desenlace considerado significativo (erosiones, úlceras gástrica y duodenal) en pacientes que tomaron ASA, se muestran en la Tabla 3, se resalta que el uso de aspirina aumenta significativamente el riesgo de padecer lesiones mucosas gastroduonales y esto no parece tener relación con la indicación del uso de este medicamento.
DISCUSIÓN
El empleo de ASA a bajas dosis (75 mg a 325 mg/ día) previene la formación de trombos en pacientes con enfermedad isquémica coronaria y/o enfermedad isquémica cerebro vascular. Se observa una tendencia creciente a la prescripción de ASA, debido principalmente al envejecimiento de la población mundial, al aumento de pacientes con diabetes mellitus, hipertensión arterial sistémica; todos ellos factores de riesgo conocidos para la enfermedad coronaria (7,8). En el presente estudio la minoría de los usuarios de ASA tenían indicaciones claras para su empleo, el antecedente de enfermedad coronaria en el 11% y de evento cerebro vascular en el 2,8%. La mayoría (35,5%) de consumidores indicaron su uso por padecer hipertensión arterial sistémica, indicación que se discute en la actualidad y que solo beneficiaría a hipertensos con diabetes mellitus o en mujeres hipertensas mayores de 65 años de edad, pero claramente no se recomienda el empleo de ASA en todos los pacientes con hipertensión arterial.
Llama poderosamente lo variopinto de las “indicaciones” para tomar ASA de manera crónica y más aún que un grupo importante de usuarios (13%) no sabía porque consumía el medicamento, lo que los pone en alto riesgo de presentar lesiones mucosas gastroduodenales, RR= 2,0 (95%IC 1,4-3,0) sin obtener ningún beneficio terapéutico por usar ASA.
Sin embargo, el uso crónico de ASA a bajas dosis puede ocasionar lesiones mucosas gastrointestinales como, petequias, equimosis, erosiones o úlceras y aumentar desenlaces graves como hemorragias digestivas y aún la muerte (9). Estudios controlados han demostrado la presencia de erosiones gastroduodenales en el 60% de los usuarios de aspirina. Otro estudio con 187 pacientes que recibieron ASA a bajas dosis sin medicamentos gastroprotectores, mostró una prevalencia de ulceras del 11% (95%IC 6,3%-15,1%) (10).
Situación similar encontramos en el presente estudio, en donde el 58% de los usuarios de ASA tenían una lesión mucosa, fue la gastritis erosiva las más frecuente (40%) seguido por las úlceras duodenales (9,3%) y las úlceras gástricas (7,5%). También este estudio mostró resultados similares a la literatura mundial, se encontró que existen mayores riesgos relativos de presentar lesiones mucosas gastroduodenales en personas que usan aspirina por más de seis meses, RR=5,5 (95%IC 4,1-7,2) (Tabla 3).
Un estudio de casos y controles japonés, mostró que los odds ratio para sangrado digestivo alto en usuarios de ASA fue de 5,5 y para usuarios de otros Aines de 6,1, lo que indica que el riesgo de sangrado es similar en los pacientes que emplean cualquier tipo de AINES (11). Un metanálisis de 24 estudios aleatorizados, evaluó la incidencia de hemorragia digestiva alta asociada al empleo de ASA por largo tiempo y la repercusión de reducir la dosis de aspirina en la incidencia de sangrado. El estudio mostró una incidencia de 2,5% de sangrado digestivo en usuarios de ASA y de 1,4% en el grupo placebo. El estudio no demostró evidencia que la disminución de la dosis de ASA disminuya la incidencia de sangrado (12).
En varios estudios de casos y controles, el OR para sangrado digestivo en usuarios de ASA, fluctuó entre 2,4-7,7 y la mortalidad atribuida está entre 20 a 25 casos por millón de usuarios (13).
Los factores de riesgo identificados para el desarrollo de sangrado digestivo secundario a lesiones mucosas gastrointestinales inducidas por ASA, son: edad mayor de 70 años, uso simultaneo de otros Aines o de anticoagulantes, uso de terapia dual antiagregante plaquetaria, consumo de alcohol, diabetes mellitus, insuficiencia renal crónica e infección por H. pylori (14-16).
Un estudio de casos y controles en pacientes hospitalizados por hemorragia digestiva alta que, mostró una asociación positiva, OR de 3,3 (95%IC 2,54,4) con el uso de ASA a bajas dosis y también con el uso de ASA y otro tipo de AINES, OR de 7,7 (95%IC 3,616,4). Otro estudio de casos y controles en pacientes hospitalizados por sangrado digestivo, mostró que el uso simultáneo de ASA y Aines aumenta el riesgo de hemorragia en comparación con los que solo reciben ASA (OR=3,8 (95%IC 1,8-7,8)) (17-19).
Las terapias combinadas de ASA con otros medicamentos antiagregantes plaquetarios o anticoagulantes, son cada vez más frecuentes en pacientes con eventos coronarios agudos, en pacientes con endoprótesis (stents) coronarios, en arritmias como la fibrilación auricular. La terapia dual ha mostrado un aumento significativo de sangrado gastrointestinal (20).
Hallas y colaboradores, calcularon el riesgo de sangrado digestivo alto grave en pacientes que reciben ASA a dosis bajas, sola o en combinación con otros medicamentos antitrombóticos. Su investigación mostró odds ratios que se asociaban a padecer sangrado digestivo en usuarios de ASA (OR=1,8; 95%IC 1,5-2,1), clopidogrel (OR=1,1; 95%IC 0,62,1), dipiridamol (OR=1,9;95%IC 1,3-2,8) y para antagonistas de la vitamina K (OR=1,8; 95%IC 1,3-2,4). Sin embargo, lo más llamativo de ese estudio fue el alto riesgo de sangrado digestivo encontrado en pacientes que usaban combinaciones de estos medicamentos; para usuarios de ASA y clopidogrel OR=7,4 (95%IC 3,5-15), aspirina y dipiridamol OR= 2,3 (95%IC 1,73,3), aspirina y antagonistas de la vitamina K, OR=5,3 (95%IC 2,9-9,5) (20).
La aspirina y H. pylori producen úlceras pépticas por diferentes mecanismos. Las lesiones inducidas por ASA son causadas por la combinación de efectos en la mucosa y en la circulación sanguínea con mínima o ninguna inflamación, caso contrario sucede con las lesiones por H. pylori en donde se observa un gran infiltrado de células inflamatorias. Está bien establecido, que la ASA ocasiona efectos locales (mucosos) y sistémicos mediante la depleción de las prostaglandinas por la inhibición de la ciclooxigenasa-1. En ausencia de una síntesis normal de prostaglandinas a nivel gastrointestinal, la mucosa es más vulnerable a agentes exógenos como el cigarrillo, a agentes endógenos como el ácido clorhídrico, la pepsina, las sales biliares y el H. pylori lo que lo hace más proclive a desarrollar úlceras y a las complicaciones de estas (21).
Lanas y colaboradores, realizaron un estudio de casos y controles que mostró que la infección por H. pylori aumenta el riesgo de sangrado digestivo alto en personas usuarios de ASA a bajas dosis, OR=4,7 (95%IC 2,010,9); la prevalencia de la infección por H. pylori fue de 89% en los pacientes con sangrado digestivo y de 68% en los controles (p=0,0001). H. pylori fue un factor de riesgo independiente para hemorragias digestiva altas por úlceras, OR=4,7 (95%Ic 2,0-10,9) (18,21). En este estudio la proporción de los pacientes de ambos grupos infectados con H. pylori fue similar y no podemos afirmar que esta infección aumente el riesgo de lesiones mucosas en los usuarios de aspirina.
Si bien la motivación para el uso de ASA puede descansar en la esperanza de disminuir la ocurrencia de eventos coronarios y cáncer del tubo digestivo, el riesgo absoluto de sangrado digestivo se incrementa cuando se utiliza ASA en la prevención primaria de eventos cardiovasculares mayores, donde la ocurrencia descrita sobrepasa los beneficios como se demostró en un meta análisis de 27 estudios que mostró que de 60 a 84 de eventos cardiacos que se evitan por 100 000 personas/ año mientras, que el riesgo de sangrado digestivo se elevó un 37% (22).
Y así, al contrastar con hechos claros respecto a la disminución del riesgo de cáncer de colon con el uso regular de ASA, el cual reduce la mortalidad por cáncer de colorectal en un 28%, (hazard ratio) HR= 0,72 95%IC 0,56-0,92 y en 12% de reducción de mortalidad por todo tipo de cáncer HR= 0,88 95% 0,81-0,96; el tiempo de latencia para lograr las cifras descritas es de hasta 10 años para las muertes por cáncer colorectal y de uno a cinco años para disminuir riesgos cardiovasculares es claro que la mortalidad del 5% para el sangrado digestivo que ocurre en hasta el 37% de los expuestos a ASA (23) por esta razón se requiere el diseño de guías de manejo de ASA claras y de difusión amplia para limitar y controlar el riesgo a quienes requieran de actividades solo de prevención secundaria y desaconsejar su uso en prevención primaria.
En conclusión, el presente estudio mostró que una importante proporción (18%) de personas adultas remitidas para endoscopia digestiva consumen aspirina, que solo en 13,8% de estos tienen una clara indicación para su uso, que un considerable porcentaje (13%) no pueden informar ningún motivo médico para usar aspirina; que el uso de aspirina por más de seis meses a dosis inferiores de 500 mg/día aumentan la prevalencia de lesiones mucosas gastroduodenales, que los riesgos relativos de padecer estas lesiones mucosas son altos, que la prevención primaria de eventos coronarios logra evitar alrededor de 80 eventos por 100 000 pacientes/ año, tiene una latencia de años como se demuestra cuando se trata de prevenir cáncer digestivo y puede ser fútil si se tiene en cuenta que el riesgo de sangrado digestivo aparece hasta en el 37% de quienes están sometidos al riesgo; por lo cual debe proscribirse su uso en prevención primaria para las condiciones en consideración.
Es obligación del cuerpo médico dar a conocer a sus pacientes las indicaciones actuales para el uso de aspirina y así disminuir en número de personas al riesgo de tomar un medicamento no exento de potenciales complicaciones graves, sin tener las indicaciones precisas para esto.
Agradecimientos:
A la enfermera Hasbleydi Camacho por su dedicación con los pacientes.
Financiación: recursos propios de los autores.
Conflictos de interés: los autores no declaran conflictos de interés.
BIBLIOGRAFÍA
1. Brune K, Hinz B. The discovery and development of antiinflammatory drugs. Arthritis Rheum. 2004;50(8):2391-9. [ Links ]
2. Singh G. Gastrointestinal complications of prescription and over-the-counter nonsteroidal anti-inflammatory drugs: a view from the ARAMIS database. Arthritis, Rheumatism, and Aging Medical Information System. Am J Ther. 2000 Mar;7(2):115-21. [ Links ]
3. Sostres C, Gargallo C, Lanas A. Nonsteroidal anti-inflammatory drugs and upper and lower gastrointestinal mucosal damage. Arthritis Res Ther. 2013;15(Suppl 3):S3. [ Links ]
4. Chan AT, Manson JE, Feskanich D, Stampfer MJ, Colditz GA, Fuchs CS. Long-term aspirin use and mortality in women. Arch Intern Med. 2007;167(6):562-72. [ Links ]
5. Cryer B, Feldman M. Effects of very low dose daily, longterm aspirin therapy on gastric, duodenal, and rectal prostaglandin levels and on mucosal injury in healthy humans. Gastroenterology. 1999;117(1):17-25. [ Links ]
6. Rivera D, Martínez JD, Tovar JR, Garzón MA, Hormaza N, Lizarazo JI, et al. Caracterización de los pacientes con hemorragia de vías digestivas altas no varicosa en un hospital de tercer nivel de Cundinamarca, Colombia. Rev Col Gastroenterol. 2013;28(4):278-85. [ Links ]
7. Laine L. Approaches to nonsteroidal anti-inflammatory drug use in the high-risk patient. Gastroenterology. 2001;120(3):594-606. [ Links ]
8. Baigent C, Blackwell L, Collins R, Emberson J, GodwinJ, Peto R, et al. Aspirin in the primary and secondary prevention of vascular disease: collaborative meta-analysis of individual participant data from randomised trials. Lancet. 2009;373(9678):1849-60. [ Links ]
9. Garcia-Rodriguez LA, Hernandez-Diaz S, de Abajo FJ. Association between aspirin and upper gastrointestinal complications: systematic review of epidemiologic studies. Br J Clin Pharmacol. 2001;52(5):563-71. [ Links ]
10. Lanas A, Bajador E, Serrano P, Fuentes J, Carreño S, Guardia J, et al. Nitrovasodilators, low-dose aspirin, other nonsteroidal antiinflammatory drugs, and the risk of upper gastrointestinal bleeding. N Engl J Med. 2000;343(12):834-9. [ Links ]
11. Sakamoto C, Sugano K, Ota S, Sakaki N, Takahashi S, Yoshida Y, et al. Case-control study on the association of upper gastrointestinal bleeding and nonsteroidal anti-inflammatory drugs in Japan. Eur J Clin Pharmacol. 2006;62(9):765-72. [ Links ]
12. Derry S, Loke YK. Risk of gastrointestinal haemorrhage with long term use of aspirin: meta-analysis. BMJ. 2000;321(7270):1183-7. [ Links ]
13. Lanas A, Perez-Aisa MA, Feu F, Ponce J, Saperas E, Santolaria S, et al. A nationwide study of mortality associated with hospital admission due to severe gastrointestinal events and those associated with nonsteroidal antiinflammatory drug use. Am J Gastroenterol. 2005;100(8):1685-93. [ Links ]
14. Cryer B, Mahaffey KW. Gastrointestinal ulcers, role of aspirin, and clinical outcomes: pathobiology, diagnosis, and treatment. J Multidiscip Healthc. 2014;7:137-46. [ Links ]
15. Cayla G, Collet JP, Silvain J, Thiefin G, Woimant F, Montalescot G. Prevalence and clinical impact of Upper Gastrointestinal Symptoms in subjects treated with low dose aspirin: the UGLA survey. Int J Cardiol. 2012;156(1):69-75. [ Links ]
16. Yeomans ND. Aspirin: old drug, new uses and challenges. J Gastroenterol Hepatol. 2011;26(3):426-31. [ Links ]
17. Cea Soriano L, Rodriguez LA. Risk of upper gastrointestinal bleeding in a cohort of new users of low-dose ASA for secondary prevention of cardiovascular outcomes. Front Pharmacol. 2010;1:126. [ Links ]
18. Lanas A, Fuentes J, Benito R, Serrano P, Bajador E, Sainz R. Helicobacter pylori increases the risk of upper gastrointestinal bleeding in patients taking low-dose aspirin. Aliment Pharmacol Ther. 2002;16(4):779-86. [ Links ]
19. Ng W, Wong WM, Chen WH, Tse HF, Lee PY, Lai KC, et al. Incidence and predictors of upper gastrointestinal bleeding in patients receiving glow-dose aspirin for secondary prevention of cardiovascular events in patients with coronary artery disease. World J Gastroenterol. 2006;12(18):2923-7. [ Links ]
20. Hallas J, Dall M, Andries A, Andersen BS, Aalykke C, Hansen JM, et al. Use of single and combined antithrombotic therapy and risk of serious upper gastrointestinal bleeding: population based case-control study. BMJ. 2006;333(7571):726. [ Links ]
21. Iwamoto J, Saito Y, Honda A, Matsuzaki Y. Clinical features of gastroduodenal injury associated with long-term low-dose aspirin therapy. World J Gastroenterol. 2013;19(11):1673-82. [ Links ]
22. Sutcliffe P, Connock M, Gurung T, Freeman K, Johnson S, Ngianga-Bakwin K, et al. Aspirin in primary prevention of cardiovascular disease and cancer: a systematic review of the balance of evidence from reviews of randomized trials. PLoS One. 2013;8(12):e81970. [ Links ]
23. Garcia-Albeniz X, Chan AT. Aspirin for the prevention of colorectal cancer. Best Pract Res Clin Gastroenterol. 2011;25(4-5):461-72. [ Links ]
Correspondencia: Julián David Martínez M.
Avenida Suba 115-57 Torre B consultorio 403. Bogotá D.C., Colombia.
E-mail: jdmartinezm@yahoo.com, jdmartinezma@unal.edu.co
Recibido: 18-6-2015
Aprobado: 20 -11-2015