Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú vol.37 no.1 Lima ene./mar. 2017
ARTÍCULO DE REVISIÓN
Abordaje diagnóstico y terapéutico de las patologías del intestino delgado mediante cápsula endoscópica y enteroscopía de doble balón
Diagnostic and therapeutic approach to small bowel disorders through capsule endoscopy and double-balloon endoscopy
Federico De Simone1,2,3, Pablo Machado1,2,3, Edson Guzmán Calderon4
1 Clínica de Gastroenterología. Montevideo, Uruguay,
2 Facultad de Medicina, Universidad de la República. Montevideo, Uruguay.
3 Servicio de endoscopía, Clínica Ce.V.En. Mucam, Uruguay.
4 Hospital Nacional Edgardo Rebagliati Martins. Lima, Perú.
a Ex Asistente, b Gastroenterólogo
RESUMEN
Las múltiples patologías del intestino delgado han supuesto un enorme desafío para gastroenterólogos y endoscopistas debido a las muy bajas tasas de rédito diagnóstico que las diferentes técnicas paraclínicas ofrecían. El advenimiento de la cápsula endoscópica y la enteroscopía de doble balón ha permitido una exploración total, segura y eficiente del intestino delgado lo que ha generado un impacto real en el diagnóstico, tratamiento y pronóstico de nuestros pacientes.La cápsula endoscópica es un procedimiento seguro, mínimamente invasivo, no precisa sedación, no genera dolor y permite observar la totalidad del intestino delgado. Por su parte la enteroscopía de doble balón es la técnica endoscópica complementaria necesaria para brindar una intervención terapéutica (cauterizar angiodisplasias, polipectomías, toma de biopsias) logrando así un abordaje resolutivo de las diversas patologías.
Palabras clave: Intestino delgado; Enteroscopía de doble balón; Enfermedad de Crohn; Enfermedad celiaca (fuente: DeCS BIREME).
ABSTRACT
Many small bowel disorders represent a great challenge for gastroenterologists and endoscopists due to the very low rates of success showed by the different diagnosis techniques. The advent of the capsule endoscopy and double-balloon endoscopy has allowed a total, secure and efficient examination of the small bowel, which represents a real impact in diagnosis, treatment, and prognosis of our patients. The capsule endoscopy is a safe, minimally invasive procedure, which does not need sedation, does not cause pain, and allows the observation of the totality of the small bowel. Furthermore, the double-balloon endoscopy is the complementary technique necessary to provide a therapeutic procedure (cauterizing angiodysplasia, polypectomy, biopsies), and hence achieving resolution of various disorders.
Keywords: Intestine, small; Double-balloon enteroscopy; Crohn disease; Celiac disease (source: MeSH NLM).
MATERIAL Y TÉCNICA
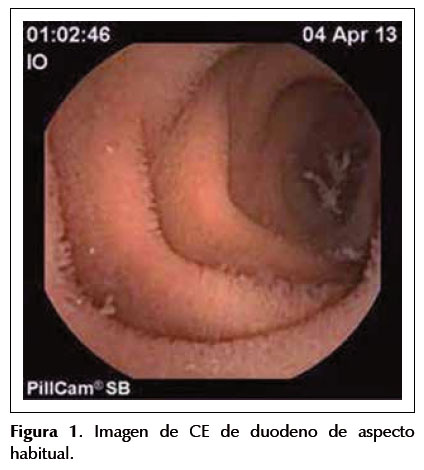
La cápsula endoscópica (CA) se comercializó por primera vez en el año 2000 por la empresa Given Imaging Ltd., dado el gran impacto generado por la misma, en el año 2003 la "Food and Drug Administration" de los Estados Unidos la avala como técnica de elección (gold standard) para el estudio de las patologías del intestino delgado (ID) (Figura 1). En la actualidad existen cinco empresas que comercializan cápsulas para explorar el ID (Given Imaging, Olympus, IntroMedic, Capsovision y Jinshan). Se trata de un pequeño dispositivo que mide entre 26 y 31 mm de largo por 11 a 13 mm de ancho (según la marca comercial), tiene un peso de 3,4 gramos, contiene una pequeña videocámara, una fuente de iluminación formada por cuatro diodos que emiten luz blanca, un sistema de transmisión de imágenes, una batería (con una duración aproximada de 14 horas) y una antena, todo ello incluido en el interior de una funda de plástico biocompatible. Posee un campo de visión de 150º y el tamaño mínimo de detección es de 0,1 mm. Una vez activada captura 2 a 6 fotos por segundo lo que genera 60 000 a 200 000 imágenes aproximadamente por procedimiento. Las mismas son transmitidas por radiofrecuencia a sensores adheridos a la pared abdominal y recogidas por una unidad portátil externa que el paciente lleva alrededor de su cintura. Finalmente, las imágenes son descargadas mediante un software especializado y se procede a observar el video creado por la secuencia de las miles de imágenes obtenidas (1). Tres meta análisis concluyeron que la visualización mucosa mejora ampliamente cuando los pacientes reciben preparación intestinal ya sea con polietilenglicol, fosfato de sodio o eritromicina en comparación con los que realizan únicamente dieta líquida previo al procedimiento (2-4). Por lo tanto, la cápsula se administra con agua luego de un ayuno de 8 horas y de recibir el día previo al estudio la preparación intestinal correspondiente. Luego de la ingesta de la CE se permite al paciente la toma de líquidos claros a las 2 horas y una comida ligera a las 4 horas. Los movimientos peristálticos ayudan a que la CE se desplace pasivamente por el intestino. En aquellos pacientes que no puedan tragar el dispositivo o presenten alteraciones conocidas en el vaciamiento gástrico se opta por depositar la CE directamente en el duodeno mediante videogastroscopía. Presenta como grandes ventajas el ser un estudio mínimamente invasivo, seguro, no insufla aire por lo que no genera molestias como distensión abdominal, no requiere sedación y permite observar rápida y completamente el ID. Puede realizarse tanto en pacientes hospitalizados como en ambulatorios.
Las contraindicaciones son escasas, estas son, los trastornos deglutorios (donde como fue mencionado puede colocarse la CE directamente en el duodeno mediante endoscopía), la presencia de estenosis de ID y el embarazo. Las ondas de radiofrecuencia emitidas por la CE para transmitir los datos al grabador teóricamente podrían interferir con marcapasos o desfibriladores cardíacos. Sin embargo, numerosos estudios han demostrado que no se genera arritmias ni ninguna otra alteración en pacientes con dispositivos cardiacos por lo que hoy en día se considera un procedimiento seguro para estos pacientes (5,6). La CE permite la visualización completa del ID en un 7990% de los casos y ha mostrado tener un rendimiento diagnóstico ampliamente superior a cualquier otra técnica de estudio (7,8). Las características de una mucosa duodenal normal se aprecian en la Figura 1. La complicación que puede presentarse es la retención del dispositivo que se define como la permanencia del mismo mas de 15 días en el ID. Esto se observa en un 1,2% de los pacientes con hemorragia digestiva oscura, 2,1% de los pacientes con tumores de ID y un 5% de los pacientes con enfermedad de Crohn; no se han reportado retenciones en pacientes sin patologías (9).
La CE suele quedar retenida en presencia de alteraciones quirúrgicas previas, tumores o estenosis. Puede optarse por su remoción endoscópica aunque generalmente sirve para guiar el tratamiento quirúrgico en el mismo acto de la extracción. La limitante de esta técnica es la imposibilidad de brindar intervención terapéutica, la incapacidad de controlar el movimiento, los hallazgos incidentales y la dificultad en topografiar precisamente las lesiones. Es por estos motivos que la enteroscopía de doble balón (EDB) es el método complementario ideal que permite generar finalmente una solución integral a las afecciones del ID. El desarrollo de la EDB lo produce Yamamoto hacia 1998 y comienza a utilizarse en Japón y China hacia el año 2003 extendiéndose rápidamente hacia el resto del mundo. Se comercializan en la actualidad dos enteroscopios de las marcas Fujinom y Olympus. El más utilizado es el videoenteroscopio EN-450, Fujinon, Japón que mide 2000 mm de longitud y posee un sobretubo flexible de 1500 mm de longitud. Ambos instrumentos acoplan balones en sus extremos distales que se rellenan de aire. El avance del enteroscopio se produce mediante sujeción al intestino mediante el inflado alternativo de los balones del endoscopio y del sobretubo, mecanismo conocido como avance-pulsión y retirada-tracción (10). Estas maniobras permiten que el ID vaya telescopándose y se pueda explorar en su totalidad con buena maniobrabilidad y con un canal de trabajo que permite intervenciones terapéuticas. Puede realizarse por abordaje anterógrado (oral) u retrógrado (anal) decisión basada en la topografía de la lesión determinada previamente por la CE. Entre las desventajas se incluyen que se trata de un proceso invasivo (riesgo de perforación 1,3% y de pancreatitis 0,6%), la necesidad de sedación, contar con un equipo entrenado en la técnica (endoscopistas y asistentes), el uso de radioscopía y la duración prolongada del procedimiento (entre 60 y 120 minutos) (11). El abordaje anterógrado permite una exploración de 250-300 cm de profundidad mientras que el retrógrado unos 100200 cm por lo que mediante abordaje combinado puede lograrse la exploración completa del ID en un 63% de los casos (12,13).
INDICACIONES
Hemorragia digestiva oscura – Hemorragia digestiva media
Tal es el impacto que han generado estas nuevas técnicas que gracias a ellas se ha redefinido la clasificación de hemorragia digestiva. Actualmente se ha incorporado el concepto de hemorragia digestiva media (HDM), como aquella topografiada entre la papila de Vater y la válvula ileocecal. Se reserva por lo tanto el término de hemorragia digestiva alta para la originada por encima de la papila de Vater y hemorragia digestiva baja a la producida por debajo de la válvula ileocecal. La hemorragia digestiva de origen oscuro se define como aquella que persiste o recurre sin etiología evidente luego de realizados los estudios endoscópicos tradicionales (videogastroscopía y videocolonoscopía) y es la que suele provenir del ID (hemorragia digestiva media). El mayor rendimiento diagnóstico-terapéutico de la CE y la EDB se logra sin dudas en este tipo de hemorragia que representa un 5-8% del total de las hemorragias digestivas. La HDM, puede presentarse con sangrado evidente (melenas, enterorragia) u oculto (anemia ferropénica) siendo múltiples las patologías que pueden provocarla. Se puede identificar el origen del sangrado mediante CE entre un 38%-91% de los casos aumentando el rédito diagnóstico cuanto más cercano se realiza el procedimiento con respecto a la hemorragia (14). Se recomienda su realización en las primeras 72 h de ocurrido el episodio de sangrado donde la CE es superior a la angiografía para detectar el origen de la hemorragia (15).
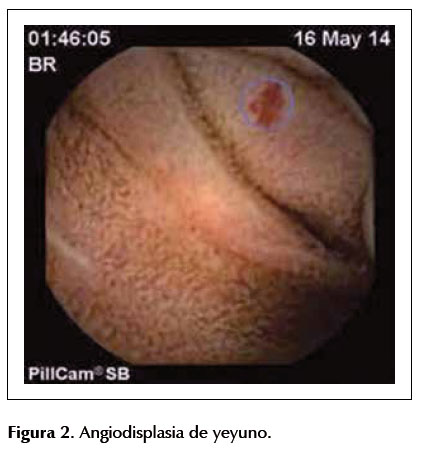
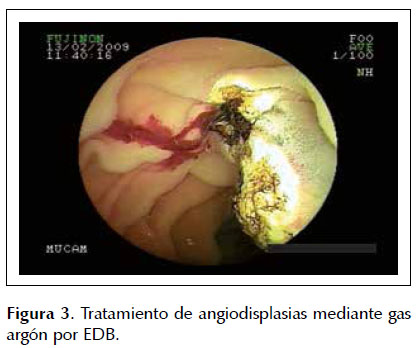
La probabilidad de hallazgos positivos con CE y EDB aumentan cuando se produce un sangrado evidente, activo, múltiples episodios, corto intervalo desde la hemorragia hasta la realización del/los procedimiento/s diagnóstico/s, anemia severa y necesidad de transfusiones (16). Ha demostrado ser un método costo-efectivo ya que establece rápidamente la estrategia de manejo evitando múltiples pruebas diagnósticas (de escaso rendimiento), necesidad de transfusiones reiteradas, internaciones prolongadas, lo que lleva a un alto índice de comorbilidades y genera importantes gastos al sistema de salud.Para la hemorragia oscura la CE tiene una tasa de rédito diagnóstico superior en un 30% a la enteroscopía por pulsión y 36% superior a los estudios imagenológicos contrastados con bario (17). Cuando la CE logra identificar la causa del sangrado posibilita que entre un 44-82% de los casos pueda realizarse una terapéutica específica o cambiar el manejo que se venía realizando con ese paciente y lograr la detención del sangrado en un 63-83% de los casos (18). La causa más frecuente de este tipo de hemorragia son las angiodisplasias (ver Figura 2), que pueden extenderse por todo el ID y son responsables del 70% de los casos. Una vez topografiadas se establece el abordaje (anterógrado o retrógrado) y se realiza la EDB con fines terapéuticos mediante la coagulación de las angiodisplasias con gas argón (ver Figura 3). La enteropatía por AINE es otra causa frecuente de HDM afectando sobre todo íleon distal y puede ser tratada también con gas argón durante la EDB. Las úlceras, várices, pólipos sangrantes, tumores son otras causas de HDM que son diagnosticadas con menor frecuencia (8). La principal indicación de EDB claramente se produce también en el estudio de HDM (63% del total de exploraciones) con un rendimiento diagnóstico del 68%. Cuando se realiza una CE con resultados positivos la EDB aumenta su rédito diagnóstico a 75% y el mismo baja a un 56% cuando no se ha realizado CE, por lo tanto, surge nuevamente el papel complementario de ambas técnicas (19). Las lesiones topografiadas en los primeros 2/3 del tiempo de transcurrida la exploración con CE nos llevan a plantear el abordaje anterógrado mediante EDB, de lo contrario se utiliza el abordaje retrógrado. Es importante destacar que continúa siendo costo efectivo solicitar dos videogastroscopías y videocolonoscopías previo a embarcarse en estudios más específicos de ID ya que muchas lesiones (angioectasias, lesión de Dieulafoy, úlceras, GAVE) pueden no ser evidentes en una primera instancia y si ser diagnosticadas en el segundo procedimiento. Los índices de resangrado y/o necesidad de transfusiones o suplementos de hierro luego de CE y/o EDB con hallazgos positivos se mantienen elevados. Un 23% de pacientes resangran y un 35% necesitan transfusiones al año de realizar una EDB terapéutica (20). Los predictores de resangrado que han sido identificados son la presencia de patología valvular o arritmias cardíacas y el número total de lesiones vasculares encontradas(21). En un estudio retrospectivo, la causa del sangrado se pudo determinar en un 81% de los pacientes mediante EDB que tenían hallazgos positivos en una EDB previa (correspondiendo casi la totalidad de los casos a angiodisplasias) mientras que en ningún paciente se pudo determinar el origen del sangrado si tenían EDB sin hallazgos realizadas anteriormente (22). Por lo tanto, es importante seleccionar al grupo de pacientes con mayor posibilidad de resangradospara poder realizar un segundo procedimiento terapéutico, aunque hasta el momento no se ha determinado su costo beneficio por lo que debe analizarse cada caso en particular.
Enfermedad de Crohn
Se trata de una enfermedad inflamatoria gastrointestinal, que puede afectar cualquier sector del tubo digestivo fundamentalmente íleon, colon y región perianal, la afectación suele ser parcheada y asimétrica. La prevalencia es similar en ambos sexos y la edad al diagnóstico presenta un comportamiento bimodal con un pico entre los 15-30 años y otro entre los 50-60 años. En un 70% de los casos el ID se encuentra afectado en la enfermedad de Crohn y en un 30% la enfermedad se encuentra limitada al ID fundamentalmente al íleo distal (23). Por lo tanto, la CE y la EDB tienen hoy en día un rol muy importante en esta patología particularmente cuando la colonoscopía con ileoscopía es negativa.
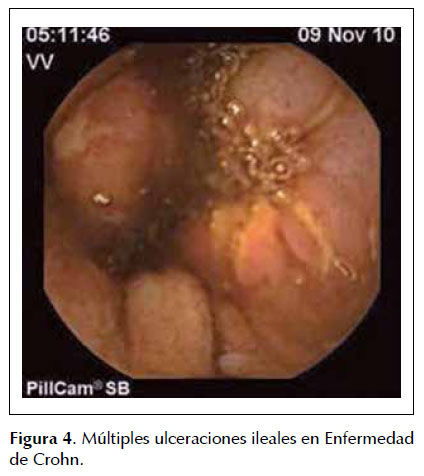
La CE está indicada ante la sospecha de la enfermedad (para valorar participación del ID), establecer su extensión y severidad, evaluar la respuesta al tratamiento, así como también valorar la recidiva post quirúrgica. A su vez adquiere importancia en los casos de colitis indeterminada (5-15% de los casos) ya que el compromiso del ID nos lleva al planteo de enfermedad de Crohn en detrimento de la colitis ulcerosa. La CE altera el diagnóstico en un 29-40% de estos pacientes lo que tiene gran importancia en el manejo de las opciones de tratamiento médico (uso de agentes biológicos, por ejemplo) así también como de tratamientos quirúrgicos. En pacientes persistentemente sintomáticos la CE identifica actividad inflamatoria en un 89% de los casos contra un 49% de la ileocolonoscopía (24). Figura 4.
Un aspecto importante antes de indicar la CE en estos pacientes es descartar la presencia de estenosis lo que contraindica formalmente este estudio. La tasa de retención si se toma en cuenta exclusivamente a los pacientes con enfermedad de Crohn es de 5% siendo reportado en un estudio cifras más altas que llegaban al 13% (25). Para minimizar esta posible complicación se debe interrogar de forma exhaustiva síntomas orientadores de suboclusión intestinal que nos pongan en la pista de posibles estenosis, en dicho caso, se realizará en primera instancia estudios radiológicos contrastados y/o cápsula Patency. La misma se trata de una cápsula biodegradable, reabsorbible, que no toma fotografías pero descarta estenosis ya que presenta las mismas medidas que la CE por lo que su expulsión entera sin deformaciones asegura permeabilidad del ID.
La CE presenta una alta sensibilidad para el diagnóstico de enfermedad de Crohn (83-93%) pero la especificidad baja notablemente (53-84%). Esto se debe a que a pesar de que son utilizados dos scores diagnósticos para la enfermedad de Crohn (CECDAI y Lewis score) estos no han sido ampliamente validados dada su pobre relación con marcadores inflamatorios como la calprotectina fecal y la proteína Creactiva por lo que existe una elevada posibilidad de detectar lesiones mucosas que en realidad corresponden a otras patologías (falsos positivos) (26,27). Por ejemplo, son muy frecuentes las erosiones por el consumo de AINES y también se ha documentado erosiones en sujetos controles sanos por lo que es importante adecuar los hallazgos con la historia clínica para no sobre diagnosticar esta patología (28). Deben considerarse diagnósticos diferenciales a su vez las lesiones provocadas por infecciones y las vasculitis. La EDB por su parte permite la toma de biopsias para diagnóstico histológico y descartar diferenciales (enteritis eosinofílica, enteropatía por AINES, enfermedad deBehcet, tuberculosis) además de la realización de dilataciones en caso de enfermedad de Crohn con patrón estenosante o estenosis posquirúrgicas con una tasa de éxito de entre 80%-89% (29). La recurrencia tras la dilatación varía entre 13% y 90% pero estos pacientes pueden seguir siendo sometidos a varias sesiones de dilatación evitando así un acto quirúrgico.
La necesidad de sesiones repetidas de dilatación no disminuye la efectividad del procedimiento por lo que pueden realizarse en los intervalos de tiempo que sean necesarios dependiendo de la clínica de los pacientes. Un tercio de los mismos requieren una sola sesión de dilatación y un 25% necesitarán sesiones repetidas (30). Si bien es un procedimiento relativamente seguro hay que tener en cuenta el riesgo de perforación el cual se ve aumentado en caso de estenosis mayores de 5 cm, ulceradas y con un importante componente inflamatorio asociado. Una estrategia adecuada parece ser la realización de dilataciones en forma gradual hasta alcanzar un diámetro óptimo que mejore la sintomatología del paciente.
Enfermedad celiaca
Se trata de una enfermedad sistémica con máxima expresión en el ID, de patogenia autoinmune, con un desencadenante ambiental determinado, el gluten y que se desarrolla en individuos genéticamente susceptibles. Los síntomas de su presentación son muy variados, pueden incluir, diarrea crónica, distensión abdominal, pérdida de peso, anemia y luego de la realización de serología (anticuerpos antitransglutaminasa, deaminados de gliadina, antiendomisio) se requiere la realización de biopsias duodenales para confirmar el diagnóstico. Sin embargo, la atrofia vellositaria característica de esta patología puede iniciarse en sectores distales, hacia el yeyuno o bien adquirir un patrón parcheado por lo que en casos de alta sospecha (síntomas y/o serología compatible) con biopsias duodenales negativas puede la CE y la EDB cumplir un importante rol. La CE, gracias a su capacidad de visualizar la mucosa de todo el ID, puede poner de manifiesto la presencia o no de elementos sugestivos de atrofia con una sensibilidad del 85% y una especificidad del 100% (similar a la alcanzada con la endoscopía de magnificación) (31).
La EDB complementa nuevamente a la VCE ya que permite la toma de biopsias que pueden establecer un correcto diagnóstico histológico. El mayor impacto de estas técnicas sin embargo se establece en aquellos pacientes que ya cuentan con el diagnóstico de la enfermedad, pero no responden al tratamiento. Se define enfermedad celiaca refractaria al tratamiento aquella que no responde a la dieta libre de gluten luego de 6 meses de iniciada y luego de descartar otras causas de atrofia vellositaria. En esta situación es fundamental el estudio endoscópico del ID mediante CE al igual que en los casos donde la enfermedad se acompaña de síntomas de alarma (pérdida de peso, fiebre, dolor abdominal intenso, sangrados digestivos) ya que es indispensabledescartar complicaciones de la enfermedad como linfomas de células T, yeyunoileítis ulcerativa y adenocarcinoma (32,33).
Tumores de intestino delgado y poliposis intestinal
Solamente el 5% de los tumores digestivos se presentan en el ID (34). Esto se debe a múltiples factores, como una elevada inmunidad local, enzimas que degradan diferentes carcinógenos y un rápido y continuo recambio celular entre otros. La sintomatología de estos tumores suele ser inespecífica y compartida con múltiples patologías (distensión abdominal, anemia, pérdida de peso, vómitos, diarrea) por lo que sumado a la falta de estudios específicos para explorar el ID su diagnóstico se realizaba en etapas tardías. La CE permite diagnosticar diferentes tumores en estadios tempranos evitando de esa forma las complicaciones de los mismos (oclusión intestinal, perforación, hemorragia digestiva franca) brindando por lo tanto mayores oportunidades para realizar tratamientos con fines pretendidamente curativos.
Un 27,3% de los tumores de ID pueden diagnosticarse exclusivamente con la CE no siendo detectables por otros métodos (35). Los tumores malignos más frecuentes son los carcinoides (35-42%) seguidos por los adenocarcinomas (30-40%), linfomas y tumores estromales (GIST) (36,37). La ubicación más frecuente es el yeyuno (40%-60%). Suelen ser tumores protruyentes, hipervascularizados, ulcerados y con engrosamiento de pliegues circundantes. También pueden encontrase tumores metastásicos, fundamentalmente de melanomas, próstata, pulmón y riñon. En el grupo de tumores benignos los estromales son los más frecuentes pudiendo encontrar además pólipos inflamatorios, lipomas, hamartomas entre otros (36).
Cuando se trata de una masa tumoral única la CE puede no observarla en un 19% de los casos (38). Esto puede deberse a una inadecuada preparación o a un tránsito acelerado que impide la correcta visualización mucosa por lo que si la sintomatología es orientadora y la CE no muestra resultados positivos está indicada la realización de la EDB que presenta un rédito diagnóstico para tumores de ID de entre 94 y 100%. La CE es el método de elección para el diagnóstico y seguimiento de pacientes portadores de síndromes polipósicos. La poliposis adenomatosa familiar (PAF) se caracteriza por la presencia de más de 100 pólipos adenomatosos a nivel de colon y recto, lo que lleva a una probabilidad del 100% de desarrollar cáncer colorrectal. Pero los pólipos pueden desarrollarse además en el ID (50%-90% de los pacientes) y presentan por tanto un aumento en las probabilidades de desarrollar neoplasias a nivel duodenal y periampular (4%-12% a lo largo de la vida) (39).
La CE permite el seguimiento de estos pacientes para diagnosticar en forma precoz lesiones pasibles de resección mediante endoscopía común, EDB o por vía quirúrgica. El síndrome de Peutz-Jeghers es una enfermedad hereditaria, de transmisión autosómica dominante caracterizada por una pigmentación oscura en la mucosa de la boca y labios junto con la presencia de pólipos intestinales hamartomatosos. El ID es donde asientan los pólipos con mayor frecuencia (70%-90%). Dado el riesgo aumentado de desarrollar una neoplasia en esta topografía deben ser seguidos mediante CE. Se recomienda la CE cada 3 años a partir de los 8 años de edad (40,41). Los pólipos mayores de 5 mm deben ser extraídos mediante polipectomía para evitar las complicaciones tanto benignas (obstrucción intestinal, intususcepción) como malignas (cáncer) por lo que la EDB nuevamente se transforma en el método complementario ideal ya que permite realizar la extracción de los pólipos evitando cirugías reiteradas. (Figura 3.)
Otras indicaciones
La accesibilidad a estas nuevas técnicas junto con los buenos resultados que muestran llevan a que estén aumentando las indicaciones de las mismas. La EDB puede permitir la realización de una colangiopancreatografía retrógrada endoscópica (CPRE), en pacientes que presenten una anatomía alterada del tracto gastrointestinal, por ejemploluego de una resección gástrica tipo Billroth II o una anastomosis en Y de Roux (42,43). Esta técnica puede servir de forma diagnóstica y sobretodo terapéutica, ya que permite la extracción de cálculos de la vía biliar, así como la colocación de prótesis biliares o la dilatación de las estenosis. Además, los pacientes que fueron sometidos a cirugía bariátrica y bypass gástrico también se pueden beneficiar con la EDB para acceder a la vía biliar (44). La CE puede tener un rol importante en el estudio de la enteropatía en pacientes con VIH, en la inmunodeficiencia variable común, en la enfermedad de injerto vs huésped y hasta en el dolor abdominal crónico, pero todavía no se ha establecido en que lugar del algoritmo diagnóstico de estas patologías deben colocarse (45).
PERSPECTIVAS FUTURAS
La CE y la EDB se han convertido en métodos confiables y certeros para explorar y tratar las múltiples patologías del ID. A su vez el desarrollo de estas nuevas tecnologías es incipiente y ya se encuentran en desarrollo prototipos de cápsulas que pueden dirigirse manualmente para poder detenerse y observar detalladamente una lesión, tomar biopsias y hasta liberar fármacos (46). La enteroscopía también cuenta con constantes avances, por ejemplo, se encuentran en desarrollo equipos con mayor definición de imagen, posibilidad de realizar tinciones electrónicas, canales de trabajo accesorios para realizar procedimientos terapéuticos complejos y sistemas de inserción automáticos (47). Por lo tanto, la CE y la EDB permiten el día de hoy diagnosticar y tratar las múltiples patologías del ID generando un cambio radical en el abordaje de estos pacientes.
Conflicto de intereses: Los autores no declaran ningún conflicto de interés.
Financiamiento: Este trabajo no ha recibido soporte financiero alguno para su elaboración.
REFERENCIAS BIBLIOGRÁFICAS
1. Rondonotti E, Villa F, Mulder CJ, Jacobs MA, de Franchis R. Small bowel capsule endoscopy in 2007: indications, risks and limitations. World J Gastroenterol. 2007;12(46):6140-9. [ Links ]
2. Niv Y. Efficiency of bowel preparation for capsule endoscopy examination: a meta analysis. World J Gastroenterol. 2008;14(9):1313-7. [ Links ]
3. Rokkas T, Papaxoinis K, Triantafyllou K, Pistiolas D, Ladas SD. Does purgative preparation influence the diagnostic yield of small bowel video capsule endoscopy? A meta analysis. Am J Gastroenterol. 2009;104(1):219-27. [ Links ]
4. Belsey J, Crosta C, Epstein O, Fischbach W, Layer P, Parente F, et al. Meta analysis: efficacy of small bowel preparation for small bowel video capsule endoscopy. Curr Med Res Opin. 2012;28(12):1882-90. [ Links ]
5. Payeras G, Piqueras J, Moreno VJ, Cabrera A, Menendez D, Jimenez R. Effects of capsule endoscopy on cardiac pacemakers. Endoscopy. 2005;37(12):1181-5. [ Links ]
6. Harris LA, Hansel SL, Rajan E, Srivathsan K, Rea R, Crowell MD, et al. Capsule endoscopy in patients with implantable electromedical devices is safe. Gastroenterol Res Pract. 2013;2013:959234. [ Links ]
7. Pennazio M, Santucci R, Rondonotti E, Abbiati C, Beccari G, Rossini FP, et al. Outcome of patients with obscure gastrointestinal bleeding after capsule endoscopy: report of 100 consecutive cases. Gastroenterology. 2004;126(3):643-53. [ Links ]
8. Triester SL, Leighton JA, Leontiadis GI, Fleischer DE, Hara AK, Heigh RI, et al. A meta analysis of the yield of capsule endoscopy compared toot her diagnostic modalities in patients with obscure gastrointestinal bleeding. Am J Gastroenterol. 2005;100(11):2407-18. [ Links ]
9. Liao Z, Gao R, Xu C, Li ZS. Indications and detection, completion, and retention rates of small bowel capsule endoscopy: a systematic review. Gastrointest Endosc. 2010;71(2):280-6. [ Links ]
10. Monkemuller K, Fry LC, Malfertheiner P. Double balloon enteroscopy: beyond feasibility, what do we do now? Endoscopy. 2007;39(3):229-31. [ Links ]
11. Honda W, Ohmiya N, Hirooka Y, Nakamura M, Miyahara R, et al. Enteroscopic and radiologic diagnoses, treatment, and prognoses of small bowel tumors. Gastrointest Endosc. 2012;76(2):344-54. [ Links ]
12. Gerson LB, Batenic MA, Newsom SL, Ross A, Semrad CE. Long-term outcomes after double-balloon enteroscopy for obscure gastrointestinal bleeding. Clin Gastroenterol Hepatol. 2009;7(6):664-9. [ Links ]
13. Yamamoto H, Kita H, Sunada K, Hayashi Y, Sato H, et al. Clinical outcomes of double-balloon endoscopy for the diagnosis and treatment of small intestinal diseases. Clin Gastroenterol Hepatol. 2004;2(11):1010-6. [ Links ]
14. Muhammad A, Pitchumoni CS. Evaluation of iron deficiency anemia in older adults: the role of wireless capsule endoscopy. J Clini Gastroenterol. 2009;43(7):627-31. [ Links ]
15. Leung WK, Ho SS, Suen BY, Lai LH, Yu S, et al. Capsule endoscopy or angiography in patients with acute overt obscure gastrointestinal bleeding: a prospective randomized study with long-term follow up. Am J Gastroenterol. 2012;107(9):1370-6. [ Links ]
16. Bresci G, Parisi G, Bertoni M, Tumino E, Capria A. The role of video capsule endoscopy for evaluating obscure gastrointestinal bleeding: usefulness of early use. J Gastroenterol. 2005;40(3):256-9. [ Links ]
17. Wiarda BM, Heine DG, Mensink P, Stolk M, Dees J, et al. Comparison of magnetic resonance enteroclysis and capsule endoscopy with balloon assisted enteroscopy in patients with obscure gastrointestinal bleeding. Endoscopy. 2012;44(7):668-73. [ Links ]
18. Viazis N, Papaxoinis K, Theodoropoulos I, Sgouros S, Vlachogiannakos J, et al. Impact of capsule endoscopy in obscure small bowel bleeding: defining strict diagnostic criteria for a favorable outcome. Gastrointest Endosc. 2005;62(5):717-22. [ Links ]
19. Teshima CW, Kuipers EJ, van Zanten SV, Mensink PBF. Double balloon enteroscopy and capsule endoscopy for obscure gastrointestinal bleeding: an updated meta analysis. J Gastroenterol Hepatol. 2011;26(5):796-801. [ Links ]
20. Gerson L, Batenic M, Ross A, Semrad C. Long-term outcomes after double balloon enteroscopy for obscure gastrointestinal bleeding. Clin Gastroenterol Hepatol. 2009;7(6):664-9. [ Links ]
21. Rahmi G, Samaha E, Vahedi K, Delvaux M, Gay G, Lamouliatte H, et al. Long-term follow up of patients undergoing capsule and double-balloon enteroscopy for identification and treatment of small-bowel vascular lesions: a prospective, multicenter study. Endoscopy. 2014;46(7):591-7. [ Links ]
22. Byeon JS, Mann NK, Jamil LH, Lo SK. Is a repeat double balloon endoscopy in the same direction useful in patients with recurrent obscure gastrointestinal bleeding? J Clin Gastroenterol. 2013;47(6):494-500. [ Links ]
23. Farmer RG, Hawk WA, Turnbull RB Jr. Clinical patterns in Crohn´s disease: a statistical study of 615 cases. Gastroenterology. 1975;68(4 pt 1):627-35. [ Links ]
24. Dubcenco E, Jeejeebhoy KN, Petroniene R, Tang SJ, Zalev AH, Gardiner GW, et al. Capsule endoscopy findings in patients with established and suspected small-bowel Crohn´s disease: correlation with radiologic, endoscopic, and histologic findings. Gastrointes Endosc. 2005;62(4):538-44. [ Links ]
25. Cheifetz AS, Kornbluth AA, Legnani P, Schmelkin I, Brown A, Lichtiger S, et al. The risk of retention of the capsule endoscope in patients with known or suspected Crohn´s disease. Am J Gastroenterol. 2006;101(10):2218-22. [ Links ]
26. Koulaouzidis A, Douglas S, Plevris JN. Lewis score correlates more closely with fecal calprotectin than capsule endoscopy Crohn´s disease activity index. Dig Dis Sci. 2012;57(4):987-93. [ Links ]
27. Yang L, Ge ZZ, Gao YJ, Li XB, Dai J, Zhang Y, et al. Assessment of capsule endoscopy scoring index, clinical disease activity, and C-reactive protein in small bowel Crohn´s disease. J Gastroenterol Hepatol. 2013;28(5):829-33. [ Links ]
28. Goldstein JL, Eisen GM, Lewis B, Gralnek IM, Zlotnick S, Fort JG et al. Video capsule endoscopy to prospectively assess small bowel injury with celecoxib, naproxen plus omeprazole, and placebo. Clin Gastroenterol Hepatol. 2005;3(2):133-41. [ Links ]
29. Despott EJ, Gupta A, Burling D, Tripoli E, Konieczko K, Hart A, et al. Effective dilation of small bowel strictures by doubleballoon enteroscopy in patients with symptomatic Crohn´s disease (with video). Gastrointest Endosc. 2009;70(5):1030-6. [ Links ]
30. Pohl J, May A, Nachbar L, Ell C. Diagnostic and therapeutic yield of push-and-pull enteroscopy for symptomatic small bowel Crohn´s disease strictures. Eur J Gastroenterol Hepatol. 2007;19(7):529-34. [ Links ]
31. Murray JA, Rubio Tapia A, Van Dyke CT, Brogan DL, Knipschield MA, Lahr B, et al. Mucosal atrophy in celiac disease: extent of involvement, correlation with clinical presentation, and response to treatment. Clin Gastroenterol Hepatol. 2008;6(2):186-93. [ Links ]
32. Barret M, Malamut G, Rahmi G, Samaha E, Edery J, Verkarre V, et al. Diagnostic yield of capsule endoscopy in refractory celiac disease. Am J Gastroenterol. 2012;107(10):1546-53. [ Links ]
33. Culliford A, Daly J, Diamond B, Rubin M, Green PH. The value of wireless capsule endoscopy in patients with complicated celiac disease. Gastrointest Endosc. 2005;62(1):55-61. [ Links ]
34. Schottenfeld D, Beebe-Dimmer JL, Vigneau FD. The epidemiology and pathogenesis of neoplasia in the small intestine. Ann Epidemiol. 2009;19(1):58-69. [ Links ]
35. Pan SY, Morrison H. Epidemiology of cancer of the small intestine. World J Gastrointest Oncol. 2011;3(3):33-42. [ Links ]
36. Cheung DY, Choi MG. Current advance in small bowel tumors. Clin Endosc. 2011;44(1):13-21. [ Links ]
37. Dabaja BS, Suki D, Pro B, Bonnen M, Ajani J. Adenocarcinoma of the small bowel: presentation, prognostic factors and outcome of 217 patients. Cancer. 2004;101(3):518-26. [ Links ]
38. Lewis BS, Eisen GM, Friedman S. A pooled analysis to evaluate results of capsule endoscopy trials. Endoscopy. 2005;37(10):960-5. [ Links ]
39. Akin E, Demirezer Bolat A, Buyukasik S, Algin O, Selvi E, Ersoy O. Comparison between capsule endoscopy and magnetic resonance enterography for the detection of polyps of the small intestine in patients with familial adenomatous polyposis. Gastroenterol Res Pract. 2012;2012:215028. [ Links ]
40. Giardello FM, Brensinger JD, Tersmette AC, Goodman SN, Petersen GM, Booker SV, et al. Very high risk of cancer in familial Peutz-Jeghers syndrome. Gastroenterology. 2000;119(6):1447-53. [ Links ]
41. Beggs AD, Latchford AR, Vasen HF, Moslein G, Alonso A, Aretz S, et al. Peutz-Jeghers syndrome: a systematic review and recomendations for management. Gut. 2010;59(7):975-86. [ Links ]
42. XinL , Liao Z, Jiang YP, Li ZS. Indications, detectability, positive findings, total enteroscopy, and complications of diagnostic double-balloon endoscopy: a systematic review of data over the first decade of use. Gastrointest Endosc 2011;74(3):563-70. [ Links ]
43. Maaser C, Lenze F, Bokemeyer M, Ullerich H, Domaqk D, et al. Double balloon enteroscopy: a useful tool for diagnostic and therapeutic procedures in the pancreaticobiliary system. AM J Gastroenterol. 2008;103(4):894-900. [ Links ]
44. Hamdan K, Somers S, Chand M. Management of late postoperative complications of bariatric surgery. Br J Surg. 2011;98(10):1345-55. [ Links ]
45. May A, Manner H, Schneider M, Ipsen A, Ell C. Prospective multicenter trial of capsule endoscopy in patients with chronic abdominal pain, diarrhea and other signs and symptoms (CEDAP-Plus Study). Endoscopy. 2007;39(7):606-12. [ Links ]
46. Lin OS. Breaching the final frontier: the future of small intestinal capsule endoscopy. Gastrointest Endosc. 2008;68(3):495-8. [ Links ]
47. Hayashi Y, Sunada K, Yamamoto H. Prototype holder adequately supports the overtube in balloon-assisted endoscopic submucosal dissection. Dig Endosc. 2014;26(5):682. [ Links ]
Correspondencia:
Federico De Simone Avda. Brasil 3062 apto 502. Montevideo. Uruguay
E-mail: fedesi05@yahoo.com.ar
Recibido: 16-4-2016
Aprobado: 22-7-2016