Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú vol.37 no.1 Lima ene./mar. 2017
REPORTE DE CASO
Hemorragia digestiva e insuficiencia hepática aguda por leptospirosis: una entidad que no debemos olvidar
Gastrointestinal bleeding and acute hepatic failure by leptospirosis: an entity that should not be forgotten
Carlos Alventosa Mateu¹, Lydia Plana Campos¹, Laura Larrey Ruíz¹, Raquel Acedo Mayordomo², Laura Sanchís Artero¹, Laura Peño Muñoz¹, Paola Concepción Núñez Martínez¹, Génesis Aurora Castillo López¹, Mercedes Latorre Sánchez¹, Juan José Urquijo Ponce¹, Moisés Diago Madrid¹, Javier Sempere García-Argüelles¹
1 Servicios de Aparato Digestivo, Consorcio Hospital General Universitario de Valencia. Valencia, España.
2 Servicio de Anatomía Patológica, Consorcio Hospital General Universitario de Valencia. Valencia, España.
RESUMEN
La leptospirosis es una enfermedad causada por la espiroqueta Leptospira. Se trata de una zoonosis de distribución mundial, con predominio en los trópicos. En España no es frecuente pero sí se observan casos en zonas más húmedas o con presencia de ríos, lagos o estanques, como son Cataluña, Andalucía o la Comunidad Valenciana, donde se relaciona con los arrozales. Los transmisores son múltiples animales como vacas o ratas, contagiándose el ser humano mediante contacto directo con estos animales o su orina, o bien de forma indirecta al consumir o estar en contacto con agua contaminada por la orina de éstos. Las manifestaciones clínicas son muy variables, siendo asintomática o poco sintomática en la mayoría de los pacientes. Aunque no ocurre siempre, la leptospirosis cursa con una primera fase con fiebre, mialgias, afectación renal o hemorragia de distintos órganos, seguida de una segunda fase con presencia de ictericia por afectación hepática. La enfermedad de Weil es una forma de leptospirosis grave caracterizada por afectación hepática con ictericia e insuficiencia renal aguda, asociada a una considerable mortalidad. El diagnóstico se basa en técnicas serológicas y detección de DNA mediante PCR. El tratamiento consta de medidas de soporte y antibioticoterapia. Presentamos un paciente con enfermedad de Weil y hemorragia digestiva por leptospirosis, con una evolución clínica fulminante, y hacemos hincapié en la necesidad de tener presente esta entidad, especialmente en ambientes epidemiológicos favorables como el de este paciente, con el fin de lograr un diagnóstico precoz.
Palabras clave: Leptospirosis; Enfermedad de Weil; Infecciones por espiroqueta; Ictericia (fuente: DeCS BIREME).
ABSTRACT
Leptospirosis disease is caused by the spirochete Leptospira. It is a worldwide distribution zoonosis, with predominance in the tropics. In Spain, it is not frequent but some cases have been noticed especially in humid areas surrounded by rivers, lakes or ponds, such as Catalonia, Andalucia or the Valencian Community. It is transmitted by a variety of animals such as cows or rats, that are infected either by direct contact with these animals or their urine, or indirectly by consuming or being in contact with water contaminated by their urine. The clinical manifestations are very variable, being asymptomatic or not very symptomatic in most of the patients. Unusually, leptospirosis presents with a first phase with fever, myalgias, liver injury or different organs hemorrhage, followed by a second phase with the presence of jaundice due to hepatic failure. Weil's disease is a kind of severe leptospirosis characterized by hepatic failure with jaundice and acute renal failure, associated with high mortality rates. The diagnosis is based on serological techniques and DNA detection by PCR. The treatment consists of life support measures and antibiotic therapy. A patient with Weil's disease and leptospirosis digestive bleeding is presented, with a fulminant clinical course. In order to achieve an early diagnosis, the need to keep this entity in mind must be emphasized, especially in favorable epidemiological environments as the one of this patient.
Keywords: Leptospirosis; Weil disease; Spirochaetales infections; Jaundice (source: MeSH NLM).
INTRODUCCIÓN
La leptospirosis es una de las zoonosis más ampliamente distribuidas por todo el mundo, siendo endémica de las zonas tropicales como Perú, con varios brotes epidémicos en este país en zonas húmedas relacionadas normalmente con consumo de agua contaminada (1).
Sin embargo, es poco prevalente en España, si bien existen casos en zonas húmedas como la Comunidad Valenciana, que es una de las regiones donde más se diagnostican, especialmente debido al cultivo de arroz. Además, los recientes cambios demográficos y el turismo a zonas endémicas han hecho que sea considerada como una enfermedad emergente (2-4).
Está causada por la espiroqueta aerobia Leptospira spp y se trasmite al ser humano a través de múltiples animales, normalmente de forma indirecta a través de agua contaminada. El diagnóstico puede ser complejo debido a la gran variedad de síntomas de presentación. Dado que existen casos en que esta entidad es grave, es de vital importancia el diagnóstico y tratamiento precoz, especialmente en zonas donde se dan las características epidemiológicas adecuadas como es la nuestra (2).
A este respecto, presentamos el caso clínico de un paciente de nuestra zona que desarrolló una leptospirosis con hemorragia digestiva, fracaso renal y afectación hepática aguda (enfermedad de Weil) con una evolución fulminante, causando la muerte del paciente.
CASO CLÍNICO
Se trata de un hombre de 60 años de edad, agricultor de profesión y con antecedentes personales de hemangiomas hepáticos y enolismo moderado (4 UBE/día) que ingresa por cuadro de dolor abdominal difuso de 3 días de evolución asociado a astenia, mialgias y fiebre termometrada sin presencia de signos meníngeos, lesiones cutáneas, adenopatías palpables ni soplos cardíacos en la exploración física. En la analítica sanguínea destaca insuficiencia renal aguda (urea de 109 mg/dL, creatinina de 2,37 mg/dL), junto con leucocitosis leve, elevación de la Proteína C Reactiva y una función hepática normal. El paciente no refería consumo de AINES u otros fármacos ni viajes al extranjero. Se realiza radiografía de tórax y sedimento de orina que son normales así como una ecografía abdominal que objetiva una colelitiasis sin signos de colecistitis y dos hemangiomas hepáticos ya conocidos, siendo la vía biliar y el sistema nefrourinario de características normales.
En las primeras 48 horas de ingreso el paciente presenta un empeoramiento de la función hepática con niveles de bilirrubina total de 11,81 mg/dL, con una bilirrubina directa de 7,56 mg/dL, y valores de GPT 73 U/L, GOT 100 U/L, FA 91 U/L y GGT 87 U/L. También destaca agravamiento de la función renal alcanzando la creatinina valores de 6,1 mg/dL por lo que se decide realizar hemodiálisis. Además, existía un descenso progresivo del número de plaquetas hasta 22 000/µlitro y de la hemostasia hasta alcanzar un Índice de Quick del 38%. Dado el empeoramiento de la función hepática se realiza estudio con autoanticuerpos, serología de virus hepatotropos, rickettsia, citomegalovirus y LUES que son negativos, junto con una nueva ecografía abdominal, que no muestra cambios respecto a la previa. Puesto que persisten la fiebre, el dolor abdominal y ante la posibilidad de un cuadro de colangitis aguda se inicia tratamiento intravenoso con Piperazilina-Tazobactam.
El quinto día de ingreso, el paciente presenta un cuadro de crisis comicial junto a sufusión hemorrágica conjuntival, siendo normales las pruebas de imagen cerebrales que se le practican en ese momento. Ante la sospecha de que se trate de un cuadro de leptospirosis icterohemorrágica se solicita la detección de su ADN mediante reacción en cadena de la polimerasa (PCR) en sangre y orina y se añade tratamiento antibiótico con ceftriaxona.
En el sexto día de ingreso, existe un deterioro del estado general asociado a epistaxis, hemorragia digestiva alta y hematuria por lo que se procede a traslado a la Unidad de Cuidados Intensivos. Se practica una gastroscopia urgente en la que se objetivan abundantes restos hemáticos frescos junto con sangrado activo por sufusión hemorrágica de toda la mucosa gástrica y esófagica, sin observar otras lesiones. Se procede a transfusión sanguínea, reposición de plaquetas y corrección de la coagulación.
En las siguientes horas se agrava el empeoramiento de la función hepática y renal, alcanzando unos niveles de Bilirrubina total de 12 mg/dL, junto a una GPT de 419 U/I, urea de 325 mg/dL y creatinina de 10,57 mg/ dL, junto a un empeoramiento clínico del paciente, falleciendo finalmente el paciente el séptimo día de ingreso.
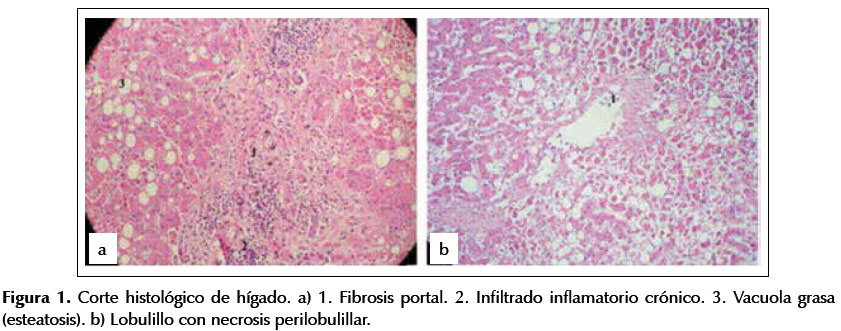
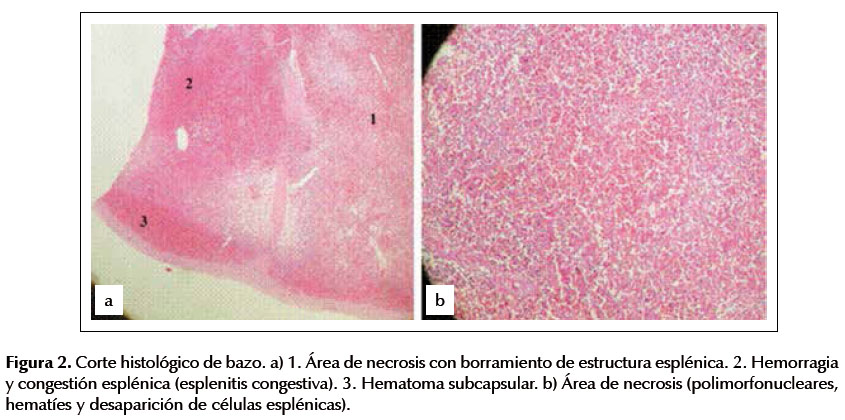
Se realiza necropsia evidenciando una gastritis y duodenitis petequial hemorrágica sin ulceraciones junto con un parénquima hepático con necrosis perilobulillar y congestión esplénica con focos de hemorragia subcapsular, hallazgos compatibles con afectación por leptospirosis (Figuras 1 y 2). Posteriormente se recibe el resultado de la PCR para espiroquetas que es positivo para Leptospira spp confirmándose definitivamente la sospecha diagnóstica.
DISCUSIÓN
La leptospirosis es una enfermedad producida por espiroquetas del género Leptospira spp. Según sus características genotípicas se divide en más de 260 subespecies y según sus características genómicas existen 21 subespecies, de las cuales 9 son patogénicas, siendo las infecciones humanas normalmente producidas por la variedad L. interrogans, siendo L. interrogans icterohemorragiae la habitualmente relacionada con los casos de mayor gravedad (2,5,6).
Se trata de una zoonosis de distribución mundial con predominio en los trópicos, ya que es más frecuente en zonas con climas templados, áridos y húmedos, especialmente en zonas con ríos, lagos o estanques, como son ciertas regiones de Perú como Loreto o Madre de Dios. El reservorio de la leptospira son animales (mamíferos, reptiles, anfibios y aves) que contaminan el agua al eliminar este microorganismo mediante la orina (2,6,7). El contagio en humanos puede darse mediante contacto directo con animales u orina infectada de éstos o bien de forma indirecta mediante contacto cutáneo o mucoso con agua contaminada, habiéndose descrito casos tanto por ingesta de agua como por inhalación de aerosoles. También puede transmitirse por leche materna o incluso de persona a persona. Las personas afectadas suele ser varones que habitan en zonas rurales o zonas con escasez de condiciones higiénicas en las grandes ciudades, aunque el turismo a zonas endémicas de leptospirosis ha convertido esta entidad en una enfermedad emergente en los viajeros (2,3,8,9).
En España se trata de una entidad poco frecuente. Fue enfermedad de declaración obligatoria hasta 1997, con entre 7 y 24 casos anuales declarados hasta ese año a nivel nacional, predominantemente en Cataluña, Andalucía y la Comunidad Valenciana (4). En esta última, que es nuestra región, probablemente esté en relación con los arrozales, pudiendo ser el contacto o la ingesta de agua contaminada la causante de la enfermedad en nuestro paciente.
Las manifestaciones clínicas cubren un amplio espectro que va desde casos asintomáticos hasta formas graves como la enfermedad de Weil, que consiste en afectación hepática con ictericia e insuficiencia renal. Tras una fase de incubación que dura entre 5 y 21 días, la leptospirosis presenta una primera fase o fase leptospirémica, de 7 días de duración, caracterizada por la presencia de leptospiras en sangre y líquido cefalorraquídeo y cursa con fiebre, cefalea, mialgias, afectación renal y fenómenos hemorrágicos. Se sigue de una segunda fase o fase inmune en la que se producen anticuerpos IgM circulantes y leptospiruria, con presencia de ictericia por afectación hepática y fenómenos de anemia hemolítica intravascular y trombopenia.
Sin embargo, la mayoría de las ocasiones el paciente está asintomático o poco sintomático y además muchas veces no se consiguen distinguir las dos fases, siendo los síntomas predominantes tos seca, fiebre, cefalea, mialgias, náuseas, vómitos o diarrea. La enfermedad de Weil es una forma grave de leptospirosis (5-10% de los casos), en la que la evolución suele ser fulminante, tal y como aconteció a nuestro paciente. El signo clínico más característico de esta enfermedad es la hemorragia conjuntival, que en nuestro caso fue el dato que nos hizo sospechar que estábamos ante un caso de leptospirosis (3,10,11).
El método diagnóstico utilizado es la serología, mediante técnicas de MAT o ELISA. Disponemos también de una técnica de reacción en cadena de la polimerasa (PCR) que proporciona un rápido diagnóstico, detectando el DNA de las leptospiras en sangre y orina desde el inicio de la enfermedad e incluso en casos en que se esté administrando antibiótico, con altas tasas de sensibilidad y especificidad (> 95%), por lo que este suele ser el mejor método diagnóstico. Sin embargo, la serología suele ser de más utilidad que la PCR en la fase inmune (12). En los últimos años están apareciendo nuevas técnicas diagnósticas moleculares basados en técnicas de análisis HRM o MLVA (6).
El tratamiento de la leptospirosis consta de medidas de soporte y antibióticos, estando recomendados doxiciclina, ampicilina, amoxicilina, eritromicina y azitromicina para los casos leves y penicilina G sódica, ampicilina, cefotaxima y ceftrixona para los casos graves. En casos graves, la ceftriaxona y la penicilina G han demostrado resultados similares, pero la ceftriaxona presenta una posología más sencilla (2,13,14). También se han mostrado útiles los glucocorticoides en las formas severas con hemorragia pulmonar, trombocitopenia y fallo renal (15). Estos pacientes presentan una importante mortalidad, por lo que es primordial iniciar tratamiento antibiótico lo más precozmente posible (2). Se han relacionado la edad mayor de 60 años, el fallo renal y la ictericia como factores pronósticos de mayor mortalidad, mientras que la mortalidad en pacientes anictéricos es baja (16).
Queremos remarcar la importancia de tener presente esta entidad, ya que, aunque es infrecuente aún siguen presentándose casos, especialmente en ambientes favorables como el de nuestro paciente. La sospecha clínica es fundamental para llegar al diagnóstico lo más precozmente posible, más teniendo en cuenta la rápida evolución que pueden tener algunos casos como el nuestro, en el cual, aunque sospechamos la enfermedad e iniciamos tratamiento antibiótico, el paciente falleció pocas horas después, siendo el diagnóstico definitivo post-mortem.
REFERENCIAS BIBLIOGRÁFICAS
1. Russell KD, Montiel-González MA, Watts DM, Lagos-Figueroa RC, Chauca G, Ore M, et al. An outbreak of leptospirosis among Peruvian military recruits. Am J Trop Med Hyg. 2003;69(1):53-7. [ Links ]
2. Bharti AR, Nally JE, Ricaldi JN, Matthias MA, Diaz MM, Lovett MA, et al. Leptospirosis: a zoonotic disease of global importance. Lancet Infect Dis. 2003;3(12):757-71. [ Links ]
3. Sarkar J, Chopra A, Katageri B, Raj H, Goel A. Leptospirosis: a re-emerging infection. Asian Pac J Trop Med. 2012;5(6):500-2. [ Links ]
4. Barragán-Casas JM, Álvarez-Suárez D, Arroyo-Burguillo P, Sánchez-Fuentes D. Medifam. 2001;11(3):171-4. [ Links ]
5. Ganoza CA, Matthias MA, Collins-Richards D, Brouwer KC, Cunningham CB, Segura ES, et al. Determining risk for severe leptospirosis by molecular analysis of environmental surface waters for pathogenic leptospira. PLoS Med. 2006;3(8):e308. [ Links ]
6. Naze F, Desvars A, Picardeau M, Bourhy P, Michault A. Use of a new high resolution melting method for genotyping pathogenic Leptospira spp. PLoS One. 2015;10(7):e0127430. [ Links ]
7. Evangelista KV, Coburn J. Leptospira as an emerging pathogen: a review of its biology, pathogenesis and host immune responses. Future Microbiol. 2010;5(9):1413-25. [ Links ]
8. Lau CL, Smythe LD, Weinstein P. Leptospirosis: an emerging disease in travelers. Travel Med infect Dis. 2010;8(1):33-9. [ Links ]
9. Lagi F, Corti G, Meli M, Pinto A, Bartoloni A. Leptospirosis acquired by tourists in Venice, Italy. Jour Trav Med. 2013;20(2):128-30. [ Links ]
10. Gancheva GI. Leptospirosis in elderly patients. Braz J Infect Dis. 2013;17(5):592-5. [ Links ]
11. Lin PC, Chi CY, Ho MW. Demographic and clinical features of leptospirosis: three-year experience in central Taiwan. J Microbiol Immunol Infect. 2008;41(2):145-50. [ Links ]
12. Lavett PN, Morey RE, Galloway RL, Turner DE, Steigerwalt AG, Mayer LW. Detection of pathogenic leptospires by realtime quantitative PCR. J MED Microbiol. 2005;54(Pt 1):45-9. [ Links ]
13. Griffith ME, Hospenthal DR, Murray CK. Antimicrobial therapy of leptospirosis. Curr Opin Infect Dis. 2006;19(6):533-7. [ Links ]
14. Panaphut T, Domrongkitchaiporn S, Vibhagool A, Thinkamrop B, Susaengrat W. Ceftriaxone compared with sodium penicillin G for treatment of severe leptospirosis. Clin Infect Dis. 2003;36(12):1507-13. [ Links ]
15. Dursun B, Bostan F, Artac M, Varan HI, Suleymanlar G. Severe pulmonary haemorrage accompanying hepatorenal failure in fulminant leptospirosis. Int J Clin Pract. 2007;61(1):164-7. [ Links ]
16. Taylor AJ, Paris HD, Newton PN. A systematic review of the mortality from untreated leptospirosis. PLoS Negl Trop Dis. 2015;9(6):e0003866. [ Links ]
Correspondencia:
Carlos Alventosa Mateu Av. Tres Cruces nº2. C.P: 46014. Valencia - España.
E-mail: almacar84@hotmail.com
Recibido: 22-2-2016
Aprobado: 12-6-2016