INTRODUCCIÓN
El primer reporte de una esofagectomía llevada a cabo con éxito en cáncer de esófago (CE) se le atribuye al cirujano germano-americano Franz Torek en 1913 1. El carcinoma de células escamosas esofágicas y el adenocarcinoma representan el 95% de todas las neoplasias malignas esofágicas. Las tasas de adenocarcinoma de esófago han aumentado en los países occidentales, siendo actualmente el tipo predominante de CE 2. El incremento en las cifras de CE y la preponderancia del adenocarcinoma, también se ve reflejado en nuestro país 3. La esofagectomía es el método estándar actual de tratamiento en el CE y ha tenido una transformación hacia un enfoque mínimamente invasivo con el uso de métodos endoscópicos que se utilizan para el cáncer superficial y un uso más frecuente de modalidades asistidas por laparoscopia y robótica para tumores localmente avanzados 4,5.
Los procedimientos estándar en cirugía por CE incluyen la disección de la porción esofágica comprometida, la formación del conducto gástrico y la creación de la anastomosis esofagogástrica. Las anastomosis esofagogástrica puede construirse a mano o con el uso de grapadoras mecánicas. Tradicionalmente, la anastomosis hecha a mano se puede realizar con 1 o 2 planos de sutura, los cuales pueden ser con puntos continuos o separados 6. La anastomosis mecánica se puede realizar utilizando grapas circulares o lineales 7. Las técnicas de anastomosis esofagogástrica utilizadas en la reconstrucción son complejas y están asociadas a complicaciones postoperatorias, las cuales se ven aumentadas por el frecuente deterioro clínico, nutricional y los avanzados estados de estos tumores en nuestro medio 8. Las complicaciones postoperatorias tempranas, como la fuga anastomótica siguen siendo una complicación importante después de la esofagectomía. Las tasas de mortalidad oscilan entre 5 y 9% 9. También se asocian con estancias hospitalarias más prolongadas, con mayores costos hospitalarios 10 y tienen un impacto negativo al afectar la sobrevida global de forma desfavorable (mediana: 36 vs 55 meses) y la supervivencia libre de enfermedad (mediana: 34 vs 48 meses) 11. Si bien existe creciente literatura sobre las complicaciones relacionadas a la fuga anastomótica, los factores asociados con estas fugas son poco conocidos 12,13.
Las tasas de estenosis de la anastomosis se encuentran reportadas entre el 10-56%, mientras que las tasas de fuga anastomótica varían entre el 2-20% en las esofagectomías con anastomosis cervical; las anastomosis cervicales muestran tasas más altas de filtración que las anastomosis intratorácicas, sin embargo, las filtraciones cervicales suelen tener menores tasas de mortalidad y su manejo, con frecuencia, es más sencillo 14. Una técnica quirúrgica adecuada en el momento de la realización de la anastomosis parece ser el factor más determinante para evitar este tipo de complicaciones, asegurando construcciones de anastomosis libres de tensión y con conductos gástricos reemplazantes que cuenten con un adecuado suministro sanguíneo, teniendo en cuenta que debido a las diferencias anatómicas inherentes entre el esófago y el estómago ascendido hacen que estas anastomosis sean más propensas a filtrar al compararse con otro tipo de anastomosis gastrointestinales 15.
En el presente estudio comparamos los resultados postoperatorios en la esofagectomía transhiatal con reconstrucción esofagogástrica cervical realizada a mano y la reconstrucción realizada con sutura mecánica en términos de fuga anastomótica y estenosis, duración de la intervención y la morbimortalidad general en un periodo de seguimiento no menor a un año.
MATERIALES Y MÉTODOS
Selección de pacientes y definiciones
Este estudio de cohorte retrospectivo en una base de datos de seguimiento prospectivo, se evaluaron 68 pacientes sometidos a esofagectomía por cáncer en el período de enero de 2011 y diciembre de 2018. Los datos recopilados incluyeron características demográficas del paciente, comorbilidades (cardíacas, pulmonares, diabetes) y características del tumor, variables intraoperatorias (anastomosis manual versus mecánica), características postoperatorias, complicaciones postoperatorias según la clasificación de Clavien-Dindo, fuga anastomótica y estenosis, y el resultado del seguimiento no menor a un año después de la cirugía.
Las cirugías fueron realizadas en tres centros hospitalarios de tercer nivel de la ciudad de Medellín, en los dos últimos años se hicieron los primeros abordajes por laparoscopia.
Los pacientes se clasificaron en dos grupos según el tipo de anastomosis recibida: manual o mecánica con grapadora de 45 mm. Se registró la duración de la estancia y la pérdida de sangre operatoria para cada procedimiento. Los resultados principales incluyeron fuga anastomótica a corto plazo, estenosis anastomótica, disfagia y mortalidad intrahospitalaria y a los 30 días; Los resultados a largo plazo incluyeron disfagia clínicamente significativa que requirió dilatación endoscópica
La técnica de anastomosis esófago-gástrica mecánica
Previo a la anastomosis enfatizamos la importancia del estado normovolémico intraoperatorio y en el postoperatorio temprano, así como el evitar los vasoconstrictores. La hipovolemia y los vasoconstrictores pueden poner en peligro el extremo proximal, relativamente isquémico, del conducto gástrico ascendido y aumentar el riesgo de una fuga anastomótica.
El esófago liberado completamente en su circunferencia (Figura 1A), es luego reparado con un dren de Penrose. El esófago se divide con una grapadora lineal (Figura 1B) preservando tanto esófago cervical como sea posible.
El esófago se alinea sobre el extremo gástrico proximal (Figura 1C). La línea de grapas del esófago se recorta abriéndolo, y se realiza una gastrotomía 2 a 3 cm distal al extremo gástrico ascendido con su línea de grapas. Se ponen suturas de anclaje de espesor total para alinear los puntos medios, derecho e izquierdo entre el conducto gástrico y el esófago para la anastomosis (Figura 1D).
Se coloca una grapadora lineal de 45 mm entre el esófago cervical y el conducto gástrico para crear la pared posterior de la anastomosis (Figura 1E).
Se avanza una sonda nasogástrica a través de la anastomosis bajo visualización directa (Figura 1F) y se coloca cerca del píloro. Esto se confirma mediante la palpación gástrica a través del abdomen al final de la intervención, antes de que la SNG se asegure firmemente en la nariz.
Luego, la cara anterior de la anastomosis se completa con una sutura de espesor total, con PDS 3-0 o 4-0 que se extienden desde las esquinas opuestas hasta unirse en el medio (Figura 1G).
Para la capa exterior se utilizan puntadas seromusculares interrumpidas de seda 4-0 o Vicryl 3-0 (Figura 1H). Por contrabertura en la fosa supraclavicular izquierda se coloca un drenaje de 10 Fr o preferiblemente un Penrose, por delante de la anastomosis y se dirige hacia el mediastino superior a lo largo del conducto gástrico.
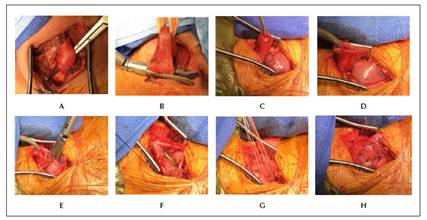
Figura 1 Secuencia en la técnica de anastomosis esofagogástrica. A. Esófago liberado completamente. B. Sección del esófago distal. C. Esófago y estómago ascendido para la anastomosis, D. Apertura del esófago. E. Paso de la grapadora de 45 mm por esófago y estómago. F. Anastomosis con SNG avanzada G. Sutura esófago-gástrica H. Anastomosis terminada.
Técnica de anastomosis esófago-gástrica manual
La anastomosis hecha a mano se realizó así: Primero, se seleccionó un sitio apropiado en la pared anterior del tubo gástrico lejos de la línea grapada, aproximadamente 2 cm por debajo del punto más alto del tubo gástrico para asegurar un buen flujo sanguíneo. Luego, se realizaron suturas seromusculares posteriores ininterrumpidas utilizando Vicryl 3-0 para aproximar el esófago y el estómago. A continuación, se abrió el estómago transversalmente aproximadamente a 3-5 mm de la línea de sutura seromuscular posterior. Se colocaron puntos de sutura ininterrumpidos a lo largo de todo el grosor del estómago y el esófago para lograr la aproximación de mucosa a mucosa. La pared anterior de la anastomosis se completó de forma similar a la de la pared posterior.
Seguimiento
En el postoperatorio los pacientes se mantuvieron nada vía oral durante 5 días después de la esofagectomía. En el día 6 postoperatorio, se realizó un estudio digestivo superior con contraste hidrosoluble y, en ausencia de signos de fuga anastomótica, se inició la alimentación oral con una dieta líquida durante 2 días y luego se avanzó a una dieta blanda. Las fugas anastomóticas se definieron y diagnosticaron según los criterios del Grupo de Consenso de Complicaciones de Esofagectomía; diagnosticado por imágenes clínicas, radiológicas (esofagograma y/o tomografía computarizada) o endoscopia del tracto digestivo superior 16. Todos los casos de disfagia después de la cirugía, confirmados por radiología y tratados por dilatación endoscópica, se clasificaron como estenosis. La mortalidad operatoria incluyó la hospitalaria y la mortalidad después de los 30 días de la intervención.
Después del alta, los pacientes fueron examinados para detectar disfagia sintomática, y cualquier síntoma de disfagia fue evaluado con endoscopia alta. La disfagia clínicamente significativa se definió como la incapacidad para pasar un gastroscopio flexible de 10 mm. Las estenosis benignas se trataron con dilatación con balón o bujía, según el operador.
Análisis estadístico
Las variables continuas se expresan como medias ± DE. Se utilizó la prueba de la χ2 o la prueba exacta de Fisher para comparar las variables categorizadas. Se utilizó la prueba de Wilcoxon para comparar variables continuas. Se utilizó la prueba U de Mann ‐ Whitney para comparar variables secuenciales. Se utilizó el modelo de regresión proporcional de Cox para analizar factores univariados y multivariados. El nivel de significancia para todas las pruebas se estableció en
RESULTADOS
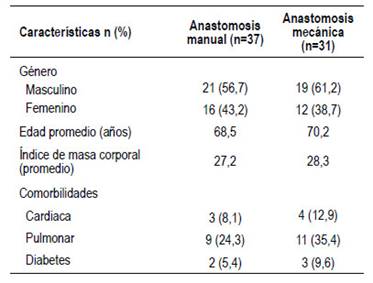
Un total de 68 pacientes fueron incluidos en el análisis, 37 en el grupo de anastomosis manual y 31 en el grupo de anastomosis mecánica. Los datos sobre la edad, el sexo y las condiciones comórbidas de los pacientes fueron reportados en la Tabla 1 sin evideciarse diferencias relevantes entre ambos grupos.
Comparativamente, la proporción de mujeres fue mayor en el grupo de anastomosis manual. El antecedente de enfermedad pulmonar fue la comorbilidad más prevalente en los dos grupos, superando a la enfermedad cardiaca y la diabetes mellitus (DM). No hubo una diferencia significativa en la edad promedio y el IMC entre ambos grupos.
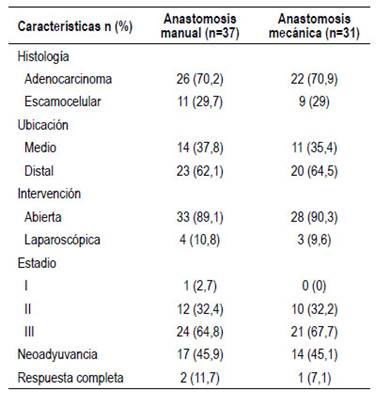
Lamayoríadelospacientesteníanunadenocarcinoma que comprometía el tercio distal del esófago. La mayoría de los tumores, tanto los adenocarcinomas como los carcinomas escamocelulares, se encontraban en estadio III al momento del diagnóstico; solo un paciente en el grupo de anastomosis manual presentaba un tumor estadio I. La terapia neoadyuvante se utilizó en menos de la mitad de los pacientes de ambos grupos [anastomosis manual: n=17 (45,9%), anastomosis mecánica: n=14 (45,1%)] con bajas tasas de respuesta patológica completa (Tabla 2).
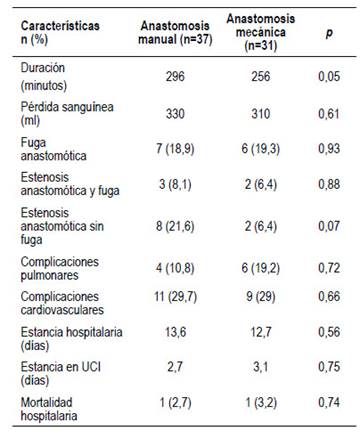
La mayoría de las cirugías se realizaron por vía abierta con 7 cirugías realizadas por vía laparoscópica [anastomosis manual: n= 4 (10,8%), anastomosis mecánica: n=3 (9,6%)]. El número de estenosis sin fuga anastomótica fue mayor en el grupo de anastomosis manual comparado con el grupo de anastomosis mecánica (8 vs 2), sin embargo, el número de pacientes con estenosis y con fuga anastomótica y el número global de fugas anastomóticas entre ambos grupos, no fueron significativamente diferentes. A pesar del hecho de que las comorbilidades pulmonares fueron más prevalentes en ambos grupos, durante el periodo postoperatorio se presentaron más casos de complicaciones cardiovasculares (arritmias, trombosis venosas) en ambos grupos en comparación con los casos de complicaciones pulmonares (20 vs 10 casos). No se observaron diferencias significativas entre ambos grupos con respecto al tiempo operatorio, las pérdidas sanguíneas estimadas y en el tiempo promedio de estancia en UCI y hospitalización; la mortalidad fue igual con un paciente fallecido en cada grupo (Tabla 3).
La mediana de seguimiento general para toda la cohorte fue de 41 meses (rango 13-107).
DISCUSIÓN
La fuga anastomótica y la estenosis de continúan siendo las complicaciones más frecuentes y temidas en el postoperatorio de los pacientes que han sido llevados a una esofagectomía. Múltiples factores se han asociado a la incidencia de estas complicaciones. Factores preoperatorios del paciente como la sarcopenia y la edad avanzada han mostrado tener una relación con el aumento de las tasas de filtraciones 17; el consumo de alcohol y cigarrillo y comorbilidades como la enfermedad pulmonar obstructiva crónica, cardiovasculares, obesidad y la diabetes mellitus (DM) también se asocian a peores resultados postoperatorios. En nuestra serie de casos el IMC corporal de ambos grupos se encontraba por encima del valor normal establecido para hombres y mujeres, lo cual estaría en consonancia con el hecho de que el tipo de cáncer más común en esta serie sea el adenocarcinoma el cual está estrechamente relacionado con la enfermedad por reflujo gastroesofágico, la cual es más común en pacientes obesos. Aunque muchos de estos factores perioperatorios pueden ser potencialmente modificados múltiples autores coinciden en que la experiencia del cirujano asociado a técnicas quirúrgicas adecuadas en la construcción del conducto reemplazante y la anastomosis continúa siendo el factor más determinante a la hora de evaluar las tasas de complicaciones de la anastomosis 17.
Kamarajah et al. publicaron una revisión sistemática en la que se incluyeron 74 533 pacientes de 174 estudios a quienes se les realizó una esofagectomía por cáncer de esófago. En este estudio se encontraron 29 factores asociados a la fuga anastomótica y los dividieron en factores preoperatorios, intraoperatorios y oncológicos, además, evaluaron las complicaciones más comúnmente asociadas a la fuga anastomótica.
La clasificación ASA del paciente y condiciones específicas como la Diabetes Mellitus, la hipertensión arterial, EPOC, obesidad, el consumo excesivo de alcohol, la enfermedad cardiovascular isquémica, el uso de esteroides y la enfermedad renal crónica fueron identificados como los principales factores preoperatorios modificables asociados con la fuga anastomótica 9.
A pesar de que este estudio no evidencio el tabaquismo ni la terapia neoadyuvante como factores asociados a la fuga anastomótica se considera por los autores que el cese del tabaquismo podría mejorar la función pulmonar y disminuir el riesgo de fuga anastomótica al igual que construir las anastomosis fuera de las áreas irradiadas como lo demostraron Juloori et al. 18. Dentro de los factores quirúrgicos se encontró que el abordaje transtorácico, las anastomosis intratorácicas y las omentoplastias se asociaron a tasas significativamente menores de fuga anastomótica; la hipotensión, las transfusiones sanguíneas y el uso intraoperatorio de esteroides se asociaron mayores tasas de fuga anastomótica. La histología tumoral, la estadificación del tumor (TNM), la localización y el tamaño de este no se asociado con la fuga anastomótica. Este estudio encontró además, que la estancia y la mortalidad hospitalaria fueron significativamente mayores en los pacientes con fuga anastomótica.
Uno de los temas más controvertidos en la actualidad es como la nutrición enteral temprana afecta las tasas de fuga anastomótica en los pacientes a los que se le realizó esofaguectomía. Una revisión sistemática y metaanálisis llevado a cabo por Xiang Li et al. 20, en el que se incluyeron 7 estudios con 1595 pacientes, buscó examinar la asociación entre el tiempo de alimentación oral y la fuga anastomótica luego de una esofaguectomía. El análisis de datos no mostró diferencias significativas en las tasas de fuga anastomótica entre aquellos pacientes a quienes se les dio nutrición oral temprana (nutrición en los primeros 7 días luego de la esofaguectomía) y aquellos pacientes a los que se les dio nutrición oral tardía (nutrición después de 7 días desde la esofaguectomía); el análisis por subgrupo evidenció un riesgo de 2,89 veces más de presentar fuga anastomótica en el grupo de pacientes de esofaguectomía abierta y nutrición enteral temprana al compararlos con aquellos a los que se les dio nutrición enteral tardía, hallazgos que no se evidenciaron en el subgrupo de esofaguectomía mínimamente invasiva en los que no hubo una diferencia significativa entre ambas estrategias de nutrición. Estos resultados deben ser interpretados teniendo en cuenta las limitaciones reportadas en el estudio.
La isquemia del conducto ascendido también es un factor determinante que aumenta de forma dramática las tasas de complicación de la anastomosis, lo que refuerza la importancia de una técnica quirúrgica prolija que lleve a un trato adecuado de los tejidos y al reconocimiento de las estructuras vasculares esenciales que no deben ser lesionadas con el fin de preservar un flujo sanguíneo optimo, especialmente en la porción distal (“punta gástrica”) cuando se usa el conducto gástrico como reemplazante. La isquemia del conducto también está determinada por el tipo de conducto que se utilice. El estómago se ha convertido en el conducto de elección debido a un suministro sanguíneo que es más robusto (asociándose a menores tasas de necrosis) y a una preparación quirúrgica más fácil; el colon y el yeyuno proximal también han sido utilizados como conductos reemplazantes, especialmente cuando no es posible usar el estómago como en los casos en los que se requiere hacer una gastrectomía completa para el adecuado control de la enfermedad; estas estructuras han mostrado ser inferiores al estómago con respecto al flujo sanguíneo, especialmente en aquellos pacientes que han tenido cirugías abdominales previas. Algunos estudios con muestras pequeñas de un solo centro han sugerido unas mayores tasas de fuga anastomótica cuando se usa la vía retroesternal para localizar el conducto reemplazante debido probablemente a la angulación esternal que se produce a nivel de la apertura torácica y la longitud mayor que esta vía requiere. El uso de la vía retroesternal puede ser necesaria cuando se hacen reconstrucciones por etapas en el consumo de cáusticos o perforaciones o cuando está determinada la realización de radioterapia postoperatoria con el fin de evitar el daño del conducto 19.
Las tasas de fuga anastomótica cervicales han sido reportada en la literatura en un rango entre el 2-20%; el éxito en la construcción de la anastomosis es probablemente el factor más determinante en la aparición de esta complicación. Múltiples métodos se han utilizado para la realización de la anastomosis posterior a la esofagectomía entre los que se incluyen el método manual, grapadoras circulares y el uso de diferentes técnicas con grapadoras lineales. Muchos estudios no han encontrado diferencias estadísticamente significativas con lo que respecta a las tasas de fuga anastomótica cuando se comparan estas tres técnicas 18,20, sin embargo, algunos metaanálisis con análisis por subgrupo han mostrado desenlaces a favor de la anastomosis mecánica con grapadora lineal en las tasas de fuga anastomótica cuando se compara con la anastomosis manual 21,22. Nuestra serie de casos mostró una tasa de fuga anastomótica del 18,9% en el grupo de anastomosis manual y del 19,3% en el grupo de anastomosis mecánica las cuales son similares a lo reportado en la literatura mundial.
La fuga anastomótica es en sí un factor de riesgo para el desarrollo postoperatorio de estenosis que podría llevar al desarrollo de disfagia afectando de forma considerable la calidad de vida de los pacientes 23. Otros factores como las enfermedades cardiacas, la DM, el uso de quimio/radioterapia neoadyuvante y el uso de grapadoras circulares para la construcción de la anastomosis se han asociado con la aparición de estenosis 17. Nuestros resultados muestran un mayor número de casos de desarrollo de estenosis anastomótica en el grupo de pacientes en quienes se realizó una construcción de anastomosis manual. Con la aparición e implementación de las anastomosis con grapadora lineal se ha evidenciado una disminución en las tasas de estenosis de anastomosis cuando se compara con las anastomosis mecánicas con grapa circular y con la construcción manual de la anastomosis, reportes que concuerdan con los hallazgos de nuestro estudio 22,24; En la actualidad el aumento en la utilización de las grapadoras lineales para la realización de una anastomosis término-terminal funcional ha mostrado resultados superiores con respecto a la disminución de las tasas de estenosis anastomótica, por lo que se está llevando a cabo un ensayo clínico controlado aleatorizado comparando la anastomosis triangular con grapadora lineal versus la anastomosis términoterminal funcional con grapadora lineal 25 que busca confirmar la superioridad de este último método en la disminución de la estenosis postoperatoria.
Aunque la realización de la anastomosis mecánica se ha relacionado con menores tiempos quirúrgicos y tasas de sangrado intraoperatorias 26,27, en nuestra serie de casos, tanto el tiempo quirúrgico como la pérdida sanguínea de ambos grupos fue muy similar. Debido a que no se midió de forma independiente el tiempo que tomaba la construcción de la anastomosis per se, no es posible determinar el impacto que tiene la realización de cada técnica en el tiempo quirúrgico total.
En un esfuerzo por disminuir las tasas de fuga anastomótica, el departamento de cirugía torácica de la Universidad de Michigan, en cabeza del Dr. Mark B. Orringer, desarrolló un modelo de simulador portátil y de bajo costo en el cual es posible realizar la construcción de una anastomosis esofagogástrica latero-lateral con grapadora, permitiendo que el personal en entrenamiento tenga exposición previa a la técnica y los pasos necesarios a seguir para la realización adecuada de esta antes de ser realizada en un paciente 28-30. Aunque las investigaciones acerca de la viabilidad, confiabilidad y utilidad de este simulador están en fases tempranas, los resultados preliminares respaldan al simulador como una valiosa herramienta de entrenamiento quirúrgico 31.
En conclusión, la anastomosis cervical manual como la mecánica son igualmente efectivas en la reconstrucción tras la esofagectomía por cáncer. El método de construcción con la anastomosis mecánica mostró una tendencia a realizarse en menos tiempo y con menor tasa de estenosis que la manual.