INTRODUCCIÓN
El cáncer de páncreas (CP) es uno de los tumores sólidos con mayor mortalidad. Se estima que en el 2030 será la segunda causa de muerte por cáncer en el mundo1. Su mal pronóstico radica en el estadio avanzado de la enfermedad en el momento del diagnóstico, lo que hace que menos del 20% se pueda beneficiar de un tratamiento quirúrgico2. A pesar de que la incidencia y mortalidad está aumentando3, el cribado a nivel poblacional no estaría indicado ya que su baja prevalencia (aproximadamente 12/100000 habitantes) reduce la posibilidad de una prueba de cribado verdaderamente positiva4.
Por tanto, los esfuerzos deben ir encaminados a identificar la población de alto riesgo que presente mayor probabilidad de padecer esta entidad y que se pueda beneficiar de una detección precoz de lesiones premalignas o de tumores en estadios iniciales. En el 2013, el Consorcio Internacional de Cribado de Cáncer de Páncreas (CAPS) recomendó el cribado en pacientes con un riesgo de presentar CP mayor del 5% o con un incremento de cinco veces el riesgo relativo con respecto a la población general5. De esta manera, seleccionaron un grupo de individuos que, por antecedentes familiares o por pertenecer a síndromes hereditarios específicos, tiene un riesgo elevado y se podría beneficiar de un programa de cribado. Estas recomendaciones fueron actualizadas posteriormente con las nuevas evidencias de los programas de cribado que ya estaban en funcionamiento6. Entre las principales diferencias con las anteriores recomendaciones destaca el consenso en comenzar el cribado a partir de los 50 años, y la inclusión de los pacientes con mutaciones en gen ATM con un familiar de primer grado afecto, entre los individuos susceptibles de cribado. En ambos consensos, se mantiene el objetivo principal que es identificar CP en estadio precoz o lesiones precursoras avanzadas como neoplasia pancreática intraepitelial (PanIN) o tumor papilar mucinoso intraductal (TPMI) ambos con displasia de alto grado. Varios metaanálisis han detectado que es factible la posibilidad de encontrar estas lesiones en un programa de cribado, resaltando así el potencial beneficio que podría afectar a la supervivencia7-9.
Sin embargo, la evidencia actual está basada en estudios con una marcada heterogeneidad en los criterios de inclusión, métodos de diagnóstico o frecuencia de los intervalos de seguimiento.
Nuestro objetivo es evaluar en la práctica clínica habitual los hallazgos de las pruebas de cribado en una población seleccionada de alto riesgo de acuerdo con los criterios establecidos, así como describir las variables asociadas a la presencia de lesiones malignas o premalignas.
MATERIAL Y MÉTODOS
Ámbito del estudio
Estudio realizado en el Hospital Universitario Infanta Leonor, centro sanitario de atención especializada, de gestión directa del Servicio Madrileño de Salud, situado en la ciudad de Madrid (España), en el distrito municipal de Villa de Vallecas. El hospital ofrece cobertura universal para una población de referencia que supera los 307000 habitantes. El reclutamiento de pacientes se centra en la consulta de alto riesgo del servicio de Digestivo de dicho centro, cuyo objetivo es identificar, realizar consejo genético y seguimiento a pacientes que presentan alto riesgo de padecer tumores digestivos.
Pacientes
Estudio observacional prospectivo y unicéntrico que abarca el periodo del 2015 al 2020, y que incluye a todos los pacientes con alto riesgo de CP, en base a antecedentes familiares o síndromes hereditarios de riesgo, quienes son remitidos a la consulta de alto riesgo del Servicio de Digestivo para valoración de cribado. También se incluyen pacientes de alto riesgo de CP, quienes ya están realizando seguimiento en nuestra consulta de alto riesgo por pertenecer a otros síndromes hereditarios.
Estos pacientes son evaluados en consulta, donde se realiza una anamnesis completa y una detallada historia familiar que incluya al menos tres generaciones. De ellos se seleccionan sólo aquellos que cumplen los criterios establecidos por el CAPS vigente en ese momento: hasta el 2019 los establecidos en el primer consenso5 y, tras la publicación de la actualización, se siguieron los criterios indicados en esta (Tabla 1)6.
Tabla 1 Individuos de alto riesgo de cáncer de páncreas según criterios CAPS 20206.

* Un 20,3 % adicional estuvo algo de acuerdo con el cribado (total 89,9%)
Grado de recomendación 1: fuerte (“definitivamente hazlo”); 2: bajo (“probablemente hazlo”); 3: no recomendado
FPG: familiar de primer grado, FAMMM: síndrome de melanoma familiar con lunares atípicos múltiples; BRCA2: cáncer de mama 2 (breast cancer 2); BRCA1: cáncer de mama 1 (breast cancer 1); PALB 2; compañero y localizador (partner and localizer) de BRCA2, ATM: mutaciones en el gen Ataxia-Telangiectasia
CP: cáncer de páncreas; Hª: historia; SCMOH: síndrome de cáncer de mama y ovario hereditario
En los individuos seleccionados se analizan variables demográficas, los antecedentes familiares, la mutación germinal en caso de presentarla y finalmente otros factores de riesgo modificables asociados al CP (tabaquismo, diabetes mellitus, pancreatitis crónica). Se evalúan el tipo de técnica de cribado empleada, los hallazgos de las mismas y el tiempo de seguimiento.
Posteriormente, se comparan los pacientes con lesiones relevantes frente a los que no tienen lesiones o éstas son benignas. Al no estar indicado el cribado en población asintomática que no sea de riesgo, no hemos podido establecer un grupo control.
Clasificación de los hallazgos de las pruebas de cribado
Se consideran como lesiones relevantes aquellas que, por práctica clínica habitual, van a requerir un seguimiento o tratamiento específico: TPMI de rama secundaria, TPMI de conducto principal, PanIN y lesiones sólidas de páncreas.
Se reconocen como lesiones benignas, aquellos hallazgos no relevantes y que no requieren en general un seguimiento específico. Incluyen lesiones quísticas aisladas subcentimétricas sin signos de riesgo no compatibles con TPMI, adenopatías sin criterios de malignidad o cambios morfológicos del parénquima pancreático sin datos de agresividad.
Técnicas de cribado empleadas
El protocolo que seguimos en nuestro centro es la combinación de ecoendoscopia (USE) y Resonancia Magnética nuclear (RM) de forma alternativa cada año si no se encuentran hallazgos o son lesiones sin datos de malignidad. Como método inicial empleamos la RM, por mayor disponibilidad de esta técnica en el momento del estudio. No obstante, tenemos en cuenta si existen contraindicaciones para alguna de los procedimientos y la preferencia del paciente a la hora de emplear una u otra prueba.
Ecoendoscopia
Se realiza en primer lugar gastroscopia seguido de exploración mediante ecoendoscopio lineal (GFUCT180, Olympus, Hamburgo, Alemania) El parénquima pancreático se visualiza con la técnica convencional empleando la estación gástrica para visualizar el cuerpo y cola de páncreas, el bulbo para explorar la cabeza pancreática y la segunda porción duodenal para examinar el proceso uncinado.
Resonancia Magnética Nuclear y Colangio- Resonancia
Las imágenes se efectuaron en un equipo de 1,5 Tesla con secuencias axiales y coronales T2 en adquisición rápida HASTE para valoración anatómica, eco de gradiente (GRE) en fase - fase opuesta y secuencias axiales potenciadas en T2 turbo spin-echo (TSE) con supresión grasa. También se realizaron secuencias habituales de colangio-pancreatografía por RM y estudio post-contraste intravenoso (ácido gadotérico Gd-DOTA 0,5 mmol/ml) con secuencias dinámicas T1 GRE con supresión grasa.
Análisis estadístico
Se realiza un análisis descriptivo de todas las variables recogidas en el estudio. Las variables cualitativas se describieron como medida de tendencia central (media o mediana) acompañadas de su medida de dispersión (desviación estándar o rango intercuartílico) según fuera la distribución de la variable. Las variables cualitativas se describieron mediante frecuencias relativas. En el análisis comparativo se emplearon la prueba de χ2 para variables cualitativas y la prueba de T-student (con la corrección de Fisher cuando fuera oportuno) o U-Mann Whitney para la comparación de variables cuantitativas, según la distribución de las variables. Valores de “p” < 0,05 fueron considerados como estadísticamente significativos
Todos los cálculos fueron realizados mediante el programa estadístico PASW versión 25.0 (SPSS, Inc, Chicago, IL, USA).
Consideraciones éticas
El estudio se realizó protegiendo la identidad del paciente en el análisis de los datos, cumpliendo los criterios de seguridad y confidencialidad compatibles con la normativa vigente. No fue necesaria la aprobación por el comité de ética por ser un estudio observacional en el que no se modifica el tratamiento o la intervención a que pudiera estar sometidos los pacientes ni se prescribe otra pauta que pudiera afectar a su integridad.
En este trabajo no ha sido necesario la obtención del consentimiento informado para la publicación, porque no se publican datos personales que permitan identificar al paciente.
RESULTADOS
Pacientes
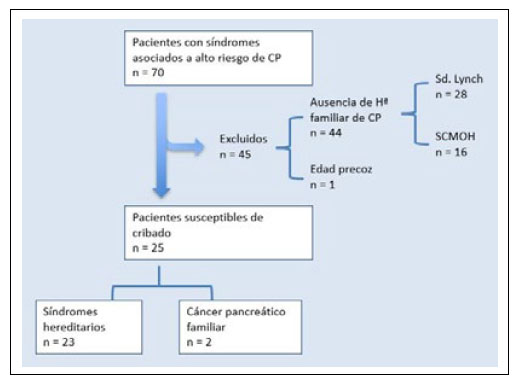
Desde el año 2015 al 2020 se incluyen 70 pacientes de alto riesgo de CP, bien por antecedentes familiares (cáncer pancreático familiar) o por pertenecer a síndromes asociados a mayor riesgo de CP. De ellos, se seleccionan 25 pacientes que cumplen los criterios del CAPS para ser considerados susceptibles de cribado. De los 45 pacientes excluidos, uno cumplía criterios de cáncer pancreático familiar, pero sin indicación por edad. En el resto, fue por ausencia de antecedentes familiares (28 pacientes con síndrome de Lynch y 16 con síndrome de cáncer de mama y ovario hereditario, SCMOH), ya que la CAPS recomienda en estos casos cribar sólo cuando exista al menos un antecedente familiar de primer grado afecto de CP (Figura 1).
Las características demográficas se muestran en la Tabla 2.
Tabla 2 Características basales.
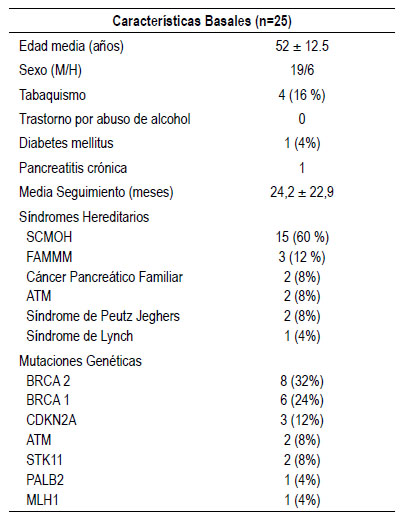
M: mujer; H: hombre; SCMOH: síndrome de cáncer de mama y ovario hereditario; FAMMM: síndrome de melanoma familiar con lunares atípicos múltiples; ATM: mutaciones en el gen Ataxia-Telangiectasia
Grupos de Riesgo
De los 25 pacientes con indicación de cribado, dos pacientes de distintas familias cumplían criterios de datos de cáncer pancreático familiar. El resto correspondían a síndromes hereditarios. Como se muestra en la tabla 2, el más frecuente fue el SCMOH, seguido del síndrome de melanoma familiar con lunares atípicos múltiples (FAMMM).
Alteraciones genéticas
Veintitrés pacientes tenían alguna mutación genética. La alteración genética más prevalente fue la mutación en el gen BRCA2 seguido de la mutación en el gen BRCA1. El resto de las mutaciones se recogen en la tabla 2.
Hallazgos en las pruebas de cribado empleadas
Lesiones benignas
En ocho pacientes se encontraron algún tipo de hallazgo sin asociación con lesiones premalignas. Cinco presentaron una lesión quística milimétrica sin datos de agresividad, dos adenopatías peripancreáticas y uno pancreatitis crónica. Un 37.5% tenía como factor de riesgo añadido el tabaquismo y una paciente era diabética. La mitad de los pacientes pertenecían al SCMOH. Destaca que en los dos pacientes con síndrome de Peutz Jeghers se encontró algún tipo de hallazgo (Tabla 3).
Tabla 3 Características de los pacientes con lesiones benignas
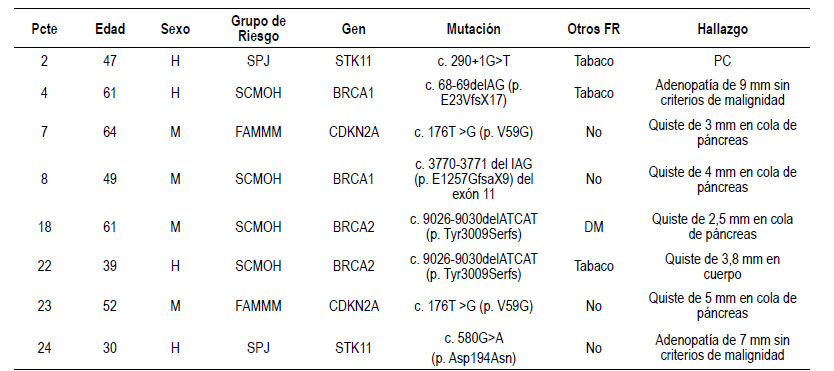
Pcte: paciente; FR: factores de riesgo; H: hombre; M: mujer; SPJ: síndrome de Peutz Jeghers; SCMO: síndrome de cáncer de mama y ovario hereditario; FAMMM: síndrome de melanoma familiar con lunares atípicos múltiples;
Lesiones patológicas
Tres pacientes (12%) presentaron lesiones patológicas (Tabla 4).
Tabla 4 Características de los pacientes con lesiones patológicas.
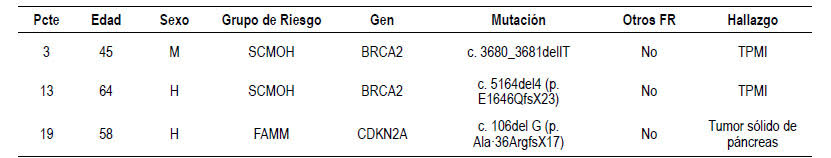
Pcte: paciente; FR: factores de riesgo; M: mujer; H: hombre; SCMO: síndrome de cáncer de mama y ovario hereditario; FAMM: síndrome de melanoma familiar con lunares atípicos múltiples; TPMI: tumor papilar mucinoso intraductal
Se encontraron hallazgos compatibles con TPMI de rama multifocal en dos de ellos. En una paciente portadora de mutación BRCA2 se visualizan tres lesiones quísticas subcentimétricas sin criterios de alarma. En el otro paciente, portador de la mutación BRCA2, se describen cuatro lesiones quísticas uniloculares subcentimétricas en cuerpo y cabeza sin criterios de agresividad. En ambos casos, el diagnóstico fue en la prueba inicial y se está realizando seguimiento con USE y RM alternativamente, sin cambios. No se encontraron signos indirectos de PanIN avanzados en la población de estudio.
El paciente con la mutación en gen CDKN2A, en la primera prueba de imagen realizada, se encontró una lesión sólida en cola de páncreas sugestiva de tumor primario. Se realiza pancreatectomía distal con hallazgo de adenocarcinoma ductal sin afectación ganglionar, estadio patológico pT1c N0 M0 (8º edición TNM). El paciente ha recibido tratamiento con quimioterapia adyuvante sin evidencia de recidiva hasta el momento.
Análisis de factores presentes en pacientes con hallazgos patológicos
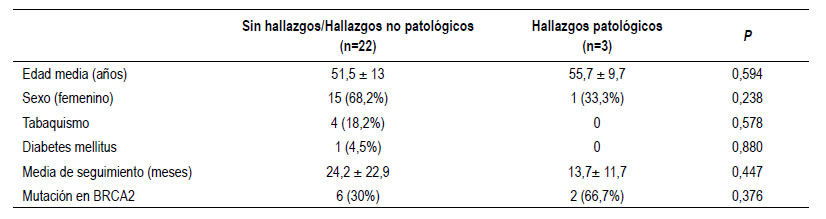
Para evaluar si existen características diferenciales entre los pacientes que tuvieron lesiones patológicas frente a los que no presentaron lesiones o éstas no fueron relevantes, comparamos las variables analizadas en ambos grupos (Tabla 5).
Los pacientes con lesiones patológicas tenían una edad ligeramente superior a los pacientes sin hallazgos (55,7 ± 9,7 vs 51,5 ± 13; p=0,594) y con predominio del sexo masculino (68,2% vs 13,3%, p=0,238). En casi un 23% de los pacientes sin hallazgos se encontraron algún otro factor asociado como tabaquismo o diabetes. Es destacable que dos terceras partes de los pacientes con patología tenían mutación en el gen BRCA2 frente al 30% de los pacientes sin hallazgos. No obstante, no se encontraron diferencias estadísticamente significativas en ninguna de las variables analizadas.
DISCUSIÓN
En el presente estudio, evaluamos los hallazgos obtenidos en el cribado de pacientes con alto riesgo de cáncer de páncreas en base a los antecedentes familiares o síndromes hereditarios conocidos y describimos si existen otras variables asociadas a la presencia de lesiones pancreáticas relevantes. Tras selección de los pacientes que cumplían los criterios establecidos de cribado, en un 12% encontramos lesiones patológicas, siendo el SCMOH el grupo de riesgo más frecuente.
El objetivo del cribado de cáncer de páncreas es prevenir la muerte por esta entidad, identificando y tratando las lesiones precursoras. De esta manera, las principales lesiones diana a identificar son el cáncer de páncreas en estadio I o sus lesiones precursoras con displasia de alto grado (TPMI o PanIN) (5, 6). En nuestro estudio hemos incluido como lesiones patológicas los TPMI, porque son lesiones con riesgo de malignidad que requieren un seguimiento específico. Estas lesiones también se incluyen como hallazgos en otros programas de cribado 10. En el presente trabajo, los dos pacientes con TPMI no han presentado cambios durante el seguimiento. La evidencia de frecuencia y tasa con la que los TPMI progresan a cáncer invasivo en los pacientes de alto riesgo comparado con los pacientes de bajo riesgo es escasa. Como en los casos esporádicos, los TPMI de rama principal y los TPMI que presenten signos de riesgo, progresan más rápidamente. Algunos individuos de alto riesgo pueden desarrollar múltiples lesiones precursoras a lo largo de todo el páncreas y, aquellos que precisan cirugía por TPMI pueden tener concomitantemente una PanIN de alto grado 11. No obstante, no se ha llegado a un consenso sobre si es necesario ampliar las indicaciones de tratamiento quirúrgico en las lesiones quísticas de pacientes de alto riesgo con respecto a la población general.
En un 44% se encontró algún tipo de lesión, siendo en el 12% lesiones patológicas: dos TPMI de rama multifocal y un adenocarcinoma de páncreas en estadio precoz. Estos resultados son parecidos a los obtenidos en un metaanálisis que incluye 1588 individuos de riesgo en el que se identificó una prevalencia agrupada de 5,8% de lesiones sólidas y 20,2% de lesiones quísticas, siendo en un 3,3% lesiones objetivo (cáncer de páncreas o lesiones precursoras con displasia de alto grado) 7. En la primera ronda de cribado italiana de pacientes de alto riesgo, se encontraron en un 25,3% alteraciones en las pruebas de imagen, la mayoría de ellas correspondía a TPMI de rama lateral con una tasa de lesiones malignas del 2,6%10). En otro metaanálisis que comprende 1660 pacientes de alto riesgo, se identificaron 55 lesiones, siendo necesario cribar a 135 pacientes para encontrar una lesión de riesgo 9. Sin embargo, estos hallazgos parecen limitarse a pacientes de alto riesgo. En una revisión sistemática que incluye paciente de riesgo alto e intermedio, se detectaron un total de 18 casos de cáncer de páncreas en 1156 individuos de riesgo y ninguno en los 161 pacientes de riesgo medio 12.
El grupo de riesgo más frecuente fue el SCMOH siendo la mutación en el gen BRCA2 la más prevalente. Las mutaciones germinales de este gen constituyen la causa más frecuente de cáncer de páncreas hereditario. Ha sido identificada en el 5-17% de las familias con cáncer pancreático 5 El riesgo relativo de cáncer de páncreas en esta población es del 3,5 (IC 95%: 1, 5: 6, 58) 13 Sin embargo, dada la relativa alta prevalencia de esta mutación, las principales guías recomiendan sólo cribar aquellos portadores con algún familiar afecto de cáncer de páncreas (6, 14).
Con el empleo cada vez más habitual de los paneles de secuenciación masiva, es frecuente que nos encontremos con genes de susceptibilidad al cáncer de páncreas. Se estima que un 5-10% de los pacientes con cáncer de páncreas aparentemente esporádico podría tener alguna alteración genética. La Sociedad Americana de Oncología y la NCCN (National Comprehensive Cancer Network) recomiendan que en todos los pacientes con diagnóstico de cáncer de páncreas se debería hacer una evaluación inicial en la historia clínica para evaluar si pertenecen a algún síndrome hereditario con riesgo de cáncer de páncreas y, en caso necesario, solicitar el estudio genético 15,16.
Finalmente, otros factores de riesgo adicionales no genéticos ni familiares, podrían aumentar el riesgo de cáncer de páncreas. Aunque este efecto no se ha podido demostrar por el tipo de estudio realizado, hemos comparado estos factores entre los pacientes en los que se encontraron lesiones patológicas frente a los que no las desarrollaron. No encontramos diferencias estadísticamente significativas con respecto a otros factores como el tabaquismo o la DM. No obstante, destaca que, en el grupo de lesiones relevantes, hubo una mayor proporción de hombres y de portadores de la mutación en el gen BRCA2. No se han evaluado si estos factores de riesgo pueden ejercer una influencia sinérgica en el desarrollo de lesiones malignas en la población de alto riesgo. En el programa de cribado italiano, sólo la edad mayor de 50 años (OR 3,3; IC 95%: 1,4-8) , el tabaquismo (OR 2,8; IC 95%: 1,1-7,5) y tener más de dos familiares con cáncer de páncreas (OR 2,7; IC 95% 1,1-6,4) se encontraron como factores de riesgo independientes de desarrollar lesiones premalignas o malignas 10.
La principal limitación de nuestro estudio es que el volumen de pacientes que finalmente fueron subsidiarios de cribado es pequeño. Esto se debe en parte a que es una población muy seleccionada a partir de los criterios estrictos y restrictivos establecidos por el CAPS. No obstante, el tamaño muestral es comparable a otros estudios similares 17-20.
Las fortalezas de este estudio recaen en que se trata de un análisis del cribado en la práctica clínica habitual, con una representación de casi todos los grupos de riesgo y con una rigurosa selección según los criterios de cribado vigentes. Todos los pacientes con síndrome hereditario presentaban un diagnóstico de confirmación genética, lo cual influye positivamente en la adecuada valoración en este limitado grupo de riesgo. Finalmente, la inclusión en una base de datos de estos pacientes y otros que puedan incluirse en el futuro, permitirá evaluar su comportamiento durante el seguimiento.
En conclusión, el cribado de cáncer de páncreas en población de alto riesgo podría ser factible y útil en pacientes de alto riesgo. Las pruebas de cribado (USE/RM) conseguirían detectar lesiones premalignas o tumores malignos en estadio precoz resecables (12% de nuestra muestra). Los pacientes con SCMOH fue el grupo de riesgo más frecuente que cumplía los criterios de cribado, siendo la mutación en el gen BRCA2 la más frecuente entre los pacientes con hallazgos patológicos.
No obstante, sería conveniente estandarizar un programa de cribado a nivel internacional que permita hacer estudios prospectivos y multicéntricos con criterios unificados para evaluar futuras cuestiones como son la influencia de otros factores de riesgo adicionales, la implementación de técnicas de cribado molecular, y realizar estudios más amplios de coste- efectividad.