INTRODUCCIÓN
El acetaminofén (paracetamol) es uno de los medicamentos más consumidos a nivel mundial por su fácil acceso y sus propiedades analgésicas, antipiréticas, entre otras. El acetaminofén una vez ingerido, se absorbe en gran porcentaje en el intestino delgado, teniendo su pico máximo a los 30 minutos cuando la administración es endovenosa y de 45 minutos en su fórmula vía oral; absorbiéndose por completo a las 4 horas, con una biodisponibilidad oral hasta del 98%. 2 Exposiciones agudas en adultos de 7,5 gramos y en niños de 150 mg/kg pueden causar toxicidad, donde las vías de su metabolismo se ven afectadas y saturadas, sobre todo la actividad de la enzima CYP2E1, lo que genera un incremento en la formación de N-acetil-para-benzoquinoneimina (NAPQI) excediendo la capacidad del glutatión para contrarrestar toxicidad, esto provoca que se una rápidamente a los hepatocitos, provocando hepatotoxicidad iniciando en la zona hepática III (centro lobular) debido al alto metabolismo oxidativo y posteriormente extendiéndose a las zonas II y I 3); todo ello generando hepatotoxicidad, cuyo espectro clínico va desde una injuria hepática aguda (IHA) leve, IHA moderada (con INR prolongado), IHA severa (con encefalopatía) e incluso la muerte. Existen factores que aumentan el riesgo de hepatotoxicidad, por ejemplo; alcoholismo crónico, medicamentos inductores del CYP2E1 y desnutrición; todo ello debido a una baja reserva de glutatión celular 4).
A continuación, se presenta el caso de una paciente con falla hepática inducida por ingesta de sobredosis masiva de acetaminofén, a la cual se da manejo basado en los protocolos SNAP (Scottish and Newcastle Anti-Emetic Pretreatment Paracetamol Poisoning Study Regimen) para la administración del antídoto N-acetilcisteína (NAC) en infusión endovenosa, con posterior mejoría clínica.
CASO CLÍNICO
Paciente mujer de 18 años, con el antecedente de depresión mayor e intento suicida previo, sin consumo actual de productos de herboristería ni dietéticos. Ingresa al servicio de emergencia 9 horas posterior a la ingesta de 80 tabletas de acetaminofén de 500 mg (ingesta total: 40 gramos) asociada a consumo de alcohol de cantidad no especificada.
Al examen físico: se encontraba con náuseas y vómitos, la tensión arterial era 130/70mmHg, frecuencia cardíaca: 120 latidos/minuto, frecuencia respiratoria: 14 respiraciones/minuto, afebril, escleras con leve ictericia, no palidez mucocutánea, no signos de dificultad respiratoria, auscultación cardiopulmonar normal, abdomen blando con dolor abdominal difuso a predominio de hipocondrio derecho sin visceromegalias palpables ni ascitis, paciente se encontraba somnolienta y confusa.
En los exámenes auxiliares de ingreso se observa: hipertransaminasemia con niveles mayores a 5 veces el límite superior normal (LSN), leve aumento de la bilirrubina total (BT) a predominio indirecto, discreto aumento del Tiempo de Protrombina (TP) e INR y acidosis metabólica hiperlactatémica anión gap elevado (Tabla 1 y 2), la ecografía abdominal no se observó alteraciones significativas.
Tabla 1 Evolución de los parámetros de laboratorio evaluados durante su estancia intrahospitalaria.
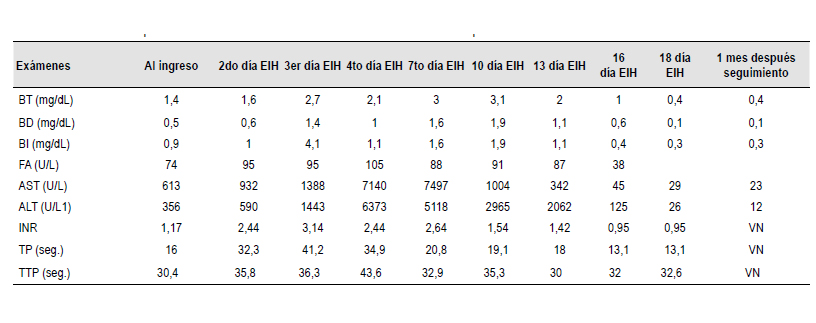
EIH: Estancia intrahospitalaria; BT: Bilirrubina Total; BD: Bilirrubina Directa; BI: Bilirrubina Indirecta; FA: Fosfatasa Alcalina; AST: Aspartato aminotransferasa; ALT: Alanino aminotransferasa; INR: Índice Internacional Normalizado de tiempo de protrombina VN: valores normales.
Tabla 2 Evolución de los parámetros gasométricos evaluados durante su estancia intrahospitalaria.
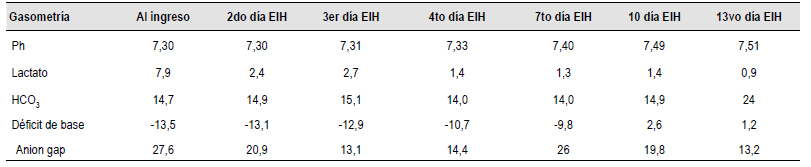
Ph: Potencial de hidrogeniones; HCO3: bicarbonato.
Se brindó tratamiento sintomático, reanimación hídrica y terapia antidotal con N-acetilcisteína endovenosa en infusión basándonos en el protocolo simplificado (SNAP): 200mg/kg en 500 mL de Dextrosa 5% en las primeras 4 h y luego 100 mg/kg en 1000 mL de Dextrosa 5% para las siguientes 16h de NAC para disminuir la incidencia de posibles reacciones adversas como las anafilactoides 5. Posterior a este tiempo se prolongó el tratamiento más allá del estimado de manera convencional por presentar niveles de ALT >50 U/L siendo uno de los criterios por laboratorio para continuarla. Durante su estancia intrahospitalaria se realizaron de manera seriada estudios de laboratorio, destacando la mejoría de los parámetros de función hepática, medio interno y tiempos de coagulación (Tabla 1-2), presentando evolución favorable.
DISCUSIÓN
La intoxicación por acetaminofén es una de las causas más comunes de falla hepática aguda, hasta el 42% de los casos en Estados Unidos (EE. UU.); se han reportado más de 136 mil por año y la mitad de ellas están relacionadas a coingestas con otras sustancias constituyendo el 12% de las muertes relacionadas a intoxicación 6).
El adecuado abordaje de estos pacientes al ingreso a los servicios de emergencias, con un interrogatorio detallado y dirigido, así como el reconocimiento de las manifestaciones clínicas y de laboratorio que puede ocasionar esta intoxicación, son de vital importancia, ya que según el reporte anual de la Asociación Americana de Control de Envenenamientos (AAPCC, por sus siglas en inglés), encabezan la lista de casos de exposición, intoxicación y fatalidad en los EE. UU. 6
Las manifestaciones clínicas dependen de la dosis y del tiempo transcurrido entre la exposición y el contacto con un facultativo; el examen puede ser normal en las primeras 24 horas e ir desarrollándose en fases, siendo estas: la Fase 1 (primeras 24 horas), en la cual se pueden hallar síntomas inespecíficos como náuseas, vómito, dolor abdominal, anorexia, letargia, diaforesis y malestar general; la Fase 2 (24 y 72 horas), con síntomas que pueden llegar a mejorar y/o aparecerán anomalías en niveles de transaminasas, bilirrubinas y un tiempo prolongado de protrombina, así como también manifestar hepatalgia o hepatomegalia; durante la Fase 3 (72 y 96 horas), se presenta el mayor daño a nivel hepático, reapareciendo las náuseas y vómitos, empeorando la ictericia, coagulopatía, desarrollan lesión renal y síntomas del sistema nervioso central como confusión, somnolencia o coma; en la última Fase 4, (96 horas y 14 días) post exposición, puede comenzar la mejoría del paciente y contar con una recuperación completa en 3 meses o progresar a insuficiencia multiorgánica y muerte 2).
Comparando las manifestaciones de nuestra paciente con la literatura podemos observar que nuestra paciente se encontraba en la Fase 1 por tiempo, correlacionando también el cuadro clínico; cabe destacar que en escenarios donde las sobredosis masivas de acetaminofén >500 mg/ kg pueden resultar en un estado mental alterado o coma dentro de las 12 horas posteriores a la exposición. Otro dato relevante en nuestra paciente fue el ascenso de ALT llegando a ser >1000 U/L considerado un dato de hepatotoxicidad severa con alto riesgo de desarrollo de falla hepática fulminante, motivo por el cual se continua con infusión de N-acetilcisteína con estrecha vigilancia por el equipo de toxicología clínica; considerando que solo se consultaría la posibilidad de trasplante hepático en caso de que cumpliera con alguno de los siguientes criterios como: a) INR >3.0 después de 48 horas post exposición o > 4.5 en cualquier momento, b) oliguria, c) incremento de la creatinina, d) persistencia de la acidosis a pesar de medidas correctivas estándar, e) hipotensión sistólica <80 mmHg a pesar de una adecuada reanimación, f) hipoglucemia, g) trombocitopenia severa o encefalopatía, y alteraciones del estado de alerta 7) .
Dentro del manejo integral del paciente intoxicado, la valoración de medidas relacionadas a evitar la absorción o facilitar la eliminación de un xenobiótico, el uso de carbón activado no se consideró de beneficio por el tiempo de exposición y la disponibilidad inmediata de N-acetilcisteína, donde la prioridad es la administración de la terapia antidotal 8).
El régimen estándar de la infusión inicial de N-acetilcisteína es de 150 mg/kg para 15-60 minutos, después 50 mg/kg para 4 horas y 100 mg/kg para 16 horas vía endovenosa, por su parte también se cuenta con una formulación oral, la cual tiene una duración estándar de 72 horas; donde la dosis de carga es de 140 mg/kg y de mantenimiento 70mg/kg cada 4 horas para 17 dosis (variable). Este régimen es altamente eficaz comparado con la no administración de ninguna medicación 7).
Sin embargo, actualmente hay otros regímenes de administración, como es el Scottish and Newcastle Anti- Emetic Pretreatment (SNAP), el cual fue utilizado para nuestra paciente: 200 mg/kg en 500 mL de solución glucosada al 5% vía endovenosa para 4 horas; la segunda dosis es 100 mg/kg en 1000 mL en solución glucosada al 5% vía endovenosa para 16 horas 9); se ha comprobado que este régimen disminuye significativamente las reacciones adversas, en particular las reacciones de tipo anafilactoide y un efecto más rápido del antídoto ante ingestas masivas 10); cesando la infusión de nuestro paciente hasta el decremento de ALT </= 50 U/L e INR <2, con mejoría clínica del paciente.
En el Perú no contamos con un registro de intoxicaciones; sin embargo, se observa en los últimos años un incremento de casos de intoxicaciones por múltiples xenobióticos, especialmente con paracetamol durante la pandemia de Covid-19 en muchos lugares del mundo, 11 por lo cual la importancia de revisión de terapias para casos de sobredosis masiva es importante en nuestra paciente.
CONCLUSIONES
Es relevante mencionar que el caso reportado es de una sobredosis masiva de acetaminofén en una paciente joven en la cual se inició de forma oportuna la terapia antidotal. Cabe destacar que el enfoque de la utilización del esquema SNAP se decidió ante la necesidad de dar el mayor beneficio posible al paciente con el mínimo de complicaciones propias del tratamiento y efecto en el menor tiempo; así como también, continuar la terapia a pesar de completar las horas descritas en los esquemas convencionales por contar aún con alteraciones como ictericia, prolongación de INR y la tan importante transaminasemia.
Existe una alta disponibilidad a este medicamento, ya sea solo o en combinación con otros, de venta libre y con pocas restricciones de uso, siendo un medicamento con alta probabilidad de toxicidad y mortalidad en nuestros pacientes. Se requiere de mayor concientización de uso y alta sospecha diagnóstica, así como también de un manejo conjunto entre los emergenciólogos, toxicólogos clínicos, gastroenterólogos y hepatólogos.














