Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Medicina
versión impresa ISSN 1025-5583
An. Fac. med. v.69 n.2 Lima jun. 2008
Estudio morfohistológico y efecto quimioprotector de las hojas de Bidens pilosa L. sobre el cáncer de colon inducido en ratas
Effect of the ethanolic extract of Bidens pilosa L. on colon cancer induced in rats
Jorge Arroyo1,2, Pablo Bonilla3, Raquel Oré4, Ernesto Ráez5, Manuel Marin6, José Valencia3, Hugo Justil3, Jaime Martínez3, Christian Palomino3
1 Instituto de Investigaciones Clínicas, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
2 Sección de Farmacología, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
3 Instituto de Ciencias Farmacéuticas y Recursos Naturales, Facultad de Farmacia y Bioquímica, Universidad Nacional Mayor de San Marcos. Lima, Perú.
4 Centro de Investigación de Bioquímica y Nutrición, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
5 Instituto de Patología, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
6 Instituto de Ciencias Biológicas Antonio Raymondi, Facultad de Ciencias Biológicas, Universidad Nacional Mayor de San Marcos. Lima, Perú.
Resumen
Objetivos: Determinar la histología vegetal y la influencia del extracto etanólico de la planta entera de Bidens pilosa L. sobre el cáncer de colón inducido en ratas. Diseño: Estudio experimental. Lugar: Facultades de Medicina, de Farmacia y Bioquímica y de Ciencias Biológicas, Universidad Nacional Mayor de San Marcos, Lima, Perú. Material biológico: Ratas Holzmann. Intervenciones: Se agrupó 48 ratas Holtzmann, de 2 meses de edad, con pesos 100 g a 130 g, en seis grupos de ocho cada uno, y se indujo cáncer de colon con 1,2-dimetilhidrazina. Los grupos estuvieron constituidos por control normal, grupo con patología y grupos con patología y tratamientos. Principales medidas de resultados: Nivel de óxido nítrico, estrés oxidativo y cambios en el patrón celular del colon. Resultados: Se encontró incremento de los niveles de óxido nítrico y lipoperoxidación en los animales con 1,2-dimetilhidracina (DMH) y disminución en los que recibieron el tóxico más extracto de la planta. Al estudio histopatológico, con la DMH se evidenció desorganización celular, adenocarcinoma indiferenciado e invasivo; en tanto que, con los tratamientos se observó citoprotección, no dependiente de la dosis, siendo mayor a 50 mg/kg. Los hallazgos probablemente se expliquen porque los flavonoides y los compuestos fenólicos presentes en el extracto cumplen un rol importante en la inhibición del estrés oxidativo y también como anticancerígenos, inhibiendo el crecimiento de tumores. Se encontró detalles histológicos que servirían como caracteres diagnósticos, ayudando a verificar la identidad de la especie vegetal en polvo. Conclusiones: En condiciones experimentales, el extracto etanólico de la planta entera de Bidens pilosa L. presentó efecto quimioprotector sobre el cáncer de colon.
Palabras clave: Bidens; neoplasias del colon; compuestos fenólicos; flavonoides.
Abstract
Objectives: To determine the influence of Bidens pilosa L. whole plant ethanolic extract on colon cancer induced in rats. Design: Experimental study. Setting: Faculties of Medicine, Pharmacy and Biochemistry and Biologic Sciences, Universidad Nacional Mayor de San Marcos, Lima, Peru. Biologic material: Holzmann rats. Interventions: Forty-eight 2 months 100 g to 130 g Holtzmann rats were separated in six groups of eight each and 1,2-dimethylhidrazine induction of colon cancer was performed. Groups were normal control, group with pathology and groups with pathology and treatments. Main outcome measures: Nitric oxide levels, oxidative stress markers and colon cellular pattern modifications. Results: There was increment of nitric oxide levels and lipoperoxidation in the 1,2-dimethylhidrazine (DMH) animals, and decrease in those receiving both the toxic and the plant extract. Histopathology revealed cellular disorganization, undifferentiated and invasive adenocarcinoma with DMH; non-dose dependent cytoprotection was evident with treatments, especially with 50 mg/kg. Findings may be due to whole extract flavonoids and phenolic compounds contained in the whole extract that may play an important role in both oxidative stress and anticarcinogenic tumor growth inhibition. Histology details could be diagnostic characteristics useful to verify the vegetable powdered species identity. Conclusions: Under experimental conditions the ethanolic extract of Bidens pilosa L. whole plant presented chemoprotective effect on colon cancer.
Key words: Bidens; colonic neoplasms; phenolic compounds; flavonoids.
INTRODUCCIÓN
El cáncer de colon muestra una marcada incidencia y mortalidad en ambos sexos (1), siendo un delicado problema de salud humana, hecho que es favorecido por la resistencia farmacológica y los marcados efectos adversos de los agentes usados clínicamente. De ahí que es necesaria la búsqueda constante de productos naturales con eficacia demostrada y con mínimos efectos adversos, con un potencial recurso terapéutico.
Existen estudios que refuerzan una actividad protectora de la célula por la presencia de flavonoides que son encontrados en Bidens pilosa L. (2), atrapadora de radicales libres, inmunomoduladora (3,4).
Es así que, el uso de la planta entera de Bidens pilosa L. (amor seco) sería fuente de un agente quimioprotector, constituiría un coadyuvante para el tratamiento de cáncer de colon, dado que es un recurso natural abundante, de costo bajo y beneficiaría a millones de personas que padecen esta enfermedad a nivel mundial. Por ello, los objetivos de la presente investigación fueron realizar el estudio de la histología vegetal de la especie, obtener la fracción con alta concentración de compuestos fenólicos y flavonoides de la planta entera de Bidens pilosa L., determinar su eficacia quimioprotectora sobre el cáncer de colon inducido en ratas y conocer la influencia sobre los niveles de óxido nítrico y marcador de estrés oxidativo.
MÉTODOS
Se usó ratas albinas de cepa Holtzmann, con peso al inicio de la investigación de 100 a 130 g, de 2 meses de edad, machos, procedentes del Bioterio del Instituto Nacional de Salud del Ministerio de Salud, mantenidas en un ambiente a temperatura de 21°C, con dieta y agua a libertad.
La planta Bidens pilosa L. fue recolectada en el caserío de San José Bajo, distrito de Santiago de Cao, provincia de Ascope, departamento de la Libertad, Perú.
Como solventes, se utilizó alcohol 96º (etanol), metanol A.C.S (Fisher), Silicagel granulado (60-200 Mesh) J.T. Baker para cromatografía en columna rápida, hidróxido de sodio (Merck), EDTA (Merck), formol 40% (Laboratorio Portugal), heparina sódica (Laboratorios Trifarma), ácido fosfórico (Sigma), sulfato de zinc (Sigma), zinc metálico (Sigma), N-1-naftil-etilendiamina (Sigma), ácido sulfanílico (Sigma); en histología, colorante Giemsa (Merck), colorante Wright (Sigma), aceite de inmersión (Merck), hematoxilina (Merck), eosina (Merck), aceite de inmersión. (Merck), ácido acético glacial (Merck), hipoclorito de sodio, safranina (Sigma) y azul de toluidina (Merck). Como inductor de cáncer de colon, se utilizó 1,2- dimetilhidrazina (Sigma).
La identificación taxonómica fue realizada en el Museo de Historia Natural de la Universidad Nacional Mayor de San Marcos. Dicha ubicación sistemática fue ratificada mediante constancia Nº 156 USM-2007, siendo determinada por el Dr. Oscar Tovar Serpa.
Para el estudio histológico de la estructura interna de Bidens pilosa, se colectó las partes aérea y subterránea de la planta, de las cuales se fijó porciones de raíces, tallos y hojas en solución FAA (formaldehído, ácido acético glacial y etanol 96°), por 72 horas, y conservados finalmente en etanol de 70°. Posteriormente, se realizó secciones transversales y longitudinales de raíces y tallos y secciones transversales y superficiales de hojas; los cortes fueron aclarados con hipoclorito de sodio 50%, lavados y teñidos con safranina 1% y azul de toluidina 0,01%; el montaje de las láminas se hizo en gelatina glicerada, según DAmbrosio de Argüeso 1986; and Johansen 1940 (5,6). Se hizo observaciones microscópicas a 100 y 400 aumentos (Zeiss), dibujos micrográficos en cámara clara (Zeiss) y tomas fotográficas en cámara digital (Kodak), a 100 y 400 aumentos.
La planta fue secada bajo sombra y en lugar fresco.
La preparación del extracto etanólico tuvo el siguiente proceso: se realizó una maceración etanólica a partir de 5 kg de polvo seco de hojas de Bidens pilosa L., en 10 litros de etanol de 96º, con agitación dos veces al día, durante ocho días, en recipientes de vidrio oscuro y protegidos de la luz natural y artificial, para evitar algún tipo de descomposición. Luego se procedió a la obtención de fracciones del extracto etanólico total mediante cromatografía en columna rápida.
En el extracto etanólico seco total se realizó una marcha fotoquímica (7,8), al igual que en las fracciones, mediante reacciones de coloración o precipitación para cada tipo de metabolito secundario presente, con los reactivos específicos, indicando en los resultados la presencia o ausencia del metabolito: 5 mg del extracto problema con 5 gts de reactivos.
La determinación de la eficacia quimioprotectora del extracto etanólico de la planta entera de Bidens pilosa L. se realizó según Namasivayam et al. (9), con modificaciones en el tiempo de administración de DMH.
Cuarentaiocho ratas Holtzmann fueron agrupadas en seis grupos de ocho cada uno, distribuyéndose de la siguiente manera: a) grupo normal, con suero fisiológico 10 mL/kg; b) grupo A con 1,2- dimetilhidrazina (DMH); c) grupo B con DMH + 50 mg/kg de extracto etanólico (EE); d) grupo C, con DMH + 100 mg/kg de EE; e) grupo D, con DMH + 200 mg/kg de EE; y, f) grupo E, con 50 mg/kg de EE. La DMH fue administrada vía subcutánea, una vez por semana, durante 17 semanas, en dosis de 20 mg/kg de peso corporal. La DMH fue preparada en una solución conteniendo 400 mg de DMH disuelta en 100 mL de agua destilada estéril, con 37 mg de EDTA como agente estabilizador; la solución fue mantenida a pH 6,5. La administración del EE fue por vía oral, haciendo uso de una sonda metálica, iniciándose una semana antes de la primera inoculación de DMH hasta las 22 semanas que duró el estudio. Luego, los animales fueron decapitados por dislocación cervical, extrayéndose el intestino, hígado y riñón, los cuales fueron conservados en una solución de formol al 10%. Posteriormente, se hizo los cortes de cada órgano, para su respectivo estudio histopatológico.
Las variables que se evaluó fueron el potencial de lipoperoxidación, niveles de óxido nítrico e histopatología.
La determinación de los niveles de óxido nítrico fue según Katrina (10). Se recolectó la sangre de los animales en estudio mediante punción cardiaca, bajo anestesia con éter y con jeringa heparinizada; se procedió a centrifugarla durante 15 minutos, a 3 500 r.p.m., para separar los elementos formes del plasma. Se extrajo el plasma mediante micropipetas, sin tomar la parte precipitada, y se las depositó en eppendorf 1,5 mL, enumerados correlativamente.
La desproteinización del plasma en medio alcalino se realizó mediante la adición de las sustancias, en la siguiente proporción: plasma 0,8 mL; H2O destilada 0,6 mL; Na(OH) 1M 0,1 mL; ZnSO4 30% 0,1 mL. Entre la adición de la sustancia alcalina, Na(OH), y la sustancia atrapadora de proteínas, ZnSO4, hubo un intervalo de 5 minutos; posteriormente, se ejerció agitación constante por 10 minutos, obteniéndose una solución lechosa. Se procedió a centrifugar durante 15 minutos y se separó el plasma desproteinizado (incluido los controles) en una nueva batería de eppendorf.
Con relación al análisis espectrofotométrico, a la batería conteniendo plasma desproteinizado se le adicionó Zn metálico, dejándolo reposar durante 1 hora y 45 minutos, para la reducción de nitratos en nitritos. Transcurrido el tiempo, se centrifugó durante 15 minutos, a 3 500 r.p.m., para separar el precipitado de la nueva solución de plasma. A la nueva solución se le adicionó reactivo de Griess A; 5 minutos después, reactivo de Griess B; se dejó reposar por 10 minutos, tornándose de un grisáceo mas claro. Finalmente, se procedió a la lectura, en el espectrofotómetro UV-VIS LaboMed, a una longitud de onda de 546 nm.
El reactivo de Griess A contuvo ácido sulfanílico al 1% en ácido fosfórico al 5%.
El reactivo de Griess B tenía N-1-naftiletilendiamina al 0,1%, en agua destilada. Se determinó los niveles de óxido nítrico indirectamente, por su conversión en nitritos y nitratos (NOx). Las lecturas de absorbancia obtenidas fueron transformadas a concentración plasmática en mM, de acuerdo a la siguiente correlación:
R2 = 0,999 y = 0,044615 x
Donde x: concentración; y: absorbancia
El potencial de oxidación de lipoproteínas se midió mediante la prueba de lipoperoxidación, siguiendo la técnica de Buege & Aust (11), con modificaciones por Suárez (12), midiendo la producción de malondialdehído (MDA) en nmol/mL, en plasma, que al reaccionar con el ácido tiobarbitúrico (TBA) forma un complejo coloreado, que será leído a 535 nm en un espectofotómetro.
La eficacia quimioprotectora fue analizada mediante el análisis de varianza con múltiples comparaciones de Duncan; los resultados fueron expresados por medias ± error estándar. Los datos de proporción de niveles de óxido nítrico y potencial de oxidación de lipoproteínas fueron evaluados por el análisis de varianza, y la media de grupos fueron comparadas con la prueba de LSD (diferencia significativa mínima). Para los diferentes análisis, se consideró una p< 0,05.
RESULTADOS
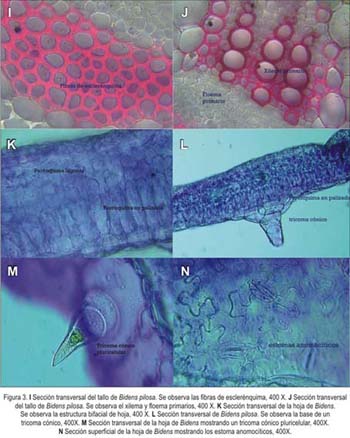
El estudio de la estructura interna de la planta evidenció una estructura primaria del tallo en sección transversal, con una delgada capa cuticular en la epidermis, corteza primaria con desarrollo de colénquima angular en las aristas del tallo y parénquima cortical clorofiliano; haces conductores primarios con refuerzos de fibras de esclerenquima, floema y xilema primarios y una amplia zona de parénquima medular (Figura 1). En la sección longitudinal, el tallo presentó vasos de xilema de tipo escaleriforme, reticulado y espiralado (Figura 2).
La raíz mostró una estructura secundaria, con una amplia corteza y parénquima reservante incoloro, presencia de espacios esquizógenos y fibras corticales. El cilindro vascular estaba conformado por floema y xilema secundarios, separados por el cambium vascular. El xilema presentó mayormente vasos de tipo reticulado (Figura 2).
La hoja presentó, en sección transversal, una estructura bifacial de dicotiledónea, con presencia de una delgada cutícula en la epidermis; el mesófilo estuvo compuesto de una capa de parénquima clorofiliano en palisada y parénquima clorofiliano lagunar; hubo presencia en ambas superficies de la epidermis de tricoma cónicos pluricelulares grandes y pequeños (ver Figura 3).
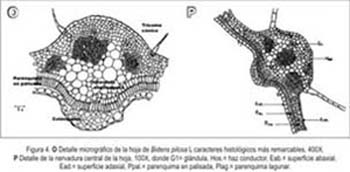
A nivel de la nervadura central, la hoja presentó haces vasculares separados, presencia de glándulas esquizógenas y refuerzos de colénquima hacia la superficie adaxial (Figura 4).
En la sección superficial, la hoja presentó estomas mayormente de tipo anomocítico, hacia la superficie abaxial de la hoja (Figura 4).
Se obtuvo un extracto etanólico total con aspecto de masa homogénea, consistencia blanda, color verde petróleo, libre de partículas extrañas; el rendimiento fue de 9,4% de planta entera.
El estudio fitoquímico indicó que los compuestos fenólicos estaban en abundante cantidad en la fracción metanólica; y que los flavonoides, taninos y glicósidos estuvieron en regular cantidad en el extracto etanólico y fracción metanólica.
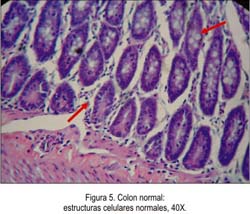
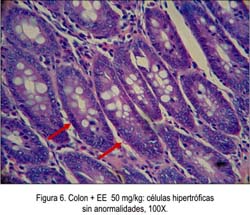
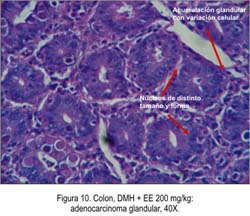
La Tabla 1 y las Figuras 5, 6, 7, 8, 9 y 10 muestran el efecto de los compuestos fenólicos y flavonoides de Bidens pilosa sobre el cáncer de colon, observándose un mejor efecto a dosis de 50 mg/kg de EE.
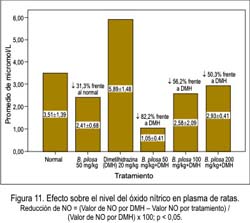
El extracto etanólico de Bidens pilosa L. (EE) disminuyó los niveles plasmáticos de nitritos, en las ratas tratadas con DMH 20 mg/kg. Se observó que la dosis de 50 mg/kg de EE disminuyó mejor los niveles de nitritos seguido de la dosis de 100 mg/kg y 200 mg/kg. Los niveles de nitritos en los animales tratados solamente con DMH fueron superiores a todos los grupos tratados EE (Figura 11).
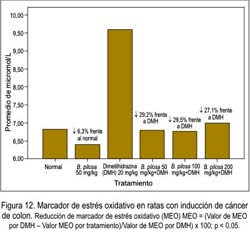
Respecto al potencial de oxidación de lipoproteínas, la Figura 12 muestra la concentración plasmática de malondialdehido (MDA) en el grupo normal y los grupos experimentales. Las concentraciones plasmáticas de MDA fueron significativamente elevadas en el grupo tratado con DMH, comparadas con el grupo normal. Los grupos tratados con EE disminuyeron significativamente las concentraciones de MDA comparadas con el grupo que recibió solamente DMH. Se observó además que el grupo que recibió las dosis de 100 mg/kg y 50 mg/kg de EE disminuyó mejor la concentración plasmática de MDA, que el grupo que recibió 200 mg/kg.
DISCUSIÓN
Desde el punto de vista histológico, existen pocos trabajos publicados para las especies de Bidens (13,14). Sin embargo, a nivel de la estructura interna se encuentra detalles histológicos, como la presencia de los tricomas cónicos y glándulas esquizógenas en la hoja y los vasos reticulado, espiralado y escaleriforme del xilema del tallo. Así mismo, es detalle importante la carencia de cristales de oxalato de calcio en la planta. Los detalles histológicos mencionados son de mucha importancia en el examen de la droga en polvo y servirían como caracteres diagnósticos, ayudando a verificar la identidad de la especie vegetal (5,13,15).
Los flavonoides contienen en su estructura química un número variable de grupos hidroxilo fenólicos y excelentes propiedades de quelación del hierro y otros metales de transición, lo que les confiere una gran capacidad antioxidante (16,17). Por ello, desempeñan un papel esencial en la protección frente a los fenómenos de daño oxidativo y tienen efectos terapéuticos en un elevado número de patologías, incluyendo la cardiopatía isquémica, la aterosclerosis o el cáncer (18,19). Está demostrado que tanto los flavonoides como los compuestos fenólicos cumplen un rol importante en la inhibición del estrés oxidativo y por lo tanto la lipoperoxidación, resultando ser potentes antioxidantes (20,21) y también anticancerígenos, inhibiendo el crecimiento de tumores (22). El estudio fitoquímico de los extractos de la especie Bidens pilosa L. indica la presencia de flavonoides, chalconas, glucósidos del ácido fenilpropanoico, poliacetilenos, un diterpeno, glucósidos de flavona, compuestos fenólicos (2,3). En el presente estudio, se aisló diversas fracciones a partir del extracto crudo Bidens pilosa L., siendo el extracto etanólico (EE) y la fracción metanólica los que contenían flavonoides y compuestos fenólicos y, por fines técnicos y económicos, el EE fue indicado para la realización de este estudio.
La DMH es un agente procarcinogenético que sufre metabolismo en el hígado, dando como resultado un agente carcinogenético (ion diazonium), que es capaz de producir efectos tóxicos en lugares diferentes del tumor (23). La producción de metabolitos oxigenados reactivos durante el metabolismo hepático del DMH o durante la carcinogénesis del colon está bien documentado; muchas publicaciones también sugieren que las células tumorales producen cantidades considerables de H2O2, que es liberada en la circulación (24).
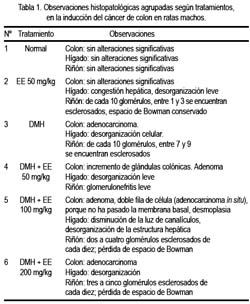
El efecto quimioprotector de las distintas dosis de EE frente a adenomas y carcinomas inducidos por DMH fue significativo, evidenciándose mejor efecto a dosis de 50 mg/kg de EE (Tabla 1). Los mecanismos por los cuales el extracto etanólico inhibirían los adenocarcinomas podrían ser explicados hasta el momento según Namasivayam (9), quien demostró que la inhibición de los adenocarcinomas se deben a la disminución de dos enzimas bacterianas presentes en la microflora del colon la b-glucoronidasa, que hidroliza los glucorónidos biliares en el colon, produciendo agliconas, que son compuestos tóxicos cancerígenos, y la mucinasa, que hidroliza a la mucina, responsable de la protección de la mucosa del colon. De esta forma, se entiende que el incremento de ambas enzimas frente a la administración de DMH potencia la actividad cancerígena y que muchos productos naturales podrían inhibir a las dos enzimas en mención. Otro mecanismo de acción es sustentado por (25), quien demostró que la inhibición de la sintetasa inducida de óxido nítrico (iNOS) disminuye el crecimiento y proliferación de tumores en el colon. Se sabe que el iNOS permite la mutación del K-ras y el crecimiento y formación de tumores. Se ha identificado también que la mutación de K-ras incrementa la producción de ciclooxigenasa–2 (26). Estos DOS mecanismos de acción podrían sustentar la protección que tendría el EE sobre los adenocarcinomas del colon de rata.
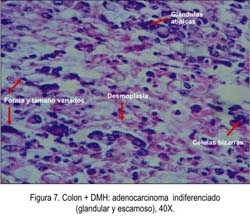
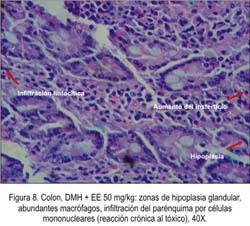
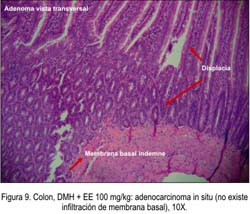
El efecto quimioprotector de las distintas dosis del EE frente a adenomas y carcinomas inducidos por DMH fue significativo, evidenciándose mejor efecto a dosis de 50 mg/kg, porque solo hubo incremento de glándulas colónicas e infiltrado celular crónico, por la presencia de mononucleares en el parénquima y zonas de hipoplasia glandular con abundantes macrófagos (Figura 8). Con dosis de 100 mg/kg, se apreció adenocarcinoma in situ, indicando que no hubo compromiso fuera de la membrana basal (Figura 9). Mientras tanto, a la dosis de 200 mg /kg se observó infiltración mixta de adenocarcinoma (Figura 10); sin embargo, los animales que solamente recibieron tóxico sin Bidens pilosa expresaron desorganización celular, llegando a provocar adenocarcinoma infiltrante, mixto, con niveles elevados de radicales libres. Estos hallazgos se correlacionan con los niveles de óxido nítrico y marcador de estrés oxidativo encontrados en la presente investigación (Figura 12). Posiblemente, el efecto quimioprotector de la planta es dado sin considerar la dependencia de la dosis.
El efecto quimioprotector frente a la lesión dado en el colon de rata por DMH fue evidenciado por Devasena (27), al utilizar bis-1,7-(2-hidroxifenil)hepta-1,6-dieno-3,5-diona, un análogo de curcumina; esta ha mostrado actividad anticancerígena sobre modelos experimentales de cáncer de colon (28); se ha observado que Coriander sativum es protector contra el deterioro del metabolismo lipídico, al inducir cáncer de colon por DMH (29).
Los nitritos dosados en plasma permiten cuantificar los niveles de óxido nítrico. Los resultados obtenidos muestran un incremento de nitritos en plasma del grupo tratado con DMH, mientras que, en los que recibieron EE más DMH, disminuyeron significativamente (Figura 11), lo que se relaciona con los resultados obtenidos con el efecto quimioprotector. Es decir, el incremento de los niveles de óxido nítrico en plasma están estrechamente relacionados con la carcinogénesis; así lo sustentó Takahashi (25), quien demostró la presencia de iNOS en tumores del colon.
El estrés oxidativo puede ser cuantificado mediante el indicador malondialdehido nmol/ml (MDA), que es una sustancia producto de la reacción con el ácido tiobarbitúrico. El nivel de MDA cuantificado en las ratas en tratamiento fue superior en las que recibieron solamente DMH, mientras que en las que recibieron tratamientos con EE disminuyó significativamente, siendo más marcado en el grupo que recibió dosis de 50 mg/kg. Estos resultados indican una reducción del estrés oxidativo por el tratamiento con EE, lo cual es favorable para la protección del colon, ya que frente a un estrés oxidativo severo se puede desencadenar una carcinogénesis por especies reactivas, como ión superóxido (O2) y radicales hidroxilos (OH), que son liberados a la circulación sanguínea, resultando en el plasma una lipoperoxidación en ratas tratadas con DMH. Desde que se sabe que el estrés oxidativo eleva la producción de prostaglandina e interrumpe la producción de la glutation peroxidasa, conllevando al cáncer de colon, se ha tomado importancia en productos que modularían el estrés oxidativo (30).
En este estudio, se observó que la lipoperoxidación asociada con el incremento de los niveles de óxido nítrico en la circulación sanguínea refuerza la inducción de cáncer con DMH en ratas.
La presente investigación estaría contribuyendo en mostrar una alternativa terapéutica en base de productos naturales, tales como Bidens pilosa L. (amor seco), a fin de coadyuvar con el mejoramiento de los signos y síntomas del cáncer de colon, dado que la terapia farmacológica estándar conlleva a un mayor riesgo de reacciones adversas medicamentosas, resistencia farmacológica, y porque caso contrario se puede conducir a incapacidad grave, situación en que se presentan alteraciones sistémicas que acortarían la vida del paciente oncológico.
En conclusión, en condiciones experimentales, el extracto etanólico de la planta entera de Bidens pilosa L. presentó efecto quimioprotector sobre el cáncer de colon inducido en ratas por 1,2-dimetilhidrazina, con reducción de los niveles de oxido nítrico y marcador de estrés oxidativo.
AGRADECIMIENTO
Se da un agradecimiento muy especial al Consejo Superior de Investigaciones de la UNMSM, por el financiamiento del Proyecto FEDU de código 060103131del año 2006.
REFERENCIAS BIBLIOGRÁFICAS
1. Jemal A, Murria T, Ward E, Samuel A, Tiwari R, Ghafoor A, et al. Cancer Statistics 2005. CA Cancer J Clin. 2005;55:10-30. [ Links ]
2. Gorriti A. Bioensayos en especies de Bidens con actividad terapéutica. Lima: Universidad Nacional Myor de San Marcos; 1998.
3. Abajo C, Boffill M, Del Campo J, Méndez M, González Y, Mitjans M, et al. In vitro study of the antioxidant and immunomodulatory activity of aqueous infusion of Bidens pilosa. J Ethnopharmacol. 2004;93(2-3):319-23.
4. Chiang YM, Chuang DY, Wang SY, Kuo YH, Tsai PW, Shyur LF. Metabolite profiling and chemopreventive bioactivity of plant extracts from Bidens pilosa. J Ethnopharmacol. 2004;95(2-3):409-19.
5. DAmbrosio de Argüeso A. Manual de técnicas en histología vegetal. 1ra ed. Buenos Aires: Ed Hemisferio Sur S.A.; 1986.
6. Johansen DA. Plant microtechnique. London: McGraw- Hill Book Company; 1940.
7. Domínguez X. Métodos de investigación fitoquímica. México DF: Ed. Limusa; 1985.
8. Lock de Ugaz O. Investigación fítoquímica; métodos en el estudio de productos naturales. 2da edición. Lima: Fondo Editorial Pontificia Universidad Católica; 1994.
9. Namasivayam N, Vaiyapuri M, Venugopal M. Effect of coconut cake on the bacterial enzyme activity in 1,2 – dimethyl hydrazine induced colon cancer. Clinica Chimica Acta. 2004;342:203-10.
10. Miranda KM, Espey MG, Wink DA. A rapid, simple spectrophotometric method for simultaneous detection of nitrate and nitrite. Nitric Oxide. 2001;5(1):62-71.
11. Buege JA, Aust SD. Microsomal lipid peroxidation. Methods Enzymol. 1978;52:302-10.
12. Suárez CS. Detoxificación hepática y defensa antioxidante por efecto de xenobióticos alimentarios. Tesis de Maestría en Bioquímica. Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú. 1995.
13. Esaú K. Anatomía Vegetal. 1ra ed. Barcelona: Ediciones Omega; 1959.
14. Metcalfe C, Chalk L. Anatomy of Dicotyledons. 1ra ed. Oxford: Clarendon Press; 1950.
15. Trease GE, Evans WC. Tratado de farmacognosia. 13ª Ed. Madrid: Editorial Interamericana; 1991.
16. Haysteen B: Flavonoids. A class of natural products of high pharmacological potency. Biochem Pharmacol. 1983;32:1141-8.
17. Peres W. Radicais Livres em nïveis biológicos. Pelotas: Ed. Universidade Católica de Pelotas; 1994. p. 49-81.
18. Pace-Asciak CR, Hahn S, Diamandis EP, Soleas G, Goldberg DM. The red wine phenolics trans-resveratrol and quercetin block human platelet aggregation and eicosanoid synthesis: implications for protection against coronary heart disease. Clin Chim Acta. 1995;235(2):207-19.
19. Jang M, Cai L, Udeani G. Cancer chemopreventive activity of resveratrol. Science. 1997;275:218-21.
20. Tapia A, Rodriguez J, Theoduloz C, Lopez S, Feresin GE, Schmeda-Hirschmann G. Free radical scavengers and antioxidants from Baccharis grisebachii. J Ethnopharmacol. 2004;95(2-3):155-61.
21. De Oliveira SQ, Dal-Pizzol F, Gosmann G, Guillaume D, Moreira JC, Schenkel EP. Antioxidant activity of Baccharis articulata extracts: isolation of a new compound with antioxidant activity [abstract]. Free Radic Res. 2003;37(5):555-9.
22. Mongolli E, Pampuro S, Coussio J, Salomon H, Ciccia G. Cytotoxic and DNA interaction activities of extracts from medicinal plants used in Argentina. Journal of Ethnopharmacology. 2000;71(1-2): 145-51.
23. Bobek S, Galbavy S, Mariassyova M. The effect of red beet (Beta vulgaris var. rubra) fiber on alimentary hypercholesterolemia and chemically induced colon carcinogenesis in rats. Nahrung. 2000;44:184-7.
24. Vaiyapuri M, Namasivayam N. Effect of ginger on bacterial enzymes in 1,2-dimethylhydrazine induced experimental colon carcinogenesis. European Journal of Cancer Prevention. 2006; 15(5):377-83.
25. Takahashi M, MIchihiro M, Yutaka S, Hidetaka S, Yosshihisa K, Masao N, Takayuki M, et al. Suppressive effect of an inducible nitric oxide inhibitor, ONO – 1714 on AOM – induced rat colon carcinogenesis. Nitric Oxide. 2006;14:130-6.
26. Bissonnette M, Khare S, Von Lintig FC, Wali RK, Nguyen L, Zhang Y, Hart J, et al. Mutational an non-mutational activation of p21ras in rat colonic azoxymethane-induced tumors: efeccts on mitogen-activated protein kinase, cycloxygenase-2, and cyclin D1. Cancer Research. 2000;60: 4602-9.
27. Devasena T, Rajasekaran K, Gunasekaran G, Viswanathan P, Menon P. Anticarcinogenic effect of bis-1,7-(2-hydroxyphenyl)-hepta-1,6-diene-3,5-dione a curcumin analog on DMH-induced colon cancer model. Pharmacological Research 2003;47:133-40.
28. Huang MT, Lou YR, Ma W, Neomark HL, Reuhl KR, Conney AH. Inhibitory effects of dietary curcumin on forestomach. Cancer Res. 1994;54:5841-7.
29. Chithra V, Leelamma S. Coriandrum sativum - effect on lipid metabolism in 1,2-dimethyl hydrazine induced colon cancer. Journal of Ethnopharmacology. 2000;71(3):457-63.
30. Drew J, Arthur J, Farquharson A, Russell W, Morrice P, Duthie G. Salicylic acid modulates oxidative stress and gluthaione peroxidase activity in the rat colon. Biochemical Pharmacology. 2005;70:888-93.
Manuscrito recibido el 10 de marzo de 2008 y aceptado para publicación el 13 de mayo de 2008.
Correspondencia:
Dr. Jorge Luis Arroyo Acevedo
Sección de Farmacología
Facultad de Medicina, UNMSM.
Av. Grau 750. Lima 1, Perú.
Correo-e: jorgeluis_arroyoacevedo@yahoo.es