Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Medicina
versión impresa ISSN 1025-5583
An. Fac. med. v.70 n.2 Lima jun. 2009
Efecto antiulceroso del extracto hidroalcohólico liofilizado de hojas de Bixa orellana (achiote), en ratas
Antiulcer effect of lyophilized hydroalcoholic extract of Bixa orellana (annatto) leaves in rats
Oscar Huamán1, Miguel Sandoval1, Inés Arnao1, Elsa Béjar1
1 Centro de Investigación de Bioquímica y Nutrición Alberto Guzmán Barrón, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
Resumen
Objetivo: Identificar los metabolitos secundarios presentes en el extracto hojas de Bixa orellana, evaluar el grado de protección del extracto frente a la injuria con etanol y estudio histopatológico de la región glandular del estómago. Diseño: Estudio prospectivo experimental. Institución: Centro de Investigación de Bioquímica y Nutrición Alberto Guzmán Barrón, Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Material biológico: Extracto de hojas de Bixa orellana y ratas albinas machos adultos. Intervenciones: Se analizó los metabolitos secundarios del extracto, mediante los reactivos específicos. Para la evaluación del efecto antiulceroso, se aplicó la técnica propuesta por Robert 1979, a dosis de extracto de 200 y 400 mg/kg. Se provocó la injuria con alcohol al 96%. La evaluación macroscópica fue mediante la escala de Marhuenda. Los tejidos fueron conservados en formol al 10%, para su estudio histopatológico por tinción hematoxilina-eosina. Principales medidas de resultados: Inhibición de las lesiones gástricas. Resultados: El extracto hidroalcohólico de hojas de Bixa orellana tiene compuestos fenólicos, tales como flavonoides y taninos, terpenos y alcaloides. El tratamiento con el extracto produjo una inhibición de las lesiones gástricas en 21,7% y 28,3%, respectivamente (p<0,01). En el estudio histológico, se encontró mayor protección y menor migración de células proinflamatorias en los grupos que recibieron el extracto a 200 y 400 mg/kg. Sin embargo, los grupos controles y los que recibieron ranitidina presentaron grados de lesión considerable y un mayor incremento de migración de células proinflamatorias. Conclusiones: El extracto hidroalcohólico de Bixa orellana presenta un efecto gastroprotector antiulceroso frente a la injuria con etanol al 96%, tanto a nivel macroscópico como microscópico.
Palabras clave: Bixa orellana; gastritis; úlcera gástrica; agentes antiulcerosos.
Abstract
Objective: To identify the secondary metabolites present in Bixa orellana leaves extract, to evaluate the extract protection against ethanol injury, and histopathology study of the stomach glandular region. Design: Prospective, experimental and analytical research. Setting: Biochemistry and Nutrition Research Center laboratories, Universidad Nacional Mayor de San Marcos. Biological material: Bixa orellana leaves extract and male albino rats. Interventions: Secondary metabolites from the extract were analyzed using identification chemical tests. For evaluation of the gastro-protective effect proposed by Robert 1979 the extract was used at 200 and 400 mg/kg doses, and for macroscopic evaluation Marhuenda scale was employed. Tissues were preserved in 10% formaldehyde for histopathology examination by hematoxylin-eosin staining. Main outcome measures: Gastric lesions inhibition. Results: Bixa orellana leaves hydroalcoholic extract has phenolic compounds such as flavonoids and tannins, terpenes and alkaloids. Treatment with 200 and 400 mg/kg extract doses produced gastric lesions inhibition in respectively 21,7% and 28,3% (p<0,01). By histology, there was bigger protection and reduced migration of proinflammatory cells in the groups receiving 200 and 400 mg/kg extract. Control groups and those receiving ranitidine showed considerable lesion degrees and increased proinflammatory cells migration. Conclusions: Bixa orellana leaves hydroalcoholic extract produced gastroprotective effect against injury with 96% ethanol at both macroscopic and microscopic levels.
Key words: Bixa orellana; gastritis, stomach ulcer; anti-ulcer agents.
INTRODUCCIÓN
El achiote pertenece a la familia Bixaceae; es una planta originaria de América tropical, se cultiva extensamente en todas las regiones tropicales del mundo. En el Perú, la Bixa orellana se encuentra en la parte montaña de los departamentos de Amazonas, Cusco, Ayacucho y San Martín. Se usa ampliamente en la medicina tradicional en las regiones montañosas y hay pocos estudios sobre sus diferentes propiedades farmacológicas. Los estudios realizados por Li (1), Alvarado (2) y Juárez (3) refieren propiedades diuréticas, antidisentérica, antivenérea, hipoglicemiante y antiinflamatorio prostático; en las zonas de cultivo, los pobladores refieren el conocimiento ancestral medicinal de las hojas para tratar las enfermedades del hígado y del estómago como antiulceroso; estas propiedades han sido estudiadas en décadas pasadas por algunos investigadores (4-6).
Dicho conocimiento fitoterapéutico prevalece en nuestros días, con riesgo de perderse, debido a la transculturización de nuestros nativos, por lo que es nuestro deber conservarlo y darle un respaldo con la metodología que la comunidad científica exige.
En nuestro país el uso de plantas medicinales con atributos antiulcerosos es muy difundido, y por ello se ha llevando a cabo diferentes estudios sobre su acción farmacológica; como ejemplo tenemos a la Buddleia globosa (árbol bola naranja) (7), Piper angustifolium (matico) (8,9), Crotón palanostigma (sangre de grado) y Aloe vera (sábila) (10).
La úlcera péptica o úlcera gástrica, es una enfermedad que se presenta entre el 10 a 15% de la población constituyendo un problema médico-social con repercusión económica y un motivo de preocupación en investigadores y especialistas (11). La úlcera gástrica se diferencia de la gastritis por la profundidad de la lesión en la mucosa. Así, las ulceras gástricas son lesiones que penetran la totalidad de la mucosa y es probable que representen el desenlace de varias anormalidades. El cráter de la úlcera con frecuencia está rodeado por una porción de mucosa inflamada pero íntegra, lo cual sugiere que la gastritis constituye una lesión predisponente para el desarrollo de la úlcera gástrica. La mayor parte de las úlceras gástricas se presenta en la curvatura menor del estómago. Se estima que algunas úlceras gástricas están relacionadas con el deterioro de la defensa de la mucosa, ya que en algunos pacientes afectados la capacidad secretora de ácido y de pepsina resulta normal e incluso menor de lo normal (12).
Inicialmente, era desconocida la etiología de la enfermedad y la elección del tratamiento había sido en gran parte empírica. Hoy, se puede entender mejor los mecanismos por los cuales se produce la enfermedad, por investigaciones para comprender las vías de su formación y evolución, mejorando las posibilidades de un adecuado tratamiento.
En el caso de la úlcera duodenal y gástrica, la atención se ha centrado en algunos trastornos. Entre ellos mencionaremos la hipersecreción del ácido, anomalía pilórica, aumento en la secreción de gastrina, trastorno de la motilidad del píloro, disminución del moco protector de la mucosa gástrica, el uso de antiinflamatorios no esteroideos (AINES), presencia de Helicobacter pylori (13), el estrés y estilo de vida (12), siendo este último uno de los factores más frecuentes en los pacientes que presentan esta enfermedad.
Actualmente, en nuestro país se utiliza las hojas de Bixa orellana para el tratamiento de inflamación prostática y, la infusión, para el tratamiento de la gastritis y úlcera, aunque esta última forma de tratamiento es poca difundida y tan solo se limita a la región de la selva alta. Es por ello que resulta de gran interés su estudio fotoquímico, farmacológico y toxicológico y considerar las características que debe poseer todo fitomedicamento, como ser seguro, eficaz y de calidad.
MÉTODOS
Se realizó un trabajo experimental en los laboratorios del Centro de Investigación de Bioquímica y Nutrición de la Facultad de Medicina de la Universidad Nacional Mayor de San Marcos (UNMSM), Lima, Perú.
Las hojas de Bixa orellana (achiote) fueron recolectadas y tratadas en el distrito La Peca, Provincia de Bagua, departamento de Amazonas. Una vez recolectadas fueron limpiadas, secadas y guardadas en bolsas de tela de color oscuro, para luego ser trasladadas a la ciudad de Lima. Para la confirmación de la especie, se envió hojas y flores de la muestra al Museo de Historia Natural de la UNMSM, cuyos especialistas dieron su conformidad (14).
Las hojas fueron seleccionadas, para finalmente molerlas en un molino de tamiz fino. La maceración se realizó con una solución de etanol al 80%, en una proporción de 1/10, utilizando 200 g de hojas secas, una botella de color ámbar con tapa, con agitación manual por 15 minutos al día, por un tiempo de 15 días. Cumplido el tiempo, la solución se filtró usando papel filtro Whatman 1, con capacidad de retención de partículas >11 µm de diámetro; el filtrado se colocó en una estufa a 40°C, para eliminar el etanol y luego se liofilizó, teniendo un rendimiento del 7% de la solución filtrada. El liofilizado se guardó en un frasco de color ámbar con tapa, a una temperatura de 4°C, con desecador, hasta el momento de su utilización (15).
La separación de los metabolitos secundarios del extracto hidroalcohólico se realizó mediante cromatografía en capa fina, con fase estacionaria de silicagel 60, utilizando como solvente cloroformo y metanol en proporción de 15:1. Se identificó los metabolitos secundarios visualizando con una lámpara de UV 340 nm y reconociendo mediante los reactivos específicos solución de gelatina (taninos), cloruro férrico (compuestos fenólicos), Shinoda (flavonoides), Molish (glucidos), 2,4 dinitrofenilhidrazina (compuestos carbonilos), Dragendorff, Mayer y Wagner (alcaloides) y Liebermann–Burchard (terpenos y esteroides) (16). En el caso de los taninos, se procedió a su reconocimiento con una solución de gelatina 5%, en tubo de ensayo.
Para evaluar el efecto protector del extracto hidroalcohólico en la mucosa gástrica, se utilizó 48 ratas machos de raza Holtzman, adquiridas en el bioterio de la Universidad Nacional Agraria La Molina, de un peso de 190 g ± 17,1, que tuvieron un tiempo de adaptación de 7 días, a una temperatura de 20 a 22°C, con dieta balanceada y agua ad libitum. Para la inducción de lesiones gástricas, se usó la técnica propuesta por Robert y colaboradores, para lo cual se usó alcohol 96% administrado vía orogástrica, mediante canulación, a dosis de 10 mL/kg (17). El alcohol es una molécula con gran capacidad de incrementar el estrés oxidantivo celular. A nivel de los tejidos, incrementa la apoptosis celular, que es uno de los principales tipos de muerte celular, además de inflamación y necrosis, especialmente gástrica y hepática (18).
Las ratas fueron sometidas previó ayuno sólido de 24 horas con solución de dextrosa 5% ad libitum y distribuidas en forma aleatoria en 6 grupos (9 ratas cada uno): a) grupo A (suero fisiológico, 1 mL/100 g de peso) para observar la mucosa gástrica sin lesiones; grupo B (suero fisiológico, 1 mL/100 g de peso), grupo control para observar las lesiones producidas por el etanol; grupo C (ranitidina 100 mg/kg, fármaco de elección como parte del tratamiento de gastritis y úlceras gástricas); grupo D (extracto 100 mg/kg); grupo E (extracto 200 mg/kg); y grupo F (extracto 400 mg/kg).
Las sustancias fueron disueltas en suero fisiológico, a las dosis anteriormente descritas; para ello se utilizó el Tween 80, que es un poliascorbato surfactante y emulgente no iónico, usado para lograr una adecuada disolución del extracto en agua, teniendo una concentración final al 12% de la solución, la cual fue administrada vía orogástrica con cánula metálica. Transcurrida una hora, se administró por la misma vía 1 mL de etanol al 96% a los grupos del B al F; al grupo A se le volvió a administrar suero fisiológico 1 mL.
Luego de 60 minutos, se procedió a anestesiar a las ratas con vapores de éter dietílico, para luego realizar laparotomía y extraer el estómago. Los estómagos fueron abiertos por la curvatura mayor y fijados en una plancha porosa con alfileres, para su evaluación por la escala de Marhuenda, observando la presencia de moco, edema, congestión del tejido y extensión de las úlceras en la zona mucosa (18); se conservó en formol al 10%, para su estudio histopatológico con tinción hematoxilina-eosina.
Los resultados obtenidos en la evaluación macroscópica fueron expresados en promedio y el porcentaje de inhibición de lesiones gástricas (ILG), comparando las de los animales con tratamiento (IGLt) con las del grupo control (IGLc) y tomando a esta última como el 100%, mediante la siguiente formula:
% de inhibición de lesiones gástricas = (ILGc – ILGt)/ILGc x 100
Los datos fueron sometidos al análisis de varianza (ANOVA); para el estudio se utilizó un p<0,01 y/o p<0,05, para lo cual se usó el software SPSS, versión 15,0.
Los animales fueron tratados y manipulados según las normas de ética de experimentación animal (19). En nuestro caso, los animales fueron anestesiados con vapores de éter dietílico y posteriormente a la extracción del estómago fueron sacrificados bajo estado anestésico.
RESULTADOS
En el estudio fitoquímico del extracto hidroalcohólico liofilizado de hojas de Bixa orellana se identificó los metabolitos mostrados en la tabla 1.
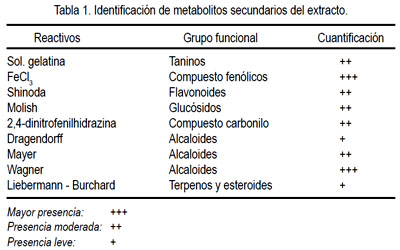
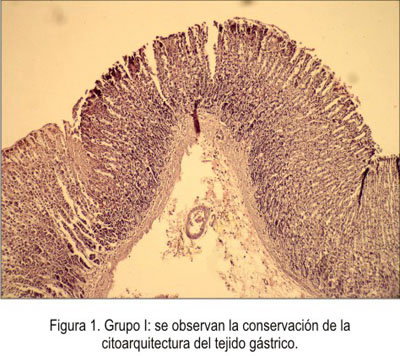
Se evidenció una mayor cantidad de compuestos fenólicos, tales como taninos y flavonoides; esto se debe a que los compuestos fenólicos por lo general están unidos a restos de azúcares, lo cual lo hace soluble en solventes polares, tales como agua, metanol y etanol. Sin embrago, en cromatografía en capa fina de silica Gel 60 y mediante reveladores específicos se identifico en una menor proporción terpenos y alcaloides. La identificación de taninos se realizó en una solución de gelatina, observándose una moderada precipitación de proteínas. En la evaluación macroscópica del grupo I (sin agente injuriante) no se observó daño , así como en la evaluación microscópica (figura 1); solo presentaron algunas petequias de forma muy aislada y en algunos de los estómagos.
El efecto del etanol al 96% se observó en el grupo II (control), con formación de úlceras en la mucosa, consistente en bandas alargadas, usualmente paralelas, con abundantes petequias, pérdidas de pliegues; el desprendimiento de moco fue intenso en todas las muestras, como también mucosa hiperémica.
El tratamiento con ranitidina, a la dosis indicada, no inhibió las lesiones gástricas inducidas por etanol de forma significativa, comparado con el control.
Sin embargo, el tratamiento con extracto a las diferentes dosis redujo la pérdida de moco, número de petequias y principalmente las úlceras. Estas características fueron notorias de manera significativa en los grupos V y VI.
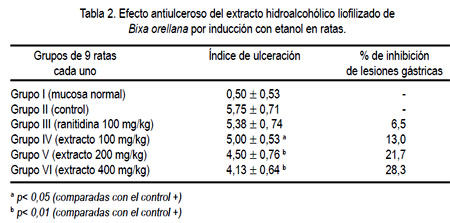
Las lesiones fueron cuantificadas por la escala de Marhuenda, tal como se observa en la tabla 2, existiendo una inhibición significativa de las lesiones gástricas a las dosis de 100 mg/kg (p<0,05) y a 200 y 400 mg/kg (p<0,01), comparados con el control. El tratamiento con ranitidina no redujo de manera significativa las lesiones gástricas (6,5%).
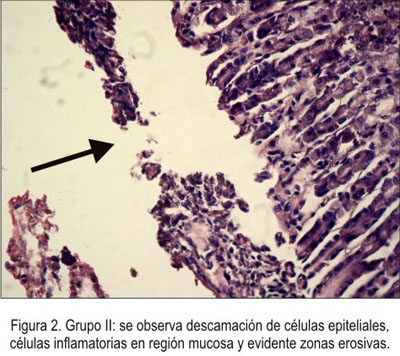
Los resultados encontrados en el estudio histológico a los estómagos inducidos a lesión con etanol, previo tratamiento con las sustancias indicadas fueron:
En el grupo II (control) se observó descamación de las células epiteliales, con evidentes zonas erosivas en la región mucosa; también, se evidenció la infiltración de células inflamatorias en la región mucosa, hipertrofia muscular e hipotrofia glandular (figura 2).
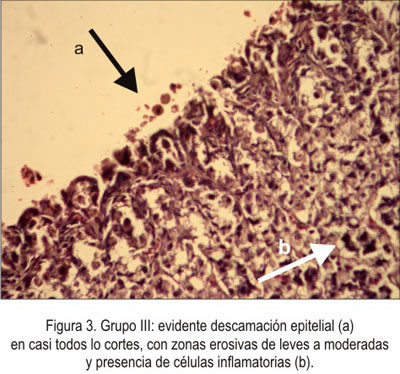
En el grupo III que recibió la ranitidina 100 mg/kg de peso, se observó descamación epitelial en casi todos los cortes y zonas erosivas, discretas hasta moderadas, en la región mucosa. Hubo una marcada infiltración de células inflamatorias en la submucosa y menor presencia en la región muscular, con adelgazamiento de la misma (figura 3).
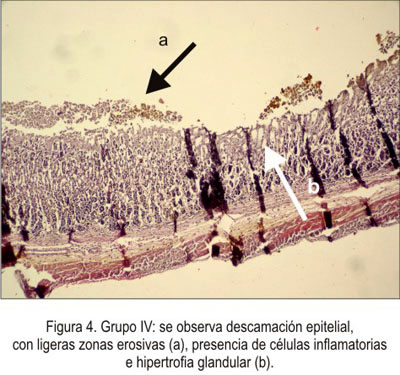
El grupo IV, que recibió el extracto 100 mg/kg, presentó el mismo compromiso de descamación de células epiteliales que el grupo de la ranitidina, con ligeras zonas erosivas. Se observó infiltración de células inflamatorias, tanto en la mucosa como en la submucosa, hipotrofia glandular y capa muscular adelgazada. En algunos cortes se observó mucosa normal y zonas hemorrágicas (figura 4).
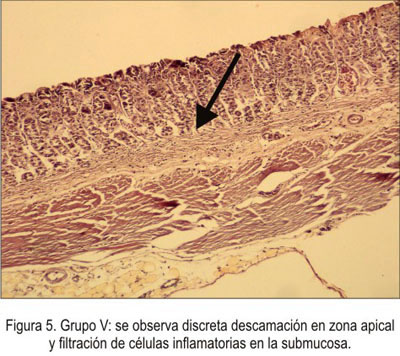
En el grupo V (200 mg/kg), se observó una discreta descamación en la zona apical y zonas erosivas, desde discretas hasta moderadas. Existió discreta infiltración de células infamatorias en la submucosa, capa muscular adelgazada, con regiones conservadas de las regiones mucosa, submucosa y muscular (figura 5).
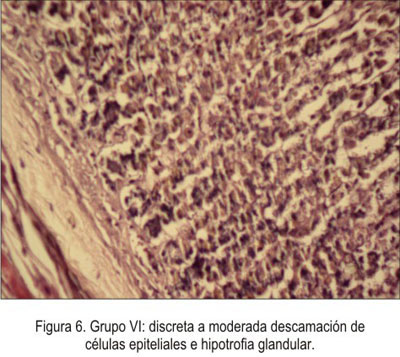
En el grupo VI, se observó una discreta a moderada descamación de células epiteliales, infiltración submucosa, capa muscular adelgazada e hipotrofia glandular (figura 6).
DISCUSIÓN
Los metabolitos secundarios presentes en las plantas poseen efectos beneficiosos que el hombre hasta la fecha sigue investigando, con la finalidad de darle aplicación farmacológica, con los criterios científicos correspondientes. Muchos de estos compuestos son solubles en soluciones alcohólicas (metanol o etanol), como son: terpenos, saponósidos, ácidos fenólicos, flavonoides y taninos, con los cuales se ha comprobado su efecto gastroprotector, antisecretor, antiinflamatorio, inhibidor de la migración de células inflamatorias y actividad antirradicalaria (20-22).
En el estudio fitoquímico realizado al extracto hidroalcohólico liofilizado de hojas de Bixa orellana (tabla 1), se comprobó la presencia de diversos metabolitos secundarios, expresados de manera semicuantitativa. Sin embargo, un estudio realizado a un extracto acuoso atomizado de Bixa orellana mostró una diferencia, la ausencia de alcaloides (1); esto sugiere que el tipo de solvente utilizado para la extracción determina la composición del extracto y con ello los resultados de los efectos biológico y toxicológico.
Shilpi y col. (21) han estudiado el efecto del extracto metabólico, semejante al nuestro, sobre la función neurofarmacológica del aparato digestivo en ratones, encontrando una reducción de la motilidad intestinal. También, han demostrado actividad antioxidante, fundamento de la protección contra la acción de radicales libres producidos por el alcohol, el cual genera inflamación, necrosis e inducción de apoptosis (17). Nosotros, en una publicación anterior, también hemos observado actividad gastroprotectora del extracto, mediante estimulación de la secreción de la glándula gástrica (16).
Se ha comprobado que muchos de estos compuestos tienen acción protectora de la mucosa gástrica (23,24), como es el caso de los flavonoides, tales como quercetina y rutina (25), los cuales son considerados protectores celulares contra los rayos ultravioleta, virus, hongos, entre otros. A la vez, se conoce su actividad como atrapadores de radicales libres y antioxidante. También, se ha demostrado que con el tratamiento de una fracción enriquecida de flavonoides (26) se induce un incremento en la producción de prostaglandinas (27) y somastostatina y la reducción de gastrina, que son algunos de los mecanismos de defensa de la mucosa gástrica, en ratas sin sometimiento a lesión (25).
En el trabajo de investigación de Li (1) se comprobó las propiedades cicatrizante y antiinflamatoria del extracto acuoso atomizado de hojas Bixa orellana, por aplicación local en animales de experimentación, lo que indicaría que en su composición química posee metabolitos secundarios a los que se les atribuyen dichas propiedades regenerativas de tejidos, metabolitos que serían los que nosotros hemos encontrado en el extracto.
En el presente estudio se observó que la administración vía orogástrica del extracto a las diferentes dosis ensayadas (200 y 400 mg/kg) ejerce un efecto inhibitorio en la formación de lesiones gástricas (tabla 2) causadas por la injuria del etanol al 96%, siendo el efecto dosis dependiente, semejante al estudio de Shilpi (21).
Existen trabajos realizados con extractos de otras especies, a las que se les atribuye la propiedad antiulcerosa. El extracto etanólico de hojas de Bidens pilosa L (24) vía orogástrica alcanzó el máximo efecto protector a la dosis de 2 000 mg/kg, utilizando etanol al 75% como sustancia de irritante, con respecto a los diferentes extractos de Byrsonima crassa (20). Se observó inhibición de lesiones en los diferentes extractos, metanol, metanol 80% y cloroformo, a las dosis de 500 y 1 000 mg/kg, siendo el extracto clorofórmico el que alcanzó el grado más bajo de inhibición; en todos ellos se utilizó como agente irritante una solución de etanol con HCl. En el extracto acuoso de Quassia amara (24) se observa que en dosis superiores de 500 mg/kg alcanza un grado de protección significativa frente al etanol 75%. Todos estos estudios, al igual que el de Solanum variabile (24), demostraron ser efectivos como antiulcerosos en modelos experimentales de lesión gástrica inducida por indometacina, etanol, etanol–HCl y estrés por inmovilización en frío. La actividad antisecretora se estudió según el modelo de la ligadura pilórica. Sin embargo, hay que resaltar que estas investigaciones se llevaron a cabo a dosis muy altas, en comparación con las trabajadas en el presente estudio.
La ranitidina, a dosis de 100 mg/kg, fármaco utilizado en el tratamiento de las úlceras, no demostró ser efectivo frente a la formación de lesiones gástricas producida por el etanol al 96%; este resultado también ha sido encontrado por otros autores (27,28).
En la patogenia del proceso inflamatorio existe la adherencia de neutrófilos y monocitos, inducida por agente quimiotáxicos, lo que implica la desgranulación y causaría un aumento notable de la captación de O2 y, como consecuencia, el incremento de aniones superóxidos (O2) y peróxido de hidrógeno (H2O2) (29-31). También, habría liberación de diversos productos secretores contenidos en los granulocitos, que incluyen diversas proteasas, como las catepsinas, elastasas y colagenasas. A todo ello se sumaría la liberación de numerosos mediadores proinflamatorios (IL-1, la IL-6, prostaglandinas y los leucotrienos), que atraerían a más células proinflamatorias a la zona lesionada, lo que ahondaría más el daño tisular. La producción de especies reactivas de oxígenos (ROS) incrementadas por el proceso inflamatorio debe ser neutralizada para no causar más daño tisular.
La presencia de metabolitos secundarios con propiedad antioxidante en el extracto actuaría como atrapador de radicales libres (32); entre ellos tenemos a la quercetina, taninos y carotenoides, como la bixina y la norbixina presentes en Bixa orellana (3); podemos suponer que dichas sustancias pueden atenuar el efecto nocivo que acarrea todo proceso inflamatorio sobre el tejido.
En un estudio realizado sobre el efecto antiulceroso de una fracción enriquecida de flavonoides del extracto Alchornea castaneaefolia (26) se observó un incremento en los niveles de prostaglandinas, siendo la quercetina el flavonoide más predominante en dicha fracción enriquecida, que a su vez se encuentra presente en el achiote (3).
Según los resultados del estudio histopatológico, se observó que a la dosis de 200 mg/kg de peso del extracto existió una discreta infiltración de células inflamatorias en la región submucosa, en comparación al grupo que recibió la ranitidina, en donde se evidenció una mayor presencia de estas células en la región submucosa y muscular; y a la dosis de 400 mg/kg se observó en algunas láminas la presencia de hipertrofia glandular, lo que significaría un cierto grado de regeneración tisular.
Por todo lo antes mencionado, el presente trabajo de investigación se ha realizado siguiendo un modelo de evaluación farmacológica para plantas de acción antiulcerosa, aportando un mayor conocimiento científico de su efecto gastroprotector.
Bajo las condiciones trabajadas se puede concluir que el tratamiento con extracto hidroalcohólico de hojas de Bixa orellana vía orogástrica inhibe las lesiones inducidas por etanol al 96% e induce a una menor migración de células proinflamtorias; los componentes del extracto hidroalcohólico estarían comprometidos sobre dicho efecto.
REFERENCIAS BIBLIOGRÁFICAS
1. Li FE. Actividad biológica del extracto acuoso atomizado de hojas de Bixa orellana L. (Achiote) en animales de experimentación. Tesis de Maestría. Facultad de Medicina, Universidad Nacional mayor de San Marcos. Lima, Perú. 1999. [ Links ]
2. Alvarado D, Beltrán C, Gutiérrez K, Lobaton M, Monzón S, Rosadio L, Huamán O. Efecto protector de los diferentes extractos de las hojas de Bixa orellana en hígados de ratones sometidos a estrés. An Fac med. 2004;65:62. [ Links ]
3. Juárez S. Caracterização, extração e purificação por cromatografia de compostos de urucum (Bixa orellana L.). Tesis de Maestría. Universidade Federal de Santa Catarina. Florianópolis, Brasil. 2005. [ Links ]
4. Juscafresa B. Enciclopedia Ilustrada. Flora medicinal, toxica, aromática, condimenticia. Barcelona: Aedos; 1940. [ Links ]
5. Mandfred L. Siete mil recetas botánicas a base de mil trescientas plantas medicinales. 11° Ed. Buenos Aires: Kier S.A.; 1977.
6. García-Barriga, H. Flora medicinal de Colombia. Botánica Médica. Tomo II. Instituto de Ciencias Naturales, Universidad Nacional de Colombia. Bogota: Talleres Editoriales de la Imprenta Nacional; 1975.
7. Placencia M. Evaluación Farmacológica de la Buddleia globosa (matico) en el tratamiento de úlcera gástrica inducida en animales de experimentación. Tesis de Maestría. Facultad de Medicina, Universidad Nacional mayor de San Marcos. Lima, Perú. 2001. [ Links ]
8. Placencia M. Actividad antiulcerosa del extracto de Piper angustifolium en animales de experimentación. Lima: CONCYTEC; 1997. [ Links ]
9. Arroyo A. Actividad antiulcerosa de Piper angustifolium (matico). Tesis de Doctor. Facultad de Medicina, Universidad Nacional mayor de San Marcos. Lima, Perú. 1998. [ Links ]
10. Ayala S, Díaz D, Palomino M, Armas S, Paz J. Efecto protector de Croton palanostigma y Aloe vera frente a la injuria aguda de mucosa gástrica inducida por etanol en ratas. An Fac med. 1999;60(1):22-9. [ Links ]
11. Bobadilla J, Vargas F, Gómez A, Villalobos J. Frecuencia de la úlcera péptica en el Instituto Nacional de la Nutrición Salvador Zubirán. Rev Gastroenterol Méx. 1996;61(1):31-5. [ Links ]
12. Wilson JD, Braunwald E, Isselbacher KJ, Petersdorf RG, Martin JB, Fauci AS, Root RK, editores. Harrissons Principios de medicina interna. 12da ed. Nueva York: McGraw-Hill Inc; 1991.
13. Lopez-Brea M. Helicobacter pylori: microbiología, clínica y tratamiento. 1° Ed. Barcelona: Mosby Doyma Libros; 1995.
14. Huamán O, Arnao I, Béjar E, Sandoval M. Efecto del extracto hidroalcohólico liofilizado de hojas de Bixa orellana (achiote), en la secreción gástrica de ratas. An Fac med. 2007;68(4):314-20. [ Links ]
15. Lock O. Investigación fotoquímica: métodos en los estudios de productos naturales. 1° ed. Lima: Fondo editorial Lima; 1988.
16. Robert A, Nezamis RA, Lancaster JE, Hanchar AJ. Cytoprotection by prostaglandins in rats. Prevention of gastric necrosis produced by alcohol, HCl, NaOH, hypertonic NaCl and thermal injury. Gastroenterol. 1979;77:433-43.
17. Areguesta-Robles U, Hernández-Ruiz E, Juárez M, Rendón-Ramírez A. Lipoperoxidación y alcoholismo en jóvenes. Bioquimia. 2004;29(Supl 1):125. [ Links ]
18. Marhuenda RE, Bravo DL. Manual de Farmacoterapia. Madrid: Elsevier; 2005. p. 729. [ Links ]
19. Pardo CA. Animal experimentation ethics. Contemporary legal and ethical rules. Cuad Bioét. 2005;XVI(3):393-417. Disponible en: http://www.aebioetica.org/rtf/08-BIOETICA-58.pdf
20. Villar del Fresno AM. Farmacología General. Madrid: Síntesis; 1999. [ Links ]
21. Shilpi JA, Taufiq-Ur-Rahman M, Uddin SJ, Alam MS, Sadhu SK, Seidel VJ. Preliminary pharmacological screening of Bixa orellana L. leaves. J Ethnopharmacol. 2006;108(2):264-71. [ Links ]
22. Sannomiya M, Fonseca V, Da Silva M, Rocha L, Dos Santos L, Hiruma-Lima C, et al. Flavonoids and antiulcerogenic activity from Birsonia crassa leaves extracts. J Ethnophatmacol. 2005;97:1-6. [ Links ]
23. CYTED. Manual de técnicas de investigación. Madrid: Cyted; 1995.
24. Hiruma-Lima CA, Calvo T, Rodriguez C, Pezzuto F, Vilegas W, Sousa Brito A. Antiulcerogenic activitiy of Alchornea castaneafolea: effects on somastostatin, gastrin and prostaglandin. J Ethnopharmacol. 2006;104:215-24. [ Links ]
25. Beil W, irkhoiiz C, Sewing K. Effectos of flavonoide on parietal cell acid secretion, gastric mucosal prostaglandin production and Helicobarter pylori growth. Arzneimittelforrschung. 1995;(6):697-700. [ Links ]
26. Tarnawski A, Hollander D, Stachura J, Krause WJ. Arachidonic acid protection of gastric mucosa against alchol injury: sequential analysis of morphogic and funtional changes. J Lab Clin Med. 1983;102(3)340-51.
27. Álvarez A, Montero M, Pomar F, Sánchez E. Actividad antiulcerosa de un extracto etanólico de Bidens pilosa L. var. radiata Schult. en ratas. Rev Cubana Plant med. 1998;3(3):12-7. [ Links ]
28. Badilla B, Miranda T, Mora G, Vargas K. Actividad gastrointestinal del extracto acuoso bruto de Quassia amara (simarubaceae). Rev Biol trop. 1998;46(2):203-10. [ Links ]
29. Antonio JM, Gracioso JS, Toma W, Lopez LC, Oliveira F, Sousa Brito A. Antiulcerogenic activity of athanol extract of Solanum variabile (false jurubeba) J Ethnopharmacol. 2004;93:83-8. [ Links ]
30. Venereo J. Daño oxidativo, radicales libres y antioxidantes. Rev Cubana Med Milit. 2002;31(2):126-33. [ Links ]
31. Domínguez X. Métodos de Investigación fitoquímica. México: Limusa S.A.; 1985.
32. Martinez-Flórez S, González-Gallegos J, Culebras J, Tuñón M. Los flavonoides: propiedades y acción antioxidantes. Nutr Hosp. 2002;XVII(6):271-8.
Manuscrito recibido el 8 de mayo de 2009 y aceptado para publicación el 2 de junio de 2009.
Correspondencia:
Mg. Oscar Gustavo Huamán-Gutiérrez
Centro de Investigación de Bioquímica y Nutrición
Facultad de Medicina - UNMSM
Av. Grau 755. Lima 1, Perú
Correo-e: oscarhuaman@hotmail.com














