Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Medicina
versión impresa ISSN 1025-5583
An. Fac. med. v.71 n.2 Lima abr./jun. 2010
CASOS CLÍNICOS
Trombocitopenia asociada a rifampicina en régimen antituberculoso diario
Rifampicin induced thrombocytopenia in daily antituberculous regimen treatment
Victor Mechan1,2 ; Wuili Valqui3 ; Luis Vilchez3 ; José Castro3 ; Fiorella Lipari4
1 Servicio de Hematología, Hospital Nacional Dos de Mayo. Lima, Perú.
2 Facultad de Medicina, Universidad Nacional Mayor de San Marcos. Lima, Perú.
3 Servicio de Medicina Interna, Hospital Nacional Dos de Mayo. Lima, Perú.
4 Interna de la Facultad de Medicina, Universidad de San Martín de Porres. Lima-Perú.
Resumen
Presentamos el caso de un varón de 31 años con diagnóstico de tuberculosis pulmonar por radiografía de torax compatible y examen bacilo ácido alcohol resistente, positivo en esputo, quien 10 días después de iniciar tratamiento oral con isoniazida, etambutol, pirazinamida y rifampicina (RFP), desarrolla un síndrome hemorrágico asociado a trombocitopenia severa (2 000/mL) y paresia leve de hemicuerpo derecho. El paciente normalizó el número de plaquetas y su función motora cinco días después del retiro de los cuatro medicamentos antituberculosos. Al decidirse re-exponer al paciente en forma secuencial a las cuatro drogas, se observó que 12 horas después de haber ingerido RFP oral, desarrolla nuevamente trombocitopenia severa, lo que no ocurrió con las otras tres drogas. Las plaquetas alcanzaron niveles normales 36 horas después del retiro de la RFP. El reemplazo ulterior de RFP por estreptomicina permitió completar exitosamente el tratamiento antituberculoso. El presente caso demuestra un efecto adverso poco frecuente, producido por un fármaco antituberculoso de primera línea, el mismo que debe considerarse como muy grave y cuyo manejo debe incluir la inmediata e indefinida suspensión de la droga en el paciente afectado, a causa de la alta probabilidad de tener la misma respuesta a lo largo de su vida.
Palabras clave: Trombocitopenia; rifampicina; tuberculosis pulmonar; efectos de drogas.
Abstract
We present the case of a 31 year-old patient with the diagnosis of lung tuberculosis by lung X-ray and positive acid alcohol resistant bacillus in sputum, who after 10 days of oral treatment with isoniazid, ethambutol, pyrazinamide and rifampicin (RFP), developed severe hemorrhagic manifestations associated with severe thrombocytopenia (2 000/mL) and slight right body hemiparesis. There was complete normalization of platelet count and motor function five days after suspension of the four drugs. We decided to re-expose the patient sequentially to the four drugs and after 12 hours of receiving RFP again developed severe thrombocytopenia (2 000/mL) not occurring with the other three drugs, and normalized completely after 36 hours of drug suspension. Later on, the addition of parenteral streptomycin successfully completed the treatment. The current case demonstrates a not very frequent adverse effect of a first line drug for the treatment of tuberculosis, which should be considered as a very serious complication and whose management should include the immediate and indefinite suspension of the drug in the affected patient, because of the high likelihood of having the same response every time he is challenged during his life.
Key words: Thrombocytopenia; rifampin; tuberculosis, pulmonary; drug effects.
INTRODUCCIÓN
El Programa Nacional de Control de la Tuberculosis (PNCT) en el Perú, entre 1991 y 2000, registró 474 834 casos de tuberculosis (TBC) (1). De ellos, 5 079 pacientes desarrollaron reacción adversa a medicamentos antituberculosos (RAM), en promedio 1,3%. De estos últimos, 35 casos fueron notificados como RAM a rifampicina (RFP) los cuales fueron mayormente reacciones de hipersensibilidad en piel y gastritis, resultando un caso de RAM a RFP por cada 13 560 pacientes tratados. El PNCT no determinó trombocitopenias inducidas por RFP, por imprecisiones en su identificación y a que es posible confundirla con púrpura tombocitopénica inmune, sepsis y otros (2). Es probable, asimismo, la existencia de subregistros de trombocitopenias inducidas por RFP y otros medicamentos antituberculosos (3,4), habida cuenta de comparaciones con datos de otros países (5). El presente estudio intenta proporcionar un modelo de diagnóstico y manejo de trombocitopenias inducidas por RFP.
CASO CLÍNICO
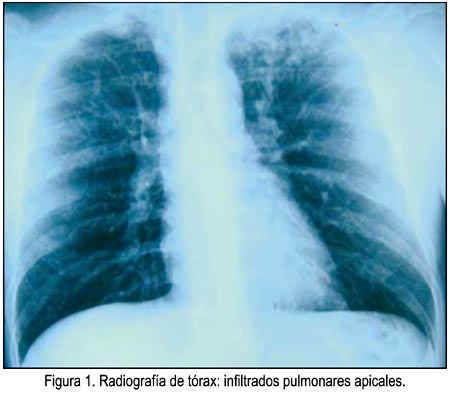
Varón de 31 años, soltero, vendedor de baratijas, quien 45 días antes de su ingreso presentó tos, fiebre y malestar general. Acudió a un centro de salud primario, donde le diagnosticaron tuberculosis pulmonar (radiografía de tórax (figura) patológica y bacilo ácido alcohol resistente (BAAR) en esputo positivo), iniciándose, 13 días antes de su ingreso a nuestro hospital, tratamiento con: isoniazida (INH) (300 mg), pirazinamida (PZN) (1 200 mg), etambutol (ETB) (1 500 mg) y RFP (600 mg/día). Después de 10 días de iniciado el tratamiento, presentó súbitamente epistaxis, petequias generalizadas, sangrado de encías y coágulos sanguíneos en cavidad oral. Conducido a Emergencia del Hospital Nacional Dos de Mayo (HNDM, 18/04/09) refirió durante el interrogatorio: cefalea y dificultad para movilizar el hemicuerpo derecho, de un día de evolución.
Tuvo tuberculosis pulmonar a los 12 años de edad, tratada con éxito durante 6 meses, con esquema 2HRZE/4H2R2 (H: isoniazida, R: rifampicina, Z: pirazinamida, E: etambutol). Tratado exitosamente de gonorrea, a los 20 años, fue operado del tabique nasal, hace 2 años. Al examen físico, se encontró paciente en mal estado general, aunque lúcido, orientado en tiempo espacio y persona. Se evidenció petequias generalizadas y coágulos sanguíneos en cavidad oral, peso 61 kg, talla 1,62 m, presión arterial 100/60, pulso 80, respiraciones 20/min. El examen neurológico reveló discreta paresia y disminución de la sensibilidad del hemicuerpo derecho. Con excepción de respiración ruda pulmonar bilateral a la auscultación, el resto del examen físico fue normal.
Ante la sospecha de sangrado intracerebral por trombocitopenia inducida por medicamentos, se retiró los cuatro antituberculostáticos, administrándose 4 mg de dexametasona parenteral; 24 h después, el paciente recuperó totalmente la función de su hemicuerpo derecho, ascendiendo el número de plaquetas, las mismas que se normalizaron 5 días después. Por razones imponderables, no hubo una planificada desensibilización con dosis iniciales reducidas de antituberculostáticos, iniciándose la reexposición a fármacos antuberculosos a partir del sexto día de su hospitalización, con 300 mg de INH. Al no evidenciarse reacciones adversas, el paciente fue ingiriendo aditivamente (cada 24 h) los restantes medicamentos antituberculosos (1). El décimo día de su hospitalización, ingirió 600 mg de RFP, evidenciándose 12 h después un nuevo descenso del nivel de plaquetas (2 000/mL) presentando petequias generalizadas, aunque sin sangrado activo; se hizo el diagnóstico de trombocitopenia inducida por RFP. En el nuevo esquema de tratamiento del paciente, la RFP fue reemplazada con éxito por estreptomicina parenteral, ya que los reportes de trombocitopenia inducida por este medicamento (6,7) son muy escasos.
Otros análisis el 18/04/09, fueron glucosa: 123 mg/100 mL (N: 70-110), proteínas totales: 7,3 g/dL, globulinas: 3,81 g/dL, orina con leucocitos 0-2 por campo y hematíes 6-8, fosfatasa alcalina 71 U/L (N: 38-126), transaminasa glutámico oxalacetica: 31 U/L (N: 17-52), transaminasa glutámico-pirúvica: 27 U/L (17-56), BAAR en esputo negativo en tres oportunidades, urea 20,5 mg/dL (N: 20-40), creatinina 0,8 mg/dL (0,5-1), grupo sanguíneo 0, factor Rh positivo, radiografía de tórax mostró hilios engrosados, infiltrados en vértices pulmonares. La ecografia abdominal sugirió esplenomegalia leve. El 23/04/09, la orina fue normal; el 29/04/09, la prueba reagin protein reactive fue negativa, aglutinaciones a brucella no reactivas, antígeno de hepatitis de superficie (HBsAg) no reactivo, virus de la inmunodeficiencia humana (VIH, método Elisa) no reactivo (05/05/09), prueba de Coombs directa negativa.
DISCUSIÓN
La trombocitopenia inducida por RFP en este paciente puede ser establecida utilizando los cuatro criterios de George JN (8), de relación causa-efecto definida entre empleo de un fármaco e inducción de trombocitopenia. Estos criterios no requieren la presencia de anticuerpos antiplaquetarios (no realizados en nuestro paciente), toda vez que la sensibilidad de estos oscila entre 49 y 66% (9). Los criterios aplicados a nuestro paciente fueron: a) La RFP fue administrada en los 10 días previos (6,10); b) Las plaquetas ascendieron, alcanzando niveles normales 36 horas después de retirar la RFP; c) La trombocitopenia reapareció 12 horas después de reexposición a RFP (11); d) Se excluyó otras causas de trombocitopenia.
Blachjman (12) comunicó el primer caso de trombocitopenia inducida por RFP, con presencia de anticuerpos fijadores del complemento. Posteriormente, Poole y col (13) demostraron que 6% de pacientes que recibía dosis altas de RFP (900 a 1 200 mg/día), en regímenes intermitentes, desarrollaban RAM, incluyendo trombocitopenia, aún en ausencia de anticuerpos específicos contra RFP. Por ello, los regímenes actuales que incluyen RFP evitan sobrepasar la barrera de los 600 mg. Cuando el paciente fue tratado por primera vez de TBC pulmonar, en 1991, recibió en los últimos cuatro meses un régimen intermitente de RFP (2 veces por semana). Según Hadfield (10), las trombocitopenias por RFP son más frecuentes con regímenes intermitentes, ya que durante los lapsos sin RFP se generan anticuerpos antiplaquetarios sin neutralizar. Contrariamente, en los regímenes diarios se generan mecanismos neutralizadores o de remoción de anticuerpos, siendo esta la razón por las que las trombocitopenias inducidas por regímenes diarios de RFP son extremadamente raras (13) y, cuando ocurren, casi siempre revelan exposición previa a RFP, como ocurrió en este caso. Los anticuerpos una vez formados permanecen viables muchos años, reteniendo su potencial de inducción de trombocitopenias, si el paciente es sometido a nuevos regímenes diarios o a reexposiciones únicas (14,15).
Aunque no es posible descartar totalmente el rol inductor de trombocitopenias de los otros medicamentos -PZN, ETB y/o INH, en ese orden (7,16)-, existen comunicaciones indicando que tras el retiro de la RFP -luego de una reexposición- el ascenso de las plaquetas ocurre 3 horas después, como sucedió en este caso (7,17). No existe reacción cruzada entre estos medicamentos, siendo la reacción altamente específica (6,18). Se ha demostrado que la RFP actúa como hapteno (inductor de anticuerpos contra plaquetas normales), uniéndose covalentemente a una proteína transportadora (carrier) de membrana, generando anticuerpos específicos contra plaquetas normales, solo en presencia de RFP (8). En trombocitopenias inducidas por RFP, se ha demostrado la presencia de anticuerpos dirigidos contra un set restringido de neoepítopes Ib/IIIa y complejo Ib/V/IX, glicoproteicos plaquetarios, a los cuales se une covalentemente la RFP (19).
Un hecho ocurrido en este paciente, encontrado constantemente en la literatura (2), es la ocurrencia de hemorragias intracerebrales asociadas a niveles de plaquetas de 20 000/mL o menos. Aunque el paciente desarrolló paresia de hemicuerpo derecho, la rápida suspensión de los medicamentos antituberculosos y otras medidas de soporte abortaron un accidente cerebrovascular de mayor magnitud. Las trombocitopenias inducidas por medicamentos, y en este caso por RFP, son verdaderas emergencias. El plan de trabajo debe incluir: a) retiro de antituberculostáticos y adición de esteroides (2), de conjunto con transfusiones de plaquetas, plasmaféresis y globulinas inmunes, cuando los niveles plaquetarios estén en 20 000/mL o menos; y b) en tanto los anticuerpos antiplaquetarios generados son permanentes, prohibir la ingesta de RFP, de por vida.
REFERENCIAS BIBLIOGRÁFICAS
1. Bonilla C, Suarez PG, Portocarrero J, Gutarra K. Patrón de presentación de reacciones adversas a fármacos antituberculosos en tratamientos directamente observados. Perú.1991-2000. En: Ministerio de Salud. Tuberculosis en el Perú. Informe 2000. Lima: Minsa; 2000. p. 107-20.
2. Aster RH, Bougie DW. Drug-induced immune thrombocytopenia. NEJM. 2007;357:580-7.
3. Rabinovitz M, Pitlik SD, Halevy J, Rosenfeld JB.
Ethambutol induced thrombocytopenia. Chest. 1982;81:765-6.4. Jain VK, Vardhar H, Prakash OM. Pyrazinamide induced thrombocytopenia. Tubercle. 1988;69(3):217-8.
5. Yee D, Valiquette C, Pelletier M, Parisien I, Rocher I, Menzies D. Incidence of serious side effects from first-line antituberculosis drugs among patients treated for active tuberculosis. Am J Respir Crit Care Med. 2003;167:1472-7.
6. Rodriguez DC, Ramirez JH, Pacheco VH, Salazar LE, Casalino E, Lizarzaburu L, Kemper R. Efectos adversos de consecuencia fatal por tratamiento con fármacos antituberculosos. Rev Med Hered. 2002;13(4):148-52.
7. Lee CH, Lee CJ. Rifampicin side effect of initial daily and interrupted use of thrombocytopenia. Chest. 1989;96;202-3.
8. George JN, Raskob GE, Shah SR, Rizvi MA, Hamilton SA, Osborne S, Vondracek T. Drug-induced thrombocytopenia :a systematic review of published cases. Ann Intern Med. 1988;129(11 Pt 1):886-90.
9. Ferguson GC. Rifampicin and thrombocytopenia. BMJ. 1971;3:638.
10. Hadfield JW. Rifampicin-induced thrombocytopenia. Postgrad Med J. 1980;56(651):59-60.
11. Onoda T, Murakami K, Eda R, Hiraki A, Makihata K, Takao K, et al. Rifampicin-induced severe thrombocytopenia in a patient with miliary tuberculosis. Tuberculosis (Kekkaku). 2003;78(7):491-6.
12. Blachjman MA, Lowry RC, Pettit JE, Stradling P. Rifampicin–induced immune thrombocytopenia. BMJ. 1970;3:24-6.
13. Poole G, Stradling P, Worlledge S. Potentially serious side effects of high dose twice weekly rifampicin. BMJ. 1971;3:343-7.
14. Cherylann UZ, Lawande D, Bagga AS.
Rifampicin induced thrombocytopenia. Ind J Tub.1995;42:173.15. Mehta YS, Jijina FF, Badakere SS, Pathare AV, Mohanty D. Rifampicin induced thrombocytopenia. Tubercle and Lung Disease. 1996;77:558-62.
16. Garg R, Gupta V, Mehra S, Singh R, Prasad R. Rifampicin- induced thrombocytopenia. Indian J Tuberc. 2007;54:94-6.
17. Sande MA, Mandell GL. The aminoglycosides antimicrobial agents. En: Goodman LS, Gilman AG, Rail TW (editors). The Pharmacological Basis of Therapeutics, Seventh Ed. New York: MacMillan Publishing Co.; 1985. p. 1150.
18. Arrizabalaga J, Casas A, Camino X, Iribarren JA, Rodríguez Arrondo F, Von Wichmann MA. Utilidad de la desensibilización a rifampicina en el tratamiento de enfermedades producidas por micobacterias en pacientes con sida. Med Clin (Barc). 1988:111:103-4.
19. Pereira J, Hidalgo P, Ocqueteau M, Blacutt M, Marchesse M, Nien Y, et al.
Glycoprotein Ib/IX complex is the target in rifampicin-induced immune thrombocytopenia. Brit J Haematol. 2000;110(4):907-10.
Manuscrito recibido el 25 de marzo de 2010 y aceptado para publicación el 10 de junio de 2010.
Correspondencia:
Victor Mechán Méndez
Departamento de Medicina, Hospital Dos de Mayo.
Parque de la Medicina s/n. Barrios Altos.
Lima 1, Perú.
Correo-e: victor.mechan@gmail.com














