Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Medicina
versión impresa ISSN 1025-5583
An. Fac. med. v.73 n.2 Lima abr./jun. 2012
ARTÍCULOS ORIGINALES
Prevalencia del síndrome metabólico en pobladores peruanos por debajo de 1 000 y por encima de los 3 000 msnm
Metabolic syndrome prevalence in Peruvians living below 1 000 and over 3 000 meters
Jaime Pajuelo1,2, José Sánchez-Abanto3, Harold L. Torres2, Marianella Miranda3
1 Instituto de Investigaciones Clínicas. Facultad de Medicina UNMSM.
2 Servicio de Endocrinología del Hospital Nacional Dos de Mayo.
3 Centro Nacional de Alimentación y Nutrición. Instituto Nacional de Salud. Ministerio de Salud.
Resumen
Objetivos: Determinar y comparar la prevalencia del síndrome metabólico y de sus diferentes componentes en población adulta peruana que habita por debajo de 1 000 y por encima de 3 000 msnm. Diseño: Análisis de los datos de la Encuesta Nacional de Indicadores Nutricionales, Bioquímicos, Socioeconómicos y Culturales Relacionados a las Enfermedades Crónicas Degenerativas 2006. Institución: Instituto Nacional de Salud Centro Nacional de Alimentación y Nutrición, Ministerio de Salud, Lima, Perú. Participantes: Personas mayores de 20 años. Métodos: Se incluyó 3 384 personas mayores de 20 años, 2 425 que habitaban por debajo de 1 000 (nivel-I) y 959 por encima de los 3 000 msnm (nivel-II). El síndrome metabólico fue definido de acuerdo a los criterios del National Cholesterol Education Program Adult Treatment Panel III (NCEP ATP III). Principales medidas de resultados: Prevalencia del síndrome metabólico y sus componentes. Resultados: La prevalencia de síndrome metabólico fue significativamente mayor en el nivel-I (19,7%) que en el nivel-II (10,2%), p<0,001. En varones, la prevalencia fue 9,2% en el nivel-I y 5,1% en el nivel-II. En mujeres fue 29,9% en el nivel-I comparado con 15,2% en el nivel-II. La obesidad central (35,5% vs. 21,1%), elevación de presión arterial (20,9% vs. 15,0%), hiperglicemia (3,9% vs. 1,7%), hipertrigliceridemia (31,3% vs. 25,7%) y concentraciones bajas de HDLc (57,4% vs. 52,5%) fueron significativamente más prevalentes en el nivel-I comparado con el nivel-II (p<0,05). Los componentes del síndrome metabólico más frecuentes en los varones fueron la hipertrigliceridemia y el HDLc bajo, mientras que en las mujeres fueron la obesidad central y el HDLc disminuido. Conclusiones: El síndrome metabólico fue significativamente más prevalente en la población por debajo de los 1 000 msnm; esto podría ser resultado de la transición nutricional, demográfica y socioeconómica en esta área. Las mujeres fueron más susceptibles a los factores de riesgo cardiovascular.
Palabras clave: Enfermedades metabólicas, obesidad, hipertensión, hiperglucemia, hipertrigliceridemia, colesterol, altitud.
Abstract
Objectives: To determine and compare the prevalence of metabolic syndrome and its components in Peruvian population living below 1000 m and over 3000 m. Design: Data analysis of Encuesta Nacional de Indicadores Nutricionales, Bioquimicos, Socioeconomicos y Culturales Relacionados a las Enfermedades Cronicas Degenerativas 2006. Setting: Instituto Nacional de Salud Centro Nacional de Alimentacion y Nutricion, Ministerio de Salud, Lima, Perú. Participants: Subjects 20 year-old and above. Methods: We included 3384 participants aged 20 year-old and above, 2425 living below 1000 m (level-1) and 959 over 3000 m (level-2). Metabolic syndrome was defined according to the National Cholesterol Education Program Adult Treatment Panel III (NCEP ATP III) criteria. Main outcome measures: Metabolic syndrome and components prevalence. Results: Prevalence of metabolic syndrome was significantly higher in level-1 (19.7%) than in level-2 (10.2%), p<0.001. Prevalence in males was 9.2% in level-1 and 5.1% in level-2, and in females 29.9% in level-1 compared to 15.2% in level-2. Central obesity (35.5% vs. 21.1%), elevated blood pressure (20.9% vs. 15.0%), hyperglycemia (3.9% vs. 1.7%), raised triglycerides (31.3% vs. 25.7%), and low concentrations of HDLc (57.4% vs. 52.5%) were significantly more prevalent in level-1 compared to level-2 (p<0.05). The most frequent components of metabolic syndrome in men were hypertriglyceridemia and low HDLc, and in women were low HDLc and central obesity. Conclusions: Metabolic syndrome was significantly more prevalent in population under 1000 m; it may be as result of the nutritional, demographic, and socioeconomic transition in this area. Women were more susceptible to cardiovascular risk factors.
Key words: Metabolic diseases, obesity, hypertension, hyperglycemia, hypertriglyceridemia, cholesterol, altitude.
INTRODUCCIÓN
El proceso de globalización ha traído, a los países desarrollados y en vías de desarrollo, una serie de enfermedades llamadas emergentes, como la obesidad, hipertensión arterial, dislipidemias y diabetes mellitus tipo 2.
Las elevadas prevalencias de obesidad en adultos han sido acompañadas por incremento en la ocurrencia de condiciones metabólicas asociadas, conocidas como síndrome metabólico (SM)(1). Este síndrome es descripto como una constelación de anormalidades metabólicas que incluyen obesidad abdominal, dislipidemia, intolerancia a los hidratos de carbono y elevada presión arterial, que representan mayores factores de riesgo de enfermedades cardiovasculares (2). Los adultos con este síndrome tienen un riesgo significativamente incrementado de desarrollar diabetes mellitus tipo 2 y morbimortalidad relacionada a los accidentes cerebro vasculares (3).
Steinberg menciona que el SM emerge de una serie de interacciones entre anormalidades vasculares, estrés oxidativo, grasa visceral, inflamación, adipocitoquinas y cortisol, como parte de un entorno dado por la obesidad y la resistencia a la insulina, bajo la influencia de una predisposición genética y étnica (4).
En el Perú, se ha comunicado que 16,8% de adultos presentan SM, siendo más prevalente en Lima Metropolitana (20,7%) y menos en la Sierra Rural (11,1%) (5). Pocos son los estudios realizados en poblaciones de altura. Mena, en el Cusco, encontró 6% en población urbana y 0,8% en rural (6); Gamarra, en la misma ciudad, 16,5% en población femenina (7); Baracco, en San Pedro de Cajas, 11,1% en varones y 31,7% en mujeres (8); Díaz Lazo, en Huancayo, 10,2% en personas con un índice de masa corporal normal (20 a 24,9 kg/m2), 42,4% en quienes tenían sobrepeso (IMC 25 a 29,9 kg/m2) y 66,7% en obesos (IMC de 30 kg/m2 y más) (9); Medina, en Arequipa, 14,3% en varones y 23,2% en mujeres (10). En todos los estudios, a excepción de este último, el diagnóstico de SM fue realizado usando los criterios del National Cholesterol Education Program (NCEP), Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) (11).
El estudio de Baracco (8) es el único que ha comparado una población a nivel del mar (Rímac, un distrito de Lima) frente a un distrito llamado San Pedro de Cajas, que está ubicado a 4 100 msnm. Sus resultados mostraron una mayor prevalencia en la población de altura, 24,2% vs. 22,1%, pero esta diferencia no presentó significación estadística (p = 0,28).
El objetivo del presente estudio es determinar y comparar la prevalencia del síndrome metabólico y de sus diferentes componentes en adultos peruanos que habitan por debajo de 1 000 (nivel-I) y por encima de 3 000 msnm (nivel-II).
MÉTODOS
Se realizó un análisis de los datos de la Encuesta Nacional de Indicadores Nutricionales, Bioquímicos, Socioeconómicos y Culturales Relacionados a las Enfermedades Crónicas Degenerativas (ENIN BSC), llevada a cabo por el Instituto Nacional de Salud Centro Nacional de Alimentación y Nutrición (CENAN) del Ministerio de Salud, durante los años 2004 a 2005 (12). La ENIN BSC fue una encuesta descriptiva, transversal, con muestreo multietápico, teniendo como universo a personas, hombres y mujeres, mayores o igual a 20 años, que en el momento de la encuesta residían en viviendas particulares ubicadas en el territorio nacional. Para los fines del estudio, se seleccionó dos grupos: el nivel-I, que incluyó personas que habitaban por debajo de los 1 000 msnm, y el nivel-II, formado por los pobladores de zonas por encima de los 3 000 msnm.
La recolección de información se llevó a cabo en dos visitas. En la primera visita, luego de la firma del consentimiento informado, se midió la tensión arterial, se aplicó los instrumentos de medición del consumo de alimentos, preguntas socioeconómicas y culturales. La segunda visita fue previamente pactada para la toma de muestras sanguíneas en ayunas y proceder luego a la toma de las mediciones antropométricas.
El tamaño muestral del ENIN-BSC fue calculado con 95% de confianza, con una tasa de no respuesta de 10% y prevalencia estimada de sobrepeso de 46% (INS-ENCA-CENAN, 2003). De ellos, 2 425 residían por debajo de los 1 000 msnm (nivel-I) y 959 por encima de los 3 000 msnm (nivel-II).
La medición del perímetro abdominal (cintura) se realizó con cinta métrica flexible, a nivel del punto medio entre el borde inferior de las costillas y la cresta iliaca, pasando por el medio centímetro más cercano al ombligo (12).
La toma de muestras sanguíneas fue en ayunas y se obtuvo mediante sistema al vacío con gel activador de la coagulación. Para la obtención del suero se utilizó centrífugas manuales Marca Handzentrifuge de 3000 RPM y crio viales que permitieron el traslado seguro y conservación de las muestras congeladas de suero y enviadas a la brevedad a Lima, al laboratorio privado donde fueron analizadas según las técnicas establecidas. Para determinar colesterol total, se usó el método enzimático (Trinder) con colorimetría; para colesterol HDL se empleó el reactivo precipitante para la separación de las lipoproteínas de densidad alta (HDL) en suero -sistema enzimático colesterol oxidasa/peroxidasa con colorimetría, según Trinder-; para determinar colesterol LDL se usó el reactivo precipitan-te para la separación de las lipoproteínas de densidad baja (LDL) en suero, con el mismo sistema enzimático anterior, sistema que también fue empleado para la determinación de triglicéridos (TG); y, finalmente, para determinar glucosa se usó el método enzimático (glucosa GOD-PAP) con colorimetría según Trinder.
La medición de la presión arterial se hizo con el tensiómetro Mac-Check-501.
El diagnóstico de SM fue realizado usando los criterios del National Cholesterol Education Program (NCEP), Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) (11). Estos criterios son: TG >= 150 mg/ dL, C-HDL en mujeres <= 50 mg/ dL y en varones <= 40 mg/dL, glucosa >= 110 mg/dL, PA 130 y/o 85 mm Hg, y obesidad abdominal definido por perímetro abdominal (PerAbd) >= 88 cm en mujeres y 102 cm en varones. La presencia de 3 o más de estos, en una persona, hacen el diagnóstico de SM.
Luego de la verificación, control de calidad y codificación de los resultados, estos fueron ingresados a una base de datos. Para el procesamiento y análisis se empleó el programa estadístico SPSS, versión 18.0 para Windows. Se calculó los promedios y desviación estándar (DE) de las variables continuas y frecuencias de las nominales. Para el análisis bivariado de las variables nominales se utilizó la prueba de chi cuadrado, y la prueba de t de Student para las variables continuas. En todo momento se consideró estadísticamente significativo un p<0,05.
RESULTADOS
El número de habitantes del nivel-I fue 2 425. De ellos, 1 216 fueron mujeres (50,1%) y 1 209 varones (49,9%). El nivel-II incluyó 959 personas, de las cuales 480 fueron mujeres (50,1%) y 479 varones (49,9%). La edad promedio fue 42,06 ± 14,9 años.
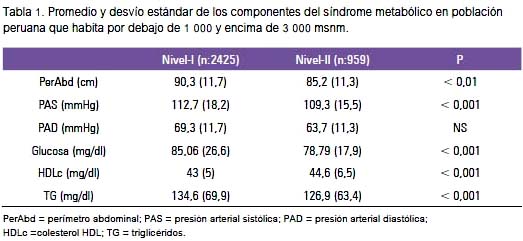
La tabla 1 presenta las medidas de tendencia central y de dispersión de las variables que intervinieron para definir el SM, según niveles de altitud. Los promedios de todas las variables fueron mayores en el nivel-I, a excepción de los valores del HDLc. Estas diferencias fueron estadísticamente significativas, salvo la presión arterial diastólica.
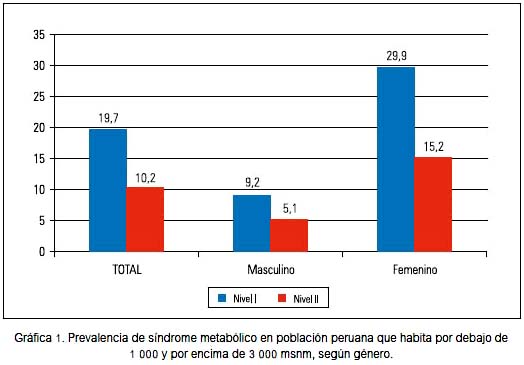
En el gráfico 1 se puede apreciar la prevalencia de SM en el total de la población estudiada y por géneros, tomando en cuenta los niveles de altitud. En lo que se refiere a la población total, la mayor prevalencia del SM se dio en el nivel-I, con 19,7% (IC95% 18,0 a 21,3%), comparado con el nivel-II con 10,2% (IC95% 8,3 a 12,1%), con un OR de 2,16 (IC95% 1,71 a 2,73), siendo la diferencia estadísticamente significativa (p< 0,001). En los varones, la prevalencia en el nivel-I alcanzó 9,2% (IC95% 7,7 a 11,0%), mientras que en el nivel-II fue 5,1% (IC95% 3,3 a 7,2%); estas diferencias fueron significativas estadísticamente (p< 0,005). siendo el OR 1,89 (IC95% 1,20 a 2,98). El género femenino presentó una prevalencia en el nivel-I de 29,9% (IC95% 27,3 a 32,6%) y de 15,2% en el nivel-II (IC95% 12,1 a 18,5%), también estadísticamente significativa (p< 0,001), con OR 2,37 (IC95% 1,80 a 3,14%).
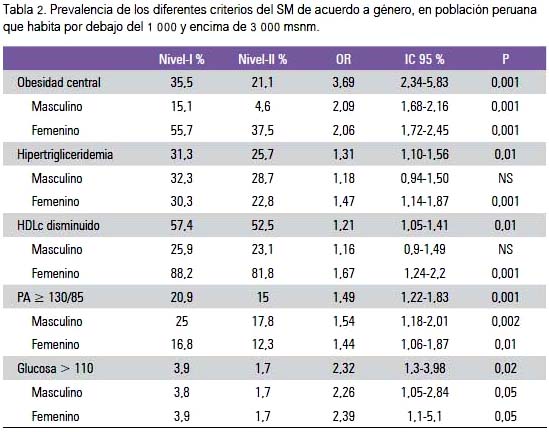
La tabla 2 permite observar las prevalencias de los diferentes componentes del SM en los niveles estudiados, tanto por género como en conjunto. En lo que corresponde a la obesidad abdominal, las prevalencias presentadas fueron mayores en el nivel-I, tanto para los varones, las mujeres y ambos, en relación al nivel-II (p< 0,001). Los OR fueron 3,69 (IC95% 2,34 a 5,83), 2,09 (IC95% 1,68 a 2,06) y 2,06 (IC95% 1,72 a 2,45), respectivamente. Independientemente del nivel, las mujeres fueron las más afectadas (55,7 vs. 37,5%). En cuanto a los TG, las prevalencias fueron mayores en el nivel-I, pero esta diferencia solo fue significativa estadísticamente en las mujeres (p< 0,001) y en el conjunto (p< 0,01). Los OR fueron 1,18 (IC95% 0,94 a 1,50), 1,47 (IC95% 1,14 a 1,87) y 1,31 (IC95% 1,10 a 1,56), en varones, mujeres y en el conjunto, respectivamente. En HDLc disminuido, también se encontró mayores prevalencias en el nivel-I; pero, así como ocurrió con los TG, estas diferencias fueron significativas solo para las mujeres (p< 0,001) y en su conjunto (p< 0,01). Los OR fueron 1,16 (IC95% 0,9 a 149), 1,67 (IC95% 1,24 a 2,2) y 1,21 (IC95% 1,05 a 1,41), en el orden de lo expuesto anteriormente. Acá también fueron las mujeres quienes presentaron las mayores prevalencias (88,2 vs. 81,8%). Las hiperglicemias encontradas representaron la menor presencia dentro de los criterios de SM; sin embargo, el nivel-I presentó mayores prevalencias que el nivel-II, siendo estas diferencias significativas (p< 0,05, p< 0,05 y p< 0,002). Sus OR fueron 2,26 (IC95% 1,05 a 2,84), 2,39 (IC95% 1,1 a 5,1) y 2,32 (IC95% 1,30 s 3,98), respectivamente.
DISCUSIÓN
El Perú es un país de una geografía rica y heterogénea; existe población que vive por debajo del nivel del mar y aquella que se encuentra por encima de los 5 000 metros sobre el nivel del mar. Esto de alguna manera condiciona cierto tipo de adaptaciones a los diferentes niveles de oxígeno y que puede traer aparejado patologías ya conocidas.
La relación de la altitud con enfermedades como el SM y sus componentes no ha sido estudiada ampliamente. Un estudio a nivel nacional muestra que los ámbitos de Lima Metropolitana (20,7%) como el resto de la costa (21,5%) presentan mayores prevalencias que la sierra urbana (15,7%) y la sierra rural (11,1%). De acuerdo a estos resultados, se asumiría que a mayor altitud menor prevalencia. Pero si se compara selva (15,3%) con la sierra urbana, no se podría aseverar lo mismo (5).
El único trabajo que ha estudiado si existe alguna diferencia de la presencia del SM entre poblaciones que viven a nivel del mar (Rímac) y otra a 4 100 msnm (San Pedro de Cajas), no ha encontrado una diferencia estadísticamente significativa (p= 0,28). La mayor prevalencia fue en San Pedro de Cajas (24,2%), en relación al Rímac (22,1%) (8).
En el presente estudio sí se ha encontrado una diferencia significativa de la prevalencia de SM entre poblaciones por debajo de los 1 000 (19,7%) y por encima de los 3 000 msnm (10,2%). Esta mayor prevalencia que se dio tanto en el género masculino como el femenino respondería a que en estas poblaciones los cambios transicionales, representados por los niveles de urbanización, educación, ingresos, accesos a los establecimientos de salud, saneamiento básico, aspectos de la tecnología, entre otros, se vienen dando más rápidamente (14). Por otro lado, y como consecuencia de lo anterior, la modificación de los estilos de vida, como son los patrones dietarios y la actividad física, no se han visto tan comprometidos en las personas que viven por encima de los 3 000 msnm, lo que explicaría de alguna manera la razón por qué a estas altitudes existe menos SM.
Independientemente a los resultados de los estudios, se observa una tendencia en lo que se refiere a la mayor presencia de los componentes para identificar el SM. En ese sentido y para ambos niveles de altitud, el C-HDL bajo (88,2 vs. 81,2%), seguido de la obesidad abdominal (55,7 vs. 37,5%) en el grupo de las mujeres y los TG (32,3 vs. 28,7%) y luego el C-HDL bajo (25,9 vs. 23,1%) en el caso de los varones, son los más representativos. Estas mismas características fueron encontradas por el estudio Prevención, con la diferencia de que sus prevalencias fueron más altas (10). Prácticamente lo mismo fue hallado por Baracco (8). Una revisión sistematizada de estudios realizados en América Latina encontró que los componentes con mayor presencia para definir SM fueron los niveles bajos de HDLc (62,9%) y la obesidad abdominal (45,8%); si bien la mayoría de estudios revisados no necesariamente fueron de altura, la tendencia independiente del nivel es esa (15). Esto de alguna manera confirma que la altitud no cumple rol determinante en el SM y sus componentes.
Si se analiza por separado cada componente del SM, se observa que para el caso de la obesidad abdominal existe una diferencia significativa en el promedio del perímetro abdominal entre los niveles, dando una mayor prevalencia en el primer nivel (p< 0,001). Estas diferencias de promedio, en relación a la altitud, también han sido encontradas en el Tibet, donde la obesidad abdominal fue 94 cm a 1 200 msnm y 84,5 cm por encima de los 3 660 msnm (16).
En pobladores de Huancavelica se halló un promedio de obesidad abdominal de 84,1 cm en varones adultos, menor aún que lo encontrado en el presente trabajo (17). Estos hallazgos guardan correspondencia con la obesidad determinada por el índice de masa corporal (IMC), ya que en la altura la prevalencia de obesidad es menor (18).
Si bien la glicemia es el elemento menos representativo en el diagnóstico de SM, su comportamiento en relación al promedio (p< 0,001) y prevalencia (p<0,05) es mayor en el primer nivel. Forbes fue uno de los primeros en señalar que la exposición a la altura indujo a un descenso de la glicemia, mejorando la respuesta a la prueba de tolerancia oral a la glucosa (19). Recientemente, Castillo comunicó una menor glicemia en habitantes de altura en relación a los de nivel del mar, que asume que se debe en parte a una mayor sensibilidad a la insulina, atribuida a mecanismos a nivel del receptor e incluso del posreceptor (20). Estas deben ser las razones por qué se ha encontrado menos diabetes mellitus en la altura (21-22).
En relación a la presión arterial, existen estudios que refieren que a mayor altitud la prevalencia de hipertensión arterial es menor (23-28). Nuestro estudio encontró una diferencia significativamente mayor en el promedio de la presión sistólica en el primer nivel, mas no así en la diastólica. Lo mismo fue comunicado por Baracco (8). Una situación muy parecida encontró Siques (25) en personas que de vivir a nivel del mar pasaron a vivir a 3 500 msnm; encontró una disminución de la sistólica y un incremento de la diastólica. Una explicación a estos resultados está relacionada con la fisiopatología de las presiones, en el caso de la sistólica con la rigidez del vaso y la frecuencia cardíaca, lo cual implicaría que la rigidez es mayor en las regiones de menor altitud; es decir, la aterosclerosis se da en mayor magnitud en estas ciudades. La menor tendencia a la arteriosclerosis que se ha observado en los habitantes de altura podría explicarse no solo por lo mencionado sino también por diversos factores como la mayor actividad física, el menor estrés psicosocial y el hallazgo de menores cifras de lípidos sanguíneos (26).
Un estudio que no es coincidente con lo mencionado es el estudio TORNASOL, en el que se refiere que la prevalencia de hipertensión arterial alcanza en la costa 27,3%, en la selva 22,7% y en la sierra 20,4%; de acuerdo a estas cifras se podría concluir que a mayor altura hay menor prevalencia; pero, el mismo estudio refiere que en poblaciones ubicadas a más de 3 000 msnm la hipertensión arterial afectó a 22,1%, mientras que en las situadas por debajo, a 18,8%. Lo más llamativo fue que en capitales como Huaraz y Puno la prevalencia fue mucho mayor que en Lima (27).
Existen algunos estudios sobre lípidos que han hallado valores más bajos de triglicéridos en la altura (28), mientras otros han encontrado prevalencias altas, responsabilizando estos hallazgos a un consumo incrementado de alimentos ricos en hidratos de carbono (8). Los estudios de Mohanna realizados en San Pedro de Cajas hallaron una hipertrigliceridemia de 57,9% en los varones y de 51,6% en las mujeres (29). Málaga encontró en la comunidad de Lari (3 600 msnm), provincia de Caylloma del departamento de Arequipa, 50% en varones y 47,8% en mujeres (30) en el mismo departamento; pero, representando a Arequipa Metropolitana (2 600 msnm) se halló 52% en varones y 35,3% en mujeres (10).
Dentro de los criterios para definir SM, el HDLc cumple el rol más protagónico, ya que en las mujeres se encuentra más presente y en los hombres ocupa el segundo lugar. Cifras más altas a las halladas en el presente estudio han sido encontradas por Málaga, 93,5% en mujeres y 50% en varones (30); lo contrario sucede con Baracco, 44,4% en mujeres y 5,6% en varones (8), Mohanna 45,3% y 5,3% (29), y Medina 32,5% y 60,9% (10), respectivamente.
Analizando cada uno de los criterios que conforman el SM en nuestro estudio, la tendencia es que todos presentaron prevalencias mayores a menor nivel de altitud en relación a los que vivían a mayor nivel. Por ende es lógico que al comparar el SM como conjunto se llegue a la misma conclusión. Otro hecho que convalida lo mencionado es que la prevalencia de obesidad fue menor en la altura (18).
Las diferencias de las prevalencias encontradas en los diferentes estudios pueden ser atribuidas a variaciones de las características de la población estudiada, a la metodología del muestreo, a la recolección de la información y a los criterios utilizados para el diagnóstico.
Si bien hay opiniones diversas en cuanto al diagnóstico y a la utilidad del SM, el estudio de Van Guilder, realizado en personas normales (IMC), obesos sin SM y obesos con SM, muestra una mayor presencia de marcadores biológicos de estrés oxidativo e inflamación (LDL oxidada, factor de necrosis tumoral, interleuquinas 6 y 18 y proteína C reactiva) a favor de estos últimos, siendo la diferencia estadísticamente significativa. Lo mismo sucedió con la resistencia de la insulina (HOMA-I) (31).
Nuestros datos muestran la presencia de SM en ambos niveles de altitud, predominando en el primer nivel. De acuerdo a los OR, parecería que la altitud representa un factor de protección frente a las complicaciones. Sin embargo, las políticas que se generen para enfrentar esta problemática deben estar orientadas, para todos, en cambios en los estilos de vida, dando pautas concretas en una alimentación de calidad que lleve a mejorar principalmente la hipertrigliceridemia; y, por otro lado, promover la actividad física, con el fin de mejorar los otros componentes del SM, como la circunferencia de cintura, la presión arterial y fundamentalmente el HDLc.
En conclusión, el SM fue significativamente más prevalente en la población por debajo de los 1 000 msnm; esto podría ser resultado de la transición nutricional, demográfica y socioeconómica en esta área. Las mujeres fueron más susceptibles a estos factores de riesgo cardiovascular.
REFERENCIAS BIBLIOGRÁFICAS
1. Osganian S, de Feranti S. Complications of obesity: Metabolic Syndrome. En: Hamilton. Nutrition in Pediatrics. 4th ed. Ontario, Canada: BC Becker, 2008.
2. Grundy S. Metabolic syndrome: connecting and reconciling cardiovascular and diabetes worlds. J Am Coll Cardiol. 2006;47:1093-100.
3. Isomaa B, Aimgren P, Tuomi T, Forsén B, Lahti K, Nissén M, Taskinen MR, Groop L. Cardiovascular morbidity and mortality associated with metabolic syndrome. Diabetes Care. 2001;24:683-9.
4. Steinberg J, Daniels S, Eckel R, Hayman L, Lustig R, Mc Crindle B, Mietus-Snyder M. Progress and challenges in metabolic syndrome in children and adolescents: a scientific statement from the American Heart Association Atherosclerosis, Hypertension, and obesity in the young Committee of the Council on Cardiovascular Disease in the young; Council on Cardiovascular Nursing; and Council on Nutrition, Physical Activity, and Metabolism. Circulation. 2009;119:628-47.
5. Pajuelo J, Sánchez Abanto J. El síndrome metabólico en el Perú. An Fac med. 2007;68(1):38-46.
6. Mena I. Influencia de la edad y del uso de la terapia de remplazo hormonal en la prevalencia del síndrome metabólico en mujeres post-menopausicas Tesis para optar el grado de Médico Cirujano. Facultad de Medicina. Universidad Nacional de San Agustín. Arequipa, 2005.
7. Gamarra M. Prevalencia comparativa de síndrome metabólico entre un distrito urbano y uno rural del departamento del Cusco. X Congreso Peruano de Endocrinología, Lima, 2006.
8. Baracco R, Mohanna S, Seclén S. A comparison of the prevalence of metabolic syndrome and its components in high and low altitude population in Peru. Metab Syndr Relat Disord. 2007;3(1):55-62.
9. Diaz Lazo A. Sobrepeso y síndrome metabólico en adultos de altura. Rev Per Cardiol. 2006;32(3):173-93.
10. Medina J, Zea H, Morey O, Bolaños J, Muñoz E, Postigo M, et al. Prevalence of the metabolic syndrome in Peruvian Andean Hispanics: The PREVENCION study. Diabetes Res Clin Pract. 2007;78:270-81.
11. Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (2001). Executive summary of the Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). JAMA. 2001;285:2486-97.
12. Ministerio de Salud. Instituto Nacional de Salud. Centro Nacional de Alimentación y Nutrición (CENAN). Encuesta Nacional de Indicadores Nutricionales, Bioquímicos, Socioeconómicos y Culturales relacionados con las enfermedades crónicas degenerativas. Lima, 2006.
13. Bray GA. Classification and evaluation of the obesities. Med Clin North Am. 1989;73:161-84.
14. Huynen M, vallebreg L, Martens P, Benavides B. The epidemiological transition in Perú. Rev Panam Salud Public. 2005(17)1:53-9.
15. Márquez-Sandoval F, Macedo-Ojeda G, Viramontes-Horner D, Fernández-Ballart J, Salas-Salvadó J, Vizmanos B. The prevalence of metabolic syndrome in Latin America: a systemic review. Public Health Nutr. 2011;14(10):1702-13.
16. Sherpa Ll, Deji H, Chongsuvivatwong v, Thelle D, Bjertness E. Obesity in Tibetian aged 30-70 living at differents altitudes under the north and south faces of Mt. Everest. Int J Environ Res Public Health. 2010;7:1670-80.
17. Toselli S, Tarazona-Santos E, Pettener D. Bodysize, composition, and blood pressure of high–altitude Quechua from the Peruvian Central Andes (Huancavelica, 3680 m). Am J Human Biol. 2001;13:539-47.
18. Pajuelo J, Sánchez Abanto J, Arbañil H. Lasenfermedades no transmisibles en el Perú y su relación con la altitud. Rev Soc Perú Med Interna. 2010;23(2):45-52.
19. Forbes W. Blood sugar and glucosa tolerance at high altitude. Am J Physiol. 1936;116:309.
20. Castillo O, Woolcott O, Gonzalez E, Tello V, Tello L, Villarreal C, Méndez N, Damas L, Florentini E. Residents at high altitude show a lower glucosa profile tan sea level residents throughout 12 hour blood continuos monitoring. High Alt Med Biol. 2007;8(4):307-11.
21. Rutte C. Contribución al estudio clínico y epidemiológico de la diabetes mellitus. Tesis de Bachiller. Facultad de Medicina UNMSM. Lima, 1966.
22. Solis J, Guerra-García R. Prevalencia de diabetes mellitus en hospitalizados de grandes alturas. Arch Inst Biol Andina. 1979;9-12.
23. Diaz A. Emergencias hipertensivas en la altura. Hipertensión. 1996;2:129-30.
24. Aste Salazar H, Ruiz L, Peñaloza D. Lípidos séricos y estado de salud cardiovascular en nativos de las grandes alturas. vII Congreso Interamericano de Cardiología. Lima, 1968.
25. Siques P, Brito J, Banegas J, León-velarde F, De la Cruz J, López V, Naveas N, Herruzo R. Blood pressure response in young adults first exposed to high altitude for 12 month at 3500 msnm. High Alt Med Biol. 2009;10(4):35-9.
26. Garmendia F. La influencia de la altura sobre la historia natural de las enfermedades. Rev Med Peruana. 1992;64:10-4.
27. Segura L, Agusti R, Parodi J e investigadores del Estudio Tornasol. Factores de riesgo de las enfermedades cardiovasculares en el Perú (Estudio TORNASOL). Rev Per Cardiol. 2006;32(2):82-126.
28. Bellido D, Barragan M, Aguilar M, Colque N. Perfil lipídico de la población de viacha. Acta Andina 1993;2:28-9.
29. Mohanna S, Baracco R, Seclén S. Lipid profile, waist circumference and body mass index in a high altitude population. High Alt Med Biol.2006;7(3):245-55.
30. Málaga G, Zevallos-Palacios C, Lazo MA, Huayanay C. Elevada frecuencia de dislipidemia y glucemia basal alterada de una población peruana de altura. Rev Perú Med Exp Salud Publica. 2010;27(4):557-61.
31. Van Guilder G, Hoetzer G, Greiner J, Stanfer B, De Souza C. Influence of metabolic syndrome on biomarkers of oxidative stress and inflammation in obese adults. Obesity. 2006;14(12):2127-31.
Artículo recibido el 1 de marzo de 2012 y aceptado para publicación el 5 de abril de 2012.
Correspondencia:
Dr. Jaime Pajuelo Ramírez
Correo electrónico: japara18@yahoo.com













