Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Anales de la Facultad de Medicina
Print version ISSN 1025-5583
An. Fac. med. vol.73 no.3 Lima July/Sep. 2012
CASO CLÍNICO
Manejo quirúrgico del síndrome de silla turca vacía primaria con compromiso visual campimétrico y sin evidencia de herniación del sistema visual
Surgical treatment of primary empty sella syndrome with visual compromise and no evidence of visual system herniation
J.L. Paz-Ibarra1, L. Álvarez-Simonetti2, A. Garrido-Peñaloza1, H. Llerena-Miranda2, D. Campos-Sánchez2, M Churampi-López1, O. Quintana-Pinto1
1
Servicio de Endocrinología y Metabolismo, Hospital Edgardo Rebagliati Martins y Facultad de Medicina San Fernando, Universidad Nacional Mayor de San Marcos, Lima, Perú2 Departamento de Neurocirugía, Hospital Edgardo Rebagliati Martins, Facultad de Medicina San Fernando, Universidad Nacional Mayor de San Marcos, Lima, Perú
Resumen
Presentamos el caso de una mujer de 36 años con síndrome de silla turca vacía primaria (STVP) caracterizado por cefalea, estrechamiento concéntrico periférico progresivo de la visión y oligomenorrea, quien fue sometida a remodelamiento selar con colocación de un autoinjerto intraselar. La evolución postoperatoria fue con mejoría importante del defecto campimétrico, en ambos ojos.
Palabras clave: Aracnoidocele intraselar, cirugía transesfenoidal, déficit visual, quiasmapexia, silla turca vacía.
Abstract
We report the case of a 36 year old woman with primary empty sella syndrome (PESS) and symptoms consisting in headache, progressive concentric peripheral narrowing of vision and oligomenorrhea, who underwent sellar remodeling with placement of an intrasellar autograft. Post operative course showed bilateral improvement in campimetric defect.
Key words: Intrasellar arachnoidocele, transsphenoidal surgery, visual deficits, chiasmapexy, empty sella.
Introducción
El término silla turca vacía (STV) fue propuesto por Busch, en 1951, para referirse a una condición anatómica observada en estudios de autopsia, particularmente en mujeres, caracterizada por una fosa hipofisiaria prácticamente vacía, ya que la glándula hipófisis se encontraba aplastada hacia el piso, dorso y paredes laterales (1-3). En 1968, Kaufman demostró que la morfología hipofisiaria se debía en realidad a un desplazamiento del espacio subaracnoideo (ESA), pero se siguió aceptando el término original (4). Leclercq propuso el término aracnoidocele intraselar, ya que de esta manera se expresa el detalle anatómico primordial (5); sin embargo, esta denominación no ha sido muy popular en la literatura internacional.
Hay dos tipos de STV. Es denominada secundaria cuando existe el antecedente de una lesión hipofisiaria que ha sido tratada ya sea mediante cirugía, radioterapia o medicamentos; se conoce como STV primaria cuando no existe alguno de estos antecedentes. Se ha propuesto varios mecanismos para explicar la patogénesis de la STV primaria, ninguno de los cuales ha sido demostrado. Se menciona como posible causa a la rotura de un quiste aracnoideo intraselar preexistente (6). Otra teoría postula que una insuficiencia vascular focal ocasionaría un infarto del tejido hipofisiario; el argumento en contra de esta hipótesis se fundamenta en la extraordinariamente baja frecuencia con que estos pacientes presentan alteraciones endocrinológicas. Otros autores proponen, en base a su alta frecuencia en mujeres multíparas, que habría una hipertrofia hipofisiaria durante los embarazos, seguida de una involución tisular, especialmente durante la menopausia; sin embargo, la multiparidad no es una condición obligada, ya que existe la posibilidad de que se presente en el sexo masculino (aunque en frecuencia baja).
Finalmente, la teoría más aceptada hasta la fecha propone una incompetencia del diafragma selar que permite la migración del líquido cefalorraquídeo (LCR) hacia la silla turca (7,8). El diafragma selar es una reflexión de la duramadre que forma el techo anatómico de la fosa hipofisiaria, que en condiciones normales mantiene al LCR fuera de esta área y presenta un orificio en su porción central para permitir el paso del tallo hipofisiario. Una debilidad o cierre insuficiente del orificio de esta membrana es el fundamento fisiopatológico del síndrome de la STV primaria; sin embargo, algún grado de incompetencia diafragmática ha sido demostrado en 22 a 77% de las personas normales, sin que necesariamente presenten herniación del ESA, lo cual hace suponer que, aunque esta anomalía es considerada esencial para la presencia de una STV primaria, otros factores deben también ser relevantes, entre ellos la presión del LCR, influencia hormonal, obesidad mórbida, hipertensión arterial, cambios hipofisiarios ocurridos durante el embarazo o combinación de alguno de estos factores.
En sentido estricto, la STV primaria no podría ser considerada una entidad patológica sino un estado anatómico con hallazgos radiológicos característicos y no siempre con manifestaciones clínicas; de hecho, la mayoría de los pacientes no tiene síntomas y se efectúa este diagnóstico como un hallazgo en los estudios de imagen que son indicados por diversos motivos, pero que no requieren tratamiento alguno. Sin embargo, existe un reducido número de pacientes que refieren algunas manifestaciones clínicas, estableciéndose el diagnóstico de síndrome de la STV primaria. Así, la fístula de LCR, déficit visual, cefalea y las alteraciones endocrinológicas son, entre otros, los signos y síntomas más frecuentes, siendo la primera y la segunda las únicas en donde se indica un manejo quirúrgico. Cuando existe fístula de LCR el objetivo quirúrgico primario es, sin discusión, sellar herméticamente el sitio de fuga; sin embargo, cuando el déficit visual es el problema, la situación se vuelve altamente controvertida, dado que existe una amplia variedad de procedimientos propuestos para su corrección.
Presentamos el caso de una mujer de 36 años con síndrome de silla turca vacía primaria (STVP) caracterizado por cefalea, estrechamiento concéntrico periférico progresivo de la visión y oligomenorrea, quien fue sometida a remodelamiento selar, con colocación de un autoinjerto intraselar.
Caso clínico
Mujer de 36 años, natural de Lima, arquitecta, soltera. Acudió a consulta refiriendo un tiempo de enfermedad de 6 meses caracterizada por cefalea intermitente, algunas veces global y otras de localización bifrontal, tipo opresión que al momento de su hospitalización había aumentado en frecuencia e intensidad; asimismo, refirió una disminución progresiva de la visión, al inicio con compromiso bitemporal, que progresó hasta visión tubular, dificultando significativamente su trabajo. Posteriormente, se agregó amenorrea sin galactorrea, de tres meses de evolución. Negaba episodio previo de cefalea aguda intensa, traumatismo craneoencefálico, así como otro antecedente de importancia. Era nulípara, sin actividad sexual en el último año, con episodios aislados de oligomenorrea.
Al examen físico, era eutrófica (IMC 23,5), normotensa (110/70 mmHg), con compromiso concéntrico de ambos campos visuales por confrontación; sin bocio, galactorrea o hirsutismo (SFG: 6 puntos). Resto del examen sin alteraciones significativas.
La evaluación neuro-oftalmológica concluyó: pupilas fotorreactivas, fondo de ojo muestra papilas redondeadas, de bordes definidos, color rosado, con pequeña excavación, relación C/D conservada, presión intraocular 15 mmHg. La exploración del campo visual se muestra en las figuras 1 y 2.
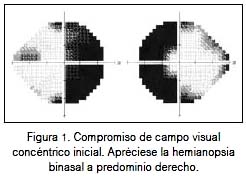
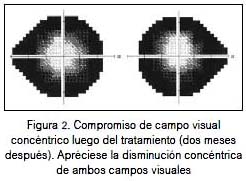
La analítica fue informada glucosa 85 mg/dL, urea 35 mg/dL, creatinina 0,70 mg/dL, densidad urinaria 1010, TGO / TGP 23 / 30 U/L, albúmina 4,28 g/dL, globulinas 3 g/dL, Na / K/ Cl 140 / 4,12 / 103 mmol/L; hemograma 6 730 leucocitos, hemoglobina 12,3 g%, volumen corpuscular medio 90 fL, plaquetas 250 mil, grupo sanguíneo A, Rh (+). Prolactina (pool) 15,1 ng/mL, hormona de crecimiento 5,26 ng/mL, factor de crecimiento insulínico 1 241 ng/mL, hormona adrenocorticotropa 29,6 pg/mL, cortisol 12,6 ug/dL, tirotropina 1,45 uUI/mL, T4 libre 1,05 ng/dL, anticuerpos contra la peroxidasa tiroidea (AbTPO) (-), LH 2,8 mUI/mL, FSH 1,43 mUI/mL, estradiol 53,7 pg/mL, androstenediona 2,64 ng/mL, sulfato de dehidroepiandrosterona (DHEAS) 223 ug/dL, testosterona libre 0,52 pg/mL, subunidad B-hCG (-).
En cuanto a los exámenes de imágenes: rayos X de tórax normal; ecografía pélvica transvaginal con endometrio de 6 mm y presencia de múltiples folículos en ambos ovarios, con volúmenes en ovario derecho de 9 mL y en ovario izquierdo de 10 mL. Se realizó tomografía y resonancia magnética, cuyas imágenes pueden ser apreciadas en las figuras 3 y 4. Fue sometida a punción lumbar, obteniéndose líquido céfalo raquídeo cristal de roca a goteo lento, con una presión de 80 mmH2O.
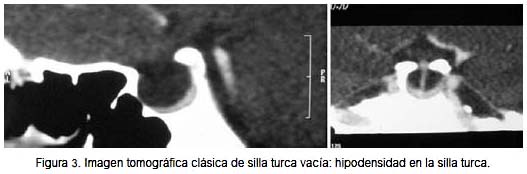
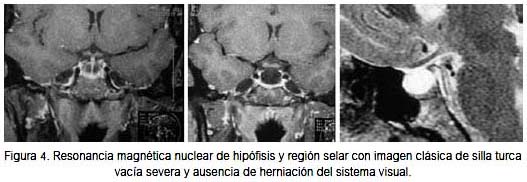
Después de una discusión multidisciplinaria y en base al deterioro visual progresivo, se decidió someter a la paciente a remodelamiento de la silla turca, a fin de elevar el contenido selar para reposicionar los elementos anatómicos, siguiendo la técnica de remodelación selar descrita por Guinto (1). Se realizó el abordaje endonasal trans-septal transesfenoidal (2). Se administró antibioticoprofilaxis con cefuroxima 1,5 gramos por vía endovenosa y durante el procedimiento 150 mg de hidrocortisona. Luego de la entubación oro-traqueal para anestesia general con agentes inhalatorios, se ubicó el tubo oro-traqueal hacia el lado izquierdo de la boca y se colocó gasa en orofaringe para prevención de aspiración aérea con sangre o secreción mucosa.
La paciente fue mantenida en posición supina, con la cabeza apoyada en cabezal de herradura, elevada aproximadamente 15 grados y con discreta rotación hacia la derecha. Se posicionó el miembro inferior derecho flexionado y con apoyo, a fin de preparar la porción proximal de la cara lateral del muslo para obtención de injerto de fascia lata. Se guió la cirugía mediante visión flouroscópica. Se realizó el aseo con jabón quirúrgico de ambas fosas nasales. El abordaje fue unilateral por la narina derecha. Bajo medidas de asepsia y antisepsia, se inyectó por debajo de la mucosa 2,5 mL de lidocaína al 2% con epinefrina 1:200 000, ingresando por la porción más anterior del séptum cartilaginoso de la narina derecha.
Se realizó incisión en la mucosa, perpendicular al eje longitudinal de la nariz, despegándola del tabique cartilaginoso. Se colocó espéculo nasal de Killian corto y se desplazó la punta hacia la izquierda, fracturando el tabique óseo en la base del seno esfenoidal, luxándolo hacia dicho lado. Se constató la llegada a la base esfenoidal con fluoroscopio. Se colocó microscopio quirúrgico, identificando el vómer y su unión a la base del esfenoides (quilla). Colocación de espéculo nasal largo. Con apoyo de cincel, se retiró un fragmento de vómer y con pinza gubia Kerrison se aperturó la base del seno esfenoidal. Se extirpó la mucosa nasal. Con apoyo fluoroscópico, se identificó el piso de la silla turca y se realizó una apertura en forma cuadrangular (de 6 x 9 mm, aproximadamente). Se expuso la duramadre y se objetivó el contenido selar discretamente tenso, por lo que con apoyo de cottonoides se le proyectó cefálicamente, dejando estos elementos en el interior de la silla turca, para hemostasia temporal.
Para la preparación del autoinjerto, se procedió a realizar incisión de 3 cm en muslo derecho. Se retiró grasa y fragmento de 3 x 1 cm de fascia lata. Se revisó la hemostasia y se suturó por planos, con sutura intradérmica en piel. Con un fragmento de la fascia lata extirpada se envolvió grasa, de tal forma que se formó un paquete como descrito por Guinto y col. (1), al que se le cubrió por ambas caras con fragmentos óseos corticales prevenientes del vómer; se les aseguró con material no reabsorbible (figura 5). Para calcular el tamaño del injerto, se trazó en la imagen tomográfica lateral una línea a nivel interclinoideo (posición del diafragma selar) y una segunda línea paralela pero inferior a nivel de la confluencia entre el dorso y el piso selar, correspondiendo al lugar donde debería asentar el injerto. La altura del implante fue el resultado de una resta de la distancia entre las dos líneas menos los 2 mm que correspondían al espesor de la hipófisis. El ancho del injerto fue de 3 mm menos que la distancia entre las dos carótidas vistas en la incidencia coronal de la resonancia magnética de la región selar.
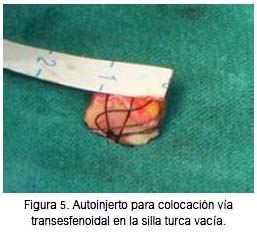
Se adaptó la apertura selar, ampliándola discretamente, para un mejor posicionamiento del injerto. Este fue colocado en el interior de la silla turca con apoyo de pinza, ingresando primero la parte posterior y finalmente la anterior. Una vez firme, se controló la posición con fluoroscopia, guiándose por las imágenes de los fragmentos óseos del injerto, calculando así que el contenido selar recuperase un nivel más anatómico (figura 6).
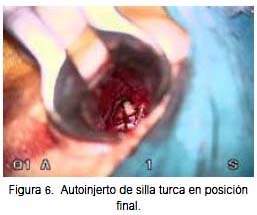
Finalmente, se colocó un pequeño fragmento de tejido conectivo procedente de la grasa triturada en el defecto quirúrgico del piso selar y pequeños fragmentos óseos planos, y el conjunto se sostuvo por un fragmento de filtro hemostático de colágeno. El resto del vómer fue recolocado y se restituyó el cartílago septal hacia la línea media; la mucosa nasal también fue reacomodada. Finalmente, se colocó empaquetamiento nasal bilateral, que fue retirado al tercer día posquirúrgico.
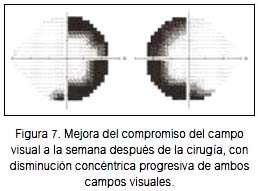
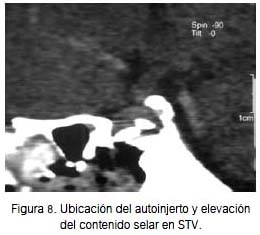
La paciente evolucionó de manera favorable luego de la cirugía, con disminución de la cefalea y mejora casi inmediata de la visión (figuras 2 y 7). El perfil hormonal hipofisiario permaneció dentro de los límites normales y la microscopia de transmisión electrónica (TEM) control de silla turca evidenció posición adecuada del autoinjerto (figura 8).
Discusión
En el síndrome de STV primaria se indica manejo quirúrgico cuando se presentan los síntomas de fístula de LCR y déficit visual. Cuando existe fístula de LCR, el objetivo quirúrgico primario es, sin discusión, sellar herméticamente el sitio de fuga; sin embargo, cuando el déficit visual es el problema, la situación se vuelve altamente controvertida, dado que existe una amplia variedad de procedimientos propuestos para su corrección.
La causa de las manifestaciones clínicas en el síndrome de la STV primaria es motivo de controversia; si bien la cefalea es considerada el síntoma más frecuente, su origen no ha sido demostrado. Se ha propuesto que la migración del ESA ocasiona tracción en las estructuras vasculares meníngeas sensibles al dolor. Esto pudo verse en nuestra paciente, así como en otras series, ya que tan pronto se reconstituyó los elementos anatómicos de la ST, este síntoma desapareció (1,9).
Al igual que la mayoría de series, vemos que en nuestra paciente las alteraciones endocrinológicas en el síndrome de la STV primaria son generalmente mínimas y sin consecuencia clínica. Es indudable que la alteración hormonal referida con mayor frecuencia es el incremento en el nivel de prolactina. Se ha encontrado que la hiperprolactinemia se presenta en alrededor de 11% de los pacientes con síndrome de la STV primaria, y se ha propuesto como causa de esta elevación hormonal a una compresión en el tallo hipofisiario como consecuencia de una alteración en la dinámica local de LCR. Sin embargo, dada su frecuencia baja, no se puede descartar una asociación coincidental, pues hay que recordar que el simple estrés (por el temor a la cirugía, cefalea o las alteraciones visuales) pudo haber sido la causa de esta elevación en algunas series y que, al desaparecer este una vez operados, se normalizaran los niveles de esta hormona. La oligomenorrea en este caso podría deberse a las alteraciones a nivel de gonadotropinas, a algunos episodios aislados de hiperprolactinemia o tener una base ovárica funcional, como ocurre en el síndrome de ovarios poliquísticos.
El déficit visual ha sido informado en 1,6 a 18% de los pacientes con síndrome de la STV primaria y se acepta que la causa en estos pacientes se debe a que parte del sistema visual supraselar se desplaza hacia la ST, debido a la tracción ejercida por el ESA; sin embargo, también se ha descrito pacientes con una afección campimétrica evidente, pero con el sistema visual supraselar intacto (10), tal y como se evidenció en nuestro caso. Aunque esto no signifique que pudiera existir algún grado de desplazamiento microscópico del mismo, pero también puede indicar la presencia de algún otro mecanismo fisiopatológico de este déficit. Así, se ha propuesto que la tracción del tallo hipofisiario ejercido por el ESA puede ocasionar alguna alteración en el aporte microvascular en el sistema visual, generando este déficit y que puede no ser visible incluso en los estudios de imagen de alta resolución (10,11). Por otro lado, llama la atención la reversibilidad de estas alteraciones visuales, tal como pudimos constatar en nuestra paciente, lo cual sugiere que cualquiera que fuese el mecanismo fisiopatológico involucrado en el déficit campimétrico, este no es lo suficientemente severo como para dañar en forma definitiva el sistema visual en la mayoría de los casos, como se ha comunicado (1). Considerando las diferentes variedades morfológicas de la vía visual supraselar, es explicable la gran variabilidad del patrón de afección campimétrica descrita en el síndrome de la STV primaria, siendo la reducción concéntrica la alteración más encontrada. Hasta el momento se desconoce el motivo por el cual ocurre la hemianopsia bitemporal, déficit clásico en lesiones quiasmáticas; no es el patrón predominante en estos casos, como sucede en los adenomas hipofisiarios.
La mayoría de los pacientes con síndrome de la STV primaria que requiere tratamiento quirúrgico son operados por vía transesfenoidal. Este procedimiento ha sido denominado quiasmapexia; sin embargo, algunos autores sostienen que este término es incorrecto, ya que al efectuar la cirugía por esta vía no solo se eleva el sistema visual sino casi la totalidad del contenido selar. Por otro lado, no todos los pacientes con síndrome de la STV primaria presentan desplazamiento del sistema visual hacia la silla turca, por lo que la posición del quiasma óptico no se modifica cuando se efectúa la cirugía (1,10). Es por ello que la denominación más correcta del procedimiento es la de elevación del contenido selar (1,12,13) o aracnoidopexia, dado que así se describe de una manera más simple el objetivo quirúrgico en esta entidad, que es la elevación del ESA.
Se ha descrito múltiples técnicas y en todas se busca mantener la elevación del contenido de la silla turca en forma definitiva; lo que varía es el material para lograrlo. Para el injerto, se ha utilizado tejidos obtenidos del propio paciente, tales como fragmentos de hueso (13,14), grasa o músculo, o una combinación de tejidos. La principal ventaja de estos materiales es que, al ser tejidos autólogos, la posibilidad de rechazo es prácticamente nula; sin embargo, su principal desventaja es que, además de que implica otra cicatriz en el sitio donde son extraídos, estudios a largo plazo han mostrado que la mayoría de estos se reabsorbe. Por ello es que se ha propuesto también el empleo de materiales sintéticos, tales como láminas de aluminio (15,16), resortes de silástico o balones desprendibles (17,18). Si bien con el uso de estos materiales se evita la realización de otra incisión y se puede lograr una reconstrucción casi exacta de la silla turca, el hecho de que sean materiales inertes y en contacto con los senos paranasales, se incrementa el riesgo de infección; además, en el caso concreto de los balones desprendibles, en un seguimiento a largo plazo tienden a desinflarse (19).
El procedimiento propuesto por el grupo mexicano de Guinto (1), si bien no evita la realización de otra incisión, permite moldear un injerto con dimensiones ajustadas casi en forma exacta al contorno de la silla turca del paciente, por lo que la denominan remodelación selar, ya que se logra una reconstrucción del contorno de la silla prácticamente a la medida del paciente. Las principales ventajas del mismo consisten en que formar el bloque fuera del campo quirúrgico es mucho más fácil que realizarlo in situ, como se efectúa en las otras técnicas que emplean materiales autólogos; el grado de elevación del contenido selar es muy preciso, lo que evita el riesgo del sobre empaquetamiento y, además, a diferencia de la grasa y músculo, su consistencia firme facilita su introducción en la fosa hipofisiaria. Por otro lado, el hecho de que esté formado por dos láminas de hueso ofrece otras ventajas: en primer lugar, se puede tener un control fluoroscópico transoperatorio del nivel de ascenso del contenido selar y, en segundo lugar, al estar ambas láminas en contacto con el hueso de la silla turca se promueve su osificación en el sitio exacto de su inserción, lo cual permite la persistencia de dicha elevación aún a largo plazo. Finalmente, al ser un procedimiento seguro, económico y técnicamente sencillo, sugerimos su aplicación en pacientes similares. Sin embargo, hay que aclarar que la elevación del contenido selar que este método ofrece no implica un sellado hermético del piso de la ST, por lo que no se recomienda su aplicación en casos de fístula de LCR asociada.
Referencias bibliográficas
1. Guinto-Balanzar G, Mercado-Atri M, Guinto-Balanzar P, Nishimura-Meguro E, Abdo-Toro M, Aréchiga-Ramos N, Nettel-Rueda B. Remodelación selar: una opción quirúrgica para el síndrome de la silla turca vacía primaria.
2008. Gac Méd Méx. 2008:144(1):15-22.2. Griffith HW, Verapen R. A direct transnasal approach to the sphenoid sinus. Technical note. J Neurosurg. 1987;66:140-2.
3. Busch W. Die Morphologie der sella turcica und ihre beziehungen zur hypophyse. Virchows Arch. 1951;320:437-58.
4. Kaufman B. The empty sella turcica-a manifestation of the intrasellar subrachnoid space. Radiology. 1968;90:931-41.
5. Leclercq TA, Hardy J, Vezina JL, Mercky F. Intrasellar arachnidocele and the so-called empty sella syndrome. Surg Neurol. 1974;2:295-9.
6. Bjerre P. The empty sella. A reappraisal of etiology and pathogenesis. Acta Neurol Scand. Suppl 1990;130:1-25.
7. De Marinis L, Bonadonna S, Bianchi A, Maira G, Giustina A. Primary empty sella. J Clin Endocrinol Metab. 2005;90:5471-7.
8. Maira G, Anile C, Mangiola A. Primary empty sella syndrome in a series of 142 patients. J Neurosurg. 2005;103:831-6.
9. Catarci T, Fiacco F, Bozzao L, Pati M, Magiar AV, Cerbo R. Empty sella and headache. Headache. 1994;34:583-6.
10. Guinto G, Del Valle R, Nishimura E, Mercado M, Nettel B, Salazar F. Primary empty sella syndrome: the role of visual system herniation. Surg Neurol. 2002;58:42-8.
11. Braatvedt GD, Corrall RJ. The empty sella syndrome: much ado about nothing. Br J Hosp Med. 1992;47:523-5.
12. Decker RE, Carras R. Transsphenoidal chiasmapexy for correction of posthypophysectomy traction syndrome of optic chiasm. Case report. J Neurosurg. 1977;46:527-9.
13. Hamlyn PJ, Baer R, Afshar F. Transsphenoidal chiasmopexy for long standing visual failure in the secondary empty sella syndrome. Br J Neurosurg. 1988;2:277-9.
14. Olson DR, Guiot G, Derome P. The symptomatic empty sella. Prevention and correction via the transsphenoidal approach. J Neurosurg. 1972;37:533-7.
15. Spaziante R, de Divitiis E, Cappabianca P. Reconstruction of pituitary fossa in transsphenoidal surgery: an experience of 140 cases. Neurosurgery. 1985;17:453-8.
16. Kobayashi S, Sugita K, Matsuo K, Inoue T. Reconstruction of the sellar floor during transsphenoidal operations using alumina ceramic. Surg Neurol. 1981;15:196-7.
17. Zona G, Testa V, Sbaffi PF, Spaziante R. Transsphenoidal treatment of empty sella by means of a silastic coil: technical note. Neurosurgery. 2002;51:1299-1303.
18. Nagao S, Kinugasa K, Nishimoto A. Obliteration of the primary empty sella by transsphenoidal extradural balloon inflation: technical note. Surg Neurol. 1987;27:455-8.
19. Spaziante R, Zona G, Testa V. Primary empty sella síndrome. Surg Neurol. 2003;60:177-8.
Artículo recibido el 14 de febrero de 2012 y aceptado para publicación el 5 de abril de 2012.
Correspondencia:
Dr. José Luis Paz Ibarra
Correo electrónico: jlpi_09@yahoo.com













