Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Anales de la Facultad de Medicina
Print version ISSN 1025-5583
An. Fac. med. vol.74 no.3 Lima July/Set. 2013
CASOS CLÍNICOS
Infliximab en pacientes con enfermedad ocular inflamatoria, refractarios a DARMES
Infliximab in patients with inflammatory DMARDs-refractory eye disease
Elmer R. García-Salazar1,2, Henry Terrazas1,2, Javier Gonzales3, Miguel Fernández3
1 Unidad Ambulatoria de Reumatología UNAR.
2 Servicio de Reumatología, Hospital Nacional Edgardo Rebagliati Martins, EsSalud, Lima, Perú.
3 Residentes de la especialidad de Reumatología, sede HNERM, Universidad Nacional Mayor de San Marcos.
Resumen
Se describe la experiencia con infliximab (anticuerpo monoclonal con una potente acción antiinflamatoria) en el tratamiento de enfermedades oculares inflamatorias secundarias a patologías reumáticas y refractarias a drogas antirreumáticas modificadoras de la enfermedad (DARMES). Se evaluó el caso de una paciente de 50 años con artritis reumatoide (AR) de fondo activo y una paciente de 37 años con vasculitis anticuerpos anticitoplasma de neutrófilos especifico para mieloperoxidasa (ANCA MPO) sin compromiso de órgano noble, ambas con escleritis bilateral y perforación con prolapso de iris del ojo izquierdo. Ellas recibieron infliximab EV en dosis de 3 a 5 mg/kg/dosis, según el esquema, a las 0, 2, 6 y 8 semanas. Infliximab resultó eficaz y seguro para el tratamiento de escleritis asociada a AR y vasculitis ANCA MPO positivo, refractaria a tratamiento con DARMES y corticoides en dosis altas. Los injertos de tejido esclerocorneal evolucionaron favorablemente con infliximab.
Palabras clave: Escleritis, infliximab, vasculitis ANCA positivo, artritis reumatoide.
Abstract
Experience with infliximab (monoclonal antibody with strong anti-inflammatory action) for treatment of ocular inflammatory disease secondary to rheumatic diseases and refractory to disease-modifying antirheumatic drugs (DMARDs) is described. We evaluated the cases of a 50 year-old patient with active rheumatoid arthritis (RA) and a 37 year-old patient with myeloperoxidase antineutrophil cytoplasmic vasculitis antibody (MPO ANCA) without noble organ affectation, both with bilateral scleritis and left eye corneal perforation with iris prolapse. They received infliximab 3-5 mg/kg IV at 0, 2, 6, and 8 weeks. Infliximab was effective and safe for treatment of scleritis associated to RA and MPO ANCA positive vasculitis refractory to treatment with both DMARDs and high dose corticosteroids. Corneoscleral tissue grafts developed favorably with infliximab.
Keywords: Scleritis, infliximab, positive ANCA vasculitis, rheumatoid arthritis.
INTRODUCCIÓN
Aproximadamente 4 a 65% de los pacientes que tienen enfermedades reumáticas pueden presentar compromiso a nivel de cualquier zona de la anatomía ocular, como síndrome de ojo seco, uveítis anterior, panuveitis, escleritis, epicescleritis, queratitis, vasculitis retinal, vitiritis, neuropatía óptica isquémica y escleritis, los cuales al no ser tratados adecuadamente derivarán en la pérdida de la visión irreversiblemente (1,2). El tratamiento para el compromiso ocular está dado de acuerdo a la patología de fondo y al tipo, siendo este último a nivel local y sistémico con corticoides e inmunosupresores denominados drogas antirreumáticas modificadoras de la enfermedad (DARMES). Ciclofosfamida y metotrexato son los que mayormente han sido utilizados, pero en muchas ocasiones los resultados no han sido satisfactorios (3,4). Por tanto, existe un grupo de pacientes con compromiso ocular refractarios a los DARMES, por lo que es necesario el manejo con otras terapias, como por ejemplo los agentes contra el factor de necrosis tumoral alfa (TNF-alfa), siendo infliximab el que mejor respuesta ha conseguido, a diferencia de los otros anti FNT-alfa, según comunicaciones publicadas en países europeos y de Norteamérica (5-8).
El FNT-alfa es una citoquina que se encuentra elevada a nivel sérico y en el humor acuoso en los pacientes con AR y espondilitis anquilosante con afección ocular, como uveítis, como se ha demostrado en modelos animales y en los estudios con seres humanos, por lo que su presencia tiene rol destacado en la fisiopatología inflamatoria de estas entidades (9,10).
Las vasculitis tipo anticuerpo citoplasmático antineutrofílico (ANCA) positivos pueden afectar el globo ocular. Se ha encontrado una gran cantidad de pacientes con escleritis, uveítis, neuropatía óptica predominantemente asociadas a ANCA PR3, las cuales han recibido tratamiento con DARMES tradicionales y corticoides, pero también terapia biológica con anti FNT-alfa y rituximab entre otros. No existen comunicaciones hasta la actualidad con respecto a vasculitis ANCA MPO positivos con escleritis refractarios al tratamiento con DARMES tradicionales y que hayan recibido tratamiento con algún anti FNT-alfa.
Infliximab es el agente anti FNT-alfa que ha sido aprobado desde agosto de 1998 para el tratamiento de los signos y síntomas de la artritis reumatoide. Es un anticuerpo monoclonal quimérico (IgG) derivado de una ADN recombinante, conformado por genes de origen humano y murino (11).
El presente es un estudio descriptivo observacional tipo reporte de casos. Se revisó las historias clínicas de dos pacientes que recibieron infliximab (Remicade, Centocor Inc., Malvern, Pennsylvania) en la unidad de Infusión de terapia biológica (UNAR) del servicio de Reumatología del Hospital Nacional Edgardo Rebagliati Martins, EsSalud, Lima, Perú, correspondiente al periodo comprendido entre enero 2011 y julio 2012. Los pacientes fueron evaluados por la Unidad de Córnea del Servicio de Oftalmología, así como por el Servicio de Reumatología.
El tratamiento convencional en los casos de escleritis y uveítis está dado por dosis altas de prednisona por un periodo de cuatro semanas, que luego se disminuye gradualmente. Así mismo, se contempla el uso de ciclofosfamida en bolos, 0,5 a 1 mg/m2 de superficie corporal, mensualmente, o metotrexato 7,5 a 25 mg semanal. La no respuesta al tratamiento con los fármacos antes mencionados es considerado como refractario, por lo que se contempla el inicio de la terapia biológica con un anti FNT-alfa, en este caso infliximab en dosis de 3 a 5 mg/kg de peso y de acuerdo al esquema estandarizado de 0, 2, 6 semanas y luego cada 8 semanas. La administración del fármaco se realizó en un periodo de dos horas por medio de una bomba de infusión, con el uso de un filtro por el personal de enfermería y bajo la supervisión del médico reumatólogo integrante de la Unidad de Infusión.
Se tomó muestras de hemograma, perfil bioquímico, perfil hepático, proteína C reactiva (PCR), velocidad de sedimentación globular (VSG), examen de orina completo, set de hepatitis, urocultivo, VDRL, radiografía de tórax y la prueba del PPD previo al inicio del tratamiento. El seguimiento se realizó en base al PCR, VSG, hemograma, TGO, TGP, urea y creatinina. Se realizó el recuento articular de 28 articulaciones; se evaluó la capacidad funcional mediante el HAQ versión Perú (Health Assessment Questionnaire); aplicamos la escala visual análoga del dolor (EVA dolor), apreciación general del médico (AGM); se obtuvo el DAS28 para PCR. A las pacientes se les brindó información sobre los riesgos y beneficios de infliximab; luego se les entregó el consentimiento informado para su respectiva firma. Paralelamente, los casos fueron sometidos a junta médica por los integrantes del servicio de Reumatología y Oftalmología.
Las evaluaciones de oftalmología fueron realizadas cada 4 a 6 semanas. Se evaluó parámetros de agudeza visual mediante la prueba de Snellen y el grado de inflamación ocular, así como la sintomatología asociada a actividad, como son hiperemia, fotofobia y dolor ocular. Así mismo, describió la evolución del tejido correspondiente al parche esclerocorneal instalado en los casos de perforación ocular.
El estudio fue aprobado por el comité de ética del HNERM; la recolección de datos se realizó respetando la declaración de Helsinki.
CASO 1
Paciente mujer de 50 años que fue diagnosticada de AR seropositiva 7 años previos a la evaluación en nuestro hospital. Recibió AINES, prednisona 7,5 mg/día y metotrexato; así mismo, ocrelizumab 4 años antes de ingreso, por un periodo de dos años, con buena respuesta a nivel articular. Dos años antes de ingreso a nuestro hospital presentó el diagnóstico de escleritis bilateral, por lo que se le inició tratamiento tópico y sistémico con corticoides. Pese a dicho tratamiento, tuvo perforación ocular izquierda. Acudió a nuestro hospital 14 meses antes de la admisión con poliartritis, rigidez matinal (RM) mayor de una hora, fotofobia, dolor ocular, sensación de cuerpo extraño, hiperemia ocular bilateral, DAS 28 (PCR) de 5 y HAQ de 2,3. Fue evaluada por la unidad de córnea, obteniendo una traducción audiovisual (TAV) de Snell OD 20/100 y OI 20/200. Por lo anterior fue diagnosticada de escleritis anterior necrotizante bilateral, con perforación ocular izquierdo. Se le indicó prednisona 1 mg/kg/día, metotrexato 15 mg/sem SC y además se la intervino quirúrgicamente para colocación de parche esclerocorneal en el ojo izquierdo, Se obtuvo buena respuesta a nivel articular, pero el compromiso ocular persistió. Así mismo, el tejido injertado no tuvo evolución favorable debido a que se presentó denudación del parche e inflamación notable en el tejido adyacente al parche. Luego de tres meses de tratamiento, se decidió añadir un anti FNT, infliximab 3 mg/kg por dosis, en el esquema 0, 2, 6 y luego cada 8 semanas. A los diez días de la primera infusión, la paciente no presentaba hiperemia ocular ni sensación de cuerpo extraño; no había fotofobia y el dolor ocular cedió completamente. Luego de la primera infusión se colocó nuevo parche, el cual tuvo evolución favorable, no presentando inflamación en la periferia del parche y no habiendo necesidad de nueva intervención quirúrgica. La paciente recibió un total de siete infusiones de infliximab. En la última evolución presentó VSG de 16 mm/h, PCR negativo, puntaje por cuestionario de incapacidad HAQ de 0,25, DAS 28 (PCR) de 2,89. En la evaluación por la unidad de córnea tuvo una prueba de agudeza visual mediante la tabla de Snellen, en el OD 20/70 y en el OI 20/100. No se comunicó reacciones adversas durante ni posterior a la infusión de infliximab.
CASO 2
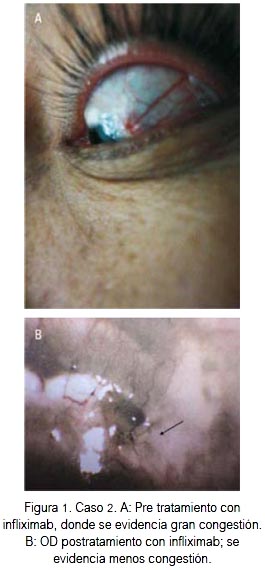
Paciente mujer de 37 años de edad que fue diagnosticada de queratitis de ambos ojos en marzo de 2011, en un centro especializado, por lo que recibió tratamiento con corticoides a nivel local, obteniendo mejoría parcial. Luego de cinco meses acudió a nuestro centro hospitalario refiriendo presencia de lesiones eritematosas ulceradas en miembros inferiores, muy dolorosas. Así también, dolor intenso más hiperemia de ambos ojos, teniendo una agudeza visual (AV) de 20/200 bilateral. En los exámenes de laboratorio se encontró PCR 0,6 mg/dL, VSG 64 mm/h, FR negativo y ANCA MPO positivo 54 y 74 RU/mL por ELISA, en dos ocasiones. Fue evaluada en unidad de córnea, donde se le diagnosticó escleritis y queratitis con prolapso de iris de ojo izquierdo, por lo que fue sometida a cirugía, con reposición de iris, colocación de parche escleral y recubrimiento conjuntival izquierdo. Se le inició tratamiento con metotrexato, dosis inicial de 7,5 mg/sem, con ascenso progresivo hasta 15 mg/semanal, asociado a prednisona 1 mg/kg/día, luego de lo cual cedió el dolor ocular, la fotofobia e hiperemia; pero, el parche no presentó buena evolución. Seis meses atrás retornó al hospital manifestando hiperemia, dolor ocular intenso que limitaba las actividades de la vida diaria y fotofobia en ambos ojos. En la evaluación por oftalmología se describió perforación corneal y prolapso de iris de OI con persistencia de úlcera corneal inmunológica, asociada a glaucoma en ambos ojos. Dicho cuadro se presentó pese a estar en tratamiento con corticoides y metotrexato. Se la intervino quirúrgicamente colocándosele parche esclerocorneal y se le subió la dosis de metotrexato a 15 mg/semanal, por VO, con incremento de prednisona a 0,5 mg/ kg/día. Así mismo, se le brindó tratamiento con antiglaucomatosos tópicos y sistémicos. Por el riesgo de pérdida de la visión, se decidió iniciar tratamiento con infliximab 5 mg/kg por dosis, en el esquema 0, 2, 6 y cada 8 semanas. Luego de la primera infusión, a los 4 días tuvo incremento del dolor ocular asociado a hiperemia, con fotofobia bilateral, y al ser evaluada por oftalmología se describió AV OD 20/50 y OI 20/200 y dehiscencia de puntos, por lo que se decidió reintervenirla quirúrgicamente y se le incrementó la dosis de prednisona a 1 mg/kg/día. Hasta el momento, la paciente recibió cuatro dosis de infliximab de 250 mg cada una, no presentando hiperemia, fotofobia, ni dolor ocular. El parche esclerocorneal evolucionó favorablemente, no requiriendo nueva intervención quirúrgica (figura 1), presentando AV en OD 20/50 y OI 20/100. Continúa al momento de esta comunicación con metotrexato 15 mg/ semanales, prednisona 10 mg/día y no requirió antiglaucomatosos. No se informó reacciones adversas durante ni después de las infusiones del agente biológico.
DISCUSIÓN
Describimos el cuadro de escleritis bilateral con perforación ocular y prolapso de iris en un ojo en una paciente con artritis reumatoide que recibió inicialmente terapia estándar en base a dosis altas de corticoides y metotrexato, con lo que respondió parcialmente. Así mismo, se le colocó un parche esclerocorneal, el cual no evolucionó favorablemente. Por la persistencia de dicho cuadro y la mala evolución de la cirugía, se decidió iniciar tratamiento con un anti FNT-alfa, en este caso infliximab, el cual según algunos informes tiene mejor respuesta ante el compromiso ocular en pacientes con AR frente a etanercept (7,12), a una dosis y esquema de manejo para pacientes con AR. Luego de la primera infusión, a los pocos días, luego de una segunda intervención quirúrgica se logró buena evolución de dicho parche; la evidencia de una buena respuesta clínica y de la agudeza visual fue progresivamente notable con el transcurrir de las semanas.
Existen muchas series de casos en las que se describe los beneficios de infliximab en el tratamiento de AR, tanto para su compromiso articular como a nivel extraarticular, especialmente a nivel de la superficie ocular en casos refractarios a la terapia con DARMES tradicionales, incluido corticoides sistémicos en dosis altas (6-8,13). Lo destacable en el presente trabajo es el hallazgo en lo referido a la buena evolución del tejido injertado en el parche esclerocorneal, lo cual determinó una mejoría en la agudeza visual y se manifestó en la no necesidad de una nueva intervención quirúrgica hasta la publicación del presente artículo. La paciente no presentó reacción adversa al fármaco, esto quizá debido a la continuación de la terapia con metotrexato y corticoides en dosis bajas.
El segundo caso es de una paciente que tuvo escleritis bilateral con perforación y prolapso de iris en el ojo izquierdo, asociada a lesiones cutáneas y al hallazgo persistente de anticuerpos anticitoplasma del neutrófilo tipo MPO, en niveles elevados, además de la presencia de elevación de los reactantes de fase aguda. Ella recibió terapia con corticoides en dosis altas asociados a metotrexato. Pero, no se obtuvo una respuesta completa y no presentó evolución favorable del parche esclerocorneal, perdiendo el injerto días posteriores a la primera infusión de infliximab. Por ello fue necesaria una segunda intervención quirúrgica, la cual hasta el momento de esta publicación ha evolucionado favorablemente, no observándose dehiscencia de puntos de sutura. Al realizar la búsqueda bibliográfica encontramos algunas publicaciones de casos de pacientes con vasculitis ANCA P positivos (14-17), pero todos los casos tenían compromiso de órganos nobles, como el riñón, los pulmones y el sistema nervioso central. No se encontró algún caso de vasculitis ANCA positivo MPO que tuviera escleritis refractaria al tratamiento con DARMES tradicionales y que hubiera recibido infliximab. Así mismo, es de resaltar que el tejido trasplantado evolucionó favorablemente.
No hubo evidencia de reacción adversa a la terapia biológica con infliximab ni complicaciones infecciosas.
En conclusión, infliximab es un anti FNT-alfa que resultó eficaz y seguro para el tratamiento de escleritis asociada a artritis reumatoide y vasculitis ANCA MPO positivo refractaria a metotrexato y corticoides en dosis altas. Así mismo, los tejidos injertados de tipo esclerocorneal evolucionaron favorablemente durante el tratamiento con infliximab, contrariamente a lo observado con otros tratamientos establecidos previamente.
Se requiere continuar el seguimiento de las pacientes, para poder evaluar las posibilidades de recurrencia o las complicaciones asociadas a la terapia biológica establecida.
REFERENCIAS BIBLIOGRÁFICAS
1. Hamideh F, Prete PE. Ophthalmologic manifestations of rheumatic diseases. Semin Arthritis Rheum. 2001;30(4):217-41.
2. Cojocaru VM, Ciurtin C, Pop M, Tomi A, Greco P. [Ophthalmological involvement in rheumatic disease]. Oftalmologia. 2006;50(2):56-61.
3. Kraus CL, Culican SM. Use of biologic agents in ocular manifestations of rheumatic disease. Int J Rheumatol. 2012;2012:203819.
4. Dunn JP. Review of immunosuppressive drug therapy in uveitis. Current opinion Ophtalmol. 2004;15(4):293-8.
5. Becker MD, Smith JR, Max R. Fiehn C. Management of sight-threatening uveitis: new therapeutic options.Drugs. 2005;4:497-519.
6. Sobrin L, Kim EC, Chritsten W. Infliximab therapy for the treatment of refractory ocular inflammatory disease. Arch Ophthalmol. 2007;125(7):893-900.
7. Galor A, Perez VL, Hammel JP, Lowder CY. Differential effectiveness of etanercept and infliximab in the treatment of ocular inflammation. Ophthalmology. 2006;113(12):2317-23.
8. Murphy CC, Ayliffe WH, booth A, Makanjuola D, Andrews PA, Jayne D. Tumor necrosis factor alpha blockade with infliximab for refractory uveitis and scleritis. Ophthalmology. 2004;111(2):352-6.
9. Seo KY, Lee HK, Kim EK, Lee JH. Expression of tumor necrosis factor alpha and matrix metalloproteinase-9 in surgically induced necrotizing scleritis. Ophthalmic Res. 2006;38:66–70.
10. Di Girolamo N, Visvanathan K, Lloyd A, Wakefield D. Expression of TNF-alpha by human plasma cells in chronic inflammation. J Leukoc biol. 1997;61:667–78.
11. Knight DM, Trinh H, Le J, Le J, Siegel S, Shealy D, et al. Construction and initial characterization of a mouse-human chimericanti-TNF antibody. Mol Immunol. 1993;30:1443–53.
12. Sassa Y, Kawano YI, Yamana T, Mashima T, Ishibashi T. A change in treatment from etanerceptto infliximab was effective to control scleritis in a patient with rheumatoid arthritis. Acta Ophthalmol. 2012;90(2):e161–e162.
13. Sen HN, Sangave A, Hammel K, Levy-Clarke G,Nussenblatt Rb. Infliximab for the treatment of active scleritis. Can J Ophthalmol. 2009;44(3):e9-e12.
14. Pulido JS, Goekenl, Nerad JA, Sobol WM, Folberg R. Ocular manifestations of patients with circulating antineutrophil cytoplasmic antibodies. Arch Ophthalmol. 1990;108:845-50.
15. Sasaki R, Taniguchi A, Narita Y, Naito Y, Kuzuhara S. A case optic neuropathy, recurrent transverse myelopathy and hypertrophy pachymeningitis associated perinuclear ANCA. Rinsho Shinkeigaku (Japan J Clin Neurol). 1995;35:513-5.
16. Harada T, Ohashi T, Harada C, Yoshida K, Maguchi S, Moriwaka F, Matsuda H. A case of bilateral optic neuropathy and recurrent transverse myelopathy associated with perynuclear anti neutrophil cytoplasmic antibodies (P-ANCA).J Neuroophtalmol. 1997;17:254-6.
17. Stasi R. An overview of pharmacotherapy foranti-neutrophil cytoplasmic antibody-associated vasculitis. Drugs of Today. 2010;46(12):919-28.
Artículo recibido el 22 de febrero de 2013 y aceptado para publicación el 5 de abril de 2013.
Conflictos de interés: ninguno.
Correspondencia:
Dr. Elmer R. García-Salazar
Servicio de Reumatología, Hospital Nacional Edgardo Rebagliati Martins, EsSalud
Av. Edgardo Rebagliati N° 490, Jesús María, Lima 11, Perú
Teléfono: 51-01-2654901 anexo 3438
Correo electrónico: egasal2003@yahoo.es.













