Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Anales de la Facultad de Medicina
Print version ISSN 1025-5583
An. Fac. med. vol.76 no.2 Lima Apr./Jun. 2015
http://dx.doi.org/dx.doi.org/10.15381/anales.v76i2.11148
CASO CLÍNICO
Adenocarcinoma pulmonar metastásico con evolución favorable al tratamiento con ITK-EGFR en un paciente fumador
Metastatic lung adenocarcinoma favorable outcome with ITK-EGFR treatment in a smoker
Joseph Jesús Exebio Jaraa,b, Roy Nick Cabrera Sandovala,b, Jackeline Karol Amaro Palominoa,b, José Carlos Revilla Lópezc
a Estudiante de Medicina Humana, Facultad de Medicina, Universidad Nacional Mayor de San Marcos, Lima, Perú.
b Miembro, Sociedad Científica de San Fernando (SCSF), Lima, Perú.
c Médico Oncólogo Clínico, Hospital Nacional Daniel Alcides Carrión, Callao, Perú.
Resumen
Introducción: El cáncer de pulmón es el cáncer con mayor mortalidad en ambos sexos. El esquema de manejo actual del adenocarcinoma pulmonar incluye determinar el estado mutacional del receptor del factor de crecimiento epidérmico (EGFR), por ser la diana para el erlotinib, una terapia biológica. Caso clínico: Varón de 62 años, con hábito tabáquico de alto riesgo oncológico, que debuta con un cuadro de cefalea de un mes de evolución, objetivándose por resonancia magnética tumor cerebral. El diagnóstico inmunohistoquímico post quirúrgico fue adenocarcinoma pulmonar metastásico (TTF-1 (+)). La tomografía identificó una lesión en el lóbulo superior derecho del pulmón; no presentaba clínica respiratoria. Al ser positivo para la mutación en el exón 21 del gen EGFR, se inició terapia con erlotinib, siendo bien tolerada por el paciente y manteniendo su estabilidad clínica. El paciente sobrevivió por el lapso de 31 meses posterior a su diagnóstico. Discusión: El tratamiento con erlotinib fue inicialmente indicado en el perfil de una paciente mujer, asiática y no fumadora. La eficacia en los estudios en pacientes con cáncer de pulmón de células no pequeñas evidencia que la sobrevida global es 15,9 meses, muy por debajo del visto en el presente caso.
Palabras clave: Adenocarcinoma de pulmón, factor de transcripción tiroideo-1, receptor del factor de crecimiento epidérmico, erlotinib.
Abstract
Background: Lung cancer has highest mortality in both sexes. Current management of lung adenocarcinoma includes determining epidermal growth factor receptor (EGFR) mutational status as this is the target of erlotinib, a biologic therapy. Case report: A 62 year old male with high smoking cancer risk presented chronic headache for a month, and magnetic resonance showed a brain tumor. Surgical specimen diagnosis was metastatic pulmonary adenocarcinoma by immunohistochemistry (TTF-1 (+)). An asymptomatic lesion in the right upper lobe of the lung was identified by tomography. Due to positivity to EGFR gene exon 21 mutation erlotinib was started; it was well tolerated by the patient. The patient died 31 months after diagnosis. Discussion: Treatment with erlotinib was initially indicated in the profile of an Asian and non-smoker woman patient. The overall survival rate with erlotinib in patients with non-small cell lung cancer is reported as 15.9 months, less time than with our patient, even considering his heavy smoker condition which should have decreased both the chance of having EGFR mutation and response to treatment.
Keywords: Lung adenocarcinoma, thyroid transcription factor-1, epidermal growth factor receptor, erlotinib.
INTRODUCCIÓN
Una de las características distintivas de la evolución natural del carcinoma pulmonar de células no pequeñas (CPCNP) es la muy elevada incidencia de compromiso del sistema nervioso central, en comparación con otras enfermedades malignas; 37% a 55,7% de las metástasis cerebrales provienen de un CPCNP (1).
El factor de crecimiento epidérmico (EGF) y su receptor EGFR han sido relacionados con el proceso de crecimiento y proliferación de las células normales, y se han identificado mutaciones que generan activación constitutiva sobre dicho receptor en CPCNP, principalmente con el perfil de paciente mujer, asiática y no fumadora (2). Actualmente, la terapia biológica dirigida contra estas mutaciones del EGFR es uno de los pilares del tratamiento cuando la mutación está presente, por su acción más específica y consiguientes menores efectos adversos (3).
El presente caso nos muestra a un paciente varón no asiático y fumador pesado con el diagnóstico de adenocarcinoma pulmonar sin clínica respiratoria en estadio clínico IV, que debutó con clínica neurológica por metástasis cerebral y que tuvo buena respuesta al tratamiento con erlotinib.
CASO CLINICO
Paciente varón de 62 años, natural de España, fumador de 30 paquetes/año. Acudió en junio de 2011 al Hospital Nacional Daniel Alcides Carrión con un tiempo de enfermedad de un mes, caracterizado por cefalea y disminución ligera de la fuerza en los miembros inferiores. La resonancia magnética nuclear (RMN) del encéfalo (figura 1) describió un proceso neoformativo intraparenquimal en el lóbulo occipital derecho, que fue intervenido quirúrgicamente con craneotomía más resección y adyuvado con radioterapia (RT) conformacional.
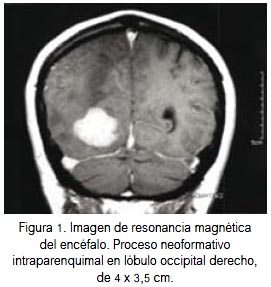
El estudio inmunohistoquímico de la pieza operatoria fue informado como citoqueratina 7 (CK7+), citoqueratina 20- (CK20-), factor de transcripción tiroideo-1 + (TTF-1+) y (antígeno carcinoembrionario + (CEA+); la conclusión fue la de metástasis de adenocarcinoma poco diferenciado primario pulmonar (anatomía patológica en figura 2).
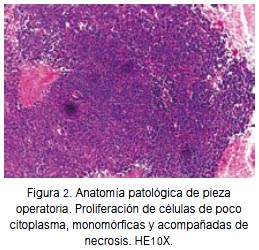
Se evidenció por tomografía axial computarizada (TAC) de tórax de julio de 2011 una lesión espiculada de 4 cm en el lóbulo superior izquierdo (figura 3), diagnosticándose adenocarcinoma en estadio clínico IV, por metástasis cerebral. Se realizó el estudio mutacional del gen EGFR, encontrando una mutación en el exón 21. Se inició el tratamiento con erlotinib 150 mg/día en agosto de 2011. Hubo buena tolerancia al tratamiento, teniéndose como único efecto adverso un rash dérmico de grado I.
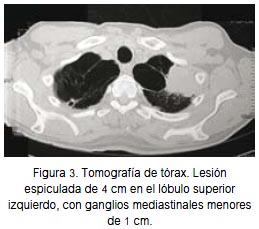
En julio de 2012, el seguimiento evidenció en una RMN del encéfalo la presencia de una nueva neoformación sólida y ovoidea de 3,2 cm que captaba contraste, localizada en la región occipital derecha y compatible con metástasis cerebral única. El paciente fue sometido a nueva cirugía por la recidiva en encéfalo, en agosto de 2012. Se decidió suspender el erlotinib y empezar una nueva RT adyuvante conformacional. Se inició una primera línea de quimioterapia.
En enero de 2013 se inició la segunda línea de quimioterapia por progresión colónica, que continuó hasta el mes de junio, luego de lo cual se indicó la tercera línea de quimioterapia por progresión pancreática.
El paciente tuvo progresión a hilio hepático, en el mes de octubre, produciéndose ictericia obstructiva y dolor oncológico grado 3. En esta situación, el paciente fue catalogado no tributario para el tratamiento quimioterápico con intención curativa y pasó a tratamiento paliativo. El paciente continuó con cuidados paliativos y de enfermería en su vivienda, falleciendo a mediados de diciembre de 2013.
DISCUSIÓN
La terapia biológica es el estándar de primera línea en el CPCNP, entre la que destacan los inhibidores de tirosina quinasa, como el erlotinib. Los estudios OPTIMAL (4) (asiático) y EURTAC (5) (europeo), ambos estudios de fase III, demostraron la superioridad de las terapias moleculares sobre la quimioterapia clásica.
Como cabe suponer, para la instauración de esta terapia biológica se necesita evaluar el estado mutacional del EFGR. El estudio de Arrieta evaluó la frecuencia de mutaciones del EGFR en los diferentes grupos étnicos latinoamericanos (6); se analizó 1 150 biopsias, encontrando que el grupo que presentaba mayor porcentaje de positividad para la mutación del EGFR era la población peruana (Argentina 19,3%, Colombia 24,8%, México 31,2% y Perú 67%).
El paciente del presente caso clínico presentó una mutación en el exón 21 del EGFR (cambio de leucina por arginina en la posición 858 (L858R)). En una investigación nacional, Mas buscó determinar la incidencia de mutaciones en los exones 19 y 21 del gen EGFR en la población peruana estudiando 133 biopsias de adenocarcinoma (7). Se encontró una frecuencia menor de mutaciones en nuestra población (39,3%) en comparación con el estudio latinoamericano, siendo las más frecuentes las mutaciones del exón 19. En este estudio, solo 8,7% mostró mutaciones en el exón 21 del EFGR, como el caso de nuestro paciente.
A propósito, el análisis cinético de estas mutaciones (8) y los estudios retrospectivos (9) han demostrado que las mutaciones del exón 19 son más sensibles a la inhibición de erlotinib que las del exón 21, lo que supondría que nuestro paciente tendría una respuesta pobre.
El estudio PIONEER, primer estudio prospectivo que confirmó altas frecuencias de mutaciones del EFGR (51,4%) en pacientes con adenocarcinoma, demostró que las mutaciones del EGFR se correlacionaron significativamente con el sexo femenino (61,1%) y con no haber fumado (60,7%, disminuyendo conforme aumentaba el índice paquete/ año) (1). Nuestro paciente era un varón fumador empedernido, lo cual escapa del perfil más frecuentemente encontrado. Considerando que un porcentaje importante de pacientes con esta mutación escapan del perfil ‘clásico’ (mujer, asiática y no fumadora), actualmente se considera que se debe evaluar el estado mutacional del EGFR a todo paciente con adenocarcinoma pulmonar, independientemente de las condiciones antes mencionadas (10).
En cuanto a la presentación, nuestro paciente debutó con clínica neurológica (cefalea y paresia de miembros inferiores), encontrándose un adenocarcinoma metastásico cerebral con tumor primario pulmonar. Entre los fumadores, como nuestro paciente, el diagnóstico suele ser precoz y con clínica local más que metastásica (11). Nuestro paciente, por el contrario, no presentaba clínica respiratoria. Debido a esta falta aparente de sintomatología, el paciente acudió en un estadio IV de la enfermedad, ya que en el Perú no existe la cultura de prevención en base al antecedente tabáquico, primando en nuestro país el diagnóstico por presentación clínica sintomática (12).
La presentación metastásica del CPCNP con positividad de la mutación del EGFR más frecuente es la pleural. La metástasis a hueso y cerebro (esta última, como la del caso presentado) también ha sido reportada con alta frecuencia en pacientes con esta mutación (13). Entre los pacientes con CPCNP, aproximadamente 20% a 40% desarrollan metástasis cerebral en algún momento de la evolución (14), presentación más comúnmente entre los no fumadores (11). Aunque nuestro paciente era un fumador empedernido, él presentó una mutación del EGFR, lo cual es compatible con su debut como una metástasis cerebral.
En el relato vemos que, en la evolución del paciente con la terapia molecular (erlotinib), este desarrolló un rash dérmico de grado I. Esta es una reacción adversa común con este tratamiento; se ha encontrado que está presente en 69,6% de los pacientes que reciben erlotinib (2). La literatura, además, describe al rash dérmico después del tratamiento con inhibidores de tirosina quinasa EGFR como un marcador predictivo de buena respuesta y buen pronóstico (15). En el caso presentado, si bien el paciente tuvo esta reacción adversa de baja intensidad, mostró una evolución favorable.
Nuestro paciente presentó una sobrevida de 31 meses. El estudio de la eficacia de los inhibidores de tirosinaquinasa del EGFR (ITK-EGFR) contra las metástasis cerebrales en pacientes con cáncer de pulmón de células no pequeñas evidencia que la sobrevida global en estos pacientes es de 15,9 meses (IC 95% 7,2 a 24,6 meses) (16), que es considerablemente inferior al tiempo de sobrevida global que tuvo nuestro paciente. Posiblemente, debido al debut en estadio clínico IV por metástasis cerebral intervenido oportunamente por neurocirugía y sin clínica respiratoria a pesar de la existencia del primario pulmonar, la evolución de nuestro paciente con el tratamiento biológico fue similar al esperado en un paciente con CPCNP sin metástasis cerebral, cuya mediana se ha estimado en 27 meses (2).
Después de la primera intervención neuroquirúrgica de la metástasis cerebral y posterior radioterapia, el paciente tuvo un tiempo libre de recidiva de 1 año. Esto es compatible con el estudio de Park (16), en el que los pacientes con CPCNP con metástasis cerebral que ingresaban a radiocirugía o seguían radioterapia tenían una mediana de 12,6 meses sin recidiva local.
Otros factores, además de la sola mutación del EGFR, tales como el número de copias genéticas y niveles de expresión de la oncoproteina, deberán ser estudiados para una mejor correlación con la respuesta al tratamiento ITK-EGFR (17). Una explicación de la buena respuesta que presentó nuestro paciente puede estar dada por estas características de la mutación, ya que, como hemos visto en el caso, a pesar de aspectos clínicos aparentemente desfavorables, esto podrá pasar a segundo plano si el perfil de la mutación (perfil que no se estudió en la mutación por las limitaciones logísticas) contribuye a la buena respuesta.
REFERENCIAS BIBLIOGRÁFICAS
1. Shi Y, Au JS-K, Thongprasert S, Srinivasan S, Tsai C-M, Khoa MT, et al. A prospective, molecular epidemiology study of EGFR mutations in Asian patients with advanced non-small-cell lung cancer of adenocarcinoma histology (PIONEER). J Thoraconcol. 2014;9(2):154–62. doi: http://dx.doi.org/10.1097%2FJTo.0000000000000033.
2. Rosell R, Moran T, Queralt C, Porta R, Cardenal F, Camps C, et al. Screening for epidermal growth factor receptor mutations in lung cancer. N Engl J med. 2009;361(10):958–67. doi: http://dx.doi.org/10.1056/nEJmoa0904554.
3. Sebastian M, Schmittel A, Reck M. First-line treatment of EGFR-mutated nonsmall cell lung cancer: critical review on study methodology. Eur Respir Rev. 2014;23(131):92–105. doi: http://dx.doi.org/10.1183/09059180.00008413.
4. Zhou C, Wu Y-L, Chen G, Feng J, Liu X-Q, Wang C, et al. Erlotinib versus chemotherapy as firstline treatment for patients with advanced EGFR mutation-positive non-small-cell lung cancer (OPTIMAL, CTONG-0802): a multicentre, openlabel, randomised, phase 3 study. Lancet oncol. 2011;12(8):735–42. doi: http://dx.doi.org/10.1016/S1470-2045(11)70184-X.
5. Rosell R, Carcereny E, Gervais R, Vergnenegre A, Massuti B, Felip E, et al. Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positivenon-small-cell lung cancer (EURTAC): a multicentre, open-label, randomised phase 3 trial. Lancet oncol. 2012;13(3):239–46. doi: http://dx.doi.org/10.1016/S1470-2045(11)70393-X.
6. Arrieta O, Cardona AF, Federico Bramuglia G, Gallo A, Campos-Parra AD, Serrano S, et al. Genotyping non-small cell lung cancer (NSCLC) in Latin America. J Thorac oncol. 2011;6(11):1955–9. doi: http://dx.doi.org/10.1097/JTo.0b013e31822f655f.
7. Mas L, Torre JG de la, Barletta C. Estado mutacional de los exones 19 y 21 de EGFR en adenocarcinoma de pulmón: Estudio en 122 pacientes peruanos y revisión de la evidencia de eficacia del inhibidor tirosina kinasa erlotinib. Carcinos. 2011;1(2):52–61.
8. Carey KD, Garton AJ, Romero MS, Kahler J, Thomson S, Ross S, et al. Kinetic analysis of epidermal growth factor receptor somatic mutant proteins shows increased sensitivity to the epidermal growth factor receptor tyrosine kinase inhibitor, erlotinib. Cancer Res. 2006;66(16):8163–71. doi: http://dx.doi.org/10.1158%2F0008-5472.cAn-06-0453.
9. Riely GJ, Pao W, Pham D, Li AR, Rizvi N, Venkatraman ES, et al. Clinical course of patients with non–small cell lung cancer and epidermal growth factor receptor exon 19 and exon 21 mutations treated with gefitinib or erlotinib. Clin cancer Res. 2006;12(3):839–44. doi: http://dx.doi.org/10.1158%2F1078-0432.ccR-05-1846.
10. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology. Non-Small cell Lung cancer. 2014.
11. Lee JY, Na II, Jang S-H, Hwang YI, Choe DH, Kim CH, et al. Differences in clinical presentation of non-small cell lung cancer in never-smokers versus smokers. J Thorac Dis. 2013;5(6):758–63.
12. Vigilancia Epidemiológica de cáncer al año 2012. Boletín epidemiológico (Lima). 2012 Dec;21(52):880–2.
13. Mujoomdar A, Austin JHM, Malhotra R, Powell CA, Pearson GDN, Shiau MC, et al. Clinical predictors of metastatic disease to the brain from non–small cell lung carcinoma: primary tumorsize, cell type, and lymph node metastases. Radiology. 2007;242(3):882–8. doi: http://dx.doi.org/10.1148%2Fradiol.2423051707.
14. Na II, Park JH, Choe DH, Lee JK, Koh JS. Association of epidermal growth factor receptor mutations with metastatic presentations in non-small cell lungcancer. ISRN oncol. 2011; 2011:e756265. doi: http://dx.doi.org/10.5402/2011/756265.
15. Liu H, Wu Y, Lv T, Yao Y, Xiao Y, Yuan D, et al. Skin rash could predict the response to egfr tyrosine kinase inhibitor and the prognosis for patients withnon-small cell lung cancer: a systematic review and meta-analysis. PLoS ONE. 2013;8(1):e55128. doi: http://dx.doi.org/10.1371/journal.pone.0055128.
16. Park SJ, Kim HT, Lee DH, Kim KP, Kim S-W, Suh C, et al. Efficacy of epidermal growth factor receptor tyrosine kinase inhibitors for brain metastasis in non-small cell lung cancer patients harboring either exon 19 or 21 mutation. Lungcancer. 2012;77(3):556–60. doi: http://dx.doi.org/10.1016%2Fj.lungcan.2012.05.092.
17. Bhatt VR, Kedia S, Kessinger A, Ganti AK. Brain metastasis in patients with non–small-cell lung cancer and epidermal growth factor receptor mutations. Jco. 2013;31(25):3162–4. doi: http://dx.doi.org/10.1200%2FJco.2013.49.8915.
Artículo recibido el 16 de octubre de 2014 y aceptado para publicación el 3 de marzo de 2015.
Fuente de financiamiento: De los autores.
Conflictos de interés: No existen.
Correspondencia:
Joseph Jesús Exebio Jara
Teléfono: 993390803 (RPC)
Correo electrónico: josephjexebioj@outlook.com














