Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Medicina
versión impresa ISSN 1025-5583
An. Fac. med. vol.77 no.2 Lima abr./jun. 2016
http://dx.doi.org/10.15381/anales.v77i2.11820
ARTÍCULOS ORIGINALES
Interferencia en las determinaciones de 24 constituyentes bioquímicos en el autoanalizador ADVIA 1800, causada por adición in vitro de emulsión comercial de nutrición parenteral a un pool de sueros
Interference in the determination of 24 biochemical constituents in the ADVIA 1800 autoanalyzer caused by in vitro addition of commercial emulsion used in parenteral nutrition to a sera pool
Italo Moisés Saldaña O1
1 Tecnólogo Médico-Químico farmacéutico, Servicio de Bioquímica, Departamento de Patología Clínica, Hospital Nacional Edgardo Rebagliati Martins, EsSalud, Lima, Perú.
Resumen
Introducción. Las interferencias analíticas por turbidez pueden causar errores clínicamente significativos en los resultados de una magnitud biológica. Objetivos. Conocer y cuantificar la posible interferencia producida por la turbidez (lipemia) en la medición rutinaria de 24 constituyentes bioquímicos, empleando para ello el criterio de interferencia clínicamente relevante cuando se supera el máximo error sistemático deseable. Diseño. Estudio experimental con pre y pos-prueba. Institución. Hospital Edgardo Rebagliati Martins, Lima, Perú. Material biológico. Pool de sueros proveniente de muestras procesadas en el laboratorio central del hospital. Intervenciones. Se añadieron cantidades crecientes de una emulsión lipídica comercial de nutrición parenteral a siete diferentes alícuotas de una mezcla de sueros y se determinó en ellas, por triplicado, la influencia del interferente en los 24 constituyentes. Para lo cual se ha seguido el protocolo de la Sociedad Española de Química Clínica. Principales medidas de resultados. Porcentaje relativo de desviación de la concentración del constituyente por influencia de la turbidez, con respecto a una muestra sin interferente. Resultados. Los constituyentes: glucosa, creatinina, potasio, colesterol total, HDL colesterol, fosfatasa alcalina, gammaglutamil transferasa, amilasa y lipasa, no presentaron interferencia en todas las alícuotas con cantidades crecientes del interferente empleado en el ensayo. Se observó interferencia para urea, ácido úrico, proteínas totales, albúmina, bilirrubina total, LDL colesterol, transferrina, fósforo, hierro, láctico deshidrogenasa, aspartato aminotransferasa, alanino aminotransferasa, creatinfosfocinasa, calcio y magnesio. Conclusiones. De los 24 constituyentes estudiados, 15 presentaron interferencia clínicamente significativa. Se recomienda que cada laboratorio investigue los efectos de dicha interferencia empleando sus propios métodos, reactivos o instrumentos.
Palabras clave. Turbidez por Lipemia, interferencia; Error Sistemático Deseable.
Abstract
Introduction. The analytical interference due to turbidity may cause clinically significant errors in the results of biological magnitude. Objectives. To identify and quantify turbidity (lipemia) possible interference in the routine measurement of 24 biochemical constituents using clinically relevant interference criterion when the maximum desirable systematic error is exceeded. Design. Experimental study with pre and post-test. Setting. Hospital Edgardo Rebagliati Martins, Lima, Peru. Biological material: Pooled sera from samples processed at the central laboratory of the hospital. Interventions. Increasing amounts of a parenteral nutrition commercial lipid emulsion were added to seven different aliquots of a pool of sera, and the influence of interference in 24 constituents was determined by triplicate. The Spanish Society of Clinical Chemistry guideline was followed. Main outcome measures. Lipemia-influenced constituent concentration relative percent deviation, compared with a sample without interference. Results. The constituents glucose, creatinine, potassium, total cholesterol, HDL cholesterol, alkaline phosphatase, gamma glutamyl transferase, amylase and lipase showed no interference in all aliquots with increasing concentrations of the assay interference. Interference was observed in urea, uric acid, total protein, albumin, total bilirubin, cholesterol LDL, transferrin, phosphorus, iron, lactate dehydrogenase, aspartate aminotransferase, alanine aminotransferase, creatine phosphokinase, calcium and magnesium. Conclusions. Of the 24 constituents studied, 15 had clinically significant interference. It is recommended that each laboratory investigates the effects of this interference using their own methods, reagents and instruments.
Keywords. Lipemia; Interference; Desirable Bias.
INTRODUCCIÓN
Las interferencias analíticas pueden causar errores clínicamente significativos en los resultados de una magnitud biológica, lo que conduce a establecer diagnósticos equivocados, aplicar tratamientos innecesarios o potencialmente desfavorables para los pacientes; además, conlleva a los laboratorios clínicos a gastos extras de reactivos, un mayor desgaste de equipos y demora en la emisión de resultados (1).
La interferencia analítica es considerada como la desviación clínicamente significativa en la medida de la concentración de un constituyente, debido al efecto de otro componente o propiedad de la muestra (1,2).
Tradicionalmente, la lipemia se define como la turbidez en las muestras de suero o plasma, producida por acumulación de partículas de lipoproteínas, especialmente las de densidad muy baja (VLDL) y los quilomicrones que son ricos en triglicéridos (3).
A diferencia de la hemólisis, que es desfavorables para los pacientes; ade-efecto de otro componente o propiedad reconocida como una de las principamás, conlleva a los laboratorios clínicos de la muestra (1,2). les causas de errores preanalíticos, la interferencia por lipemia es a menudo ignorada; existen pocos estudios que estimen este tipo de interferencia.
La prevalencia de muestras lipémicas en los laboratorios clínicos oscila entre 0,5 y 2,5%. Esta prevalencia depende del tipo de hospital y la proporción de pacientes internos y ambulatorios que son atendidos en el centro hospitalario (3,4).
Entre las causas más frecuentes de la ocurrencia de muestras lipemicas en el laboratorio se encuentran: el insuficiente tiempo entre la ingesta de alimentos y la obtención de muestra sanguíneas, algunas enfermedades metabólicas como la diabetes mellitus, hipertrigliceridemia, insuficiencia renal crónica, hipotiroidismo, pancreatitis, mieloma múltiple, cirrosis biliar primaria o lupus eritematoso, la obtención de muestras sanguíneas después de infusión intravenosa con emulsiones lipídicas para nutrición parenteral, la ingestión de alcohol y fármacos como los inhibidores de proteasa (infección por el VIH), estrógenos, anticonceptivos orales, entre otros (4).
La lipemia puede producir interferencia en la determinación de los constituyentes bioquímicos por tres mecanismos: a) puede causar una interferencia espectral, porque absorbe y dispersa la luz en un amplio rango de longitudes de onda; b) la fracción acuosa del plasma puede disminuir como consecuencia del elevado volumen de la fracción lipídica, originando valores bajos en la concentración de diversos constituyentes; y c) los lípidos, por su naturaleza hidrofóbica, pueden disolver en su interior analitos, reactivos o productos de la reacción, ocasionando errores en la medida de algunas magnitudes (4,5).
Existen varios criterios para establecer el límite de error máximo admisible para este tipo de interferencia. La mayoría de proveedores de reactivos consideran una interferencia por lipemia significativa cuando el resultado de la muestra con interferente se desvía en 10%. Este criterio es más permisivo en las magnitudes con pequeña variabilidad biológica y puede ser menos permisivo en aquellas con elevada variabilidad intraindividual o interindividual (5,6).
La Organización Mundial de la Salud, con sustentación en las recomendaciones de la Sociedad Alemana de Química Clínica, define interferencia clínicamente relevante cuando se supera el error sistemático deseable (6).
El objetivo central del presente estudio fue conocer y cuantificar la posible interferencia producida por la turbidez (lipemia) en la medición rutinaria de 24 constituyentes bioquímicos, empleando para ello el criterio de interferencia clínicamente relevante cuando se supera el máximo error sistemático deseable.
MÉTODOS
Los 24 constituyentes investigados: glucosa (método de hexocinasa), urea (método de ureasa con glutamato deshidrogenasa), creatinina (método enzimático/ creatininasa), ácido úrico (método de uricasa/peroxidasa), proteínas totales (método de Biuret), albúmina (método de unión al colorante verde de bromocresol), bilirrubina total (método de oxidación por vanadato), colesterol total (método de colesterol oxidasa/Trinder), HDL colesterol (método de eliminación/ catalasa. Directo), LDLc (método de eliminación/catalasa. Directo), transferrina (método inmunoturbidimétrico con polietilenglicol), potasio (método de potenciometría indirecta), calcio (método de o-cresolftaleìna complexona), fósforo (método de fosfomolibdato UV), magnesio (método de azul de xilidilo), hierro (método de ferrocina), lactato deshidrogenasa (LDH) (método de Lactato/NAD+), creatina cinasa (CK) (método de la Federación Internacional de Química Clínica (IFCC) activado con N- acetil-L- cisteína), aspartato aminotransferasa (AST) (método de la IFCC modificado), alanina aminotransferasa (ALT) (método de la IFCC modificado), fosfatasa alcalina (FAL) ( método de la IFCC con tampón 2-amino-2-metil- 1-propanol), gamma glutamil transferasa (GGT) (método de L. M. Shaw y cols. usando L-g-glutamil-3-carboxi4-nitroanilida), amilasa (método del p-nitrofenil-maltoheptaósido bloqueado con etilideno), lipasa (método cinético colorimétrico / metilresorufina), fueron valorados en el analizador ADVIA1800 con reactivos y calibradores de SIEMENS®. Los métodos analíticos se realizaron según las indicaciones del fabricante.
El analizador fue calibrado previo al estudio, de acuerdo a las recomendaciones del fabricante. El programa de control de calidad interno incluyó la evaluación de sueros controles BIORAD® de dos niveles de decisión (nivel 1 y nivel 2), pertenecientes a los lotes 14441 y 14442 respectivamente, los que fueron procesados diariamente, y una muestra mensual de un control de calidad externo internacional (RIQAS), con lote de referencia RQ9128 ciclo 12B.
Se realizó un estudio experimental con pre y pos-prueba, donde se comparó el valor medido de la magnitud en una muestra sin interferente con los valores obtenidos cuando se adicionaron a la misma muestra cantidades crecientes del interferente. Se siguió el protocolo de la Comisión de Metrología y Sistemas Analíticos de la Sociedad Española de Química Clínica (5).
Para la solución concentrada del interferente se utilizó la emulsión comercial para nutrición parenteral SMOFlipid® al 20%, la que contiene triglicéridos de cadena media y ácidos grasos esenciales (7).
Para el suero base, se recolectó 25 mL de un pool de sueros libres de hemólisis, lipemia o ictericia, los que provenían de muestras procesadas en el laboratorio central del Hospital Edgardo Rebagliati Martins de EsSalud, Lima, Perú.
En la preparación de las diluciones con el interferente, de manera de conseguir varios grados de turbidez se añadieron cantidades crecientes de la emulsión comercial SMOFlipid® a siete alícuotas diferentes del pool de sueros (suero base). En esta preparación, la mezcla libre de interferente se igualó en volumen a las alícuotas con interferente mediante la utilización de agua destilada, para evitar el error por dilución. Se obtuvo siete alícuotas con intensidades crecientes de turbidez y una basal sin interferente.
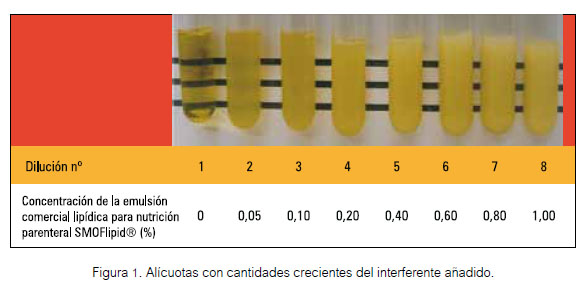
Luego de las respectivas diluciones en las alícuotas, las concentraciones de emulsión comercial resultaron ser: 1º 0 %, 2º 0,05%, 3º 0,1%, 4º 0,2%, 5º 0,4%, 6º 0,6%, 7º 0,8% y 8º 1% (Figura 1).
Cada una de las diluciones fue analizada por triplicado de forma independiente, y pudo determinarse de esta forma el porcentaje de variación en la concentración de cada constituyente en función del incremento en el grado de lipemia de las muestras.
La evaluación de las interferencias se realizó mediante el método de Glick y col (8), expresándose los resultados como un porcentaje del resultado original. Para ello, se hizo una representación gráfica de esta relación mediante un interferograma, en la que se representó (C/CO) x100 frente a la concentración del interferente de cada alícuota, donde (CO) fue la concentración inicial sin interferente y (C) la concentración medida experimentalmente del constituyente en estudio.
Las interferencias fueron compararon con las actuales especificaciones de calidad analítica para el máximo error sistemático deseable (MESD), provenientes de la base de datos que compila artículos publicados hasta diciembre de 2013 sobre los componentes de la variación biológica en personas sanas, e incluye 357 magnitudes biológicas con las especificaciones de la calidad analítica (deseable, mínima y óptima), actualizada al año 2014 (9,10).
Se consideró a la interferencia como clínicamente relevante cuando era superior al MESD.
RESULTADOS
Basándonos en el criterio de la Organización Mundial de la Salud de que existe interferencia significativa cuando se supera el error sistemático deseable (6), encontramos interferencia clínicamente relevante en 15 de los 24 constituyentes estudiados.
Destaca en nuestros resultados, el nulo efecto que causó la turbidez por lipemia en todas las alícuotas con cantidades crecientes de la emulsión empleada, en la medición de glucosa, creatinina, potasio, colesterol total, HDL colesterol, fosfatasa alcalina, gammaglutamil transferasa, amilasa y lipasa.
Encontramos interferencia en la medición de urea, ácido úrico, proteínas totales, albúmina, bilirrubina total, LDL colesterol, transferrina, fósforo, hierro, láctico deshidrogenasa, aspar-tato aminotransferasa, alanino aminotransferasa, creatinfosfocinasa, calcio y magnesio.
Hay que indicar que la actividad de las enzimas aspartato aminotransferasa y alanino aminotransferasa en la última alícuota no se pudo determinar, debido a que estos valores estarían por debajo del límite de detección del analizador bioquímico.
La imprecisión expresada en términos de coeficiente de variación presentó un valor mínimo de 0% y máximo de 3,02% para todos los constituyentes analizados por triplicado.
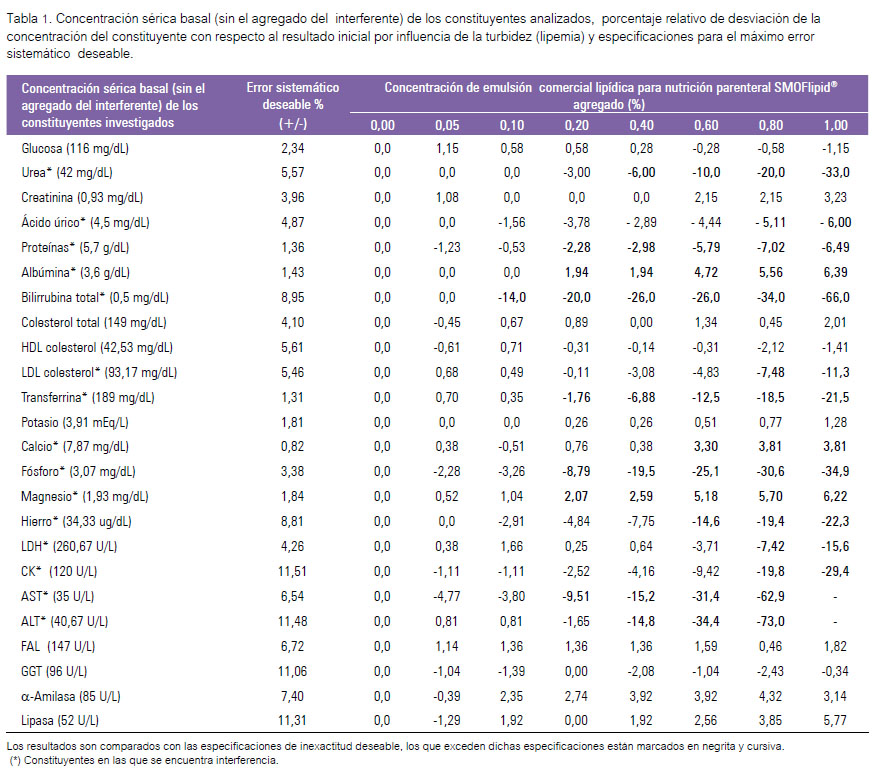
En la tabla I, se muestra los constituyentes analizados, la concentración sérica basal (sin el agregado del interferente) de los constituyentes en estudio, los porcentajes relativos de desviación de la concentración del constituyente con respecto al resultado inicial y las especificaciones de calidad analítica para el máximo error sistemático deseable.
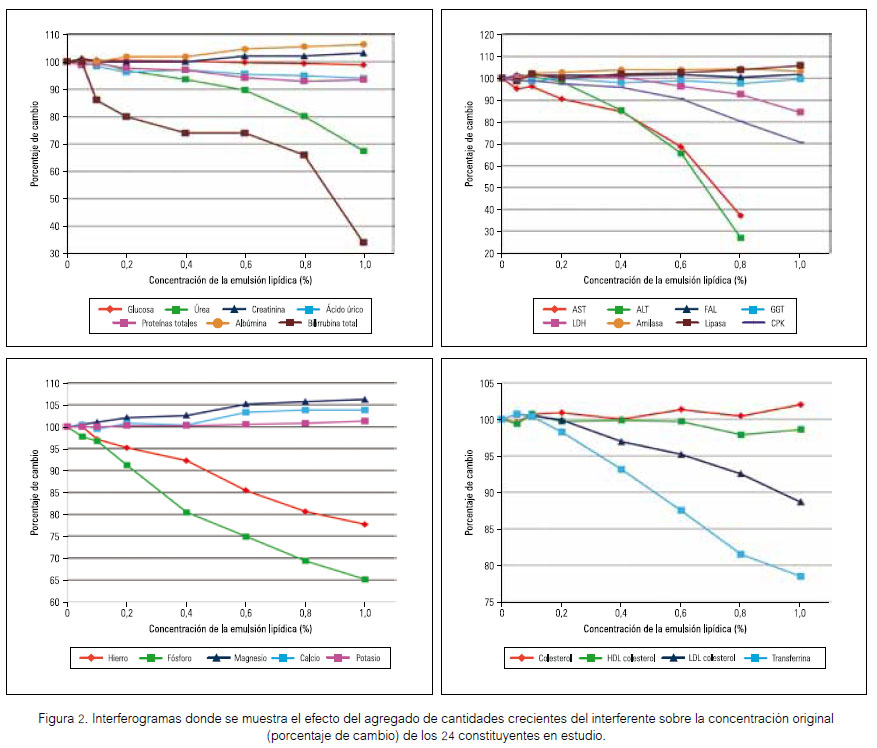
En la Figura 2 se representa los interferogramas (8), donde se aprecia el efecto de la adición de cantidades crecientes del interferente sobre la concentración de los analitos estudiados.
DISCUSIÓN
La interferencia analítica por lipemia es un problema que afecta a todos los laboratorios clínicos. Siempre se cuestiona la exactitud de los resultados cuando se analiza este tipo de muestras. La solución no solo está en añadir comentarios como ‘muestra lipémica’ a los reportes de laboratorio. Es importante también conocer el signo posible de dicha interferencia y la mínima cantidad de interferente responsable de errores significativos en los resultados.
Los primeros estudios publicados sobre interferencia en muestras biológicas consideraban como interferencia significativa un 10% de variación sobre el resultado de la muestra sin interferente. Este criterio es utilizado por muchos fabricantes en sus estudios de evaluación (5,6). Nuestros resultados indican que, si hubiéramos utilizado dicho criterio, algunos constituyentes, como el ácido úrico, proteínas totales, albúmina, calcio y magnesio, no hubieran sido detectados como sensibles a la presencia del interferente. Estos resultados son avalados por Nikolac (11), quien demostró que la información brindada por los fabricantes con respecto a la interferencia por lipemia no siempre es confirmada en la práctica. Proponemos que, en lugar de límites arbitrarios, los fabricantes utilicen las especificaciones de calidad basadas en la evidencia para evaluar los sesgos permisibles. Por otra parte, los laboratorios deben ser conscientes de la posible falta de replicabilidad de las declaraciones de los fabricantes.
La interferencia descrita en nuestro estudio para el calcio fósforo, hierro, magnesio albumina, urea, ácido úrico, proteínas totales y albumina no coinciden con los resultado de Ji y Meng (12) quienes, utilizando el analizador COBAS 6000 de Roche y el criterio de 10% de variación del resultado con respecto a la muestra sin interferente, no encontraron interferencia para los constituyentes antes mencionados.
Es posible que la dirección y el grado de interferencia sean diferentes cuando se comparan diferentes métodos para el mismo parámetro. Esto fue confirmado por Nikolac (11), quien investigó la influencia de la lipemia utilizando reactivos y plataformas analíticas de tres fabricantes. Sus resultados para el caso específico de la bilirrubina fueron una interferencia con aumento aparente del constituyente para el analizador Dimensión Vista System de Siemens, utilizando un método de diazo-reacción, además de una interferencia con una disminución aparente de la bilirrubina para el Cobas 6000 de Roche y una interferencia nula para el analizador Beckman Coulter, empleando la técnica de diclorofenil-diazonio–tetrafluoroborato. Nosotros, empleando el método de oxidación química de la bilirrubina por la acción del vanadato, encontramos una notoria interferencia que se tradujo en una disminución aparente para este constituyente.
La interferencia espectral es probablemente el mecanismo más común en que la lipemia afecta los resultados de las pruebas de laboratorio. La cantidad de luz absorbida por las partículas de lipoproteínas es inversamente proporcional a la longitud de onda. Por lo tanto, los métodos que utilizan longitudes de ondas cortas son los más afectados debido a que la absorbancia es más alta en esa parte del espectro. Diversos métodos en química clínica utilizan la conversión del NAD+ y NADH medida a 340 nanómetros como reacción indicadora para determinar la concentración o actividad de cierto analito. La mayoría de estos métodos son fuertemente afectados por la lipemia (4). Esto explicaría la interferencia hallada en el presente estudio para láctico deshidrogenasa, aspartato aminotransferasa, alanino aminotransferasa y creatinfosfocinasa.
El uso de sueros de pacientes para el estudio de este tipo de interferencia imita mejor el proceso fisiopatológico de la lipemia. Sin embargo, su uso no es lo ideal, debido a la heterogeneidad de las muestras de suero. La composición de las partículas de lipoproteínas difiere en dos muestras lipémicas; tal estudio apenas podría ser replicado. Para tal efecto se recomienda el empleo de sueros lipémicos inducidos con emulsiones comerciales para nutrición parenteral. La desventaja de su empleo es que estas emulsiones solo poseen lípidos de tamaño de 200 a 600 nanómetros (nm) y no de 50 a 1 000 nm, como son los lípidos nativos (4,11,13).
La mayoría de los actuales autoanalizadores tienen la capacidad de detectar la lipemia en las muestras de suero mediante unos índices séricos que se correlacionan linealmente con las concentraciones del interferente. Los índices pueden ser usados para detectar la interferencia generando unas tablas de tolerancia, con unos índices de decisión que nos indican la presencia de interferencia (4,11,13,14,17).
La causa más común de la ocurrencia de muestras lipémicas es el insuficiente tiempo entre la ingesta de alimentos y la obtención de la muestra sanguínea. Existe heterogeneidad en las definiciones de ‘ayuno’ que actualmente se utiliza entre los trabajadores de la salud y en la literatura. Se recomienda la estandarización de los requisitos de toma de muestras sanguíneas en los centros hospitalarios (4,13,15).
Es interesante notar que metodologías teóricamente idénticas o muy semejantes brinden resultados distintos ante la presencia de turbidez, lo que nos indicaría que el análisis de interferencia aquí realizado no puede ser generalizado para otros reactivos o equipos. Es recomendable que cada laboratorio investigue los efectos de dicha interferencia empleando sus propios reactivos, métodos o instrumentos (11,16).
En conclusión, la interferencia por lipemia es una importante fuente de errores de laboratorio. Cada laboratorio debe ser consciente de la influencia que la lipemia tiene sobre los resultados de las pruebas de laboratorio. La verificación de las afirmaciones del fabricante debe realizarse en los laboratorios basándose en la evidencia de criterios de aceptación. Además, debe describirse los procedimientos para su detección, con el fin de estandarizar los procedimientos, reducir los errores y aumentar la seguridad del paciente.
AGRADECIMIENTOS
A los estudiantes de pregrado de Tecnología Médica Carlos Flórez Butrón y Gustavo Jaimes Huamán, por sus aportes en el desarrollo de la presente investigación.
REFERENCIAS BIBLIOGRÁFICAS
1. Castaño J. Estudio de las interferencias analíticas endógenas en química clínica. Quím Clín. 1994; 13:84-92. [ Links ]
2. Comisión de Interferencias y Efectos de los Medicamentos SEQC. Errores relacionados con el laboratorio clínico. Quím Clín. 2007; 26 (1):23-8. [ Links ]
3. Lippi G, Becan-Mcbride K, Behúlová D, Bowen RA, Church S, et al. Preanalytical quality improvement: in quality we trust. Clin Chem Lab Med. 2013;51(1):229-41. doi: 10.1515/cclm-2012-0597. [ Links ]
4. Nikolac N. Lipemia: causes, interference mechanisms, detection and management. Biochemia Medica. 2014; 24(1):57-67. doi: 10.11613/ bM.2014.008. [ Links ]
5. Sociedad Española de Bioquímica Clínica y Patología Molecular. Procedimiento para el estudio de la interferencia por hemólisis, bilirrubina y turbidez y para la verificación de los índices de hemólisis, ictericia y lipemia. Comisión de Metrología y Sistemas analíticos. Documento Técnico, 2013. [ Links ]
6. Gómez R, Alsina MJ, Álvarez V, Barba N, et al. Hemólisis en las muestras para diagnóstico. Rev Lab clin. 2009; 2(4):185-95. doi: 10.1016/j. labcli.2009.08.002 [ Links ]
7. Smoflipid 20% aceite de soja, triglicéridos de cadena media, aceite de oliva, aceite de pescado. Disponible en: http://www.fresenius-kabi.com.ar/pdf/ smoflipid_20.pdf. Consultado el 10 de julio 2015. [ Links ]
8. Glick MR, Ryder KW, Jackson SA. Graphical comparisons of interferences in clinical chemistry instrumentation. Clin Chem. 1986; 32:470-5. [ Links ]
9. Ricós C, García Lario JV, Álvarez V, Cava F, Doménech MV, Hernández A, et al. Biological variation database. The 2014 update. [ consultado 8/7/2015]. Disponible en: http://www. westgard.com/biodatabase1.htm. [ Links ]
10. Sociedad Española de Bioquímica Clínica y Patología Molecular. Comité de garantía de la Calidad y Acreditación de Laboratorios. Comisión de calidad Analítica. Base de datos De variación biológica. Actualización del año 2014: Disponible en http:// www.seqc.es/es/Sociedad/51/102. [ Links ]
11. Nikolac N, Simundic AM, Miksa M, Lima-Oliveira G, Salvagno GL, Caruso B, Guidi GC. Heterogeneity of manufacturers declarations for lipemia interference - urgent call for standardization. Clin Chim Acta. 2013; 426:33-40. doi: 10.1016/j.cca.2013.08.015. [ Links ]
12. Ji JZ, Meng QH. Evaluation of the interference of hemoglobin, bilirubin, and lipids on Roche Cobas 6000 assays. Clin Chim Acta. 2011; 412:1550-3. doi: 10.1016/j.cca.2011.04.034. [ Links ]
13. Kroll MH. Evaluating interference caused by lipemia. Clin Chem. 2004; 50:1968-9. [ Links ]
14. García Aguilar GD, Pico Picos MA, Quintana Hidalgo L, Cabrera Argany A, Lorenzo Medina M, Aguilar Doreste JA. Utilidad de los índices séricos para la valoración de las interferencias causadas por la hemólisis y la bilirrubina en la medición de distintos constituyentes bioquímicos. Quím Clín. 2007; 26:196-201. [ Links ]
15. Simundic AM, Cornes M, Grankvist K, Lippi G, Nybo M. Standardisation of collection requirements for fasting samples. For the Working Group on Preanalytical Phase of the European Federation of Clinical Chemistry and Laboratory Medicine. Clin Chim Acta. 2014 May 15; 432:33-7. doi: 10.1016/j. cca.2013.11.008. [ Links ]
16. Calmarza P, Cordero J. Lipemia interferences in routine clinical biochemical test. Biochem Med. 2011; 21(2):160-6. [ Links ]
17. Simundic AM, Nikolac N, Ivankovic V, Ferenec-Ruzic D, Magdic B, Kvaternik M, Topic E. Comparison of visual versus automated detection of lipemic, icteric and hemolyzed specimens: can we rely on a human eye? Clin Chem Lab Med. 2009; 47:1361-5. doi: 10.1515/ccLM.2009.306. [ Links ]
Artículo recibido el 24 de setiembre de 2015 y aceptado para publicación el 18 de enero de 2016.
Conflicto de interés: El autor refiere que no existe conflicto de interés con el presente artículo.
Correspondencia: Italo Moisés Saldaña Orejón. Correo electrónico: imso_biochemical@yahoo.es