Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Medicina
versión impresa ISSN 1025-5583
An. Fac. med. vol.78 no.1 Lima ene./mar. 2017
http://dx.doi.org/10.15381/anales.v78i1.13015
http://dx.doi.org/10.15381/anales.v78i1.13015
ARTÍCULOS ORIGINALES
Infección del tracto urinario en receptores de trasplante renal
Urinary tract infection in renal transplant recipients
Pedro Méndez Chacón1,2, Fernando Bardales Viguria2, Ángel Ardiles Aniceto2, Carlos Cervera Álvarez3, Carla Méndez Chacón Rodriguez4, Armando Vidalón Fernández1,2
1 Profesor Principal, Facultad de Medicina Humana, Universidad Nacional Mayor de San Marcos, Lima, Perú.
2 Médico Asistente, Departamento de Nefrología, Hospital Nacional Edgardo Rebagliati Martins, EsSalud, Lima, Perú.
3 Profesor Asistente, División de Enfermedades Infecciosas, Departamento de Medicina, Universidad de Alberta, Edmonton, Canadá.
4 Médico Asistente, Servicio de Patolología Clínica, Instituto Nacional Del Niño, Lima ,Perú.
Resumen
Introducción. La infección del tracto urinario (ITU) es común en receptores de trasplante renal (TR). La frecuencia de ITU depende de factores previos y posteriores al trasplante. Objetivos. Determinar la cronología de aparición de ITU sintomática, los microorganismos causantes y la incidencia de ITU resistente a antibióticos en receptores de TR. Diseño. Estudio retrospectivo. Lugar. Unidad de Trasplante Renal, Hospital Edgardo Rebagliati Martins, EsSalud, Lima, Perú. Participantes. Pacientes sometidos a TR. Intervenciones. Se revisó la historia clínica de 304 pacientes sometidos a TR en el período 2002-2011, con seguimiento de hasta cuatro años por paciente. Se constató 215 episodios de ITU sintomática confirmada mediante urocultivo en 84 receptores. Principales medidas de resultados. Incidencia, cronología, determinación microbiológica/susceptibilidad, resistencia bacteriana, factores de riesgo, estrategias diagnósticas, presencia o no de bacteriemia y manejo terapéutico. Resultados. En 50% de los 84 receptores el episodio inicial ocurrió durante los primeros tres meses, y en 39% se constató más de un episodio de ITU. Las bacterias representaron la etiología más frecuente (94%), siendo la Escherichia coli (77%) el uropatógeno prevalente, con tasa productora betalactamasa espectro extendido (BLEE) en 38%, seguida de Klebsiella pneumonie (11%) con BLEE 65%. En 12% de los 215 episodios de ITU el hemocultivo fue positivo. Entre los factores de riesgo se detectó luego del trasplante 19% receptores con anormalidades anatómicas del tracto urinario. Conclusiones. La ITU ocurrió tempranamente luego del trasplante y la Escherichia coli fue el microorganismo etiológico más frecuente. La resistencia antibiótica estuvo presente en 37% de los 215 episodios de ITU, representando un desafío contínuo a resolver en la práctica clínica.
Palabras clave. Bacteriuria Asintomática; Pielonefritis; Tracto Urinario; Trasplante Renal.
Abstract
Introduction. Urinary tract infections (UTI) are common among renal transplant recipients (RTR) and their frequency depends on pre- and post-transplant factors. Objectives. To determine the time of appearance of symptomatic UTI among renal transplant recipients, microorganisms causing the infection, and incidence of UTI resistant to antibiotics. Design. Retrospective study. Setting. Renal Transplant Unit, Hospital Edgardo Rebagliati Martins, EsSalud, Lima, Peru. Participants. Patients who have undergone renal transplantation. Interventions. The clinical records of 304 patients subject to kidney transplantation performed between 2002 and 2011 and followed for up to four years were reviewed. There were 215 urine culture-confirmed UTI episodes in 84 transplant recipients. Main outcome measures. Incidence, chronology, microbiological determination/ susceptibility, bacterial resistance, risk factors, diagnostic strategies, presence or absence of bacteremia, and therapeutic management. Results. In 42 of the 84 recipients, the initial episode occurred during the first three months, and 33 (39%) had more than one UTI episode. Bacteria represented the most common etiology (94%), and Escherichia coli was the most prevalent uropathogen, with an extended-spectrum beta-lactamase (ESBL) production rate of 38%, followed by Klebsiella pneumoniae (11%) with an ESBL of 65%. Blood culture was positive in 25 (12%) of the 215 UTI episodes. In 17 recipients (19%), anatomic anomalies of the urinary tract were detected following the transplant. Conclusions. UTI occurred early following kidney transplantation, and Escherichia coli was the most common microorganism found. Antibiotic resistance was present in 79 (37%) of the 215 UTI episodes, representing a continuous challenge in clinical practice.
Keywords. Asymptomatic Bacteriuria; Urinary Tract; Pyelonephritis; Renal Transplantation.
INTRODUCCIÓN
El rechazo agudo y las infecciones constituyen dos barreras importantes a vencer para el éxito temprano de los trasplantes de órganos. A partir del año 1992, se constató que las hospitalizaciones debido a infecciones eran cada vez más frecuentes que las ocasionadas por rechazo agudo(1). La localización más común de infección post trasplante en general está relacionada a la herida operatoria, seguida de las infecciones urinarias(2). Aun cuando existen significativos avances en la técnica quirúrgica y en la profilaxis antimicrobiana, la incidencia de infecciones urinarias (ITU) permanece elevada(3). Los estudios retrospectivos evidencian que la frecuencia de ITU en los receptores de trasplante renal (TR) es mayor que en la población general, sobretodo durante el primer mes postoperatorio. El porcentaje de ITU en TR oscila entre 4% y 74%(4), siendo la Escherichia coli y los enterococos los patógenos bacterianos más frecuentes, superando el 50% de las ITU(4). Desde 1983, se describe cepas BLEE que afectan la respuesta a la antibioticoterapia (5). La resistencia bacteriana actualmente representa un serio problema de salud global (6). Un evento no menos importante está constituido por las infecciones recurrentes del tracto urinario, complicación a prevenir en esta clase de pacientes.
El presente estudio analiza la inciden cia, cronología, microbiología y perfil de susceptibilidad, resistencia bacteriana, factores de riesgo de recurrencia y evaluación del pronóstico, con miras a implementar estrategias de diagnóstico y manejo terapéutico.
MÉTODOS
Este estudio es retrospectivo, mediante revisión de las historias clínicas de 304 de nuestros pacientes trasplantados renales en el período 2002 a 2011, hasta un lapso de cuatro años por cada paciente. Se enfatizó el estudio de aquellos casos con diagnóstico de cistitis y/o pielonefritis aguda y urocultivo positivo (microbiología y susceptibilidad), además del análisis de la presencia o no de bacteriemia concomitante, urianálisis, cuadro clínico al momento del urocultivo, tipo de tratamiento y rechazo agudo coincidente en el mes de la bacteriuria. Se excluyó las bacteriurias asintomáticas y las ITU sintomáticas con urocultivo negativo.
Las otras variables epidemiológicas evaluadas fueron la duración del trasplante, tipo de donante, edad del receptor, género, etiología de la enfermedad renal crónica terminal, tipo y tiempo de diálisis pretrasplante, función demorada del injerto, profilaxis antibiótica, complicaciones urológicas post trasplante, niveles de creatinina sérica, terapia inmunosupresora al momento del cultivo, pérdida o no del injerto y fallecimiento del paciente si fuera el caso.
Se evaluó adicionalmente la existencia de malformaciones urológicas previas al trasplante, como reflujo vesicoureteral, enfermedad poliquística renal, uropatía obstructiva y otros.
Algunos pacientes tuvieron inserción de stent ureteral doble J siliconado durante el intraoperatorio, que fue removido en dos a tres semanas del trasplante. La sonda vesical usualmente fue retirada del 5° al 10° día del postoperatorio, dependiendo de la calidad de la vejiga y del urocultivo correspondiente. La profilaxis de la infección urinaria se efectuó en base a trimetropim-sulfametoxazol (80/400) diariamente durante los tres primeros meses. El diagnóstico clínico de infección urinaria se basó en la presencia de bacteriuria (más de 100 000 colonias/ mL de orina) y examen de orina sugerente (leucocituria con más de 10 leucocitos/ campo, estearasa positiva y/o positividad de nitritos) asociado a síntomas clínicos (fiebre, injertalgia, polaquiuria, disuria).
Se consideró episodio exitosamente tratado cuando la piuria y bacteriuria desaparecieron en el seguimiento de control y sin recurrencia de bacteriuria con el mismo patógeno, durante un período de tres semanas.
RESULTADOS
Durante el período de estudio de cuatro años máximo por paciente se consignó ITU bacteriana post trasplante en 84 (28%) de los 304 receptores. Esta población seleccionada presentó en total 215 episodios de infección urinaria; 51 pacientes cursaron con un solo episodio de ITU, nueve con dos, 11 con tres, cinco con cuatro y tres pacientes con más de 10 episodios.
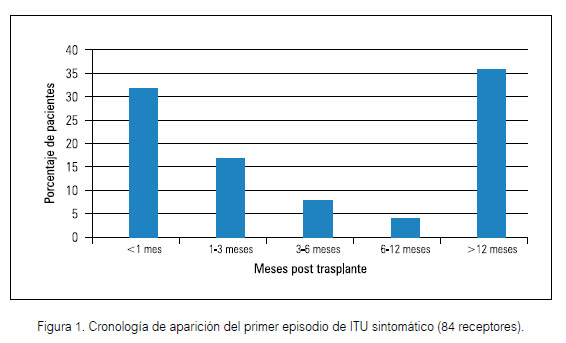
La mayoría de los episodios de ITU ocurrió dentro los primeros tres meses del post trasplante (en 42 de los 84 receptores), con predominancia en el primer mes, observándose luego apreciable declinación (Figura 1).
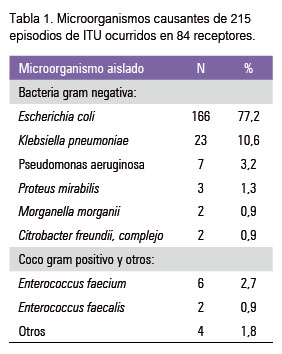
Las bacterias entéricas gram negativas fueron responsables del 94% de las ITU, siendo la Escherichia coli (77 %) y la Klebsiella pneumoniae (11%) las predominantes (Tabla 1).
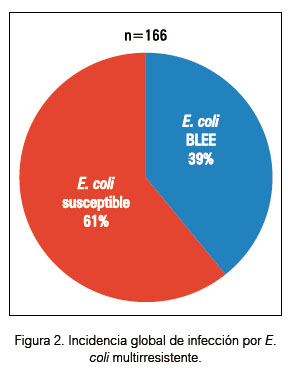
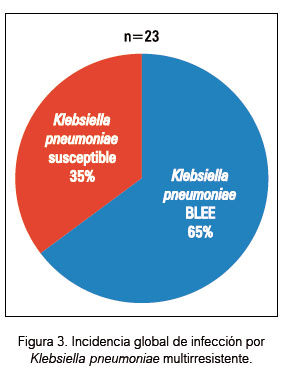
Del total de 215 cepas bacterianas aisladas en las ITU, 79 (37%) fueron multidrogo resistentes (por lo menos a 3 clases de antibióticos de amplio espectro) y productoras de BLEE; la Klebsiella pneumoniae ofreció la mayor tasa de resistencia 65% (15 de 23 cepas), seguida de la E.coli 38% (64 de 168 cepas) (figuras 2 y 3).
DISCUSIÓN
La incidencia de rechazo agudo en trasplante renal ha disminuido significativamente en los últimos años a cifras menores del 15%(7), como lo advertido también en nuestra unidad de trasplante renal (UTR), 13% (año 2011), consecuencia del advenimiento y uso de potentes inmunosupresores. Sin embargo, esta mayor inmunosupresión ha devenido paralelamente en aumento de las tasas de infección, tanto así que probablemente no haya paciente que presente al menos un episodio de infección en la etapa evolutiva post trasplante(7). Regularmente observamos que las hospitalizaciones por infecciones en la UTR exceden largamente a los episodios inmunológicos(8).
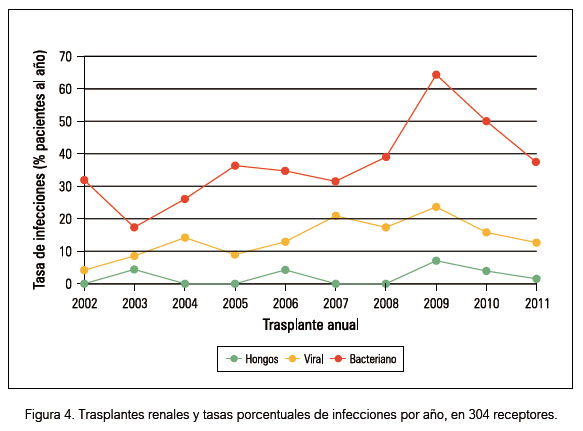
Por tanto, las infecciones permanecen como la mayor causa de morbimortalidad en los receptores de trasplante de órganos(3). En el análisis de nuestra casuística período 2002 a 2011 (Figura 4), a diferencia de las infecciones virales y micóticas, la tasa de infección bacteriana tuvo mayor incidencia durante el primer año post trasplante, cursando con oscilaciones anuales de 18% a 64%, siendo la ITU la localización más frecuente (73%) seguida del tracto respiratorio (7%). Al igual que en otras series, la ITU bacteriana representa la complicación más común de infecciones post trasplante renal y en porcentajes que fluctúan entre 16% a 79%(3,5,9-13), amplitud debida probablemente a la falta de criterio único de diagnóstico, profilaxis diversa de antibióticos, terapia de inmunosupresión y duración del seguimiento(3). Para este reporte seleccionamos 84 receptores con ITU bacteriana sintomática confirmada mediante urocultivo(12). El trasplante renal es un procedimiento susceptible de contaminación debido a la manipulación de la vejiga, la cual es expuesta para realizar la anastomosis uretero–vesical y que podría estar previamente infectada como resultado de orina residual estancada(14).
Se ha demostrado que la vejiga de los pacientes con enfermedad renal crónica terminal está colonizada por diversos patógenos (15), predisponiendo al riesgo de infecciones urinarias hasta cuatro veces mayor en el post trasplante (16), aun cuando la frecuencia global de ITU experimentó declinación gracias a la mejor técnica quirúrgica y adecuada profilaxis antimicrobiana (17). En nuestra investigación, 42 (50%) de los 84 receptores inició episodios de ITU durante los primeros tres meses del post trasplante y mayormente durante el primer mes (Figura 1), con porcentaje alto como si el paciente no hubiese recibido profilaxis antibiótica(10). Este período inicial es considerado crítico por la alta dosis de inmunosupresores y/o por intervenciones urológicas recientes, como la colocación del stent ureteral además de la sonda Foley vesical(15,16,18). El registro español consigna que 84% de las ITU sintomáticas se manifiestan en los primeros seis meses del post trasplante renal(16) y luego gradualmente disminuyen paralelamente a la disminución de la inmunosupresión, en los meses subsiguientes(19). Contemplamos por otro lado que los episodios de ITU ocurren en cualquier momento después del trasplante. Durante el período de nuestro estudio individualizado de cuatro años en los 84 casos, 33 (39%) desarrollaron más de un episodio de ITU, nueve tuvieron dos, 11 desarrollaron tres y tres pacientes cursaron con más de 10 episodios (16). Estos últimos fueron registrados como infección urinaria recurrente (38%), porcentaje alto comparado con otras series (3% a 27%)(3). La infección recurrente es resultado de recidiva endógena más que re-infección por nuevos microorganismos(10) y se asienta mayormente en anormalidades anatómicas del tracto urinario(3,7,20)
Diversos factores contribuyeron a esta mayor incidencia de ITU, tales como algunas infecciones previas al trasplante, anormalidades anatómicas y, como en nuestra serie, el sexo femenino (57%), factor relevante comparado con el sexo masculino (44%)(21, 23). Las ITU igualmente se incrementan en mujeres diabéticas, hasta cinco veces más que en las mujeres trasplantadas sin este padecimiento(24). La diabetes mellitus estuvo presente en cinco de nuestras pacientes (3), destacando el estudio dinámico vesical en ellas y en pacientes añosos (9,28), que consistió en medir la capacidad vesical máxima, particularmente en aquellos de larga evolución en diálisis con anuria(22,25-27). Corregir las anormalidades anatómicas es la constante en el manejo para minimizar cuadros de ITU. Cinco de nuestros pacientes fueron sometidos a nefrectomías pretrasplante por reflujo vesicoureteral severo y litiasis urinaria; dos fueron prostatectomizados por hipertrofia benigna de la próstata; otros dos requirieron corrección quirúrgica de la vejiga por cistocele severo, y un paciente con microvejiga necesitó creación de neovejiga. Aun con estas y otras correcciones quirúrgicas pretrasplante y profilaxis, un reporte señala que en 1 022 receptores, 16% no lograron protección contra la ITU(28).
El riesgo de las ITU, en consecuencia, es multifactorial y está determinado por la interacción de la condición clínica del huésped, agentes patológicos y anormalidades anatómicas (21). Las investigaciones sobre procedimientos invasivos vesicales post trasplante (9,27) encuentran riesgo de incremento de bacteriuria 5 a 10% por día a partir del segundo día de la cateterización vesical(29,30), además de los problemas técnicos urológicos adicionales como la uretero-neocistostomía(17,27,28,31). En nuestra serie, 17 (19%) de los 84 receptores contrajeron anormalidades del tracto urinario en el post trasplante, porcentaje elevado si comparamos con otras series (6%)(7,9-11,32,33). Los casos con fuga urinaria fueron sometidos a reimplante ureteral y, los de estrechez, a medidas endourológicas con inserción de stent. A propósito, se reporta que los stents ureterales incrementan 4 veces la presencia de ITU(7,12,13,22) y se señala que aun después de su remoción pueden quedar nidos de infección residual(13). Por tanto, el pronto retiro(32,34,35) es la indicación apropiada. Nosotros recurrimos a la colocación del catéter ureteral (doble J) solo para casos con vejigas de paredes delgadas, microvejigas o trasplantes renales en bloque(22).
Otro factor de riesgo de ITU en receptores de trasplante renal es sin duda el uso intensivo de inmunosupresión en el periodo inicial, que al deprimir la inmunidad celular aumenta la susceptibilidad a complicaciones infecciosas(36). Ciertos inmunosupresores predisponen a su mayor desarrollo(3,22,37), tales como los antimetabolitos (azatioprina o micofenolatomofetilo). Concordantemente, las ITU en los trasplantados renales serían mayormente debidas a la inmunosupresión y a las anormalidades anatómicas(21,22).
Ocasionalmente las ITU pueden presentarse como pielonefrtis aguda del injerto y adquirir diferentes formas clínicas, desde leves hasta incluso el absceso renal(15,21,22), cursando con o sin bacteriemia y/o disfunción del injerto. Hemos constatado bacteriemia en 25 (12%) de los 215 episodios de ITU, porcentaje disminuido comparado con otras series (18% a 39%)(3,5,16,27). Señalamos un manejo exitoso de pielonefritis aguda enfisematosa por Klebsiella pneumoniae, mediante drenaje percutáneo de la colección purulenta realizado por el radiólogo intervencionista(3,24,38).
La pielonefritis aguda es causa también de disfunción del injerto renal(39). La invasión bacteriana puede ocasionar inflamación intersticial y necrosis tubular aguda(23). En 13 (6%) de los 215 episodios de ITU hubo elevación de la creatinina sérica a más del 50% de su nivel basal, acompañándose de disminución del flujo urinario a niveles menores de 0,5 mL por kg por hora, durante 6 horas(37,56); dos de estos casos requirieron apoyo temporal de hemodiálisis por falla renal aguda del injerto.
Las bacterias entéricas gram negativas fueron la etiología más frecuente de las ITU en nuestra serie (94%). La Escherichia coli (77%) (Tabla 1) fue el uropatógeno prevalente, seguido de la Klebsiella pneumoniae (11%), Pseudomonas aeruginosa (3%) y Enterococcus faecium (3%)(3,10,12,42), prevalencia bacteriana no coincidente con el mapa microbiológico de nuestras infecciones intrahospitalarias (año 2011), que señalaron en orden de frecuencia la Pseudomona aeruginosa 17%, Escherichia coli 16%, estafilococos coagulasa negativo 15% y Klebsiella pneumoniae 12%, como patógenos predominantes(41).
En la última década, las bacterias gram negativas de las ITU empiezan a mostrarse resistentes a múltiples fármacos(44), representando serio problema de salud pública(10,14,35,45).
Un estudio prospectivo de 6 meses en una unidad de hemodiálisis en una serie de 85 pacientes, ellos tenían el tracto urinario colonizado con bacterias gram negativas BLEE (16%), enterococos resistentes a la vancomicina (13%) y estafilococos resistentes a la meticilina (5%)(46). Por tanto, se presume que estas bacterias resistentes a fármacos preceden a la infección en la mayoría de los casos(22) post trasplante. Los estudios revelaron que los pacientes en hemodiálisis tenían 13 veces mayor riesgo de colonización por bacterias BLEE (22,46), comparados con la población general no trasplantada. La mucosa vesicoureteral de estos pacientes es deficiente como barrera y se muestra susceptible a la colonización.
En nuestra experiencia, ocasionalmente administramos antibióticos intravesicalmente (amikacina) previo a la anastomosis ureterovesical, durante el acto del trasplante renal; no obstante, se requiere estudios para convalidar el efecto protector de este procedimiento(15).
La resistencia bacteriana de los gram negativos varía según países y/o áreas geográficas (21), reportándose que el mayor porcentaje de resistencia antibiótica corresponde a la América Latina (45%), Europa (39%) y en menor cuantía EE UU y Canadá, con 8% y 5%, respectivamente (3,9,22). En los últimos años, la drogo-resistencia se está incrementando en forma significativa en diversos países (48). Un estudio americano señala que la resistencia de Klebsiella pneumoniae a cefalosporinas de tercera generación se incrementó de 4% (1990) a 14% (1993) (47). En un estudio de nuestra sede hospitalaria se señala sensibilidad antimicrobiana disminuida encontrada en 960 bacterias aisladas de 599 pacientes hospitalizados en el año 2014, demostrando prevalencia de E.coli BLEE en tasas altas (58%) y de Klebsiella pneumoniae BLEE en cifras aun mayores (84%) (43).
En el análisis de nuestra investigación, el porcentaje de resistencia antibiótica de cepas bacterianas estuvo presente en 79 (37%) de los 215 episodios de ITU y en 11 (44%) de las 25 bacteriemias asociadas a ITU(9,35,47,48,50). La Klebsiella pneumoniae ofreció la mayor resistencia 65%, seguida de la Escherichia coli 38% (49,50) (figuras 2 y 3).
Los cambios constantes en el uso de antimicrobianos corren paralelos a los cambios en el porcentaje de resistencia en las UTR(44). Debemos tender al uso apropiado de antibióticos a fin de disminuir el porcentaje de resistencia antimicrobiana(16) e identificar pacientes colonizados o infectados por estos gérmenes a fin de aislarlos(48,51,52). El plásmido de resistencia puede desarrollarse secundariamente al uso masivo e indiscriminado de antibióticos(43) y trasmitirse de bacteria en bacteria con riesgo de extenderse a la comunidad(22) o propender a la coexistencia de varias cepas BLEE en urocultivos, como lo detectado en uno de nuestros pacientes.
La terapia antibiótica empírica se prescribe sin disponibilidad del urocultivo y en numerosos casos el organismo aislado puede no ser susceptible a la terapia inicial, hasta en 45%, con las consecuencias previsibles. Por tanto, es preciso mejorar el sistema de reporte de antibiogramas, evitando así tratamientos inadecuados en los receptores, optimizando la prescripción de drogas y disminuyendo costos en cuidados de salud(53-55).
La principal limitante de este estudio corresponde a la naturaleza de ser retrospectivo, por la dificultad de obtener información fiable, referente a otros factores de riesgo en esta población.
En conclusión, la aparición temprana de ITU en el post trasplante aunado a múltiples episodios recurrentes ocasionan consiguiente costo de hospitalizaciones(3). Disminuir las complicaciones quirúrgicas y administrar profilaxis antimicrobiana apropiadamente constituyen medidas importantes en la disminución de la incidencia de ITU, señalando además que el incremento de bacterias BLEE representan un desafío clínico que conducen actualmente al uso profiláctico perioperatorio con carbapenems. El rol de estrategias simples, como lavado de manos y capacitación del personal de salud, disminuiría eficientemente la aparición de bacterias productoras de BLEE en los receptores de trasplante renal(51).
REFERENCIAS BIBLIOGRÁFICAS
1. Dharnidharka VR, Stablein DM, Harmon WE. Posttransplant infections now exceed acute rejection as cause for hospitalization: a report of the NAPRTCS. Am J Transplant. 2004;4(3):384-9. [ Links ]
2. Snyder JJ, Israni AK, Peng Y, Zhang L, Simon TA, Kasiske BL. Rates of first infection following kidney transplant in the United States. Kidney Int. 2008;75(3):317-26. doi: 10.1038/ki.2008.580. [ Links ]
3. Parasuraman R, Julian K, the AST Infectious Diseases Community of Practice. Urinary tract infections in solid organ transplantation. Am J Transplant. 2013;13(s4):327–36. Doi: 10.1111/ajt.12124. [ Links ]
4. Boffi El Amari E, Hadaya K, Bühler L, Berney T, Rohner P, et al. Outcome of treated and untreated asymptomatic bacteriuria in renal transplant recipients. Nephrol Dial Transplant. 2011;26(12):4109-14. Doi: 10.1093/ndt/gfr198. [ Links ]
5. Rupp ME , Fey PD. Extended spectrum β-lactamase (ESBL)-producing enterobacteriaceae. Drugs. 2003;63(4):353-65. DOI:10.2165/00003495-200363040-00002. [ Links ]
6. Di Cocco P, Orlando G, Mazzotta C, Rizza V, D'Angelo M, Clemente K, et al. Incidence of urinary tract infections caused by germs resistant to antibiotics commonly used after renal transplantation. Transplant Proc. 2008;40(6):1881-4. [ Links ]
7. Kamath NS, John GT, Neelakantan N, Kirubakaran MG, Jacob CK. Acute graft pyelonephritis following renal transplantation. Transplant Infect Dis. 2006;8(3):140–7. DOI: 10.1111/j.1399-3062.2006.00148.x. [ Links ]
8. Graeme F. Is there a role for antimicrobial management in organ transplantation?.Current Opinion in Organ Transplantation. 2007;12(6):604–9. doi: 10.1097/MOT.0b013e3282f0d39e. [ Links ]
9. Fiorante S, Fernández-Ruiz M, López-Medrano F, Lizasoain M, Lalueza A, Morales JM, et al. Acute graft pyelonephritis in renal transplant recipients: incidence, risk factors and long-term outcome. Nephrol Dial Transplant. 2010;26(3):1065-73. doi: 10.1093/ndt/gfq531. [ Links ]
10. Aguado JM, Fortun J, Gavalda J, Pahissa A, De la Torre Cisneros J. Infecciones en pacientes trasplantados 3ª. edición. 2010.
11. Englesbe MJ, Dubay DA, Gillespie BW, Moyer AS, Pelletier SJ, Sung RS, et al. Risk factors for urinary complications after renal transplantation. Am J Transplant. 2007;7(6):1536–41. doi: 10.1111/j.1600-6143.2007.01790.x. [ Links ]
12. Wojciechowski D, Chandran S. Effect of Ciprofloxacin combined with sulfamethoxazoletrimethoprim prophylaxis on the incidence of urinary tract infections after kidney transplantation. Transplantation. 2013;96(4):400-5. Doi: 10.1097/TP.0b013e3182962cab. [ Links ]
13. Memikoğlu KO, Keven K, Şengül Ş, Soypaçaci Z, Ertürk Ş, Erbay B. Urinary tract infections following renal transplantation: a single-center experience. Transplant Proc. 2007;39(10):3131-4. DOI: http://dx.doi.org/10.1016/j.transproceed.2007.10.005.
14. Orlando G, Di Cocco P, D'Angelo M, Clemente K, Manzia TM, Angelico R, et al. Surgical antibiotic prophylaxis after renal transplantation: time to reconsider. Transplant Proc. 2010;42(4):1118-9. doi: 10.1016/j.transproceed.2010.03.055. [ Links ]
15. Salehipour M, Salahi H, Fathikalajahi A, Mohammadian R, Emadmarvasti V, Bahador A, Nikeghbalian S, Kazemi K, Dehghani M, Malek-Hosseini SA. Is perioperative intravesically applied antibiotic solution effective in the prophylaxis of urinary tract infections after renal transplantation? Urol Int. 2010;85(1):66-9. doi: 10.1159/000296303. Epub 2010 Mar 17. [ Links ]
16. Vidal E, Torre-Cisneros J, Blanes M, Montejo M, Cervera C, Aguado JM, et al. Bacterial urinary tract infection after solid organ transplantation in the RESITRA cohort. Transpl Infect Dis. 2012;14(6):595-603. Doi: 10.1111/j.1399-3062.2012.00744.x. [ Links ]
17. Silva MJR, Marra AR, Pereira CAP, Medina-Pestana JO, Camargo LFA. Blood stream infection after kidney transplantation: epidemiology, microbiology, associated risk factors, and outcome. Transplantation. 2010;90(5):581-7. Doi: 10.1097/TP.0b013e3181e8a680. [ Links ]
18. Giral M, Pascuariello G, Karam G, Hourmant M, Cantarovich D, Dantal J, et al. Acute graft pyelonephritis and long-term kidney allograft outcome. Kidney Intern. 2002;61:1880–6. doi:10.1046/j.1523-1755.2002.00323.x. [ Links ]
19. Cervera C, Fernández-Ruiz M, Valledor A, Linares L, Antón A, Ángeles Marcos M, et al. Epidemiology and risk factors for late infection in solid organ transplant recipients. Transplant Infect Dis. 2011;13(6):598-607. DOI: 10.1111/j.1399- 3062.2011.00646.x. [ Links ]
20. Linares L, Cofán F, Cervera C, Ricart MJ, Oppenheimer F, Campistol JM, et al. Infection-Related mortality in a large cohort of renal transplant recipients. Transplant Proc. 2007;39(7):2225–7. doi:10.1016/j.transproceed.2007.07.047. [ Links ]
21. Delgado J, Calvo N, Gomis A, Pérez-Flores I, Rodríguez A, Ridao N, et al. Candiduria in renal transplant recipients: incidence, clinical repercussion, and treatment indication. Transplant Proc. 2010;42(8):2944–6. doi:10.1016/j.transproceed. 2010.08.019. [ Links ]
22. Pelle G, Vimont S, Levy PP, Hertig A, Ouali N, Chassin C, et al. Acute pyelonephritis represents a risk factor impairing long-term kidney graft function. Am J Transplant. 2007;7:899–907. [ Links ]
23. Georgi A, Yuvaram NVR, Gautam G. Diagnosis of acute pyelonephritis with recent trends in management. Nephrol Dial Transplant. 2012;27:1–4. doi: 10.1093/ndt/gfs327. [ Links ]
24. Dalal S, Nicolle L, Marrs CF, Zhang L, Harding G, Foxman B. Long-term Escherichia coli asymptomatic bacteriuria among women with diabetes mellitus. Clin Infect Dis. 2009;49(4):491-7. doi: 10.1086/600883. [ Links ]
25. Dion M, Cristea O, Langford S, Luke PP, Sener A. Debilitating lower urinary tract symptoms in the post-renal transplant population can be predicted pre-transplantation. Transplantation. 2013;95(4):589-94. doi: 10.1097/ TP.0b013e3182782f7e. [ Links ]
26. Coussement J, Abramowicz D. Should we treat asymptomatic bacteriuria after renal transplantation? Nephrol Dial Transplant. 2013;0:1–3. doi: 10.1093/ndt/gft432. [ Links ]
27. Muñoz P. Management of urinary tract infections and lymphocele in renal transplant recipients. Clin Infect Dis. 2001;33(1):S53-S57. doi: 10.1086/320905. [ Links ]
28. Marty FM, Rubin RH. The persistent challenges of bacterial infections in the transplant recipient. Transpl Infect Dis. 2006;8(3):125–7. DOI: 10.1111/j.1399-3062.2006.00168.x. [ Links ]
29. Peleg AY, Hooper DC. Hospital-acquired infections due to gram-negative bacteria. N Engl J Med. 2010;362:1804-13. DOI: 10.1056/NEJMra0904124. [ Links ]
30. Chuang P, Parikh CR, Langone A. Urinary tract infections after renal transplantation: a retrospective review at two US transplant centers. Clinical Transplantation. 2005;19(2):230–5. doi: 10.1111/j.1399- 0012.2005.00327.x. [ Links ]
31. Rice JC, SafdarN, the AST Infectious Diseases Community of Practice. Urinary Tract infections in solid organ transplant recipients. Am J Transplant. 2009;9(S4): S267–S272. DOI: 10.1111/j.1600- 6143.2009.02919.x. [ Links ]
32. Kevin C, Abbott S, Swanson J, Richter ER, Bohen EM, Agodoa LY, et al. Late urinary tract infection after renal transplantation in the United States. AJKD. 2004;44(2):353-62. Doi: http://dx.doi.org/10.1053/j.ajkd.2004.04.040. [ Links ]
33. Green M. Introduction: Infections in solid organ transplantation. Am J Transplant. 2013;13(s4):3–8. DOI: 10.1111/ajt.12093. [ Links ]
34. Cole T, Hakim J, Shapiro R, Kayler LK. Early urethral (Foley) catheter removal positively affects length of stay after renal transplantation. Transplantation. 2007;83(7):995-6. Doi: 10.1097/01.tp.0000259723.92943.8f. [ Links ]
35. Bhattacharya S. ESBL – from petridish to the patient. Indian J Med Microbiol. 2006;24(1):20-4. [ Links ]
36. Hamandi B, Holbrook AM, Humar A, Brunton J, Papadimitropoulos EA, Wong GG, Thabane L. Delay of adequate empiric antibiotic therapies associated with increased mortality among solid-organtransplant patients. Am J Transplant. 2009;9(7):1657– 65. Doi: 10.1111/j.1600-6143.2009.02664.x. [ Links ]
37. De Souza RM, Olsburgh J. Urinary tract infection in the renal transplant patient. Nature Rev Nephrol. 2008;4:252-64. doi:10.1038/ncpneph078. [ Links ]
38. Alexander S, Varughese S, David VG, Kodgire SV, Mukha RP, Kekre NS, et al. Extensive emphysematous pyelonephritis in a renal allograft treated conservatively: case report and review of the literature. Transpl Infect Dis. 2012;14(6):E150-5. doi: 10.1111/tid.12016. [ Links ]
39. Sharma M, Rani S, Johnson LB. Effect of time after transplantation on microbiology of urinary tract infections among renal transplant recipients. Transplant Infect Dis. 2009;10(2):145–8. DOI: 10.1111/j.1399-3062.2007.00263.x. [ Links ]
40. Merçon M, Regua-Mangia AH, Teixeira LM,Irino K, Tuboi SH, Goncalves RT, et al. Urinary tract infections in renal transplant recipients: virulencetraits of uropathogenic Escherichia coli. Transplant Proc. 201042(2):483-5. DOI: .
41. Arias-Schreiber BM, Serida MJ, Espinoza AR. Mapa microbiológico de las infecciones intrahospitalarias. 2013. Essalud Red Asistencial Rebagliati. Oficina de inteligencia sanitaria RAR Rebagliati.
42. Senger SS, Arslan H, Azap OK, Timurkaynak F, Çağır Ü, Haberal M. Urinary tract infections in renal transplant recipients. Transplant Proc. 2007;39(4):1016-7.
43. Arias-Schreiber BM, Serida MJ, Carrillo-Velásquez L. Mapa microbiológico de las infecciones intrahospitalarias. 2014. Essalud Red Asistencial Rebagliati . Oficina de inteligencia sanitaria RAR Rebagliati.
44. Dellit TH, Owens RC, McGowan JE, Gerding DN, Weinstein RA, Burke JP, et al. Infectious Diseases Society of America and the Society for Health care Epidemiology of America Guidelines for Developing an Institutional Program to Enhance Antimicrobial Stewardship. Clin Infect Dis. 2007;44(2):159- 77. doi: 10.1086/510393. [ Links ]
45. Linares L, Cervera C, Cofán F, Ricart MJ, Esforzado N, Torregrosa V, et al. Epidemiology and outcomes of multipleantibiotic–resistant bacterial infection in renal transplantation. Transplant Proc. 2007;39(7):2222–4. doi:10.1016/j.transproceed. 2007.06.061. [ Links ]
46. Snyder GM, D’Agata EMC. Novel antimicrobialresistant bacteria among patients requiring chronic hemodialysis. Current Opinion Nephrol Hypertension. 2012;21(2):211–5. doi: 10.1097/ MNH.0b013e328350089b.
47. Giamarellou H. Multidrug resistance in gramnegative bacteria that produce extended-spectrum beta lactamases ESBLS. Clin microbiol infection. 2005;11(4):1-16. [ Links ]
48. Castro N, Carreón ED, Godínez ME, Alarcón LC. Caracterización molecular de B-lactamasas de espectro extendido em aislamientos clínicos de Escherichia coli. En inf microbiol. 2008;28(3):114-20. [ Links ]
49. Moreno A, Cervera C, Gavaldá J, Rovira M, De La Cámara R, Jarque I, et al. Bloodstream Infections among transplant recipients: results of a nation wide surveillance in Spain. Am J Transplant. 2007;7(11):2579–86. DOI: 10.1111/j.1600- 6143.2007.01964.x. [ Links ]
50. Linares L, Cervera C, Hoyo I, Sanclemente G, Marco F, Cofán F, et al. Klebsiella pneumoniae infection in solid organ transplant recipients: epidemiology and antibiotic resistance. Transplant Proc. 2010;42(8):2941-3. DOI: http://dx.doi.org/10.1016/j.transproceed.2010.07.080 [ Links ]
51. Calderon R, Sacsaquispe R, Pasteran FG, Galas MF, Soto J, Riveros J, et al. Caracterización molecular de klebsiella pneumoniae y enterobacter cloacae productoras de B-lactamasas de espectro extendido tipo SHC-5 en una unidad de cuidados intensivos neonatal de Lima. Rev peru med exp salud publica. 2003;20(3):121- 7. [ Links ]
52. Grossi PA, Costa AN, Fehily D, Blumberg EA, Kuehnert MJ, Fishman JA, et al. Infections and organ transplantation: new challenges for prevention and treatment- a colloquium. Transplantation. 2012;93(5s):s4-s39. [ Links ]
53. Lorenz EC, CosioFG. The impact of urinary tract infections in renal transplant recipients. Kidney International. 2010;78:719–21. doi: 10.1038/ ki.2010.219. [ Links ]
54. Friedman CR, Whitney CG. It’s time for a change in practice: reducing antibiotic use can alter antibiotic resistance. J Infect Dis. 2008;197(8):1082-3. doi: 10.1086/533450.
55. Spellberg B, Bartlett JG, Gilbert DN.The future of antibiotics and resistance. N Engl J Med. 2013;368:299-302. doi: 10.1056/NEJMp1215093. [ Links ]
56. Kidney Disease: Improving global outcomes (KDIGO) acute kidney injury work group. Kdigo Practice guideline for acute kidney injury. Kidney Int. 2012;2(1):1-138. [ Links ]
Autofinanciado.
Ningún conflicto de interes.
Correspondencia
Dr. Pedro Méndez Chacón pjmendez2010@hotmail.com Av. Caminos de Inca Nº 2439. Santiago de Surco. Lima
Recibido, 27 junio 2016
Evaluado, 19 diciembre 2016
Aceptado, 13 enero 2017