INTRODUCCIÓN
Ante la ocurrencia de la pandemia COVID-19 que afectó a millones de personas en el mundo y en el Perú, se realizaron diversas acciones preventivas inmediatas 1,2. Por tanto, se buscó disponer cuanto antes de la vacuna porque es considerada la mejor estrategia para la prevención de casos graves y muertes por SARS-CoV-2 y frenar la pandemia. Al culminar el primer año de la pandemia en el 2020 ya se contaba con vacunas disponibles a nivel mundial, cuyas características más importantes son: la eficacia, definida como la disminución del riesgo de enfermar en personas vacunadas comparado con no vacunadas en condiciones ideales como en ensayos clínicos; y la efectividad, que representa el comportamiento de las vacunas en colectivos poblacionales a los que están destinados en condiciones de campo, administradas a la población objetivo 3,4.
Las ventajas de realizar estudios de efectividad a nivel poblacional son la disminución de costos frente a la posibilidad de diseños individualizados como el de casos - controles y cohortes prospectivas y que además requieren enfoques particulares que no brindan información aplicable a la población general 5.
Para calcular la efectividad de la vacuna se necesita determinar la capacidad de protección inmunológica, tanto para evitar un futuro contagio o la hospitalización y muerte. Para la vacuna Pfizer-BioNTech, los estudios de dos dosis de ARN mensajero consideran una efectividad del 95% en la prevención de los contagios y 100% contra casos graves. Ante la aparición de nuevas variantes del virus, Pfizer informó que su vacuna había alcanzado el 95% contra cuadros graves por las cepas Alpha y Beta, y 88% por la variante Delta 6. Por otro lado, la vacuna AstraZeneca cuenta con una efectividad del 76% evitando contagios y del 100% contra las formas graves de la enfermedad. Asimismo, la vacuna Sinopharm de China, tiene una eficacia del 79% para casos sintomáticos 7.
Considerando que la vacunación es la principal estrategia para luchar contra la pandemia, el Estado Peruano aprobó el Plan Nacional de Vacunación contra la COVID-19 el 16 de octubre de 2020 8, iniciando las actividades de vacunación el 9 de febrero del 2021 9. Este se inició con el personal de salud, se continuó inmediatamente con la vacunación en los grupos de mayor edad y mayor vulnerabilidad, y en forma progresiva con el resto de grupos de edad para alcanzar a la mayor parte de la población objetivo de 18 años a más durante el año 2021. El Plan Nacional de Vacunación fue actualizado el 14 de abril del 2021, incluyendo el enfoque territorial 10,11. Se han usado tres tipos de vacunas, Sinopharm (virus inactivado), Pfizer (ARNm) y AstraZeneca (vector viral recombinante). Hasta el 6 de noviembre 2021, fecha de corte del estudio se han aplicado 15 847 512 segunda dosis de vacunas, con una cobertura de 55,18% 12,13,14.
Se inició la vacunación priorizando al personal de salud, adultos mayores y personas con comorbilidades, grupos poblacionales más vulnerables de enfermar gravemente y morir por esta enfermedad 15. Para abril 2021 se encontró disminución en hospitalización y mortalidad en la población priorizada vacunada, indistintamente del tipo o marca de la vacuna 16. También, se comparó la variación según el sexo, teniendo en cuenta el riesgo de mortalidad por esta enfermedad entre ambos grupos 17,18.
En nuestro país, existen múltiples sistemas de información de alcance nacional en el ámbito de salud en lo que respecta a pruebas de laboratorio y fallecidos, tales como NETLAB y SICOVID y SINADEF. Para este estudio, con el objetivo de estimar la efectividad de vacunas COVID-19 y el riesgo de mortalidad en pacientes hospitalizados por COVID-19, se utilizó la Plataforma Nacional de Datos Abiertos del Estado Peruano (PNDA) 19.
MÉTODOS
Diseño de estudio
Estudio observacional de base poblacional, analítico, retrospectivo, de cohorte cerrada y con apareamiento de todos los pacientes diagnosticados con COVID-19 que ingresaron al servicio de hospitalización del área COVID en diferentes hospitales del país durante la pandemia registrados en la PNDA (https://www.datosabiertos.gob.pe/search/field_topic/covid-19-917/type/dataset?sort_by=changed), que contiene datos de fuentes secundarias provenientes de los registros rutinarios de hospitalizados, vacunados y fallecidos (HVF) por COVID-19. El estudio incluye datos desde el 9 de febrero del 2020 que tuvieron un seguimiento hasta la fecha de corte, el 27 de octubre del 2021 a las 16:10 pm, hora de descarga.
Población de estudio
La base de datos HVF del PNDA es de libre acceso y descarga y contiene los registros del universo de personas residentes en Perú (indistintamente de la nacionalidad) que están incluidos en el programa de vacunación de COVID-19, contiene además la información de estado de hospitalización, vacunación y defunción por COVID-19. El estudio consideró el total de registros de la base de datos en el periodo antes mencionado, excluyendo sólo a los menores de 18 años y los registros incompletos según las variables de estudio.
Variables
Muerte por COVID-19: característica de desenlace final en el proceso de hospitalización hasta el corte de seguimiento, con los siguientes valores: 1= muerte y 0= no muerte.
Tiempo de seguimiento: tiempo en días desde el ingreso de hospitalización hasta la última observación de hospitalización y el corte de seguimiento en ambas cohortes.
Inmunizado: variable definida para la persona que recibió o no las dos dosis de vacuna anti COVID-19 disponible en el Perú para el periodo de observación, 0= no inmunizado, 1= inmunizado.
Se estudiaron además las variables sexo, categoría de edad (0= de 18 a 35, 1= de 36 a 50, 2= de 51 a 65, 3= de 66 a 85, y 4= de 86 a más), y tipo de vacuna (0 = no vacunado o no inmunizado, 1= AstraZeneca, 2= Pfizer, 3= Sinopharm).
Para estimar la efectividad de las vacunas COVID-19 para prevenir la muerte en personas hospitalizadas en el Perú, se compara el evento de interés "muerte por COVID-19" entre dos cohortes:
Cohorte de expuestos, conformada por pacientes hospitalizados por COVID-19 de 18 años a más que recibieron ambas dosis de la vacuna COVID-19 (AstraZeneca, Pfizer o Sinopharm) a los 15 días o más antes de la hospitalización.
Cohorte de no expuestos, conformada por pacientes hospitalizados por COVID-19 de 18 años a más que no estaban vacunados, tenían sólo una dosis de vacuna, o habían sido vacunados entre los 14 días previos a la hospitalización.
Análisis estadístico
Se exportó la base de HVF del PNDA en formato Microsoft Excel 2016 y se empleó el software estadístico R versión 4.1.0 (The R Foundation for Statistical Computing Platform) para la construcción, limpieza y análisis de la base de datos (BD). Esta primera BD fue dividida en dos, una primera que contiene a la cohorte de expuestos y otra que contiene la cohorte de no expuestos. Para efectos de la estimación del efecto de la vacunación se procedió a seleccionar muestras emparejadas para ambas BD con distribución similar en las variables sexo y edad, para ello se empleó la librería "MatchIt" del software R que selecciona muestras emparejadas o balanceadas mediante técnicas de emparejamiento computacional.
Luego, se realizó el análisis descriptivo de las variables de estudio a través de la distribución de frecuencias y porcentajes. Finalmente se realizó el análisis de sobrevivencia (censura aleatoria) para determinar la probabilidad y la mediana del número de días de sobrevida durante el proceso de hospitalización. Las funciones de sobrevivencia se calcularon a partir del estimador de Kaplan-Meier, acompañado de las tablas de riesgos; además, se estimaron curvas de sobrevida según grupos de edad, exposición a inmunización y tipo de vacuna, haciendo la comparación mediante el Test de Log Rank (Mantel-Cox), considerando estadísticamente significativo un valor p<0,05 (Intervalo de Confianza de 95%).
La estimación de la efectividad se realizó a través de la construcción de modelos de regresión de Cox de causa-específica en presencia de riesgos competitivos.
La efectividad de la vacunación se estimó como 1 - HR. La estimación del HR (Hazard Ratio o razón de riesgos) se hizo con modelos crudos.
Se utilizó el Software libre R, versión 4.1.0. y la librería "MatchIt" para la obtención de muestras balanceadas de ambas cohortes, y las librerías "survival", "KMsurv"; "survMisc" y "survminer" para el análisis de sobrevivencia.
RESULTADOS
Los datos corresponden a la cohorte de personas con COVID-19 hospitalizadas hasta el 27 de octubre del 2021, con un total de 119 957 registros. Luego, se realizó una limpieza de la base de datos omitiendo los registros de pacientes menores de 18 años y registros sin datos para los campos de edad, sexo y evolución última de hospitalización, resultando al final un total de 107 410 registros (se omitieron un total de 12 547 registros), dentro de ellos 2254 (2,1%) fueron pacientes hospitalizados inmunizados y 105 156 (97,9%) fueron pacientes hospitalizados no inmunizados.
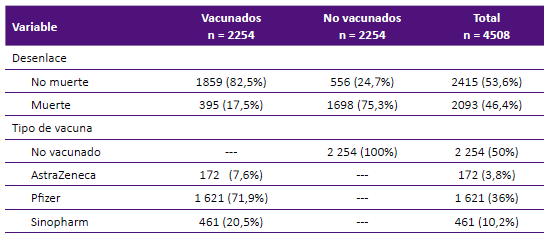
A partir de la base de datos general, se construyó dos submuestras correspondientes a las cohortes de pacientes expuestos o inmunizados y de pacientes no expuestos o no inmunizados. Para la cohorte de expuestos: se construyeron las variables "tiempo de seguimiento", "muerte por COVID-19" y "tipo de vacuna". Para la cohorte de no expuestos: se construyeron las variables "tiempo de seguimiento", "muerte por COVID-19" y "tipo de vacuna" en donde se asignó el valor de 0 a todos los registros. Definidas ambas muestras se realizó el pareamiento o emparejamiento para la muestra de expuestos y no expuestos según las variables edad y sexo, obteniendo finalmente una muestra de 4508 registros. La muestra pareada según sexo estuvo conformada por 2362 mujeres (52,4% de la muestra) y 2146 varones (47,6% de la muestra); y según grupos de edad, por 582 (12,9%) de 18 a 35 años, 678 (15%) de 36 a 50, 974 (21,6%) de 51 a 65 años, 1776 (39,4%) de 66 a 85 años y 498 (11,1%) de 86 años a más. En la tabla 1 se presentan características generales de los pacientes hospitalizados.
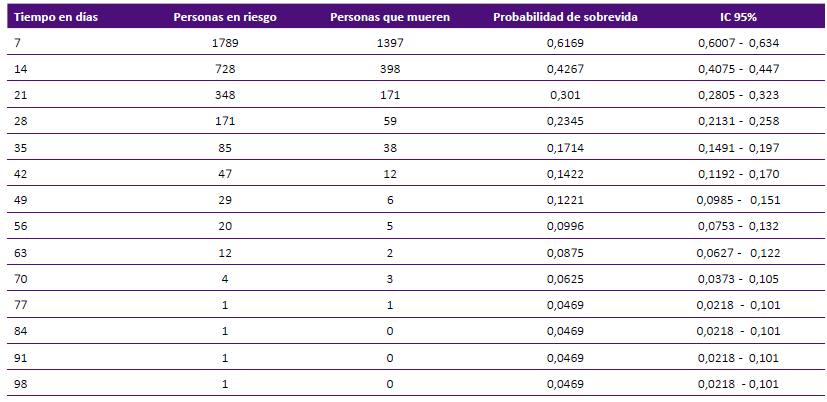
El análisis de sobrevivencia describe el tiempo transcurrido desde el inicio de la hospitalización por COVID-19 hasta el desenlace final o muerte en la cohorte de personas (n= 4508) seguidas independientemente uno a uno. Un 46,4% (2093/4508) representan las personas que han sufrido el deceso durante la hospitalización. La tasa de letalidad fue de 17,5% (395/2254) en los expuestos (vacunados) y 78,8% (1698/2254) en los no vacunados. La mediana del tiempo de sobrevida global fue de 11 días (IC 95% 10-11 días), siendo la probabilidad de sobrevida (no muerte durante la hospitalización) decreciente conforme aumenta el número de días en hospitalización. Así, en la primera semana la probabilidad de sobrevida fue de 0,61, en la segunda semana fue de 0,412, en la tercera semana fue de 0,286 (Tabla 2).
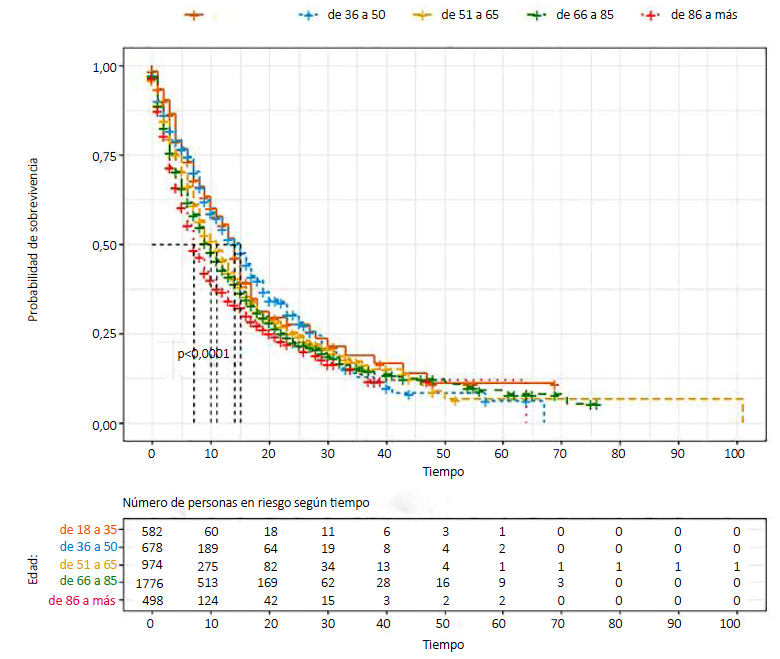
Según grupo de edad, la mediana del tiempo de sobrevivencia decrece a partir de las edades de 36 a 50 años; en personas de 36 a 50 años la mediana del tiempo de sobrevida fue de 15 días, en personas de 51 a 65 años fue de 11 días, en personas de 66 a 85 años fue de 10 días y en personas de 86 a más fue de 7 días. La diferencia entre estos grupos fue significativa (p < 0,001, test de Long- Rank) (Figura 1).
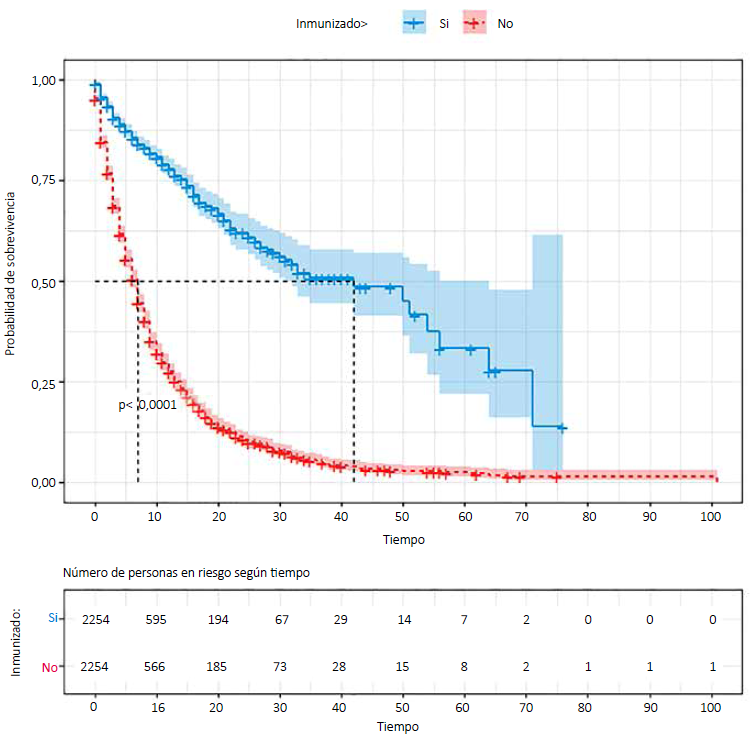
Para el caso de la sobrevivencia según grupo de exposición (inmunizado vs no inmunizado), la mediana del tiempo de sobrevivencia en la cohorte de personas hospitalizadas con vacunas completas fue de 42 (IC 95%: 31-64) días mientas que en el grupo de personas hospitalizadas sin vacunas o vacunas incompletas fue de 7 días (IC 95%: 6-7) (Figura 2). Estas diferencias resultaron estadísticamente significativas (p < 0,001, test de Long-Rank), por lo cual podemos decir que la vacuna tuvo un efecto en el tiempo de sobrevivencia durante la hospitalización por COVID-19.
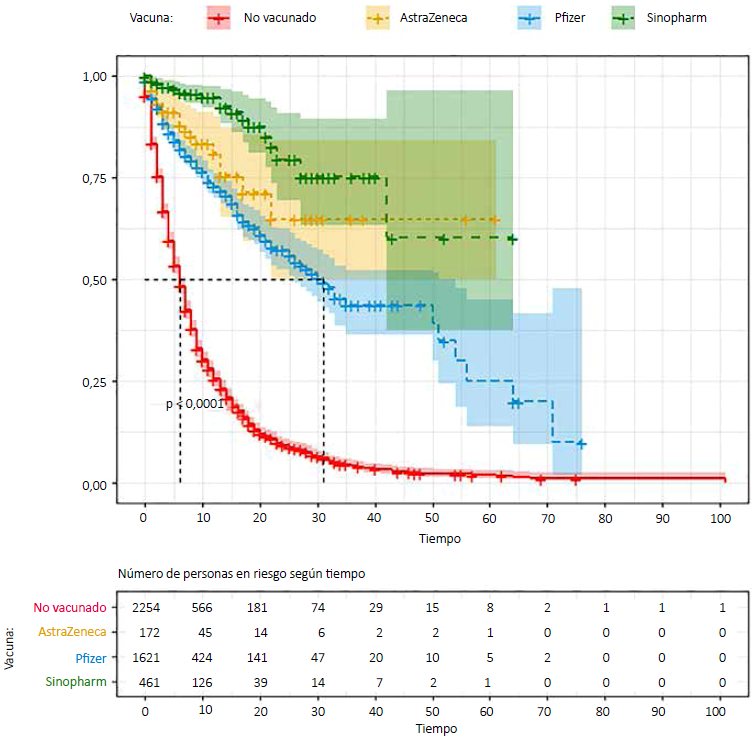
Para el caso de la sobrevivencia según los tipos de vacunas (AstraZeneca, Pfizer y Sinopharm) y los no vacunados, las personas vacunadas con Sinopharm tuvieron las mejores probabilidades de sobrevivencia, pero con un periodo de tiempo de vida relativamente menor que los vacunados con otro tipo de vacunas; es decir, la tasa de letalidad en personas vacunadas con Sinopharm fue de 50 por 1000 personas (26/524), con una probabilidad de sobrevida de 0,960 a los 7 días de hospitalización.
Las personas vacunas con AstraZeneca tuvieron una probabilidad de sobrevivencia menor que las personas vacunadas con Sinopharm, pero mayor que las personas vacunadas con Pfizer. La tasa de letalidad en las personas inmunizadas con este tipo de vacuna fue de 145 por 1000 personas (25/173), con una probabilidad de sobrevida de 0,866 a los 7 días de hospitalización.
La probabilidad de sobrevivencia en personas vacunadas con Pfizer fue menor que la de otras vacunas, la tasa de letalidad de 0,203 (344/1692) y a los 7 días esta probabilidad fue de 0,812 (Figura 3).
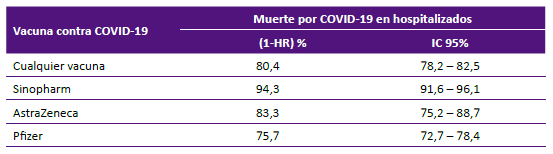
En este estudio, los datos del conjunto de las vacunas (Pfizer, AstraZeneca y Sinopaharm) para prevenir la mortalidad en personas hospitalizadas por COVID-19 mostró una eficacia de 80,4% (IC 95% 78,2%- 82,5%) (Tabla 3).
DISCUSIÓN
El estudio mostró que el plan de vacunación consistente en la administración de tres tipos de vacunas utilizado por el estado peruano, tuvo una efectividad de 80,4% para prevenir los decesos en hospitalizaciones por COVID-19 (IC 95% 78,2%- 82,5%). Cada una de las tres vacunas contra el COVID-19 comprendidas en el plan de vacunación son recomendadas por la OMS por tener porcentajes de eficacia aceptables (AstraZeneca 72%, Pfizer 91% y Sinopharm 78,1%) 20,21. En este estudio los datos hallados de efectividad de las vacunas son similares para evitar muertes en personas hospitalizadas.
Los valores de estudios de efectividad en otros países fueron también similares al hallado en este estudio. El Ministerio de Salud de Colombia en una investigación en adultos mayores, halló que la efectividad de las vacunas para evitar muerte luego de ser hospitalizados era del 79,4% (IC 95% 77,2% - 81,4%) 22. En España, en un contexto muy restringido de asilos para la atención de las personas, se halló 97% de efectividad de la vacunación para prevenir la muerte por COVID-19 (IC 95% 92-99%) 23. Chung y col. presentaron la evaluación de efectividad de dos vacunas (BNT162b2 y mRNA1273) en adultos en Canadá, reportando 80% a más de efectividad luego de 2 dosis contra el COVID-19 sintomático causado por diferentes variantes, entre ellas alfa, beta y gamma; sin embargo, la efectividad disminuyó (43-61%) con una sola dosis 24.
En cuanto al diseño de estudio de cohorte empleado los autores reconocen la limitación de no capturar todas las variables que diferencian los grupos de vacunados y no vacunados, tales como: estado de salud en general, oportunidad y acceso a servicios de salud, entre otros 25,26.
El modelo de riesgos competitivos utilizado en nuestro estudio permite ajustar un modelo simultáneo para cada desenlace, con la posibilidad de presentar ambos desenlaces en diferentes momentos, lo que es útil cuando uno de ellos puede afectar las censuras y el riesgo del otro, como es el caso de hospitalización y muerte por COVID-19 27.
Entre las limitaciones de este estudio se cuenta que la PNDA utilizado sólo brinda datos de mortalidad más no datos de inmunización para prevenir hospitalizaciones; este sistema de registro no permite hacer la estimación de sujetos inmunizados que no están hospitalizados vs sujetos no inmunizados hospitalizados. Otras limitaciones son la representatividad de los casos dado que se cuenta solamente con la información brindada por el sistema, el desconocimiento del control de la calidad en el registro de datos de la PNDA y que la base de datos no contiene otras variables que enriquezcan el estudio tales como las comorbilidades y otros resultados de laboratorio. Por tanto, los hallazgos de este estudio se refieren sólo a la mortalidad y constituyen una aproximación al impacto que podría tener la vacunación en la población general.
En este estudio se halla que el conjunto de las vacunas (Sinopharm, Pfizer y Astra Zeneca) utilizadas en el plan de vacunación del Perú proveen una efectividad de 80,4% (IC 95% 78,2%- 82,5%) para prevenir la mortalidad en hospitalizados por COVID-19, reiterando que la vacunación es la estrategia más efectiva disponible en la prevención de muerte por COVID-19. Esta información se obtiene con el 55,18% de población blanco de 18 años a más inmunizada con segunda dosis y 3,5 millones de población blanco sin segunda dosis. La mortalidad sin duda disminuiría con mayor cobertura y proporción de peruanos inmunizados con esquema completo.