INTRODUCCIÓN
La diabetes mellitus es una enfermedad crónica, degenerativa, discapacitante y multifactorial que constituye un problema de salud pública. En el Perú, la producción científica sobre diabetes es limitada y se reportan prevalencias entre 3,9 y 7%, según diferentes autores 1. La nefropatía diabética (ND) es una de las complicaciones microangiopáticas más graves de la enfermedad, y cursa con proteinuria mayor a 300 mg/día, hipertensión y disminución progresiva de la función renal 2,3.
Sin embargo, existe una alta prevalencia de lesiones renales no diabéticas, que pueden determinarse mediante biopsia renal, confirmando una nefropatía diabética aislada, ND con nefropatía no diabética (NND) o NND aislada, lo que alteraría el curso de la enfermedad y, por tanto, el manejo y pronóstico del paciente 4. Dado que la nefropatía diabética, es una de las principales causas de enfermedad renal crónica, con reportes que varían entre 13 y 44% en nuestro país 5, y que además aumenta los costos de la enfermedad y genera peor calidad de vida en los pacientes, se debe evaluar a todo paciente diabético con presencia de microhematuria, niveles elevados de proteinuria o ausencia de retinopatía ante la posibilidad de cursar con una nefropatía no diabética asociada o aislada.
El objetivo de este reporte fue describir el caso de un paciente diabético habitante de una ciudad de altura (3824 msnm), que cursó con hematuria microscópica persistente, proteinuria, elevación de creatinina y fondo de ojo negativo, a quien se le realizó biopsia renal por sospecha de glomerulopatía no diabética asociada; sin embargo, se encontró nefropatía diabética, por lo que sospechamos que la altura pudo influir en la presencia de proteinuria elevada y empeoramiento de la función renal. La presencia de policitemia, proteinuria, deterioro de la función renal e hipertensión arterial, se ha denominado síndrome renal de gran altura y es característico de las habitantes de ciudades por encima de los 2500 msnm.
REPORTE DE CASO
Paciente varón de 54 años, procedente de Puno (3824 msnm), Perú, con antecedente de 5 años de diabetes mellitus tipo 2, en tratamiento con metformina y glibenclamida e hipertensión arterial controlada, de un año de evolución, tratada con irbesartán; que ingresó por presentar orinas espumosas, nicturia, edema de miembros inferiores de siete meses de evolución. Al examen se encontró un paciente con presión arterial de 130/80 mmHg, índice de masa corporal 30 kg/ m2, con edemas en miembros inferiores de intensidad +/+++ hasta rodillas, resto de examen no contributorio.
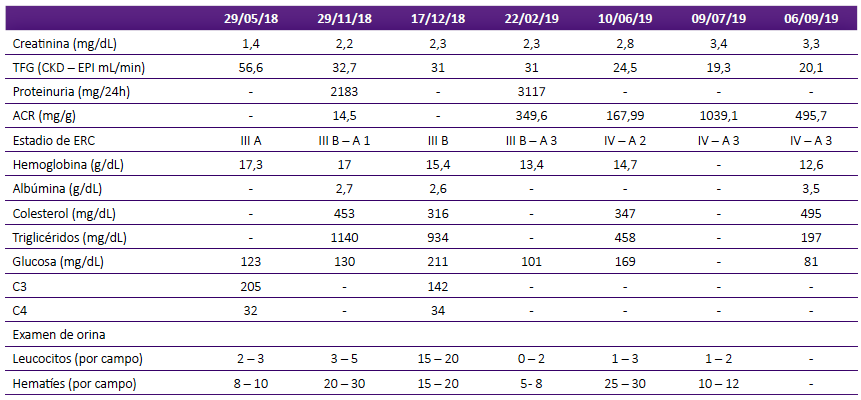
Dentro de sus exámenes auxiliares destacaron la presencia de azoemia, hematuria microscópica persistente, elevación de hemoglobina, creatinina y proteinuria, dislipidemia e hipoalbuminemia (Tabla 1). La ecografía renal mostró riñones incrementados de tamaño (derecho 134 x 68 x 20 mm e izquierdo 128 x 63 x 20 mm) con pérdida de la diferenciación córtico medular, vejiga sin residuo post miccional y próstata de volumen conservado. Se descartó secundarismo (lupus, vasculitis, hepatitis, VIH, hipotiroidismo, neoplasias); sin embargo, se realizó biopsia renal, por sospecha de nefropatía no diabética debido al hallazgo de hematuria microscópica y ausencia de retinopatía diabética.
El informe anatomopatológico concluyó el diagnóstico histológico de glomeruloesclerosis nodular diabética (nefropatía diabética) y arterio-arterioloesclerosis moderada. Se encontró 18 glomérulos, tres de ellos globalmente esclerosados, todos incrementados de tamaño con expansión e hipercelularidad mesangial (1+ a 2+); asas capilares engrosadas (2+), un glomérulo con nódulo mesangial acelular rodeado por capilares, de aspecto lamelar, con coloraciones de PAS Negativo y MASSON positivo; 3 glomérulos con retracción del penacho hacia el polo vascular; otros tres con capuchón fibrosis capsular PAS (-); se reconoció algunas arteriolas con hialinosis de la capa media y PAS positivo; túbulos con degeneración turbia, cilindros hemáticos (1+), atrofia tubular leve; membranas basales tubulares engrosadas (1+) en aquellos no atróficos, además intersticio con infiltrado a células linfomononucleares leve multifocal, y fibrosis leve y arterias con esclerosis concéntrica de la íntima (Figuras 1 y 2). En la inmunofluorescencia, se evidenció 14/14 glomérulos con depósitos lineales de IgG en membrana basal capsular y tubular, con negatividad para IgA, IgM, C3 y C1q.
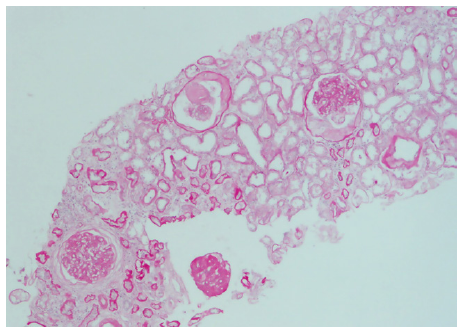
Figura 1 Glomérulos con hipercelularidad mesangial, uno de ellos con nódulo mesangial acelular y otro globalmente esclerosado (PAS, 10X).
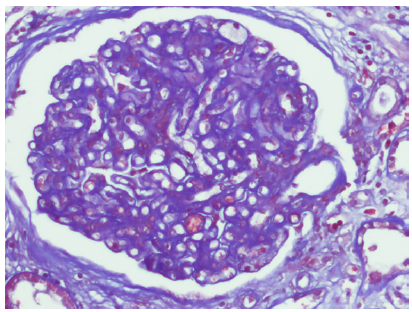
Figura 2 Glomérulo incrementado de tamaño con expansión e hipercelularidad mesangial (Tricrómico de Masson, 20X).
El paciente cursó con evolución desfavorable, aumentando niveles de proteinuria y microalbuminuria, pese a uso de antiproteinúricos a dosis altas (espironolactona e irbesartán), progresando a enfermedad renal crónica estadio IV.
DISCUSIÓN
La nefropatía diabética es una de las principales complicaciones crónicas de la diabetes mellitus, llevando al desarrollo de enfermedad renal crónica (ERC), con el consiguiente aumento de la morbimortalidad y de los costos en salud, sobre todo cuando el paciente requiere terapia de reemplazo renal (diálisis).
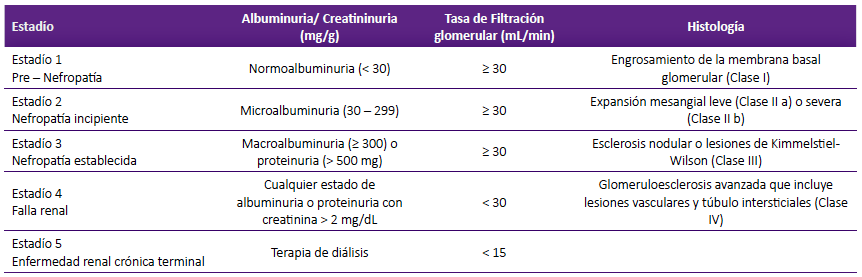
Recientemente, se ha cambiado el término de nefropatía diabética por "enfermedad renal diabética". Esta se caracteriza por proteinuria (mayor a 300 mg/24 horas) o albuminuria persistente y elevada (mayor de 300 mg/24h o relación albuminuria/creatininuria mayor de 300 mg/g), asociado a disminución de la tasa de filtración glomerular, generalmente tras 10 a 20 años de enfermedad, en diabéticos tipo 1 y 2 2,6,7. La microalbuminuria, se utiliza para el diagnóstico y clasificación de la enfermedad renal crónica y de la nefropatía diabética, ya que, se presenta en forma precoz y precede a la aparición de proteinuria entre 5 a 10 años después del diagnóstico de diabetes, considerándose una relación albuminuria/creatininuria entre 30 y 300 mg/g como precursor de nefropatía diabética. Asimismo, en base a biopsias renales se ha realizado una clasificación histológica, y a su vez, se han planteado clasificaciones clínicas 3,6,8,9. (Tabla 2)
No todos los pacientes siguen esta regla, pudiendo encontrarse tres grupos histológicos de acuerdo a los hallazgos de la biopsia renal: nefropatía diabética, nefropatía no diabética y nefropatía diabética asociada con nefropatía no diabética. La prevalencia de nefropatía no diabética (NND), oscila entre 33 y 72.5% 10, por lo que es importante evaluar los factores predictivos de NND e indicar la biopsia renal en pacientes diabéticos ante la presencia de síndrome nefrótico severo o incremento rápido de proteinuria, ausencia de retinopatía diabética con proteinuria nefrótica, proteinuria mayor de 1 g en pacientes con tiempo de diabetes menor de 5 años, disminución abrupta de la tasa de filtración glomerular, injuria renal aguda y micro o macrohematuria 4,11.
La microhematuria, la ausencia de retinopatía diabética y la edad avanzada son fuertes predictores de nefropatía no diabética 11. La hematuria predice nefropatía no diabética, aunque los eritrocitos dismórficos son más útiles en pacientes con DM2 y proteinuria 12. Sin embargo, también se ha asociado a nefropatía diabética avanzada demostrada por biopsia e incluso es un factor de riesgo para enfermedad renal crónica terminal en pacientes con nefropatía diabética 13,14. Un estudio de 260 pacientes con nefropatía diabética (diagnosticada por biopsia), encontró que el 39% presentó hematuria y el 20,5% no tuvo retinopatía diabética 13. No se conoce a ciencia cierta, porqué sucede esto, pero otro autor encontró que los pacientes con nefropatía sin retinopatía diabética pueden cursar con menor daño renal y menos complicaciones diabéticas que aquellos que si tienen retinopatía 15. Nuestro paciente no tenía retinopatía diabética, pero tuvo mayor compromiso renal, por lo que consideramos que otros factores estuvieron involucrados en la progresión del daño renal.
El tiempo de duración de la diabetes mellitus también se ha considerado un factor predictor de NND, encontrándose que los diabéticos tipo 2, con menos de 5 años de evolución, tienen más probabilidad de NND 16. Otros factores son: niveles más elevados de hemoglobina, menor glicemia y hemoglobina glicosilada, menores cifras de presión arterial, evidencia de púrpura o artralgias y presencia de ANCA positivo 4,16.
La evolución clínica "típica" de la nefropatía diabética puede verse afectada en pacientes con NND. Un estudio encontró que la mitad de los pacientes diabéticos que progresaron a ERC e iniciaron diálisis, tuvieron mayor duración de diabetes, menor tasa de filtración glomerular, hematuria, aumento de proteinuria, engrosamiento de la membrana basal glomerular y mayor nivel de fibrosis túbulo - intersticial y atrofia tubular 17.
A pesar de que varios hallazgos clínicos (hematuria y ausencia de retinopatía diabética), sugerían la posibilidad de una nefropatía no diabética, la biopsia renal realizada confirmó la nefropatía diabética, por lo que no se adicionó inmunosupresores en la terapia del paciente. Cabe resaltar que, la clínica y la mala evolución del paciente justificaron la indicación de la biopsia renal, debido a la alta sospecha de nefropatía no diabética. Además, la presión arterial y la glicemia estuvieron controladas y no hubo mejoría de la proteinuria a pesar del incremento de dosis de antiproteinúricos.
Los patrones histológicos de nefropatía no diabética más frecuentes, son la glomerulonefritis por Ig A y la nefropatía membranosa 18,19, aunque también son frecuentes la glomeruloesclerosis focal y segmentaria y nefroangioesclerosis 20. Entre otros hallazgos histológicos se mencionan a la glomerulonefritis pauci inmune, enfermedad por cambios mínimos, amiloidosis, glomerulonefritis fibrilar, nefritis lúpica, glomerulonefritis membranoproliferativa, riñón de mieloma, gammapatía monoclonal, microangiopatía trombótica, embolismo de colesterol, nefritis por IgG4 y nefritis túbulo intersticial aguda como causa de NND 21.
Otro hecho que nos llamó la atención fue la rápida progresión de la enfermedad renal crónica, que podría explicarse por la altura. Se sabe que, la exposición crónica a la altura produce cambios fisio-patológicos en el riñón, que empeoran la función renal. El síndrome renal de gran altura caracterizado por policitemia, proteinuria, hipertensión arterial e hiperuricemia, es frecuente en pacientes que viven en ciudades de gran altitud y se ha asociado a peor función renal 22. Se ha demostrado que los pobladores de altura, tienen menor tasa de filtración glomerular y mayor creatinina, proteinuria y policitemia, secundarias a la hipoxia hipobárica 23, 24. La influencia de la altura sobre la proteinuria se ha reportado en una paciente residente de altura con glomerulonefritis focal y segmentaria, que presentó proteinuria persistente sin respuesta a antiproteinúricos, pero que, mejoró con el uso de acetazolamida 25. Por todo ello, consideramos que la altura pudo influir en la mala evolución de nuestro paciente.
En conclusión, se debe evaluar a todo paciente con enfermedad renal diabética, ante la posibilidad de cursar con nefropatía no diabética, y plantear la biopsia renal, lo que podría cambiar el curso y tratamiento de la enfermedad. Esta entidad debe ser considerada por médicos internistas, endocrinólogos y de atención primaria para la referencia temprana al nefrólogo. Asimismo, en pacientes que viven en altura, se debe valorar la presencia de síndrome renal de gran altura, el cual podría contribuir al empeoramiento de la función renal.