INTRODUCCIÓN
Desde el 2019, cuando inició el brote de la enfermedad por coronavirus 2019 (COVID-19), las infecciones a nivel mundial se han incrementado hasta más de 242 millones, llegando a causar más de 5 millones de muertes 1. Debido a esta enfermedad, se impusieron diversas medidas como: uso de máscaras, trabajo remoto, aislamiento, cuarentenas; sin embargo, la medida más eficiente fue vacunación.
Para lograr la vacunación, diversos laboratorios trabajaron para el desarrollo de esta tecnología sanitaria. Se lograron nueve vacunas líderes fabricadas por Pfizer, BioNTech, Moderna, Gamaleya, Novavax, Oxford, Aztra Zeneca, Sinopharm, Bharat BioNTech, Johnson & Johnson y Sinovac; estas se basaron principalmente en el uso como antígeno de la glicoproteína S. A pesar del diverso número de vacunas, hay preocupación por el desarrollo de nuevas mutaciones de dicho virus. Además, que se han descrito diversos efectos adversos asociados a la vacunación como dolor en el lugar de inyección, fatiga, dolor de cabeza 2,3.
También se ha encontrado ―con menor frecuencia― complicaciones renales, las más importantes incluyen: necrosis tubular aguda, efecto directo del virus en el riñón; mecanismos de invasión celular, esto asociado a la expresión de ECA-2 3. Al parecer, este aumento en la relación ECA/ECA-2 también jugaría un rol en la infección por COVID-19 generando peores resultados en el desenlace de los pacientes, esto también se evidencia en patologías como la hipertensión, cardiopatía isquémica, insuficiencia renal crónica e insuficiencia cardiaca 4.
Entre las complicaciones asociadas a la vacunación, se ha encontrado nefritis tubulointersticial aguda 5 y enfermedad de cambios mínimos 6. En Italia, se encontraron 17 casos de nefropatías de nueva aparición asociada a la vacunación contra el SARS-CoV- 2, entre las cuales 5 fueron enfermedad de cambios mínimos, 3 nefropatía intersticial aguda, 3 nefropatía membranosa, 2 nefropatía por IgA y los 4 restantes otros tipos de glomerulopatías, esta es una de las series más grandes reportadas 7. Además en Argentina, se han reportado 4 casos de aparición o recurrencia de novo de glomerulopatías asociadas a la vacunación frente al COVID-19, 2 nefropatías por IgA, 1 glomerulonefritis membranoproliferativa y 1 paciente con recurrencia de enfermedad de cambios mínimo 8.
El presente caso es el primer reporte en el Perú de una glomerulopatía, específicamente la glomeruloesclerosis focal y segmentaria, la cual se desarrolló posvacunación contra el COVID-19. Para la publicación del presente reporte, se obtuvo el consentimiento informado de la paciente.
REPORTE DE CASO
Se presenta el caso de una mujer de 26 años, personal de salud, con antecedente de hipotiroidismo primario. Ella presentó edema +++ / +++ en miembros inferiores, a los dos días tras la aplicación de la vacuna contra el SARS-CoV2 (Sinopharm) que evolucionó a la anasarca. Asociado a ello, manifestó orina espumosa, malestar general y cefalea, por lo cual fue internada. Tuvo una proteinuria de 24 gramos en 24 horas, la albúmina sérica estuvo en 2,36 mg/dL, la prueba COVID-19 fue negativa (Tabla 1). Se estableció el diagnóstico de síndrome nefrótico y se procedió a realizar estudios para descartar etiología secundaria de glomerulopatía, tales como: ANA (anticuerpos antinucleares), ANCA (anticuerpos anti citoplasmáticos), complemento C3, complemento C4, perfil de hepatitis, perfil de sífilis, VIH, marcadores tumorales, todos fueron negativos.
Tabla 1. Resultados de laboratorio durante el internamiento.
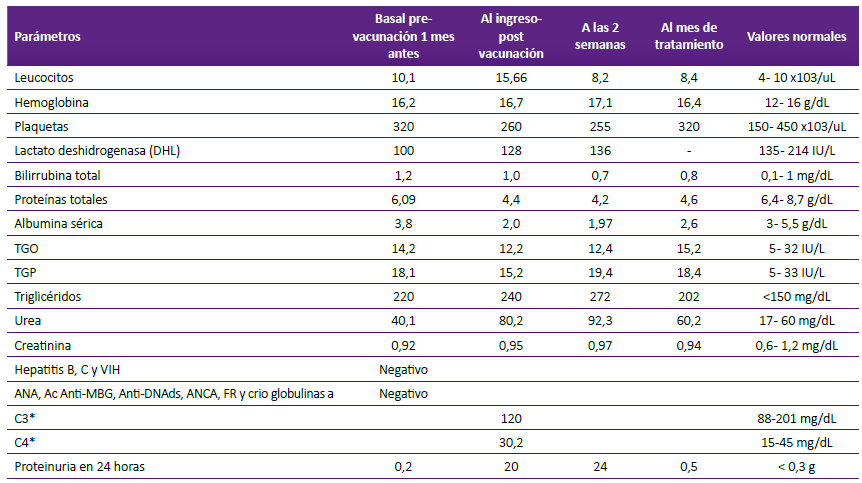
a ANA (Anticuerpo antinucleares). AC Anti-MBG (Anticuerpos antimembrana basal glomerular). Anti-DNAds (Anticuerpos anti-ADN de doble cadena). ANCA (Anticuerpos anticitoplasma de neutrófilos). FR: Factor Reumatoideo .C3: Complemento C3 .C4: Complemento C4
Se le realizó una biopsia renal con guía ecográfica, los resultados anatomo-patológicos muestran 17 glomérulos, ninguno globalmente esclerosado. (Figura 1A), la mayoría de los glomérulos incrementados de tamaño, algunos con expansión mesangial leve, hay rigidez segmentaria de asas capilares e hiperplasia e hipertrofia de podocitos; dos glomérulos tenían esclerosis segmentaria, uno de ellos con protrusión y esclerosis segmentaria a nivel del polo urinario y otro a nivel peri hiliar. Los túbulos tuvieron degeneración turbia, cilindros hialinos (1+); hubo atrofia tubular leve focal, y túbulos dilatados con epitelio atenuado. El intersticio tenía infiltrado de células linfomononucleares leve focal y fibrosis mínima. Los vasos sanguíneos no tenían alteraciones significativas (Figura 1B). En la inmunofluorescencia, IgG negativo, IgM 2/10 con depósitos, IgA, C3, C1q, Kappa, Lambda negativos.
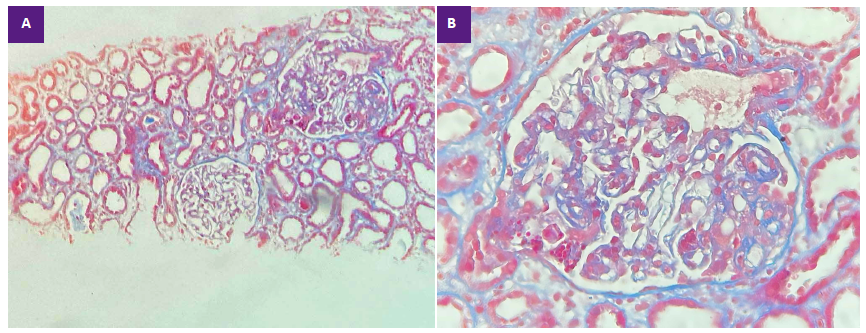
Figura 1. A. Se evidencia glomeruesclerosis focal y segmentaria en varios glomérulos en todo el campo. Coloración: tricrómica de Masson. Aumento: 10x. B. Glomeruloesclerosis focal y segmentaria Coloración: tricrómica de Masson. Aumento: 100 x
La paciente fue hospitalizada y recibió inmunosupresión con pulsos de metilprednisolona 1 gramo diario por 3 días, prednisona vía oral (1 mg/kg/día) con una dosis total de 60 mg por día, atorvastatina (20 mg/día), antiagregación plaquetaria con AAS (100 mg/día), omeprazol (20mg/día) y profilaxis con trimetoprima-sulfametoxazol.
Dos semanas después, la paciente presentó un descenso de peso de 10 kg y los edemas disminuyeron notoriamente. Luego de cuatro semanas de iniciar el tratamiento, se evidenció un resultado de proteinuria menor de 500 mg/día, la paciente fue dada de alta, continuando sus controles por consultorio externo de nefrología; en el último control, a los tres meses, la paciente presentó control de proteinuria de 140 mg en 24 horas, estando controlada la enfermedad, continuando con prednisona 5mg cada 24 horas como corticoterapia.
DISCUSIÓN
La vacuna Sinopharm es el resultado de la inactivación de una cepa de SARS CoV-2, que pertenece a la clase de vacunas que utilizan parte del virus para activar el sistema inmunológico (vacuna con virus atenuado) 9 y es una de las primeras vacunas desarrolladas en el mundo y que llegó al Perú, para ser inoculada en el personal de primera línea. Las diferentes moléculas virales contenidas en la vacuna generaron una respuesta amplificadora de citoquinas que produjo una reacción inmune inadecuada tras la aplicación de la vacuna SARS-CoV-2, esto probablemente debido a factores predisponentes de la paciente para dicha respuesta 10.
Este tipo de complicaciones renales asociada a la vacunación es poco frecuente, pero se ha encontrado la aparición del síndrome nefrótico por cambios mínimos, asociado a vacunación por virus de influenza 11 y por vacunación contra tétano-difteria y poliomielitis (vacunas con virus atenuados) 12. La glomeruloesclerosis focal y segmentaria (GEFS) es el patrón histológico más frecuente de las glomerulonefritis primarias en nuestro país 13 y a nivel mundial 14, esta puede ser primaria a daño glomerular o secundaria a una enfermedad que la origine. La presentación clínica habitual es con edemas, examen de orina anormal (albuminuria, hematuria y/o leucocituria, proteinuria significativa incluso en rango nefrótico) y disminución variable de la función renal 15. En nuestro caso, la paciente presentó la clínica y el diagnóstico histológico de esta patología.
Hasta la fecha, la glomerulopatía de cambios mínimos es la enfermedad glomerular más frecuente relacionada con la vacunación contra el COVID-19 16 con vacunas de la marca Pfizer, AstraZeneca y Moderna. Estos datos fueron encontrados en Italia, 5 de los 17 casos presentaron esta glomerulopatía, y 2 necesitaron hemodiálisis. Todos los pacientes recibieron inmunosupresión y corticoides como nuestro caso y recuperaron la función renal 7.
Asimismo, en Argentina, Arias et al.6) encontraron el caso de una paciente que presentó enfermedad de cambios mínimos, a las 48 horas de la vacunación con la marca Astra-Zeneca. Sin embargo, a diferencia de nuestro caso, esta paciente tuvo el antecedente de síndrome nefrótico en la infancia, pero hubo respuesta clínica favorable a las 4 semanas de iniciado el tratamiento con remisión completa de la proteinuria.
En España, un estudio reportó un caso de nefritis tubulointersticial aguda, el cual no respondió a tratamiento con pulsos de metilprednisolona, por lo que, al no haber recuperación renal requirió hemodiálisis. Este caso es uno de los que presentó mayor complicación renal posvacunación 5. Recientemente, se han descrito casos de síndrome nefrítico con hematuria marcada, debido a nefropatía por IgA 17,18, y debido a glomerulopatía proliferativa extra capilar con semilunas tras la vacunación contra SARS-CoV-2, los cuales requirieron inmunosupresión y plasmaféresis con respuesta favorable 19.
La explicación de las glomerulopatías debido a la vacunación parece ser explicado en estudios previos donde las vacunas producen una respuesta inmunitaria mediada por células a través del reconocimiento de los linfocitos T CD8 20. Como muchas en glomerulopatías, las células T y células B, la respuesta inmune celular y humoral mediada por la vacuna ARNm (Pfizer, Moderna) causan el daño de los podocitos y la aparición de la enfermedad (21. En el caso de la vacuna inactivada como la vacuna Sinopharm, la explicación estaría en una mayor función amplificadora de citoquinas, que desencadenaría el daño glomerular 10.
Existen varios reportes de glomerulopatías después de la administración de vacunas de diversos fabricantes. Se espera que este primer caso reportado en el Perú sea el inicio de más estudios en nuestro país con respecto a los mecanismos inmunes que puedan gatillar los antígenos de la vacuna. Es posible el desarrollo de una glomeruloesclerosis focal y segmentaria de novo, tras la administración de la vacuna contra el SARS-CoV-2, esta condición respondió al uso de corticoides.















