INTRODUCCIÓN
Un aneurisma se refiere a una dilatación localizada de una arteria que es de 1,5 a 2,0 veces más grande que el diámetro de una arteria normal. El aneurisma de la arteria visceral (AAV) es una condición poco común. La verdadera tasa de incidencia no es conocida debido a que la mayoría de los casos de AAV presenta síntomas inespecíficos o incluso puede ser asintomática. Se estima que la tasa de incidencia varía entre 0,01% y 2% 1. El aneurisma de arteria mesentérica superior (AAMS) es una patología vascular mucho menos frecuente, correspondería solo al 6% de los AAV 2. Este caso clínico tiene como objetivo presentar el primer caso tratado de un AAMS en en el Hospital Regional III Honorio Delgado de Arequipa (HRHD) en noviembre 2022; así como brindar una aproximación teórica a sus complicaciones, diagnósticos y tratamiento quirúrgico. Se obtuvo el consentimiento informado del paciente para la publicación del presente reporte.
REPORTE DE CASO
El paciente fue de sexo masculino de 43 años, soltero, con grado de instrucción superior, raza mestiza, natural de Arequipa y religión católica. Como antecedentes se le realizó apendicectomía por laparotomía a los 16 años. El paciente relató un tiempo de enfermedad de 18 meses, caracterizado por dolor en epigastrio. Se le realizó controles y estudios de índole gastroenterológico, llegó a cumplir tratamiento erradicador para Helicobacter pylori; sin embargo, el paciente persistió con la sintomatología descrita, motivo por el cual se decidió ampliar estudios. Se le solicitó tomografía abdominal, en donde se evidencia dilatación aneurismática visceral. Ante el hallazgo, el paciente fue derivado al Servicio de Cirugía de Tórax y Cardiovascular del Hospital Regional III Honorio Delgado de Arequipa.
Al examen físico se halló presión arterial de 120/70 mmHg, temperatura de 36,7°C, frecuencia cardiaca de 90 lpm, y 18 respiraciones por minuto. El abdomen fue blando depresible, con leve dolor a la palpación en epigastrio y mesogastrio, no tuvo masas palpables, y el resto del examen no tuvo otros hallazgos. Se decidió el ingreso del paciente por emergencia, para ser hospitalizado en nuestro servicio.
Se ampliaron los estudios imagenológicos, solicitando angiotomografía (Figura 1A y 1B) que fue informada como aneurisma de tronco celíaco. Se decidió realizar los estudios preparativos, riesgo quirúrgico y tomar las precauciones necesarias para programar al paciente a sala de operaciones.
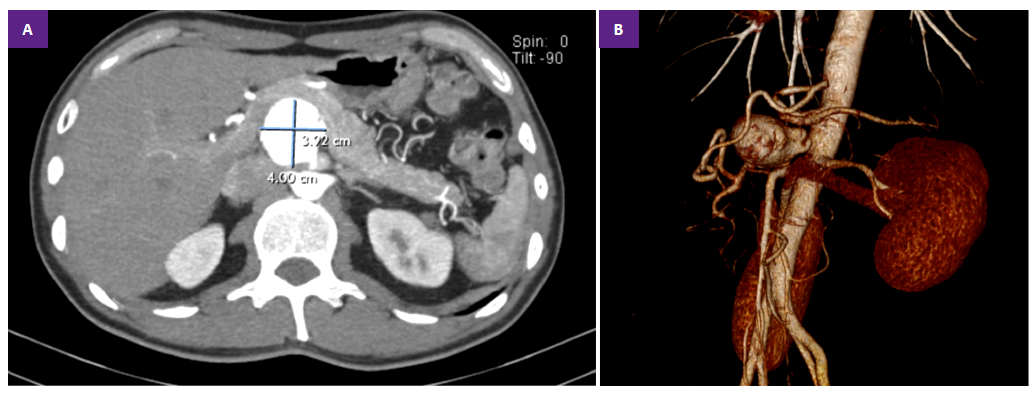
Figura 1. A. Angiografía por tomografía computarizada: Dilatación aneurismática de 4 cm de diámetro aproximadamente, preaórtico, retrayendo el páncreas hacia delante. B. Imagen de reconstrucción: Se observa aneurisma tipo sacular, dependiente de arteria mesentérica superior.
Se realizó la intervención quirúrgica mediante el siguiente procedimiento: el paciente fue ingresado a sala de operaciones con ayuno previo mayor a 8 horas y se le administró anestesia total intravenosa. Se procedió con la asepsia y antisepsia adecuadas y se le colocaron los campos estériles. Se decidió realizar una incisión toracoabdominal izquierda, el abordaje utilizado fue intraperitoneal, se abrió en epiplón menor y mediante palpación se ubicó el aneurisma, luego se dividió la reflexión peritoneal esplenorrenal y se continuó la incisión caudalmente en el canal paracólico izquierdo a lo largo de la línea de Toldt y por un plano anterior a la fascia de Gerota. Se realizó la movilización del estómago, bazo, páncreas y colon descendente (izquierdo) hacia la derecha, dejando en su posición habitual al riñón izquierdo y su glándula suprarrenal. Se logró visualizar el nacimiento de la arteria mesentérica superior (AMS) y la vena renal izquierda; inspeccionando el trayecto del vaso arterial, se ubicó la dilatación aneurismática a 2 cm de su nacimiento. Se evidenció aneurisma de 5 cm x 5cm x 4cm (Figura 2A). Posteriormente, se realizó la liberación de aorta y cadalzamiento de la raíz de la AMS y se realizó la disección de la AMS (tercio medio).
Para realizar control hemostático proximal y distal del aneurisma, se realizó clampaje de AMS (distal) seguido del clampaje transversal de aorta abdominal (proximal), previa administración de heparina sódica no fraccionada 5000 UI EV. Se avisó al equipo de anestesiología antes de la apertura del saco aneurismático. Se realizó la incisión con hoja de bisturí 11 en la cara aneurismática que daba al epiplón menor, hubo un sangrado aproximado de 750 ml. Se resecó completamente el saco aneurismático (Figura 2B). Se realizó bypass con PTFE (politetrafluoroetileno) anillado de 5 mm recto, desde el origen de la mesentérica superior hacia mesentérica superior (tercio medio), con sutura de polipropileno 4/0 y 6/0, respectivamente. El lavado fue realizado con cloruro de sodio al 0,9% y se revisó la hemostasia. La fijación del colon descendente fue con vycril 2/0. Se realizó el cierre de pared por planos. El paciente recibió transfusión sanguínea de dos paquetes globulares dentro de sala de operaciones con adecuada tolerancia al procedimiento.
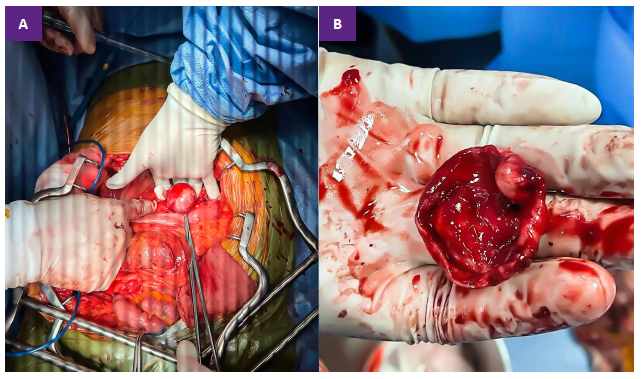
Figura 2. A. Aneurisma de arteria mesentérica superior, vista anterior, previa incisión del epiplón menor. B. Saco aneurismático resecado completamente.
Posterior al acto quirúrgico el paciente pasó a la unidad de vigilancia intensiva (UVI), con infusión de aminas y ventilación mecánica invasiva, donde permaneció por una semana en monitoreo estricto y vigilancia de signos de isquemia mesentérica. Se realizó destete de aminas al segundo día postoperatorio. El informe anatomopatológico reportó pieza de resección parcial de arteria mes-entérica con aneurisma ateroesclerótico y fibroateromas calcificados.
Posteriormente el paciente pasó a nuestro servicio, donde completó tratamiento antibiótico de amplio espectro por 14 días por proceso neumónico intrahospitalario adquirido durante su estancia en UVI. Fue dado de alta, sin requerimiento de oxígeno, realizaba actividades por su propia cuenta, toleraba dieta y realizaba deposiciones.
DISCUSIÓN
Los síntomas del AAMS varían según su ubicación anatómica y suelen ser vagos, lo que retrasa el diagnóstico. Los síntomas incluyen dolor abdominal vago, náuseas y/o vómitos. Si el aneurisma se rompe, el paciente puede experimentar un fuerte dolor abdominal, puede causar una hemorragia potencialmente mortal con inestabilidad hemodinámica, y puede incluso progresar a un síndrome compartimental abdominal 3, que requerirá intervención quirúrgica urgente.
El primer caso reportado en la literatura médica ocurrió en 1912, en el que se describe el AAMS como un hallazgo en la necropsia de una paciente que cursó con epigastralgia con 3 meses de evolución 4, de igual forma los primeros casos reportados fueron hallazgos post mortem. Actualmente la mayoría de los casos son diagnosticados en ruptura 1. Los AAMS no rotos, por lo general, se detectan incidentalmente en la tomografía computarizada (TC), y debido al mayor uso de esta tecnología en la atención médica su detección ha aumentado. Otras técnicas de imagen diagnóstica son la resonancia magnética (RM), la angiografía por tomografía computarizada (CTA) y la ecografía abdominal 5.
La CTA es la herramienta diagnóstica de elección y se recomienda enérgicamente para la detección de AAMS y debe realizarse incluso en aquellos pacientes que fueron diagnosticados por otros métodos imagenológicos 6 (Tabla 1). La imagenología tiene un papel muy importante no solo en el diagnóstico sino también en la planificación del tratamiento. Es importante realizar imágenes abdominales axiales adicionales ya que en estas imágenes es posible determinar múltiples parámetros para la cirugía, como el tamaño del aneurisma, del cuello aneurismático, los vasos accesorios 5, e incluso para detectar variaciones anatómicas que complicarían el tratamiento 7.
Tabla 1. Resumen de las recomendaciones para los aneurismas de arteria mesentérica superior
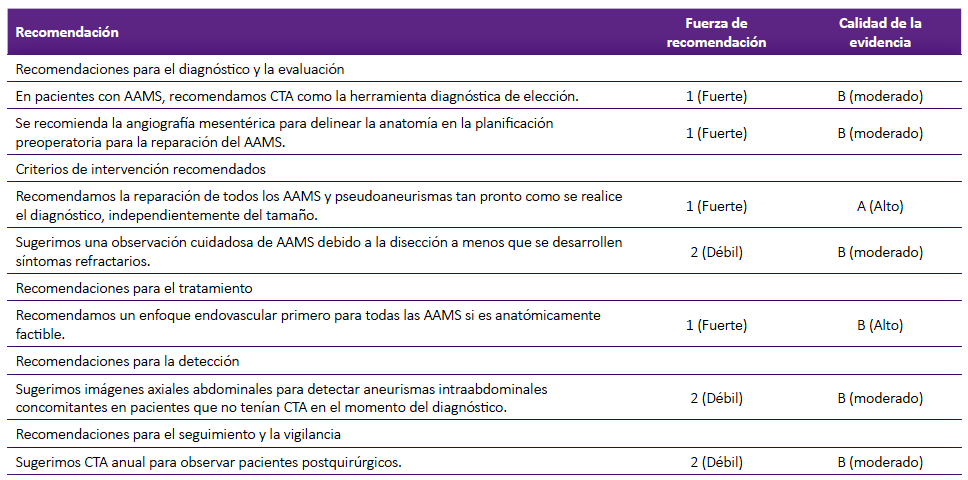
AAMS: aneurisma de arteria mesentérica superior, CTA: angiografía por tomografía computarizada
Elaborado en base a las Guías de práctica clínica de la Sociedad de Cirugía Vascular sobre el manejo de los aneurismas viscerales, 2020.
Nuestro paciente presentó como manifestación clínica epigastralgia persistente, lo que llevó a la sospecha, diagnóstico y tratamiento de gastritis. Gracias a la decisión de realizar una tomografía para evaluar otras etiologías, se logró el diagnóstico de AAV. Aunque el AAMS es una causa poco común de dolor abdominal, debe ser considerado al menos como un diagnóstico de exclusión. La realización de CTA para delinear con mayor precisión la anatomía del aneurisma y las posibles colaterales también fue adecuada (Tabla 1).
El objetivo principal de la cirugía es prevenir la ruptura del aneurisma y restaurar el flujo sanguíneo normal en la mesentérica, permitiendo así una mejor calidad de vida para el paciente. Los AAMS y pseudoaneurismas deben ser reparados tan pronto como se haga el diagnóstico, independientemente del tamaño 6.
Es importante adaptar el tratamiento a las características específicas del AAMS considerando sus manifestaciones clínicas, anatomía, etiología y peculiaridades 8. Para ello, resulta crítico realizar una angiografía que permita delinear la anatomía de la AMS y sus colaterales 6. En general, tanto las técnicas quirúrgicas abiertas como las endovasculares deben quitar el aneurisma y mantener la permeabilidad de los vasos. No obstante, los procedimientos endovasculares suelen tener menos complicaciones que los abiertos 9, por lo que se prefieren si es posible 6. En particular, entre las técnicas endovasculares se incluyen la embolización con muelle y el uso de stents cubiertos, que han demostrado buenos resultados.
Sin embargo, en los AAMS que se extienden más allá de los primeros centímetros proximales, existe un problema importante. En estos casos, el aneurisma involucra tributarios importantes que deben preservarse. Si estos vasos son sacrificados durante un procedimiento endovascular, puede generar complicaciones significativas. Por ello, si el abordaje endovascular conduce a una pérdida importante de colaterales, es recomendable considerar una reparación abierta 10.
Dentro de las opciones de reparación abierta se incluyen la ligadura simple del aneurisma, la aneurismorrafia en caso de aneurismas saculares y la reparación con un injerto de interposición 2,6. Cabe destacar que, en algunos casos, la resección abierta puede requerir la resección intestinal 10. En cualquier caso, es importante observar de cerca la aparición de síntomas peritoneales después de cualquiera de los dos tipos de reparación.
Durante el manejo de nuestro paciente, se intentó cumplir con las recomendaciones establecidas en las guías de práctica clínica de la Sociedad de Cirugía Vascular sobre el manejo de los AAMS de 2020 (Tabla 1). Sin embargo, debido a las limitaciones del hospital, no fue posible realizar una angiografía para delinear la anatomía del AAMS y sus colaterales.
Además, de que no se cuenta con equipamiento para cirugía endovascular, por lo que esta opción tampoco estaba disponible. Por lo tanto, se optó por una técnica abierta para excluir el aneurisma, se trabajó para brindar la mejor atención posible al paciente.
En conclusión, el AAMS es una causa muy rara de epigastralgia, pero debe ser incluido en el diagnóstico diferencial, sobre todo en casos como este. El diagnóstico en su mayoría es incidental, además, debe ser estudiado más detalladamente con una angiotomografía. Todos los AAMS deben ser reparados, independientemente del tamaño, en el menor tiempo posible ya que estos pacientes son considerados una bomba de tiempo por el alto riesgo de ruptura y la mortalidad asociada.















