Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista de Investigaciones Veterinarias del Perú
versión impresa ISSN 1609-9117
Rev. investig. vet. Perú v.23 n.3 Lima ago. 2012
ARTÍCULO DE REVISIÓN
El complejo entérico neonatal en alpacas andinas
Neonatal enteric complex in andean alpacas
Raúl Rosadio A.1,2,3, Lenin Maturrano H.1,2, David Pérez J.2, Luis Luna E.2
1 Unidad de Biología y Genética Molecular, Laboratorio de Microbiología y Parasitología Veterinaria, Facultad de Medicina Veterinaria, Universidad Nacional Mayor de San Marcos, Lima
2CONOPA- Instituto de Investigación y Desarrollo de Camélidos Sudamericanos, Lima
3 E-mail: rrosadio@gmail.com
RESUMEN
Se revisan avances de investigaciones sobre los principales agentes causales de morbilidad y mortalidad en alpacas neonatales asociadas a procesos entéricos en el sur peruano. Análisis microbiológicos confirman al Clostridium perfringens tipo A como el agente prevalente en fatalidades asociadas con enterotoxemia e identifican por primera vez la presencia del gen secundario β2. El análisis in vitro argumenta la existencia de cepas con tres perfiles en la actividad fosfolipídica (alta, mediana y baja), mostrando que las cepas de medianas y altas producciones fueron capaces de producir lesiones intestinales en conejos pero incapaces de producir similares lesiones en crías de alpacas. Estudios histopatológicos revelan la coexistencia de Clostridium y E. macusaniensis en lesiones de enteritis hemorrágica en muestras intestinales de crías muertas por enterotoxemia, sugiriendo a las infecciones coccidiales como posibles agentes desencadenantes de fatalidades conocidas como enterotoxemia. Por otro lado, estudios realizados en hisopados clínicos o contenidos intestinales han identificado molecularmente cepas de E. coli patogénicas (enteropatogénicas y enterohemorrágicas). Adicionalmente, en casos clínicos de diarreas neonatales, mediante inmunofluorescencia directa y PCR, se ha detectado Giardia intestinalis coexistiendo con cepas de E. coli enteropatogénicas, así como un coronavirus similar al virus bovino. Estos patógenos son potenciales causantes de procesos diarreicos en animales incluyendo a poblaciones humanas.
Palabras clave: enteritis neonatal, Clostridium perfringens, E. coli, Eimeria macusaniensis, Giardia intestinalis, alpacas
ABSTRACT
Advances in research on the major causative agents of morbidity and mortality in newborn alpacas associated with enteric processes in southern Peru were reviewed. Microbiology and molecular analyses performed on intestinal samples from enterotoxemia fatalities confirmed the predominance of C. perfringens type A carrying only the gene coding for the major α exotoxin and identifiying for the first time the presence of the novel β2 toxin gene. In vitro studies have yielded three profiles for phospholipase activity (high, medium and low) with biological activity when high and medium strains were inoculated intraintestinally in mice and rabbits, but did not induce intestinal pathology in an alpaca cria. A detailed histopathological investigation has reveled that within necrotizing hemorrhagic enteritis Clostridium coexist with massive presence of Eimeria macusaniensis suggesting that primary parasite tissue destruction may well predispose overgrowth of clostridium and toxin production, triggering enteric fatalities. Additionally, studies on diarrheas intestinal swabs and/or intestinal contents identified Escherichia coli pathogenic strains (enteropathogenic and enterohemorrhagic). The immunofluorescent direct test and PCR revealed the presence of Giardia intestinalis coexisting with mostly enteropathogenic and enterohemorrhagic E. coli strains, as well as with a virus similar to bovine coronavirus. These microbes are potentially diarrheagenic pathogens and a possible infection source for Andean people.
Key words: neonatal enteritis, Clostridium perfringens, E. coli, Eimeria macusaniensis, Giardia intestinalis, alpacas
Introducción
Las elevadas tasas de mortalidad por causas infecciosas, principalmente en las crías de las alpacas, son uno de los factores limitantes para el desarrollo económico de las actividades pecuarias en el mundo andino (Ameghino, 1991). Elucidar las causas de muerte de las crías de alpacas ha sido tema de estudios por investigadores pioneros cuyos esfuerzos estuvieron concentrados en identificar los agentes causales, describir signos clínicos y alteraciones patológicas, así como recomendar posibles tratamientos y medidas de control (Moro y Guerrero, 1971). Posteriormente, los estudios microbiológicos y epidemiológicos ayudaron a entender la ciclicidad de la enterotoxemia y sugerir a la enterotoxina como la responsable de esta patología intestinal (Novoa y Flores, 1991; Ramírez, 1991). Recientemente, una nueva generación de investigadores, utilizando tecnología moderna, intenta identificar los posibles factores de virulencia responsables de los procesos entéricos causantes de las mayores pérdidas económicas de los neonatos en los primeros meses de edad (Rosadio et al., 2008).
Causas de Mortalidad Neonatal
En la actualidad, se acepta que el 80- 85% de los 4-4.5 millones de alpacas del país se concentra en comunidades y parcelas campesinas, mientras que la diferencia pertenece a empresas, todavía existentes, de tipo social, y cooperativas, pequeños y medianos criadores, así como empresas privadas (Ameghino y DeMartini, 1991; Wheeler, 1991; Bustinza, 2001). La crianza de alpacas por los productores comunales es rudimentaria, carente de tecnología y manejo sanitario apropiado, mientras que las empresas utilizan conocimientos y tecnologías productivas que incluyen algunos programas de tratamiento y prevención sanitaria (Bustinza, 2001).
La crianza de alpacas en ambientes comunales es prácticamente de subsistencia, caracterizadas por un pobre rendimiento productivo, con reducidas tasas de fertilidad y elevadas pérdidas neonatales que desgraciadamente no pueden ser analizadas por carencia de registros productivos y sanitarios. Las empresas sociales, contrariamente, manejan registros poblacionales y sanitarios, in cluyendo causas de muertes basadas en diagnósticos de campo y en informes semanales (quiebras). Estos reportes, aunque no muy eficientes, son depositarios de incidencias de mortalidades calendarizadas y por edades (crías, tuis y animales adultos) que permiten analizar el comportamiento de pérdida de animales en una determinada región geográfica y tiempo (Ameghino, 1991; Ramírez, 1991).
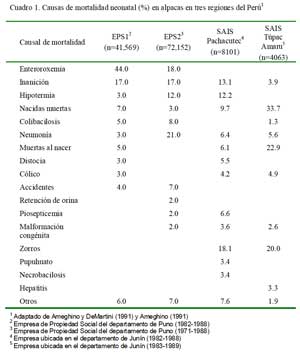
La recolección y análisis de informes mensuales de mortalidad neonatal evidencia que las mayores mortalidades ocurren en animales neonatos hasta los 30 días de edad. Ameghino (1991) y Ameghino y DeMartini (1991) evaluaron las causas de muerte en alpacas neonatas en cuatro organizaciones alpaqueras (dos en el sur y dos de la Sierra Central del Perú), encontrando que en el departamento sureño de Puno predominan las muertes por enfermedades infecciosas y en la Sierra Central predominan las causas no infecciosas (Cuadro 1). Las causas de muertes en el departamento de Puno se circunscriben principalmente a enterotoxemia y neumonías agudas mientras que en las empresas de la Sierra Central predominan las muertes perinatales y las ocasionadas por depredadores. Las diferentes causas de muertes en ambos departamentos reflejan, tal vez, una sobrepoblación animal en las organizaciones puneñas y/o mejores sistemas de manejo en la Sierra Central. Las dos empresas del departamento de Junín son principalmente ovejeras, con un amplio historial de adecuado manejo sanitario y reducida mortalidad de corderos, que al parecer, extrapolan a la crianza de alpacas.
Una de las empresas puneñas perdió el 10% de las 72 152 crías nacidas durante los años 1971-1988, donde la neumonía, la inanición y la enterotoxemia fueron responsable del 57.2% de la mortalidad (Cuadro 1). La otra empresa perdió el 29.9% de 41 569 crías nacidas entre 1982-1988, donde la enterotoxemia y muerte por inanición ocasionaron el 61% de las pérdidas (Cuadro 1). Las tasas de mortalidad en las dos empresas del centro del país son menores del 10%, donde animales depredadores (zorros), inanición, hipotermia y nacidas muertas representaron el 53% del total de la mortalidad en una de las empresas, en tanto que nacidas muertas y muertas al nacer fueron responsables del 56.6% del total de las muertes en la otra empresa (Ameghino, 1991).
Enterotoxemia
La enterotoxemia es la principal causa de mortalidad neonatal en el sur del Perú (Ameghino y DeMartini et al., 1991; Ramírez, 1991). Históricamente, Clostridium perfringens tipos A y C ha sido considerados como los agentes desencadenantes del proceso infeccioso (Ramírez, 1991). Investigaciones realizadas por nuestro grupo de investigadores durante los últimos cinco años corroboran estas afirmaciones (Pérez, 2006, 2010; Rosadio et al., 2008), donde se encontró que el 99.6% de 224 aislados de casos fatales de la enfermedad correspondían a C. perfringens tipo A y el diferencial al tipo C. En esos estudios, el 91.1% de las cepas tipo A contenían únicamente el gen cpa codificante de la exotoxina α, mientras que las 19 restantes (8.5%) tenían, además, la toxina secundaria β2 (Pérez, 2006; Rosadio et al., 2008), pero ninguna contenía el gen cpe codificante de la enterotoxina, toxina sugerida en el pasado de ser responsable de la enterotoxemia (Ramírez, 1991). Asimismo, en un análisis realizado in vitro con toxinas (fosfolipasas) semipurificadas de 12 cepas de tipo A, se detectaron tres perfiles en la producción enzimática (alta, mediana y baja) con capacidad de producir lesiones en ratones y conejos al inocularse intraintestinalmente (cepas de alta y mediana producción), pero incapaces de causar lesiones similares en crías de alpacas (Pérez, 2010). Estos resultados sugieren que el complejo enterotoxémico no es producto de una infección única y, tal vez, sea consecuencia de interacciones patológicas de exotoxinas clostridiales con infecciones primarias de parásitos intracelulares (Ejem. Eimeria spp) o virus enteropatogénicos (Ejem. Coronavirus, Rotavirus).
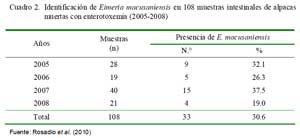
La presencia de E. macusaniensis en animales muertos por enterotoxemia o por diarrea ha sido reportada (Rosadio y Ameghino, 1994; Palacios et al., 2006). En el 30.6% (33/108) de muestras intestinales de animales con enterotoxemia se demostró coexistencia de masiva presencia de Eimeria macusaniensis (Cuadro 2), sugiriendo que las infecciones coccidiales podrían ser un factor facilitador de la multiplicación clostridial o de la excesiva producción de toxinas necesarias para generar la enfermedad. Asimismo, en todas estas muestras se aisló C. perfringens tipo A. Por otro lado, las severas lesiones necróticas de las mucosas intestinales fueron consideradas, inicialmente, como consecuencia de las toxinas α y β2 del C. perfringens, tipo A (Pérez, 2006); sin embargo, la presencia de numerosas estructuras parasitarias correspondientes a E. macusaniensis fueron, también, interpretadas como potenciales patologías producto de la replicación de estadios inmaduros coccidiales (Rosadio et al., 2010).
La presencia de E. macusaniensis en animales muertos por enterotoxemia o por diarreas permite proponer a las infecciones por Eimeria spp como uno de los posibles factores desencadenantes o predisponentes para el establecimiento de la enterotoxemia de la alpaca. La coexistencia de Eimeria y Clostridium merece ser ampliamente investigada, pues estas interacciones patológicas pueden causar severa enteritis hemorrágica necrotizante en otras especies de animales, muy similar a las descritas en la enterotoxemia en alpacas. La asociación entre Eimeria y Clostridium ha sido descrita en procesos enterotoxigénicos en camellos (Kinne y Wernery, 1998), pero es un concepto nuevo en camélidos sudamericanos.
Enteritis Infecciosa Neonatal
Las diarreas neonatales, causantes de muertes y reportadas como colibacilosis o enteritis (Ameghino y DeMartini, 1991), han sido pocos estudiadas en el Perú. La poca información existente evidencia la presencia de numerosos agentes e incluyen al C. perfringens, Eimeria spp, Cryptosporidium spp y Escherichia coli como potenciales patógenos productores de alteraciones entéricas (Ramírez et al., 1985; Rosadio y Ameghino, 1994; Palacios et al., 2006). Por otro lado, es conocido que en la mayoría de animales domésticos, la E. coli causa una diversidad de patologías, desde infecciones entéricas restringidas hasta septicemias, que se explican por la presencia de una gama diversa de genes virulentos.
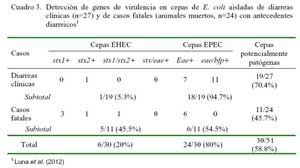
En muestras fecales de 51 alpacas menores de 50 días de edad, cuya muerte estuvo asociada a diarreas o presentaban signos clínicos de diarrea, se aisló E. coli utilizando metodología convencional y se descartó la presencia de rotavirus mediante análisis de electroforesis y coloraciones de nitrato de plata. Las cepas de E. coli fueron analizadas con la prueba PCR Multiplex empleando cebadores para amplificar los genes codificantes de las toxinas shiga 1 y 2 (stx1 y stx2), toxinas termo-labiles (lt) y termo-resistentes a y b (sta y stb), así como genes de la intimina (eae) y del Bundle-forming Pili (bfp) (Luna et al., 2012). El análisis genotípico evidenció que 58.8% (n=30) contenían genes asociados a virulencia, encontrándose 24 cepas con el gen eae o bfp (cepas potencialmente enteropatogénicas/EPEC) y seis cepas donde se amplificaron segmentos correspondientes a genes enterohemorrágicos/ ECEH (stx2, stx1 o ambas), pero en ninguna se logró identificar genes lt, sta o stb correspondientes a E. coli enterotoxigénicas (Cuadro 3) (Luna et al., 2012).
Las cepas enteropatogénicas eae y bfp son productoras de diarrea debida a su capacidad de adherirse a los enterocitos, inicialmente en forma laxa, a través del producto bfp y, posteriormente, en una forma más fuerte que elimina (cepillado) a las microvellosidades intestinales a consecuencia de la proteína intimina codificada por el gen eae (Nataro y Kaper, 1998). Las cepas de E. coli enterohemorrágicas son, teóricamente, más agresivas que las EPEC a consecuencia de genes con capacidad de secretar proteínas altamente tóxicas (veroci-totoxinas) y codificadas por cualquiera de los genes stx (Nataro y Kaper, 1998). Interesantemente, estas cepas EHEC podrían incrementar su patogenicidad si expresaran simultáneamente genes con capacidad de adherencia productora de la intimina (Alikhani et al., 2006). En el estudio de Luna et al. (2012), ninguna de las cepas EHEC tenía el gen eae; sin embargo, las lesiones intestinales de las crías muertas con historia de diarrea correspondieron mayoritariamente a enteritis hemorrágica, detectándose mayormente cepas positivas a genes stx (EHEC) y al gen eae (EPEC).
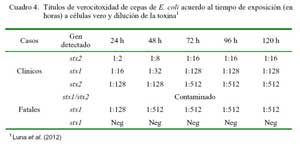
La asociación positiva entre presencia de cepas EPEC con signos clínicos diarreicos sugieren causalidad de cuadros diarreicos, pero llama la atención la significativa presencia de cepas EHEC en intestinos hemorrágicos sin expresar factores de adherencia, impidiendo asociar su presencia con las lesiones patológicas descritas. Sin embargo, se llegó a detectar algunas cepas stx-positivas que fueron capaces de producir verocitotoxinas para células Vero (Cuadro 4, Luna et al., 2012). Consecuentemente, las cepas EHEC son altamente activas a nivel intestinal, por lo que se debe descartar la potencialidad patogénica de las cepas EHEC, sobre todo en lesiones enterohemorrágicas muy similares a enterotoxemia.
En otra investigación con 100 muestras de diarreas neonatales procedentes de cuatro establecimientos del sur del Perú se detectaron cepas similares. Dos de 94 aislados fueron cepas EPEC (eae y bfp), 10/94 cepas APEC atípicas (solamente eae) y 11/94 cepas EHEC (dos de ellas eae positivas) (Cid et al., 2010). El potencial de causalidad de diarrea de estas también ha sido observado en cepas conteniendo genes stx1, stx2 y eae en el 20% de diarreas fatales en crías de 1-2 meses de edad (Bravo de Rueda, 2006), y en un brote de severa diarrea catarral en guanacos patagónicos cuya cepa fue genotipificada como ECEH (Mercado et al., 2004). Esta última cepa argentina, identificada como O26:H11, además de ser positiva para los genes stx1 y eae, fue productora de verocitotoxina con presencia de un factor de adherencia focalizada (prueba de adhesión en células HEp-2) (Mercado et al., 2004).
La presencia de cepas de E. coli conteniendo genes patogénicos en cuadros clínicos diarreicos y en casos de muertes en alpacas neonatas demuestran la existencia de una gran diversidad genética de esta bacteria, ya que puede producir diversos cuadros diarreicos que varían desde procesos autolimitantes (cepas enteropatógenas) hasta patologías más dramáticas, asociadas con posibles enteritis necrotizantes, producto de la presencia de genes con capacidad de penetración celular conferidos por genes enteroinvasivos como las toxinas shiga (stx) (Blanco et al., 1997). La presencia de cepas potencialmente enterohemorrágicas en camélidos, además, revela un potencial riesgo para las poblaciones humanas, pues cepas similares son productoras de patologías intestinales y sistémicas en el hombre (Alikhani et al., 2006). Este riesgo es relevante pues el manejo de alpacas en el mundo andino implica un estrecho contacto de los pastores y su familia con las crías, especialmente con las más débiles y las que se encuentran enfermas.
Infecciones Parasitarias Neonatales
Las infecciones parasitarias han sido frecuentemente reportadas en alpacas, pero informaciones sobre asociación entre presencia parasitaria y presentaciones clínicas patológicas, principalmente diarreas neonatales, son casi inexistentes. Hubo cierto interés por elucidar la presencia de Cryptosporidium spp en neonatos con resultados un tanto controversiales (Fernández, 1995), pero hasta la fecha se le sigue sugiriendo como un posible factor de riesgo en la producción de diarrea (Palacios, 2008).
En un estudio reciente, realizado en 200 muestras diarreicas de alpacas menores de un mes de edad se evidenció la coexistencia de otros agentes parasitarios potencialmente enterogénicos. Así, mediante inmunofluorescencia indirecta y PCR se encontró cerca del 50% de muestras positivas a Giardia spp (Gómez-Couso et al., 2011), lo que podría confirmar a este agente como uno de los principales agentes potencialmente productores de diarreas en alpacas neonatas y jóvenes (Cebra et al., 2003). En estas mismas muestras, se detectó además la presencia de cepas E. coli conteniendo genes asociados a virulencia enteropatogénicas y clasificadas como ECEP (2/94 típicas y 10/94 atípicas) y EHEC (11/94) (Cid et al., 2010). Además, en 6/18 de estas muestras se amplificó material geonómico similar a un coronavirus bovino (L. Luna, Lima, comunicación personal). La actividad patológica de estos patógenos en forma individual y en coinfecciones tendrá que ser analizada minuciosamente.
Las alpacas son susceptibles a infecciones por coccidias, siendo los neonatos los más susceptibles a todos los tipos de Eimeria, especialmente a infecciones fatales de E. macusaniensis (Rosadio y Ameghino, 1994; Palacios et al., 2006). Los adultos son resistentes a eimeriosis clínicas, pero algunos de estos animales se mantienen infectados y actuarían como posibles fuentes de infección para poblaciones altamente susceptibles (neonatos) durante la época de parición.
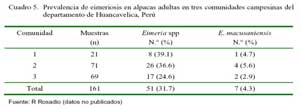
Resultados de un análisis coprológico en 161 alpacas en el segundo tercio de la gestación revelaron que 31.7 y 4.3% de los animales eran positivos a Eimeria spp y E. macusaniensis, respectivamente (Cuadro 5) (R. Rosadio, datos no publicados). Estos animales portadores actuarían como posibles fuentes de infección para las primeras crías en los meses iniciales de la parición y, estos a su vez, actuarían como animales amplificadores de infecciones para el resto de las crías en los meses siguientes de la campaña de parición.
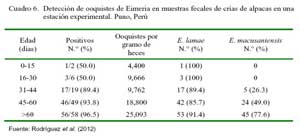
En otro estudio en alpacas neonatas, realizado en una estación experimental, se demostró que el 94.3% eliminaba ooquistes de E. lamae y el 60.1% de E. macusaniensis (Rodríguez et al., 2012), donde el número de ooquistes por gramo de heces se incrementó con la edad. Las alpacas, en las primeras semanas de vida eliminan ooquistes de eimerias pequeñas (lamae, alpacae y punoensis) y a partir de los 45 días comienzan a eliminar en grandes cantidades la Eimeria más patogénica (E. macusaniensis) (Cuadro 6); lo cual indica que las crías se infectan muy tempranamente y que es probable que ocurra un daño a nivel instestinal durante la etapa prepatente por infecciones con E. macusaniensis (Cebra et al., 2007).
Consecuentemente, las lesiones de tipo necróticas y hemorrágicas observadas comúnmente en lesiones atribuidas a enterotoxemia podrían ser producto de multiplicaciones eimeriales. Asimismo, este tipo de lesiones podrían predisponer a coinfecciones microbiológicas incluyendo infecciones clostridiales (Rosadio et al., 2010).
CONCLUSIONES
-
Las investigaciones realizadas para elucidar la etiopatogénesis de la enterotoxemia de la alpaca en el Perú están llevando a entender que el tracto intestinal del neonato es blanco de múltiple infecciones con capacidad de alterar la salud intestinal conducente a patologías directas o predisposiciones que conduzcan al desencadenamiento del complejo enterotoxémico.
-
La detección de cepas de C. perfringens con diferentes perfiles en la producción de fosfolipasas (toxina α) evidencian la existencia de poblaciones bacterianas con diversas habilidades patológicas que deben ser analizadas experimentalmente para determinar su capacidad patológica individual y en asociación sinérgica con otros agentes (Ejem. E. macusaniensis) en procesos intestinales.
-
La patogenicidad clostridial puede expresarse e incrementarse si el estado e integridad de la salud intestinal se encuentra alterado por ciertos factores biológicos y fisiológicos.
-
La búsqueda de potenciales patógenos intestinales primarios ha permitido identificar agentes microbianos en edades tempranas del neonato incluyendo Giardia spp, Eimeria spp, E. coli y coronavirus que podrían actuar como posibles agentes biológicos productores de diarreas o predisponentes de infecciones clostridiales para desencadenar afecciones intestinales, incluyendo la enterotoxemia.
LITERATURA CITADA
1. Alikhani MY, Mirsalehian A, Aslani MM. 2006. Detection of typical and atypical enteropathogenic Escherichia coli (EPEC) in Iranian children with and without diarrhoea. J Med Microbiol 55: 1159-1163.
2. Ameghino E. 1991. Causas de mortalidad en crías de alpacas. En: Fernández- Baca S (ed). Avances y perspectivas del conocimiento de los camélidos sudamericanos. Santiago de Chile: FAO. p 149-200.
3. Ameghino E, DeMartini J. 1991. Mortalidad de crías de alpacas. Bol Div IVITA, Lima. p 71-80.
4. Blanco M, Blanco JE, Blanco J, Mora A, Prado C, Alonso MP, Mourino M, et al. 1997. Distribution and characterization of faecal verotoxin producing Escherichia coli (VTEC) isolated from healthy cattle. Vet Microbiol 54: 309-319.
5. Bustinza V. 2001. La alpaca: conocimiento del gran potencial andino. Puno, Perú: Univ Nac del Altiplano. 496 p.
6. Bravo de Rueda C. 2006. Caracterización molecular de los genes stx1, stx2 y eae en aislados de Escherichia coli de crías de alpacas con diarrea. Tesis de Médico Veterinario Zootecnista. Lima: Univ Peruana Cayetano Heredia. 73 p.
7. Cebra CK, Mattson DE, Baker RJ, Sonn RJ, Dearing PL. 2003. Potential pathogens in feces from unweaned llamas and alpacas with diarrhea. J Am Vet Med Assoc 223: 1806-1808.
8. Cebra CK, Valentine BA, Schlipf JW, Bildfell RJ, McKenzie E, Waitt LH, Heidel JR, et al. 2007. Eimeria macusaniensis infection in 15 llamas and 34 alpacas. J Am Vet Med Assoc 230: 94-100.
9. Cid D, Martin-Espada C, Maturrano L, García A, Luna L, Rosadio R. 2010. Diarrheagenic Escherichia coli strains isolated from neonatal Peruvian alpacas (Vicugna pacos) with diarrhea. V Simposio Europeo sobre Camélidos y otras Fibras. Sevilla, España.
10. Fernández M. 1995. Prevalencia de Crytosporidium parvum en alpacas neonatas del Centro Experimental La Raya-Cuzco. Tesis de Médico Veterinario. Lima: Univ Nac Mayor de San Marcos. 48 p.
11. Gómez-Couso H, Ortega-Mora LM, Aguado-Martínez A, Rosadio- Alcántara R, Maturrano-Hernández L, Luna-Espinoza, et al. 2011. Molecular characterization of Giardia and Cryptosporidium in alpacas (Vicugna pacos) from Peru. XXIII Internat Conf World Association for Advancement of Veterinary Parasitology. Buenos Aires, Argentina.
12. Kinne J, Wernery U. 1998. Pathological studies on camel coccidiosis in the United Arab Emirates. Proc III Meeting for Animal Production under Arid Conditions 1: 131-142.
13. Luna L, Maturrano L, Rivera H, Zanabria V, Rosadio R. 2012. Genotipificación, evaluación toxigénica in vitro y sensibilidad a antibióticos de cepas de Escherichia coli aisladas de casos diarreicos y fatales en alpacas neonatas. Rev Inv Vet, Perú 23: 280-288.
14. Mercado EC, Rodríguez S, Elizondo A, Marcoppido G, Parreño V. 2004. Isolation of Shiga toxin-producing Escherichia coli from a South American camelid (Lama guanicoe) with diarrhea. J Clin Microbiol 42: 4809-4811.
15. Moro M, Guerrero C. 1971. La alpaca: enfermedades infecciosas y parasitarias. Bol Div IVITA, Lima. 63 p.
16. Nataro J, Kaper J. 1998. Diarrheagenic Escherichia coli. Clin Microbiol Rev 11: 142-201.
17. Novoa C, Flores A. 1991. Producción de rumiantes menores: alpacas. Lima: Rerumen. 358 p.
18. Palacios C, Perales R, Chavera A, López M, Braga W, Moro M. 2006. Eimeria macusaniensis and Eimeria ivitaensis co-infection in fatal cases of diarrhea in young alpacas (Lama pacos) in Peru. Vet Rec 158: 344-345.
19. Palacios C. 2008. Estudio caso control del Crytosporidium como factor de riesgo en la diarrea neonatal en alpacas menores a 15 días. Tesis de Magíster. Lima: Univ Nac Mayor de San Marcos. 73 p.
20. Pérez D. 2006. Genotipificación y subtificación de Clostridium perfringens aislados de crías de alpacas muertas por enterotoxemia. Tesis de Médico Veterinario. Lima: Univ Nac Mayor de San Marcos. 91 p.
21. Pérez D. 2010. Caracterización toxigénica de la fosfolipasa C del Clostridium perfringens (Cp-PLC) y su relación con aislados casos de enterotoxemia en alpacas. Tesis de Magíster. Lima: Univ Nac Mayor de San Marcos. 151 p.
22. Ramírez A, Huamán D, Ellis RP. 1985. Enterotoxemia de la alpaca. Programa colaborativo de apoyo a la investigación en rumiantes menores. Serie Reporte Técnico. Lima 63: 1-17.
23. Ramírez A. 1991. Enfermedades infecciosas. En: Fernández-Baca S (ed). Avances y perspectivas del conocimiento de los camélidos sudamericanos. Santiago de Chile: FAO. p 263-324.
24. Rosadio R, Ameghino E. 1994. Coccidial infections in neonatal Peruvian alpacas. Vet Rec 135: 459-460.
25. Rosadio R, Maturrano L, Pérez D, Llanco L, Castillo H, Veliz A, Yaya K, Londoñe P. 2008. Enterotoxemia: new evidence on pathogenesis and prevention of the number one cause of neonatal alpaca mortality in South America. Proc World Alpaca Conference. Sydney, Australia. p 50-55.
26. Rosadio R, Londoñe P, Pérez D, Castillo H, Véliz A, Llanco L, Yaya K, Maturrano L. 2010. Eimeria macusaniensis associated lesions in neonate alpacas dying from enterotoxemia. Vet Parasitol 168: 116-120.
27. Wheeler J. 1991. Origen, evolución y status actual. En: Fernández-Baca S (ed). Avances y perspectivas del conocimiento de los camélidos sudamericanos. Santiago de Chile: FAO. p 11-48.