Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista de Investigaciones Veterinarias del Perú
versión impresa ISSN 1609-9117
Rev. investig. vet. Perú vol.29 no.1 Lima ene./mar. 2018
http://dx.doi.org/10.15381/rivep.v29i1.14159
ARTÍCULOS PRIMARIOS
Efecto del ácido retinoico sobre la expresión del receptor CCR9 y la integrina alfa 4 beta 7 en leucocitos sanguíneos de alpacas(Vicugna pacos)
Effect of retinoic ccid on expression of receptor CCR9 and alpha 4 beta 7 integrin in alpaca blood leukocytes (Vicugna pacos)
Eduardo Hermoza C.1, Alberto Manchego S.1,4, Gina Castro S.1, Danilo Pezo C.3, Nieves Sandoval C.2
1 Laboratorio de Microbiología y Parasitología Veterinaria,
2 Laboratorio de Histología, Embriología y Patología Veterinaria, Facultad de Medicina Veterinaria, Universidad Nacional Mayor de San Marcos, Lima, Perú
3 Estación Experimental del Centro de Investigación IVITA, Sede Maranganí, Universidad Nacional Mayor de San Marcos, Cusco, Perú
4 E-mail: amanchegos@unmsm.edu.pe
RESUMEN
Las células T efectoras (CD4+ y CD8+) y de memoria pueden migrar a la mayoría de los tejidos extra-linfoides en el cuerpo, pero requieren la expresión de receptores de alojamiento (homing) específicos en las células T, la integrina α4β7 y el receptor de quimiocina CCR9. Los linfocitos circulantes CD4+ o CD8+ carecen de receptores CCR9 y α4β7; sin embargo, expresan este tipo de receptores al alcanzar la mucosa intestinal. El objetivo del estudio fue determinar el efecto del ácido retinoico sobre la expresión de los receptores CCR9 y la integrina α4β7 en linfocitos sanguíneos de alpacas (Vicugna pacos). Se realizó un análisis in vitro de muestra de sangre circulante de alpaca. Los leucocitos obtenidos se colocaron en placas de cultivo celular en medio esencial mínimo (MEM) suplementados e inoculados con ácido retinoico a concentraciones de 10, 50 y 100 ìg/ml disuelto en DMSO. Se empleó un control a base de suero fisiológico. Las placas de cultivo celular fueron incubadas por 12, 24 y 48 h a 37 ºC con CO2 al 5%. Se realizó las PCR en Tiempo Real de losARNm del receptor CCR9 y la integrina α4β7 yla cuantificación relativa con el método 2-ΔΔCt. Las máximas expresiones para CCR9 se dieron a las 48 h para las concentraciones de 10 y 100 µg/ml de ácido retinoico y DMSO, y a las 24 h para la concentración de 50 µg/ml. El control presentó expresiones mucho más elevadas en comparación con las dosis de ácido retinoico y DMSO. No hubo expresión para la integrina α4β7.
Palabras clave: CCR9; alfa4beta7; ácido retinoico; homing; intestino; alpacas
ABSTRACT
Effector T cells (CD4+ and CD8+) and memorycells can migrate to most extra lymphoid tissues in the body, but require the expression of specific homing receptors in T cells, α4β7 integrin and receptor chemokine CCR9. CD4+ or CD8+ circulating lymphocytes lack CCR9 and α4β7 receptors; however, these receptors are expressed upon reaching the intestinal mucosa. The aim of the study was to determine the effect of retinoic acid on the expression of CCR9 receptors and α4β7 integrin on alpaca lymphocytes (Vicugna pacos). An in vitro analysis of circulating alpaca blood sample was performed. The obtained leukocytes were placed in cell culture plates in minimal essential medium (MEM) supplemented with retinoic acid at concentrations of 10, 50 and 100 ìg/ml dissolved in DMSO. A control based on physiological serum was used. Cell culture plates were incubated for 12, 24 and 48 h at 37 °C with 5% CO2. Real-time PCR of the CCR9 receptor mRNA and α4β7 integrin and relative quantification with the 2-ΔΔCt method were performed. The maximum expressions for CCR9 were given at 48 h for concentrations of 10 and 100 µg/ml of retinoic acid and DMSO, and at 24 h for the concentration of 50 µg/ml. The control had much higher expressions compared to the doses of retinoic acid and DMSO. There was no expression for the α4β7 integrin.
Key words: CCR9; alfa4beta7; retinoic acid; homing; intestine; alpaca
INTRODUCCIÓN
Una de las principales limitantes para el buen desarrollo y crianza de la alpaca son los problemas entéricos de origen infeccioso que reducen la eficiencia productiva y que generan grandes pérdidas económicas a los criadores. Estos problemas entéricos son controlados por la inmunidad de la mucosa intestinal; sin embargo, es poco lo que se conoce sobre el desarrollo y establecimiento de la respuesta inmune de mucosas en alpacas y la manera que se puede incrementar esta respuesta.
Los linfocitos T que se dirigen al intestino expresan α4β7 y CCR9. Este mecanismo permite a las células migrar específicamente a sitios mucosos (gut homing). Esta migración de células hacia el intestino es influenciada por el receptor de quimiocina CCR9 y su ligando CCL25, expresado en el epitelio intestinal. El rodamiento de linfocitos en el endotelio intestinal está mediado por la integrina á4â7 expresada en linfocitos T y B de la lámina propia del tracto intestinal y su interacción con la molécula 1 de adhesión celular adhesina vascular mucosa (MAdCAM1), expresada en células endoteliales (Cassani et al., 2011). El ácido retinoico, compuesto derivado de la vitamina A producido a nivel de la mucosa intestinal, promueve la expresión de α4β7 y CCR9 en linfocitos T provocando su activación y marcación con el tropismo intestinal (Iwata et al., 2004).
El ácido retinoico regula las respuestas inmunes intestinales a través de acciones inmunomoduladoras sobre las células intestinales dendríticas (DCs) y linfocitos. Zeng et al.(2013) mostraronqueelARtambiéncontrola la generación de precursores de DC migratorias intestinales, denominadas DCs pre-mucosales (pre-uDCs). Estas expresan el receptor intestinal α4β7 y se alojan preferentemente en el intestino. Se desarrollan en la médula ósea, pueden diferenciarse en células dendríticas plasmacitoides CCR9+, así como en CDs convencionales, pero preferentemente dan lugar a CDs intestinales CD103+. La generación de pre-uDCs in vivo en la médula ósea o in vitro está regulada por la señalización de ácido retinoico con su receptor RARα. La frecuencia de pre-u-DCs se reduce en animales con avitaminosis A y en animales tratados con inhibidores de RAR (Zeng et al., 2013).
El ácido retinoico regula directa e indirectamente la actividad de células T incluyendo la apoptosis inducida por activación y el desarrollo de linfocitos Th1 y Th2 (Iwata et al., 2004). El ATRA, o ácido retinoico alltrans, es un regulador transcripcional de células troncales hematopoyéticas al promover la retención de las mismas en cultivos celulares (Purton et al., 2000; Leung y Verfaillie, 2005). Se ha visto que el número de células madre hematopoyéticas fue bajo en ratones tratados con receptor de ácido retinoico (RAR) y gen RARã, mientras que los progenitores hematopoyéticos se incrementaron anormalmente (Purton et al., 2006). Algunos genes regulados por retinoides son c-myc, stra-13, hoxb4 y notch 1, todos relacionados a la hematopoyesis (Collins, 2002; Purton et al., 2006).
La presencia de ácido retinoico ha sido asociada al alojamiento u homing de linfocitos T y B en el intestino delgado (Kim, 2008). Los linfocitos T CD4 memoria y CD8 y linfocitos B secretores de IgA que se dirigen al intestino expresan la integrina α4β7, que se une a la molécula 1 de adhesión celular adhesina vascular mucosa (MAdCAM1) expresada en células endoteliales, y el receptor de quimiocina CCR9, que se une a su ligando CCL25 expresado en el epitelio intestinal (Cassani et al., 2011). De esta manera, el AR promueve la expresión de α4β7 y CCR9 en linfocitos T favoreciendo el tropismo intestinal.
Se ha demostrado que el ácido retinoico en conjunción con TGF-β, promueve la conversión de células T nativas en células T reguladoras (Treg) Foxp3+, lo que evidencia la producción de células Treg periféricas en condiciones normales (Coombes et al., 2007; Elías et al., 2008). Por tanto, el ácido retinoico es considerado una señal reguladora clave en la inducción de la tolerancia inmune intestinal (Wang et al., 2010) al estimular la producción de TGF-β (Maynard et al., 2009) y favorecer la generación de células Treg por células dendríticas (Sun et al., 2007). Es importante recalcar que existen dos tipos de células Treg: las naturales, generadas a nivel tímico, y las inducidas, generadas a partir de células T nativas en diferentes zonas del organismo, principalmente en el tracto intestinal (Housley et al., 2009).
El presente estudio in vitro tuvo como objetivo evaluar el efecto del ácido retinoico como inmunoestimulante, cuantificando relativamente la expresión de CCR9 y α4β7 de linfocitos a través de la prueba molecular de la reacción en cadena de la polimerasa a tiempo real (RT-PCR) para determinar indirectamente su acción sobre el establecimiento linfoide a nivel intestinal. Este estudio brinda una visión de una nueva estrategia de control de las enfermedades entéricas para diseñar vacunas que permitan reducir infecciones en el tracto intestinal.
MATERIALES Y MÉTODOS
Lugar de Estudio y Muestras
Se utilizó sangre entera periférica (10 ml) de cinco alpacas adultas del Laboratorio deQuímica,Bioquímica yNutriciónAnimal y el estudio de la expresión génica de CCR9 y α4β7 se realizó en las instalaciones del Laboratorio de Inmunología de la Facultad de Medicina Veterinaria (FMV) de la Universidad Nacional Mayor de San Marcos (UNMSM) (Lima, Perú).
Las muestras de sangre fueron colectadas en tubos tipo vacutainer con EDTA, por punción de la vena yugular. Los tubos fueron centrifugados a 2000 g por 5 min y la parte celular fue vertida a cuatro tubos Falcon conteniendo (1.5 por tubo). Luego se vertió 12.5 ml de solución de lisis de eritrocitos (cloruro de amonio) en cada tubo completando a 14 ml de solución total. Todos los tubos fueron agitados manualmente por 5 min y centrifugados a 1800 g por 5 min. Se eliminó el sobrenadante y el pellet celular se lavó con suero fisiológico. Finalmente, los tubos fueron centrifugados dos veces a 1800 g por 5 min.
Cultivo Celular
Los leucocitos obtenidos fueron disueltos en medio de cultivo RPMI en una concentración de 500 000 células por mililitro de medio y cultivados en una placa de cultivo celular de 24 pocillos. Se colocó 1 ml en cada pocilloyse agregó100µldeATRAendiversas diluciones para obtener concentraciones de 10, 50 y 100 µg/ml de ATRA en cada columna de la placa, cada una con tres repeticiones. Los controles consistieron en células sin aditivos y células con DMSO, ambas con tres repeticiones cada una. El medio de cultivo celular RPMI fue suplementado con 10% de suero fetal bovino (GIBCO) y penicilina 1% (Sigma Aldrich).
Las placas fueron incubadas a 37 °C por 12, 24 y 48 h. La primera cosecha de todo el pocillo se hizo a las 0 h y luego a las 12, 24 y 48 h. El total del medio cosechado fue congelado a -70 °C en viales, hasta su uso para la extracción de ARN total.
Extracción de ARN Total
Se tomó 1 ml de cada uno de los pocillos para la extracción de los ARN totales. Se empleó el reactivo TRIZOL® (Invitrogen, EEUU) siguiendo las instrucciones del fabricante. El ARN total fue precipitado con alcohol isopropílico frío, centrifugado e inmediatamente lavado con etanol frío al 70%. Finalmente, el ARN total fue resuspendido en 60 µl de agua libre de nucleasas y almacenado a 0 ºC hasta su uso en el RT-PCR.
Síntesis de ADN Complementario por Transcripción Inversa (RT)
El ARN obtenido de cada pocillo fue tomado como templado para la síntesis de ADNc, empleándose el kit ‘SYBR® GreenERTM Two-Step qRT-PCR Kit Universal’ (Invitrogen, EEUU), siguiendo las instrucciones del fabricante. El volumen final para la Transcripción Reversa (RT) fue de 20 µl por reacción/muestra, compuesta por 18 µl del master mix (2x RT reaction mix 10 µl x n, RTenzyme mix 1 µl x n, hexámeros al azar 1 µl x n, H2O 6 µl x n (n=número de muestras a trabajar) más 2 µl de ARN templado de cada una de las muestras en los tubos correspondientes.
Las muestras se llevaron al termociclador ABI7500 (Life Technologies, EEUU) programado con el siguiente protocolo: 25 ºC por 10 min, 50 ºC por 30 min, 85 ºC por 5 min. Seguidamente, las muestras fueron conservadas en hielo por 5 min, se adicionó 1 µl de ARNasa H (RNAse H) y se incubaron a 37 °C por 20 min. El ADNc obtenido fue congelado a -70 °C hasta su uso en la reacción de PCR Tiempo Real.
PCR Tiempo Real
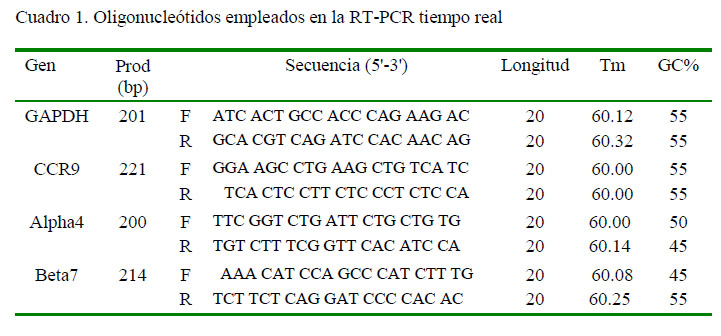
Los oligonucleótidos empleados fueron diseñados en el Laboratorio de Inmunología (FMV-UNMSM) con base de los genes disponibles en el GenBank. Se muestran en el Cuadro 1.
Se empleó el ADNc de cada una de las muestras como templado para la reacción de PCR con el kit ‘SuperScriptTM III First-Strand Synthesis SuperMix for qRT-PCR’ (Invitrogen, EEUU), siguiendo las recomendaciones del fabricante. Los oligonucleótidos fueron diluidos a 10 µM en agua libre de nucleasas como solución de trabajo, colocando el volumen adecuado para obtener una concentración final en la reacción de 0.2 µM en todos los casos. La mezcla de reacción fue de 20 µl final (12.5 µl Sybr green super mix, 0.5 µl primer forward [10 µM], 0.5 µl primer reverse [10 µM], 0.5 µl ROX [1:10], 9.0 µl agua libre de nucleasas, 2.0 µl cDNA) Se utilizó el termociclador ABI7500 (Life Technologies, EEUU) programado, según el siguiente protocolo: 50 ºC por 2 min, 95 °C por 10 min; 50 ciclos de 95 ºC por 15 s, 60 ºC por 60 s. Al final de cada ciclo se realizó la medición de la densidad óptica de la placa. Posteriormente se programó la obtención de la temperatura de disociación del producto de en el rango de 65-95 °C cada 0.3 °C, 30 s. Los resultados fueron observados y analizados utilizando el software ABI 7500 2.0.6 (Life Technologies, EEUU).
Análisis de la Expresión de Genes
Se empleó la técnica 2-ΔΔct como técnica de cuantificación de la expresión relativa de genes detectables a través de RT-PCR Tiempo Real (Livak y Smittdgen, 2001). El método se basa en el análisis comparativo de los ciclos ciclo umbral (Ct) de las muestras a estudiar con el Ct del calibrador (células a las 0 horas sin ningún aditivo). Tanto el Ct de los tratamientos como el del calibrador se comparan con el Ct de un control endógeno. Como gen endógeno para la normalización de la cuantificación relativa se utilizó el gen de gliceraldehido-3-fosfato deshidrogenasa (GAPDH).
Análisis Estadístico
Para evaluar las diferencias entre grupos se calculó el intervalo de confianza al 95% y los intervalos se emplearon para evaluar las diferencias entre los grupos.
RESULTADOS
Expresión y Cuantificación Relativa de CCR9
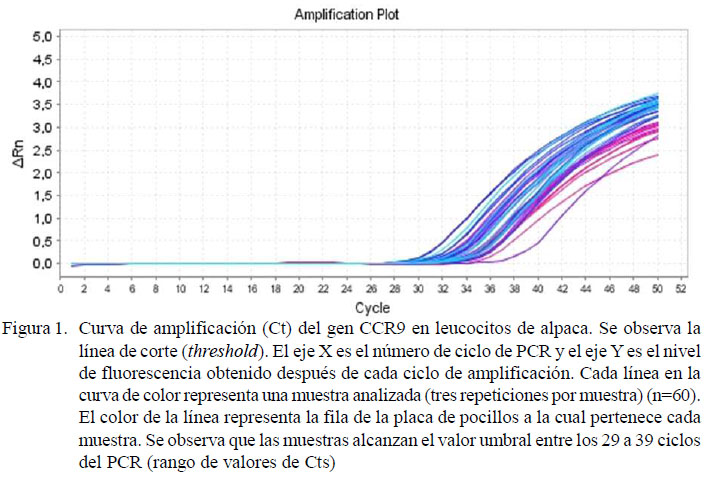
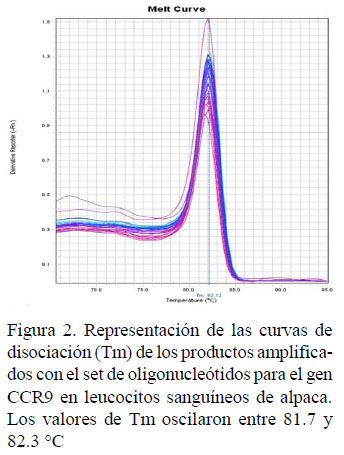
La expresión del gen de CCR9 muestra un patrón de crecimiento progresivo que se manifiesta por las curvas de amplificación (Ct) en un rango de 29 a 39 (Figura 1). Los productos amplificados tuvieron valores de Tm entre 81.7 y 82.3 (Figura 2), demostrando la amplificación de un producto único y especifico. Todos los tratamientos presentaron niveles detectables de ARNm de este gen.
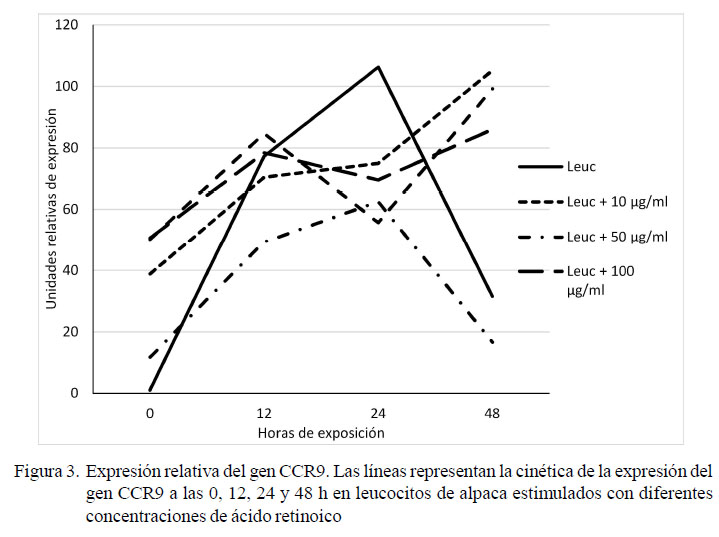
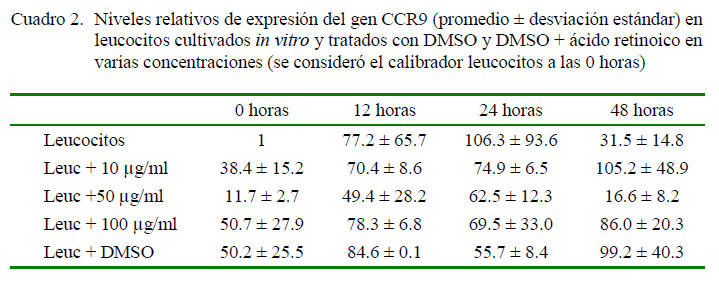
En la Figura 3 se observa que las concentraciones de 10 y 100 µg y leucocitos con DMSO muestran una cinética similar aumentando progresivamente con el paso del tiempo, mientras que el control y la concentración de 50 µg aumentan su expresión hasta las 24 h para descender a las 48 h. En síntesis, las dosis utilizadas aumentaron su expresión hasta las 48 h, tiempo que duró el estudio (excepto el control y la concentración de 50 ìg).
En el Cuadro 2 se presenta la cuantificación relativa del gen de CCR9. Se determinó que todos los tratamientos con ácido retinoico incrementan la expresión del gen de CCR9, así como el tratamiento con solo DMSO. Las máximas expresiones se dieron a las 48 h para las concentraciones de 10 y 100 µg/ml de ácido retinoico (105.19 y 86.0 veces con respecto al calibrador, respectivamente) y DMSO (99.18 veces con respecto al calibrador), y a las 24 horas para la concentración de 50 µg/ml de ácido retinoico (62.5 veces con respecto al calibrador) y el control de leucocitos (106.26 veces con respecto al calibrador).
Expresión y Cuantificación Relativa de las Cadenas Polipeptídicas α4 y β7
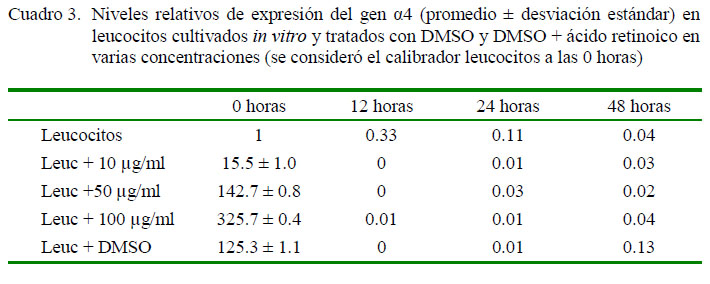
El gen de la cadena α4 de la integrina α4β7 solo se incrementó en una exposición a los 10 min de ácido retinoico (hora 0 en este trabajo), luego de las cuales no se observa la expresión. El incremento es dependiente de la concentración del ácido retinoico, siendo de 1.00 para el control de 15.4 veces para 10 µg/ml, 142.7 veces para 50 µg/ml y 325.7 veces para 100 µg/ml.Asimismo, se determinó que el DMSO incrementó la expresión en 125.3 veces el control (Cuadro 3).
No se observó amplificación para el gen β7 de la integrina α4β7 y, por lo tanto, no se pudo hacer la cuantificación relativa. Pese a que se consideró el último ciclo de la PCR (ciclo 45) como Ct, los valores de cuantificación para este gen se mostraron por debajo de lo normal.
DISCUSIÓN
El presente estudio evaluó in vitro el efecto del ácido retinoico (sustancia inmunoestimulante), en tres distintas concentraciones sobre la expresión del receptor CCR9 y la integrina α4β7 en linfocitos intestinales circulantes de alpaca, utilizando la prueba RT-PCR con cebadores específicos. Esto permitió detectar la presencia de los ARN mensajeros de los tres genes (CCR9, α4 y β7), los cuales se transcriben independientemente y se unen las cadenas α4 y β7 para formar la integrina α4β7 necesaria para el alojamiento de los linfocitos en la mucosa intestinal (Picarella et al., 1997)
La expresión del gen α4 solo se observó en las muestras de 0 horas de cultivo (tiempo de 10 minuntos entre la cosecha y su congelación) y que es dependiente de la concentración de ácido retinoico (ATRA), elevándose hasta 326 veces más que el control. Esto puede ser debido a que su expresión está condicionada a la presencia de otras moléculas co-estimuladoras, como el factor de crecimiento transformante β (TGF-β) y otros compuestos producidos por las células epiteliales de la mucosa intestinal (Zhang y Bevan, 2013).
La expresión del gen α4 indicaría que existen células estimuladas en la mucosa intestinal que están migrando por el torrente sanguíneo. Estas células son estimuladas por el ácido retinoico induciendo su expresión en los primeros 10 minutos, pero que luego desaparecen al no encontrar el nicho adecuado para establecerse. La presencia de leucocitos diferenciados en la circulación sanguínea de las alpacas y estimulados por ATRA se confirma en el trabajo de More (2013), donde se demuestra el incremento de expresión de genes de varias interleucinas cuando son estimuladas con distintas concentraciones de ATRA y antígenos clostridiales in vitro.
La expresión del gen β7 no se manifestó en ninguna concentración de ATRA, indicando que este gen no es estimulado por esta molécula. Este gen se expresa cuando los linfocitos entran al nicho de la mucosa intestinal, siendo estimulados en presencia de TGF-β y metabolitos del ácido retinoico producido por las células dendríticas. La falta de activación por solo ATRA indica que debe ser por vías de co-estimulación en conjunto (Sheen et al., 2013). Es importante indicar que previamente se realizó un RT-PCR con cinco muestras de mucosa intestinal de alpaca donde se determinó la expresión de los genes de la cadena polipeptida de á4, â7 y CCR9 que sirvió para la estandarización de esta prueba.
En general se puede afirmar que la integrina α4β7 no se expresa en el cultivo in vitro de leucocitos de alpacas en presencia de ATRA a distintas concentraciones y requieren que co-estimulen su expresión moléculas como el TGF-β, que es producido en la mucosa intestinal y que junto al ácido retinoico generan el ambiente ideal para expresión de las proteínas del alojamiento linfoide (Homing linfoide) en la mucosa intestinal, sumado a efectos secundarios no determinados (Biancheri et al., 2013). Aparentemente el TGF-β sería un factor importante a tener en cuenta para la expresión constante de los genes α4 y β7, complementando de esta ma-nera la expresión de la integrina α4β7, la cual interviene junto con CCR9 en el homing de los linfocitos T activados hacia la mucosa intestinal (Zhang y Bevan, 2013).
La expresión máxima de CCR9 se evidenció a las 48 horas para las concentraciones de 10 y 100 µg/ml de ácido retinoico y DMSO, lo que podría deberse a la liberación de moléculas de alarma celular liberadas al medio por la muerte y lisis de leucocitos en el cultivo. Además, el control celular presentó también expresiones crecientes de CCR9 indicando que este receptor tiene, además, otras funciones no determinadas en la sobrevivencia celular. Por otra parte, el incremento en la expresión del gen de CCR9 en presencia de DMSO se observó en los primeros 10 minutos. Es muy probable que exista una respuesta inmunológica en primera instancia hacia este agente extraño, produciéndose quimiocinas que estimulen la expresión de dicho receptor. No obstante, esta expresión disminuye con el tiempo de incubación, debido a que el DMSO afecta a la viabilidad celular por cierta citotoxicidad (Da Violante et al., 2002).
Se ha demostrado que la quimiocina CCL25 /TECK es el ligando para CCR9 en los linfocitos B y T y que se localiza en el epitelio de las criptas del yeyuno y el íleon (Kunkel et al., 2000). Se conoce que CCL25 se expresa también en células endoteliales y en subconjuntos de células en la lámina propia del intestino delgado (Papadakis et al., 2000). De esta manera, CCL25/TECK demuestra un rol importante en la migración de linfocitos en condiciones inflamatorias y no inflamatorias, siendo determinante para el homing intestinal (Hosoe et al., 2004).
Se sabe, además, que el CCR9 también tiene como ligandos a CCL-2 (MCP-1) y CCL7 (MCP-3) (Mackay, 2001). Por tanto, la expresión de CCR9 demostrada en el presente estudio evidencia que no solo el homing intestinal juega un papel importante en la expresión de este receptor, sino que además existen ciertas quimiocinas que se expresan en una variedad de células cuando ocurre un evento de estrés oxidativo celular, tal es el caso de la quimiocina CCL2 (MCP-1), la cual podría estar estimulando la expresión de este receptor (Deshmane et al., 2009).
En este estudio in vitro con sangre periférica de alpaca no se pudo comprobar el rol que desempeñaría ATRA como inmunoestimulante hallado en otros estudios in vivo e in vitro. Existe una expresión evidente del receptor de CCR9 en todos los tratamientos, demostrado a través del método de cuantificación relativa, de allí que es probable que el incremento en la expresión de CCR9 pueda deberse a otros factores que estén estimulando su expresión, como el estrés oxidativo celular o el mismo DMSO. Estos hallazgos contrastan con los pocos estudios in vitro que evalúan el ácido retinoico como inmunoestimulante en mucosa intestinal de alpacas (More, 2013; Lázaro et al., 2015) en los que se observa una expresión marcada de genes de interleucinas e Ig A, respectivamente.
El grupo de tratamiento de leucocitos con DMSO es el que exhibe una desviación estándar considerablemente elevada. Mientras más elevado sea este valor en un tratamiento significa que la expresión de los genes evaluados es menor, ya que se estaría enmascarando la expresión por la elevada variabilidad. La desviación estándar elevada en muchos de los tratamientos se debe a la cantidad de células que están muriendo; es decir, en un pocillo mueren más células que en otros, resultando en una alta variabilidad entre pocillos. Las causas de la muerte celular pueden ser diversas; por ejemplo, por lisis de los leucocitos recuperados, por pérdidas de células durante el cultivo, y por el tiempo transcurrido entre la inoculación y la cosecha (Olofsson, 1991). Es probable que las células reaccionen al DMSO, expresando estas proteínas en su superficie en respuesta a un factor extraño (Platas, 2015).
Todas las concentraciones de ácido retinoico evaluadas aumentaron la expresión de CCR9 hasta las 48 horas, tiempo que duró el estudio, excepto para el grupo control y la concentración de 50 µg de ácido retinoico. La explicación para estos dos últimos casos está relacionado a la cantidad de células presentes en los pocillos; donde es probable el número de células inoculadas haya sido mínimo en esos tratamientos, asociado también a la vida media del leucocito. Esto pudo haber ocasionado que los genes evaluados no pudieron ser detectados por la PCR (Williams et al., 1992).
Se debe tener en cuenta que en el cultivo hay una dinámica de expresiones muy activa existiendo mucha interacción celular. A esto se le suma que los leucocitos son difíciles de cultivar y van muriendo en forma progresiva. Sin embargo, hay leucocitos que se pueden fijar dentro de las placas como los macrófagos, monocitos y células dendríticas. Estos últimas se pueden adherir a la placa al igual que los macrófagos. Esta es una de las razones de la cinética de la expresión de CCR9 la cual aumenta a las 12 horas para disminuir a las 24 horas y volver a aumentar a las 48 horas. Eso explica el primer aumento y descenso de la expresión, respectivamente. Por otro lado, las células dendríticas y macrófagos que se fijan a las placas pueden vivir más tiempo y esto explicaría el segundo aumento. Por consiguiente, el aumento de expresión a las 48 horas estaría indicando que algunas células se están adhiriendo y que permanecen vivas en el cultivo. La adhesión de las células al pocillo podría inducir la expresión de nuevos genotipos y uno de ellos podría ser CCR9, aunque principalmente se sabe que solo los linfocitos expresan CCR9. No se ha establecido si otras células pueden expresar también estos genes (Wilson et al., 2005). Los resultados evidencian una imagen muy amplia de muchas subpoblaciones que podrían distinguirse si solamente se trabajase con linfocitos. Hay técnicas especializadas como la citometría de flujo para hacer esta separación (Barrera et al., 2004).
El DMSO, solvente utilizado para la dilución del ácido retinoico y que se evidencia que tuvo un efecto sobre la expresión del receptor CCR9, es conocido y utilizado como agente criopreservante intracelular (al igual que el glicerol), minimizando la formación de hielo intracelular y reduciendo el daño celular. El DMSO es un líquido orgánico que contiene sulfuro con atribuciones de múltiples propiedades terapéuticas. Es usado comúnmente como disolvente orgánico en la industria, y como medicamento. Tiene la propiedad de atravesar rápidamente las membranas celulares, sirviendo también como acarreador de drogas. Es un disolvente altamente polar, por lo que es miscible en agua, alcoholes y cetonas. Se requiere investigar más sobre el mecanismo de este disolvente y de qué manera estaría alterando el genotipo de las células para la expresión de receptores en su membrana.
CONCLUSIONES
-
Se observa expresión del receptor de quimiocina CCR9 en los leucocitos de alpaca cultivados in vitro estimulados por ácido retinoico en las dosis de 10, 50 y 100 µg/ml a las 0, 12 y 24 horas.
-
No se observa estimulación con ácido retinoico para la expresión de los genes de la integrina α4β7 en leucocitos de alpacas obtenidos de sangre periférica cultivados in vitro.
-
No se evidencia el efecto del ácido retinoico sobre la expresión de receptor de quimiocina CCR9 en los leucocitos de alpaca cultivados in vitro.
-
No se observa estimulación con ácido retinoico para la expresión de los genes de la integrina α4β7 en leucocitos de alpacas obtenidos de sangre periférica cultivados in vitro.
Agradecimientos
Se agradece al INNOVATE PERU Proyecto N.°180 FINCYT 2013 por el financiamiento del trabajo de investigación.
LITERATURA CITADA
1. Barrera L, Drago M, Zamora A, Sainz T, Mendoza F. 2004. Citometría de flujo: vínculo entre la investigación básica y la aplicación clínica. Rev Inst Nal Enf Resp Mex 17(1): 42-55. [ Links ]
2. Biancheri P, Giuffrida P, Docena GH, MacDonald TT, Corazza GR, Di Sabatino A. 2013. The role of transforming growth factor (TGF)-β in modulating the immune response and fibrogenesis in the gut. Cytokine Growth Factor Rev 25: 45-55. doi: 10.1016/ j.cytogfr.2013.11.001 [ Links ]
3. Cassani B, Villablanca EJ, Quintana FJ, Love PE, Lacy-Hulbert A, Blaner WS, Sparwasser T, et al. 2011. Guttropic T cells that express integrin α4β7 and CCR9 are required for induction of oral immune tolerance in mice. Gastroenterology 141: 2109-2118. doi: 10.1053/j.gastro.2011.09.015 [ Links ]
4. Collins SJ. 2002. The role of retinoids and retinoic acid receptors in normal hematopoiesis. Leukemia 16: 1896-1905. doi: 10.1038/sj.leu.2402718 [ Links ]
5. Coombes JL, Siddiqui KR, Arancibia- Cárcamo CV, Hall J, Sun CM, Belkaid Y, Powrie F. 2007. A functionally specialized population of mucosal CD103+ DCs induces Foxp3+ regulatory T cells via a TGF-β and retinoic acid-dependent mechanism. J Exp Med 204: 1757-1764. doi: 10.1084/ jem.20070590 [ Links ]
6. Da Violante G, Zerrouk N, Richard L, Provot G, Chaymeil JC, Arnauld P. 2002. Evaluation of the cytotoxicity effect of dimethyl sulfoxide (DMSO) on Caco2/TC7 colon tumor cell cultures. Biol Pharm Bull 25: 1600-1603. doi: 10.1248/bpb.25.1600 [ Links ]
7. Deshmane S, Kremlev S, Amini S, Sawaya B. 2009. Monocyte chemoattractant protein-1 (MCP-1): an overview. J Interferon Cytokine Res 29: 313-326. doi: 10.1089/jir.2008.0027 [ Links ]
8. Elias KM, Laurence A, Davidson TS, Stephens G, Kanno Y, Shevach EM, O’Shea JJ. 2008. Retinoic acid inhibits Th17 polarization and enhances FoxP3 expression through a STAT-3/STAT-5 independent signaling pathway. Blood 111: 1013-1020. doi: 10.1182/blood-2007- 06-096438
9. Hosoe N, Miura S, Watanabe C, Tsuzuki Y, Hokari R, Oyama T, Fujiyama Y. 2004. Demonstration of functional role of TECK/CCL25 in T lymphocyte-endothelium interaction in inflamed and uninflamed intestinal mucosa. Am J Physiol Gastrointest Liver Physiol 286: G458-466. doi: 10.1152/ ajpgi.00167.2003 [ Links ]
10. Housley WJ, O´Connor CA, Nichols F, Puddington L, Lingenheld EG, Zhu L, Clark RB. 2009. PPARγ regulates retinoic acid-mediated DC induction of Tregs. J Leukoc Biol 86: 293-301. doi: 10.1189/jlb.1208733 [ Links ]
11. Iwata M, Hirakiyama A, Eshima Y, Kagechika H, Kato C, Song SY. 2004. Retinoic acid imprints gut-homing specificity on T cells. Immunity 21: 527- 528. doi: 10.1016/j.immuni.2004.08.011 [ Links ]
12. Kim CH. 2008. Roles of retinoic acid in induction of immunity and immune tolerance. Endocr Metab Immune Disord Drug Targets 8: 289-294. doi: 10.2174/ 187153008786848312 [ Links ]
13. Kunkel EJ, Campbell JJ, Haraldsen G, Pan J, Boisvert J, Roberts AI, Ebert EC, et al. 2000. Lymphocyte CC chemokine receptor 9 and epithelial thymus expressed chemokine (TECK) expression distinguish the small intestinal immune compartment : epithelial expression of tissue-pecific chemokines as an organizing principle in regional immunity. J Exp Med 192 : 761-768. [ Links ]
14. Lázaro R, Manchego A, Pezo D, More J, Castro G, Sauce J, Sandoval N. 2015. Efecto de antígenos de Clostridium perfringens y ácido retinoico sobre la expresión de IgA en la mucosa intestinal de crías de alpacas (Vicugna pacos). Rev Inv Vet Perú 26: 689-697. doi: 10.15381/rivep.v26i4.11216 [ Links ]
15. Leung AY, Verfaillie CM. 2005. Alltrans retinoic acid (ATRA) enhances maintenance of primitive human hematopoietic progenitors and skews them towards myeloid differentiation in a stroma-noncontact culture system. Exp Hematol 33: 422-427. doi: 10.1016/ j.exphem.2004.12.007 [ Links ]
16. Livak KJ, Schmittgen TD. 2001. Analysis of relative gene expression data using real-time quantitative PCR and the 2-ΔΔCT method. Methods 25: 402-408. doi: 10.1006/meth.2001.1262 [ Links ]
17. Mackay CR. 2001. Chemokines: immunology’s high impact factors. Nat Immunol 2: 95-101. doi: 10.1038/84298
18. Maynard CL, Hatton RD, Helms WS, Oliver JR, Stephensen CB, Weaver CT. 2009. Contrasting roles for all-trans retinoic acid in TGF-β-mediated induction of Foxp3 and IL10 genes in developing regulatory T cells. J Exp Med 206: 343- 357. doi: 10.1084/jem.20080950 [ Links ]
19. More J. 2013. Efecto de antígenos clostridiales con ácido retinoico sobre la expresión de citoquinas de la respuesta inmune humoral y celular de la mucosa intestinal de crías de alpacas (Vicugna pacos). Tesis de Maestría. Lima: Univ Nacional Mayor de San Marcos. 104 p. [ Links ]
20. Olofsson T. 1991. Growth regulation of hematopoietic cells: an overview. Acta Oncol 30: 889-902. doi: 10.3109/ 02841869109088241 [ Links ]
21. Papadakis KA, Prehn J, Nelson V, Cheng L Binder SW, Ponath PD, Andrew DP, Targan SR. 2000. The role of thymus expressed chemokine and its receptor CCR9 on lymphocytes in the regional specialization of the mucosa immune system. J Immunol 165: 5069-5076 [ Links ]
22. Picarella D, Hurlbut P, Rottman J, Shi X, Butcher E, Ringler DJ. 1997. Monoclonal antibodies specific for beta- 7 integrin and mucosal addressin cell - adhesion molecule-1 (MAdCAM-1) reduce inflammation in the colon of scid mice reconstituted with CD45RBhigh CD4+ T cells. J Immunol 158: 2099-2106. [ Links ]
23. Platas JH. 2015. Uso de dimetilsufóxido y glicerol para la preservación de células endocrinas. Tesis de Médico Veterinario Zootecnista. México: Univ Veracruzana. 34 p. [ Links ]
24. Purton LE, Bernstein ID, Collins SJ. 2000. All-trans retinoic acid enhances the long-term repopulating activity of cultured hematopoietic stem cells. Blood 95: 470-477. [ Links ]
25. Purton LE, Dworkin S, Olsen GH, Walkley CR, Fabb SA, Collins SJ, Chambon P. 2006. RARγ is critical for maintaining a balance between hematopoietic stem cell self-renewal and differentiation. J Exp Med 203: 1283- 1293. doi: 10.1084/jem.20052105 [ Links ]
26. Sheen YY, Kim MJ, Park SA, Park SY, Nam JS. 2013. Targeting the transforming growth factor-β signaling in cancer therapy. Biomol Ther 21: 323-331. [ Links ]
27. Sun CM, Hall JA, Blank RB, Bouladoux N, Oukka M, Mora JR, Belkaid Y. 2007. Small intestine lamina propria dendritic cells promote de novo generation of Foxp3 T reg cells via retinoic acid. J Exp Med 204: 1775-1785. doi: 10.1084/jem.20070602 [ Links ]
28. Wang C, Kang SG, HogenEsch H, Love PE, Kim CH. 2010. Retinoic acid determines the precice tissue tropism of inflammatory Th17 cells in the intestine. J Immunol 184: 5519-5526. doi: 10.4049/ jimmunol.0903942 [ Links ]
29. Williams W, Rosenbaum H, Weiner D. 1992. Effect of RNA concentration on cDNA synthesis for DNA amplification. Genome Res 2: 86-88. [ Links ]
30. Wilson C, Clegg R, Leavesley D, Pearcy M. 2005. Mediation of biomaterial-cell interactions by adsorbed proteins: a review. Tissue Eng 1-2: 1-18. doi: 10.1089/ten.2005.11.1 [ Links ]
31. Zhang N, Bevan M. 2013. Transforming growth factor-β signaling controls the formation and maintenance of gut resident memory T cells by regulating migration and retention. Immunity 39: 687-696. doi: 10.1016/j.immuni.- 2013.08.019 [ Links ]
32. Zeng R, Oderup C, Yuan R, Lee M, Habtezion A, Hadeiba H, Butcher EC. 2013. Retinoic acid regulates the development of a gut-homing precursor for intestinal dendritic cells. Mucosal Immunol 6: 847-856. doi: 10.1038/mi.2012.123 [ Links ]
Recibido: 1 de junio de 2017
Aceptado para publicación: 28 de noviembre de 2017