Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista de Investigaciones Veterinarias del Perú
versión impresa ISSN 1609-9117
Rev. investig. vet. Perú vol.30 no.1 Lima ene./mar. 2019
http://dx.doi.org/10.15381/rivep.v30i1.15686
COMUNICACIÓN
Termorresistencia de espermatozoides caninos en semen fresco diluido
Canine sperm thermoresistance in diluted fresh semen
Alfonso Sánchez Riquelme1,2
1 Escuela de Medicina Veterinaria, Facultad de Medicina Veterinaria y Agronomía, Universidad de Las Américas, Viña del Mar, Chile
2 E-mail: asanchez@udla.cl /www.udla.cl
RESUMEN
Con el propósito de comparar el efecto de dos tipos de diluyentes seminales, suero fisiológico (SF) y leche descremada (LD), sobre la funcionalidad de espermatozoides caninos en semen fresco sometidos a una prueba termorresistencia (PTR), se obtuvieron 15 eyaculados mediante la técnica de masaje manual sobre la porción caudal del bulbo del glande. Se utilizaron 15 machos, clínicamente sanos, de razas pequeñas y medianas, todos con fertilidad probada. Se recolectó la segunda fracción de cada eyaculado. La evaluación seminal consideró motilidad progresiva (MP) y funcionalidad de membrana con una prueba hipoosmótica simplificada (HOST-s). Se tomaron alícuotas de 100 µl de semen de cada eyaculado para ser diluidas en 200 µl de SF o LD, respectivamente, y luego incubadas a 38 °C durante 30 minutos (PTR). Como control se incubaron 300 µl de semen sin diluir. A continuación, se evaluó MP y HOST-s. La MP en el semen fresco fue 81.4 ± 8.1 y la respuesta al HOST-s de 94.0 ± 7.80, ambos valores superiores a los observados en las muestras diluidas e incubadas (p<0.05). Sin embargo, no se observaron diferencias significativas entre diluyentes luego de la PTR, obteniéndose MP: 71.0 ± 27.2 y HOST-s: 87.0 ± 10.5% para SF y MP: 69.0 ± 18.5 y HOST-s: 86.0 ± 10.6% para LD.
Palabras clave: semen canino; termorresistencia; leche semidescremada
ABSTRACT
In order to compare the effect of two types of seminal extenders, physiological saline (PS) and skim-milk (SM), on the functionality of canine spermatozoa in fresh semen subjected to a thermo-resistance test (TRT), 15 ejaculates were obtained by manual massage on the caudal portion of the bulb of the glans penis. Fifteen males, clinically healthy, of different small and medium breeds were used, all with proven fertility. The second fraction of each ejaculate was collected. The seminal evaluation considered progressive motility (PM) and membrane functionality with a simplified hypoosmotic test (HOST-s). Then, from each ejaculate, aliquots of 100 µl of semen were taken to be diluted in 200 µl of PS and SM respectively and then incubated at 38 °C for 30 minutes (TRT). As control, 300 µl of undiluted fresh semen was incubated. Next, PM and HOSTs were evaluated. The PM in the fresh semen was 81.4 ± 8.1 and the response to the HOST-t 94.0 ± 7.80, both values higher than those observed after the TRT in the diluted samples (p<0.05). However, when comparing both diluents after the TRT, no significant differences were observed: PS (PM: 71.0 ± 27.2 and HOST-s: 87 ± 10.5%) and SM (PM: 69.0 ± 18.5 and HOST-s: 86.0 ± 10.6%).
Key words: canine semen; thermoresistance; skim-milk
INTRODUCCIÓN
La adecuada evaluación de los reproductores y del semen, la preservación de los espermatozoides y la inseminación artificial (IA) en perros se han constituido en temas de alto interés, tanto para los médicos veterinarios como para los criadores de perros. En la mayoría de las especies de interés zootécnico, la IA es una biotecnología empleada fundamentalmente para acelerar el mejoramiento genético (Hafez y Hafez, 2002). Según Farstad (2010), la IA en caninos tiene además una serie de aplicaciones clínicas, destacándose como una herramienta para la solución de problemas físicos en el apareamiento, característicos de razas tales como el Bulldog Inglés.
La IA es una práctica habitual en el manejo reproductivo canino, reportándose que alrededor del 65% de las inseminaciones se realizan con semen recién recolectado y depositado con un catéter a nivel vaginal (Linde-Forsberg, 2006). El volumen de semen apropiado para realizar la IA intravaginal se encuentra entre 2 y 8 ml de acuerdo con el tamaño de las hembras inseminadas. En aquellos casos en que el volumen seminal sea bajo, como ocurre en razas pequeñas o en machos con alteraciones prostáticas, se recomienda la incorporación de fluido prostático o un diluyente seminal a la segunda fracción del eyaculado (Linde-Forsberg, 2006; Farstad, 2010).
En la clínica reproductiva canina se debe evaluar el semen para estimar la fertilidad potencial de los reproductores. En el perro, se consideran como parámetros básicos de calidad seminal la motilidad progresiva, la morfología espermática y la concentración espermática (Root Kustritz, 2014). No obstante la relativa simplicidad de estos parámetros, cabe destacar que uno de los desafíos para el trabajo en terreno o en condiciones clínicas, es la búsqueda de técnicas complementarias de evaluación. Una prueba sencilla y de bajo costo para semen canino es la prueba de termorresistencia (Sánchez y Bravo, 2013), la cual tiene por principio la exposición de los espermatozoides a las condiciones fisiológicas de temperatura del tracto genital femenino, a fin de estimar su capacidad de mantener la motilidad espermática, valorando que la temperatura intravaginal canina fluctúa entre 37.5 y 38.5 ºC (Maeder et al., 2012).
Con el objetivo de aumentar el volumen de las dosis inseminantes, se ha comparado la adición de fluido prostático autólogo, fluido prostático heterólogo o suero fisiológico a la fracción espermática de los eyaculados, no registrándose diferencias en la motilidad progresiva después de incubar el semen a 38 °C por 60 minutos (Sánchez y Bravo, 2013). Si bien, uno de los propósitos de la dilución de los eyaculados de bajo volumen es permitir su manejo en la aspiración e inyección intravaginal, también resulta fundamental que el diluyente mantenga la calidad del eyaculado. La leche semidescremada, dadas sus propiedades antioxidantes y estabilizadoras de membrana, ha sido empleada satisfactoriamente en la preservación de semen canino en condiciones de estrés térmico, refrigerado y congelado (Province et al., 1984; Abe et al., 2008, 2018); así mismo, se ha demostrado que la leche descremada mejora las características espermáticas en semen almacenado a 17 °C (Fu et al., 2017).
En el presente estudio se postuló que el uso de leche semidescremada como diluyente seminal para semen canino fresco tendría mejores resultados de funcionalidad espermática respecto del uso de suero fisiológico. El propósito del presente ensayo fue evaluar, mediante una prueba de termorresistencia, el efecto de la dilución de semen canino fresco con suero fisiológico o leche descremada, sobre parámetros de funcionalidad espermática.
MATERIALES Y MÉTODOS
Con el consentimiento de sus propietarios, se utilizaron 15 perros reproductores, clínicamente sanos, de razas pequeñas (2 Yorkshire Terrier, 1 Shiba Inu, 1 Shih Tzu, 1 Pug) y medianas (8 Bulldog Inglés y 2 Bull Terrier), todos con antecedentes de fertilidad probada en IA. La edad de los ejemplares fluctuó entre 2 y 5 años. De cada donante se obtuvo una muestra seminal, mediante la técnica de compresión manual sobre la porción caudal del bulbo del glande, recolectándose solo la segunda fracción del eyaculado (fracción espermática). Los criterios de inclusión de los eyaculados fueron: aspecto blanco-lechoso, volumen >500 µl y motilidad progresiva >70 %.
Los eyaculados fueron evaluados según Root Kustritz (2014), registrándose volumen, color, motilidad progresiva (MP), concentración y morfología espermática. Además, para la evaluación de funcionalidad de membrana, se realizó una prueba hipoosmótica simplificada (HOST-s), diluyendo 5 µl de semen con 45 µl de agua bidestilada (osmolaridad = 0 mOsm/l) e incubando por 5 min a 37 °C para registrar el porcentaje de espermatozoides dilatados (Sánchez y Garrido, 2013).
Los medios empleados como diluyentes en el presente estudio fueron ensayados para comparar su capacidad de favorecer o proteger a los espermatozoides en el tracto genital femenino y proponerlos como opción para aumentar el volumen de la dosis de inseminación. Ambos diluyentes poseen osmolaridades similares (leche descremada: 273 ± 7.7 mOsm/l; suero fisiológico: 305 ± 6.8 mOsm/l).
Se tomaron alícuotas de 100 µl de semen de cada eyaculado para ser diluidas en 250 µl de suero fisiológico al 0.9% (SF) o de leche descremada (LD). Como control se incubaron 300 µl de semen sin diluir. Ambos diluyentes fueron almacenados en tubos Eppendorf® de 5 ml y mantenidos a 37 °C previo a su utilización. La LD utilizada correspondió a leche fluida UHT, 0.5% de materia grasa. Finalmente, las muestras diluidas fueron sometidas a una prueba de termorresistencia (PTR), la que consistió en incubarlas a 38 °C durante 30 minutos en baño maría (Sánchez y Bravo, 2013), para posteriormente evaluar MP y respuesta a HOST-s como indicadores de funcionalidad espermática.
Los datos porcentuales fueron transformados a valores angulares (ángulo = arcoseno x) para llevarlos a la distribución normal y realizar un análisis unilateral de la varianza (Zar, 1999). Las diferencias entre diluyentes se estimaron mediante la prueba de hipótesis específica de Tukey. Los programas empleados fueron Prisma® 5.0 y Excel®.
RESULTADOS Y DISCUSIÓN
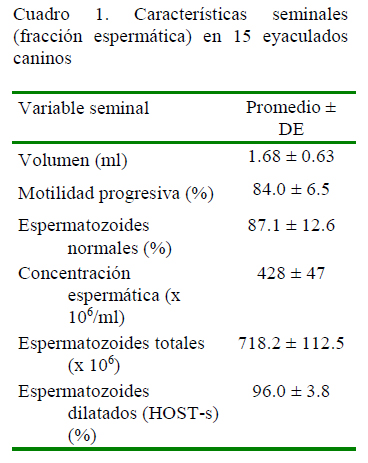
Las características seminales de los eyaculados en estudio (n=15) se presentan en el Cuadro 1, las que pueden ser consideradas como normales para la especie (Linde-Forsberg, 2006; Sánchez y Garrido, 2013; Root Kustritz, 2014).
Los valores de MP y respuesta al HOST-s en el semen fresco (84 ± 6.5% y 96 ± 3.8%, respectivamente), concuerdan con lo registrado para eyaculados caninos evaluados en condiciones similares (Sánchez y Garrido, 2013; Sánchez y Zamora, 2016).
Los valores funcionalidad espermática en semen fresco fueron superiores a los registrados luego de la dilución con SF y LD y sometidos la PTR (Cuadro 2). Dicha situación denotaría un efecto negativo de la incubación a 38 °C, posiblemente inducido por estrés celular (Batellier et al., 2001), el que afectaría principalmente al metabolismo aeróbico de las células espermáticas (O’Connell et al., 2002). Esta situación podría verse acentuado, además, por la falta de fuentes energéticas adicionales, como glucosa o rafinosa, en los diluyentes empleados (Abe et al., 2008). Los resultados del presente estudio concuerdan con los descritos por Sánchez y Bravo (2013), quienes observaron que la motilidad progresiva y el vigor espermático de semen canino diluido con fluido prostático autólogo y heterólogo fueron similares al diluido con suero fisiólogo después de una PTR hasta por 60 minutos.
No se observaron diferencias significativas en la funcionalidad espermática al comparar el efecto de los dos dilutores posterior a la PTR, con valores que fluctuaron alrededor del 70% para MP y 85% para la dilatación espermática (HOST-s). Estos valores, no obstante ser menores al del semen fresco, resultarían aceptables para uso de semen en IA intravaginal (Linde-Forsberg, 2006; Root Kustritz, 2014). Dados los resultados de la presente comunicación, se puede sugerir el uso de suero fisiológico al 0.9% como una alternativa para diluir semen canino fresco en condiciones clínicas, en que sea necesario incorporar volumen a las dosis inseminantes.
Literatura citada
1. Abe Y, Lee D, Sano H, Akiyama K, Yanagimoto-Ueta Y, Asano T, Suwa Y, et al. 2008. Artificial insemination with canine spermatozoa frozen in a skim milk/glucose-based extender. J Reprod Develop 54: 290-294. doi: 10.1262/jrd.19148 [ Links ]
2. Abe Y, Yokosawa S, UmemiyaShirafuji R, Moumouni O, Suwa Y, Suzuki H. 2018. Fertilizing ability of canine spermatozoa cryopreserved with skim milk-based extender in a retrospective study. Reprod Domest Anim 53: 237-242. doi: 10.1111/rda.13098. [ Links ]
3. Batellier F, Vidament M, Fauquant J, Duchamp G, Arnaud G, Yvon J, Magistrini M. 2001. Advances in cooled semen technology. Anim Reprod Sci 68: 181-190. doi: 10.1016/S03784320(01)00155-5 [ Links ]
4. Farstad W. 2010. Artificial insemination in dogs. In: England G, von Heimendahl A (eds). BSAVA Manual of canine and feline reproduction and neonatology. 2nd ed. Gloucester: British Small Animal Veterinary Association. p 80-88. [ Links ]
5. Fu J, Li Y, Wang L, Zhen L, Yang Q, Li Y, Li X. 2017. Bovine serum albumin and skim-milk improve boar sperm motility by enhancing energy metabolism and protein modifications during liquid storage al 17 °C. Theriogenology 102: 87-97. doi: 10.1016/j.theriogenology.2017.07.020 [ Links ]
6. Hafez E, Hafez B. 2002. Reproducción e inseminación artificial en animales. McGraw-Hill Interamericana. México. 256 p. [ Links ]
7. Linde-Forsberg C. 2006. Inseminación artificial. En: Reproducción en caninos y felinos domésticos. Wanke M, Gobello G (eds). Buenos Aires. Inter-Médica. p 175-194. [ Links ]
8. Maeder B, Arlt S, Burfeind O, Heuwieser W. 2012. Application of vaginal temperature measurement in bitches. Reprod Domest Anim 47 (Suppl 6): 359-361. doi: 10.1111/rda.12100 [ Links ]
9. O’Connell M, McClure N, Lewis S. 2002. The effects of cryopreservation on sperm morphology, motility and mitochondrial function. Hum Reprod 17: 704-709. doi: 10.1093/humrep/17.3.704
10. Province CA, Amann RP, Pickett BW, Squires EL.1984. Extenders for preservation of canine and equine spermatozoa at 5 ºC. Theriogenology 22: 409-415. doi: 10.1016/0093-691X(84)-90461-8 [ Links ]
11. Root Kustritz M. 2014. Applied small animal andrology. In: Animal andrology: theories and applications. Chenoweth P, Lorton S (eds). CAB International. p.177-196. [ Links ]
12. Sánchez A, Garrido D. 2013. Evaluación de una prueba hipoosmótica simplificada en semen canino fresco y refrigerado. Rev Cient Fac Cien V 30: 124-128. [ Links ]
13. Sánchez A, Bravo C. 2013. Efecto de la adición de fluido prostático autólogo y heterólogo sobre la calidad espermática del semen canino. Rev Inv Vet Peru 24: 466-472. doi: 10.15381/rivep.v24i4.2745 [ Links ]
14. Sánchez A, Zamora P. 2016. Efecto del medio hipoosmótico sobre la vitalidad espermática en semen canino. Rev Inv Vet Peru 27: 288-293. doi: 10.15381/rivep.v27i2.11649 [ Links ]
15. Zar J. 1999. Biostatistical analysis. 4th ed. New Jersey: Prentice Hall. 929 p. [ Links ]
Recibido: 23 de mayo de 2018
Aceptado para publicación: 20 de octubre de 2018