INTRODUCCIÓN
Astronotus ocellatus Agassiz, 1831, es un pez de la familia Cichlidae que se distribuye ampliamente en varias regiones de la Amazonía (Kullander, 2003; Santos et al., 2006; Pouilly et al., 2010; García-Ayala et al., 2017). En el medio natural habita en aguas lénticas, poco profundas, con bajos niveles de oxígeno (Echevarria y Machado-Allison, 2005; Sloman et al., 2006). Es de régimen alimenticio omnívoro con tendencia a carnívoro (Tello-Martin et al., 1992). En la Amazonía peruana es conocido como óscar o acarahuazú y es una especie de alto valor comercial, debido a que es usado como pez ornamental, así como para consumo local (García et al., 2009). A partir de 2015 se ha observado incrementos en el desembarque pesquero de esta especie de hasta más de 200 TM por año acumulado (García-Dávila et al., 2018).
Los peces para venta como ornamental son usualmente mantenidos por largos periodos en centros de acopio, en condiciones no siempre adecuadas, las cuales pueden alterar la homeostasis del pez hasta comprometer la salud y ser causante de mortalidad. Por lo tanto, la acuariofilia como la piscicultura tienen necesidad de información con respecto a los cambios fisiológicos de estas especies, con el propósito de mantener la salud de los animales en cautiverio (Tavares-Dias y Moraes, 2003).
En este sentido, los análisis hematológicos son una herramienta eficaz y, en algunos casos de uso rutinario, para determinar el estado de salud de los peces (Hesser, 1960; Tavares-Dias y Moraes, 2004; Ranzani-Paiva et al., 2013), frente a diversos factores que pueden estar ocasionando las malas prácticas de crianza (Ranzani-Paiva y Godinho, 1988). Por otro lado, factores endógenos como peso, longitud, edad, sexo, genética, etc., pueden afectar el cuadro hemático (Ranzani-Paiva y Godinho, 1988).
Algunos parámetros hematológicos de A. ocellatus mantenidos en acuario ya han sido evaluados (Iannacone et al., 2006). Así mismo, otros estudios evaluaron el efecto de la inclusión de probióticos en la alimentación y condiciones de hipoxia sobre los parámetros hematológicos en esta especie (Firouzbakhsh
et al., 2011; Baptista et al., 2016). Sin embargo, aún no existe información con respecto a los parámetros sanguíneos en A. ocellatus y su relación con parámetros endógenos. Por lo tanto, este estudio tuvo como objetivo caracterizar los valores de parámetros eritrocitarios, leucocitarios y bioquímicos en A. ocellatus en cautiverio y determinar la existencia de posibles correlaciones entre estas variables.
MATERIALES Y MÉTODOS
Condiciones de Cultivo
Quince especímenes de A. ocellatus (109.4 ± 22.9 g y 15.43 ± 1.28 cm) se mantuvieron en tanques de concreto a densidad de 1 pez/60 L, en las instalaciones del Instituto de Investigaciones de la Amazonía Peruana IIAP (Loreto, Perú). Los peces fueron alimentados con una dieta comercial extruida Aquatech® Naltech, Lima (Composición proximal: 42% proteína, 10% lípidos, 12% cenizas; 1.5% calcio; 1% fosforo) de 4 mm, con frecuencia de dos veces al día.
Se analizaron parámetros de agua con mediciones diarias de temperatura (26.16 ± 0.36 °C), oxígeno disuelto (6.31 ± 0.71 mg/l), pH (6.47 ± 0.25) y conductividad (0.42 ± 0.15 µS/cm) con un multiparámetro portátil (Hach, HQ40D). El amonio (0.70 ± 0.21 mg/l), amoniaco (0.66 ± 0.2 mg/l) y los nitritos (0.2 ± 0.1 mg/l) se evaluaron una vez por semana mediante un fotómetro colorimétrico (Hanna Instruments, HI 83203).
Colecta y Análisis de Sangre
Se extrajo sangre de los peces mediante punción de la vena caudal utilizando jeringas desechables de 1 ml con aguja (0.5 x 16 mm) conteniendo EDTA (10%). Una parte de sangre fue transferida a tubos de 1 ml y conservada a 4 °C. Para la determinación de eritro-citos y leucocitos se usó la solución Natt-Herrick (Natt y Herrick, 1952) en la cámara de Neubauer. La hemoglobina se determinó por el método de la cianometahemoglobina (Laboratorios Diagtest®) a 540 nm, y el hematocrito por el método del microhe-matocrito (Goldenfarb et al., 1971). La determinación de los índices hematimétricos: volumen corpuscular medio (VCM) y concentración de hemoglobina corpuscular media (CHCM) se realizó según el método de Wintrobe (1934). Para el recuento diferencial de leucocitos se confeccionaron extensiones sanguíneas teñidas con reactivo Rosenfeld modificado (Tavares-Dias y Moraes, 2003) por un periodo de 10 minutos y la identificación de las células se realizó siguiendo el criterio de Tavares-Dias y Moraes (2004).
La segunda porción de la muestra de sangre fue transferida a tubos de 0.5 ml para ser centrifugados a 75 g por cinco minutos para obtención de plasma. Se determinaron parámetros bioquímicos como proteína, glucosa y colesterol. La concentración de proteínas totales se determinó por el método colorimétrico de Biuret a 540 nm, glucosa por el método fotométrico enzimático GOP-PAP y el colesterol por el método enzimático fotométrico CHOD-PAP a 500 nm, utilizando kits de los Laboratorios DiaSys®. Las lecturas fueron realizadas en un espectrofotómetro UV visible (Thermo Scientific, Genesys 6, USA).
RESULTADOS Y DISCUSIÓN
Los valores hematológicos de A. ocellatus se muestran en el Cuadro 1. Resultados de hematocrito, hemoglobina, eritrocitos y CHCM son similares a los reportados por otros estudios con este mismo pez. Sin embargo, al comparar con ejemplares de A. ocellatus de menor porte se observaron valores más elevados (Cuadro 2). Este mismo comportamiento fue registrado en Salmo trutta para los valores de hematocrito (Navarro et al., 1991) y en Micropterus salmonoides con CHCM (Clark et al., 1979), lo que demostraría que existe una tendencia a disminuir los valores de algunos parámetros del eritrograma a medida que los peces aumentan de tamaño y edad (Tavares-Dias y Moraes, 2004).
Cuadro 1 Valores de la serie eritrocítica y bioquímica de Astronotus ocellatus cultivado en la Amazonía peruana
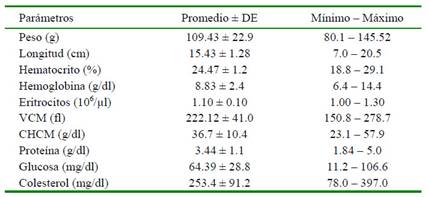
VCM = volumen corpuscular medio, CHCM = concentración de hemoglobina corpuscular media, DE: desviación estándar
Cuadro 2 Valores promedio y desviación estándar de la serie eritrocítica de Astronotus ocellatus en diferentes condiciones de cultivo, según reportes de la literatura científica
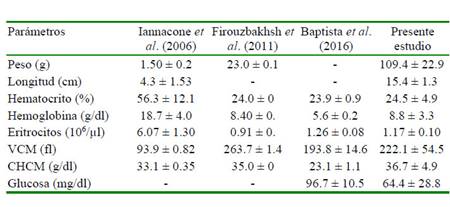
VCM = volumen corpuscular medio, CHCM = concentración de hemoglobina corpuscular media
Los valores de VCM mostraron variaciones en comparación con otros estudios (Cuadro 2), debido a que este parámetro es dependiente de los valores de eritrocitos y del hematocrito (McCarthy et al., 1973; Gonzales et al., 2019). Sin embargo, en el estudio de Seriani et al. (2012) para determinar la toxicidad de selenio en Oreochromis niloticus se observó un aumento de VCM, posiblemente debido a la liberación de eritroblastos de gran tamaño, lo cual no necesariamente indica que contengan grandes cantidades de hemoglobina.
En la diferenciación leucocitaria se encontró 67.3% de linfocitos, 4.13% de monocitos, 27.5% de células granulocíticas eosinófilos y 1.08% de neutrófilos, no encontrándose basófilos (Cuadro 3). Otros estudios también determinaron que los linfocitos son las células con mayor porcentaje en la sangre de ejemplares de A. ocellatus de cautiverio (Pitombeira, 1972; Iannacone et al., 2006; Maciel et al., 2016). Por otro lado, Tavares-Dias y Moraes (2004), al caracterizar los leucocitos de especies de las familias Anostomidae, Pimelodidae, Erythrinidae, Ictaluridae, Characidae, Prochilodontidae, Cichlidae, Mugilidae y Cyprinidae observaron una mayor frecuencia de estas células leucocitarias. Según Ranzani-Paiva et al. (2013), la abundancia de linfocitos está ligado a la respuesta inmune en peces. Es importante indicar, asimismo, que los porcentajes de eosinófilos y neutrófilos encontrados en el presente estudio difieren de los hallazgos reportados por Pitombeira (1972) y Iannacone et al. (2006).
Cuadro 3 Valores la serie leucocítica de Astronotus ocellatus cultivado en la Amazonía peruana
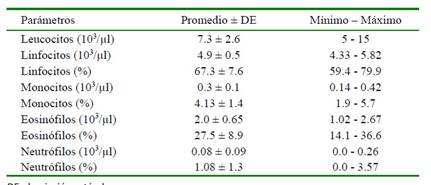
DE: desviación estándar
Los parámetros bioquímicos se encuentran relacionados con el tipo de alimentación que reciben los peces en la crianza (Groff y Zinkl, 1999). En el presente estudio (Cuadro 1) se observó que el nivel de glucosa fue in ferior a lo reportado por Baptista et al. (2016), donde evaluaron niveles de glucosa en condiciones de normoxia, hipoxia y de recuperación. Así mismo, los niveles fueron superiores al reporte de Crivelenti et al. (2011) en individuos de la familia Cichlidae como O. niloticus. Es ampliamente conocido que la glucosa en plasma refleja condiciones de estrés en peces (Zaragoza et al., 2008; Sánchez et al., 2017). Por lo tanto, esta variación de valores de glucosa puede estar influenciado por factores como calidad de agua, densidad y hasta tipo de alimentación (Hrubec et al., 2000; Gonzales et al., 2016; Sánchez et al., 2017).
Los valores de proteína (Cuadro 1) estuvieron dentro de los rangos reportados para O. niloticus cultivados en sistema intensivo (Crivelenti et al., 2011) y para híbrido de Oreochromis cultivados (Hrubec et al., 2000). Sin embargo, los valores de colesterol se mostraron elevados en comparación con otros estudios (Hrubec et al., 2000).
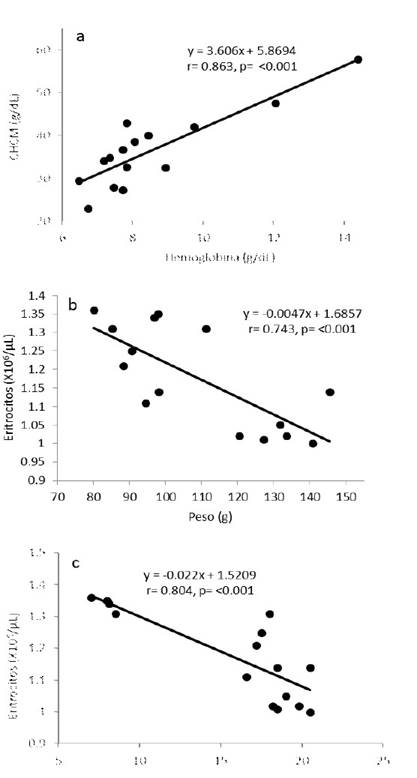
En el análisis de las correlaciones, se encontró que a medida que se incrementa la hemoglobina aumentan los valores de CHCM (Figura 1a), tal y como ha sido observado en el hibrido de Salminus maxillosus, en Piaractus mesopotamicus y en el hibrido de tambacu Piaractus mesopotamicus x Colossoma macropomum (Tavares-Dias et al., 1999, 2000; Ranzani-Paiva et al., 2001). Este resultado es esperado, dado que cuanto más concentración y cantidad de hemoglobina se encuentra en los eritrocitos, mayor es su concentración en la sangre (Ranzani-Paiva et al., 2001). Así mismo, se encontraron correlaciones negativas (p<0.05) entre el peso y la longitud del pez con el número de eritrocitos (Figuras 1b, c). Esto mismo ha sido observado en otros estudios (Martinez et al., 1994; Ranzani-Paiva et al., 2001), aunque a veces con valores de correlación bajos (Ranzani-Paiva et al., 2001).












 uBio
uBio