INTRODUCCIÓN
La producción mundial de tilapia (Oreochromis sp) alcanzó 6.4 millones de toneladas métricas (t), siendo China, Egipto, Filipinas, Tailandia e Indonesia los principales productores (FAO, 2017). En el Perú, el cultivo de tilapia ha llegado a ser la segunda especie piscícola de mayor producción por detrás de la trucha Oncorhynchus mykiss, alcanzando las 2950 t en 2016, pudiendo llegar según estimaciones a 3579 t en 2022 (PRODUCE, 2017). La producción de tilapia se concentra principalmente en las regiones de Piura y San Martín, representando aproximadamente el 95% del total de producción (PRODUCE, 2016).
A pesar del continuo crecimiento productivo de la tilapia, el estrés producto de la crianza intensiva ha conducido a un incremento de brotes de infecciones en las granjas piscícolas, tanto de origen bacteriano (Aeromonas sp, Streptococcus sp) (Huicab-Pech et al., 2016;Asencios et al., 2016) como de virosis (virus de la tilapia del lago [TiLV]) (Eyngor et al., 2014). El TiLV es un patógeno emergente que pertenece al género Tilapinevirus (Adams et al., 2017), y es considerado el causante de la hepatitis sincitial de la tilapia (SHT) (Ferguson et al., 2014; Del Pozo et al., 2017) y del síndrome de mortalidad de verano (SMS) o síndrome de mortalidad de un mes de la tilapia (TOMMS) (Fathi et al., 2017; Tattiyapong et al., 2017). Este virus ha sido identificado en tilapias de Sudamérica (Bacharach et al., 2016; Kembou Tsofack et al., 2017; OIE, 2018), Asia (Amal et al., 2018; Behera et al., 2018; Dong et al., 2017a; OIE, 2018) y África (Fathi et al., 2017; Mugimba et al., 2018), mayormente en los meses con temperaturas mayores de 22 °C.
El TiLV es un virus de ARN de simple cadena, de sentido negativo, y tiene un genoma de 10 323 kb organizado en 10 segmentos que codifican 10 proteínas (Bacharach et al., 2016). Este patógeno tiene la cualidad de infectar varias especies de cíclidos, principalmente la tilapia, y de replicar y transcribir su genoma en múltiples órganos como el hígado, riñón, bazo, cerebro, branquias y tejido muscular (Eyingor et al., 2014; Dong et al., 2017a).
Los signos clínicos incluyen letargia, distención abdominal, lesiones oculares, y erosiones de la piel, aunque también se le puede encontrar en peces sin signos clínicos aparentes (Senapin et al., 2018). Además de la transmisión horizontal, su presencia en huevos embrionados y alevinos sugieren una transmisión vertical (Dong et al., 2017b). Varios métodos moleculares han sido propuestos para su detección, principalmente la PCR y sus variantes con el objetivo de amplificar el segmento 3 del genoma viral (Eyngor et al., 2014; Dong et al., 2017a; Tattiyapong et al., 2017; Waiyamitra et al., 2018), seguido de la secuenciación de los productos de PCR para su confirmación.
En el Perú, el primer brote de TiLV fue detectado en Piura a fines de 2017 produciendo mortalidades masivas, tanto en medios naturales como en centros comerciales, habiéndose propagado a otras regiones del Perú. En este sentido, el presente estudio tuvo como objetivo detectar la presencia del TiLV asociado a eventos de mortalidades masivas en centros piscícolas de tilapia localizados en dos regiones del Perú.
MATERIALES Y MÉTODOS
Localización del Estudio
El estudio fue realizado entre diciembre de 2017 y abril de 2018. La colección de especímenes de tilapia (Oreochromis niloticus) se realizó en dos centros de cultivo ubicados en Sullana (Piura) y Tarapoto (San Martín). Las muestras se procesaron en el laboratorio de biotecnología molecular Incabiotec, Tumbes, Perú.
Muestras
Se colectaron 70 especímenes con sintomatología clínica sugerente de enfermedad (presencia de lesiones) de diferentes fases de cultivo, entre ambos centros de producción. Se procedió a la eutanasia previa anestesia con eugenol. La necropsia se realizó siguiendo la metodología propuesta por Fisher y Myer (2000), realizándose la toma de muestras de tejido hepático y cerebral (<0.5 cm de diámetro) por cada individuo. Los órganos se agruparon en pooles de tres a cinco individuos y se colocaron en tubos con solución preservante de ARN.
Extracción de ARN Total y Síntesis de ADNc
ElARNtotalfueextraídoapartir delos tejidos diana después de una purificación utilizando el método de extracción con ácido de tiocianato de fenol - cloroformo de guanidina con el reactivo TRizol® (Thermo Fisher Scientific), seguido de un tratamiento con DNaseI (Thermo Fisher Scientific). La síntesis de ADNc se llevó a cabo utilizando el ReverdAidTM Reverse Transcriptase (Thermo Fisher Scientific). En ambos casos, se siguieron los instructivos del fabricante. La transcripción reversa se realizó utilizando el iniciador específico Nested ext-2 (Eyngor et al., 2014).
Semi-nested PCR y Secuenciación
La técnica de PCR fue adaptada de Dong et al. (2017a), que amplifica un fragmento inicial de 415 pb (ext.1 anidado - TATGACAGTACTTTCCCTGCC y ME - GTTGGGCACAAGGCATCCTA) y un fragmento final de 250 pb (ME2 - TATCACGTGCGTACTCGTTCAGT y ME1- GTTGGGCACAAGGCATCCTA) (Cuadro 1), correspondientes al segmento 3 del genoma viral. Se utilizó un plásmido pGEM415 pb como control positivo. Se hicieron 30 ciclos bajo las condiciones siguientes: 95 °C durante 5 min, 94 °C durante 30 s, 60 °C durante 30 s, 72 °C durante 30 s y finalmente 72 °C durante 5 min. Los productos amplificados se sometieron a electroforesis en gel de agarosa al 2.5%, se tiñeron con bromuro de etidio y se visualizaron en un transiluminador ultravioleta. Los productos amplificados se secuenciaron mediante el método de Sanger en Macrogen (USA).
Análisis Filogenético
El análisis fue inferido tomando como referencia el segmento 3 de la cepa viral israelí (KU751816.1)-Así mismo, como control externo se utilizó una secuencia de Orthpneumovirus. Para el análisis se utilizó el método de máxima verosimilitud y un valor de Bootstrap de 2000 para estimar la confianza en el software MEGA 7.
RESULTADOS Y DISCUSIÓN
Los brotes producidos por el virus de la tilapia del lago (TiLV) produjeron tasas de mortalidades superiores al 60% durante el verano en los centros de cultivo de Piura y San Martín, abarcando todas las fases de producción. Solamente se afectaron tilapias del Nilo (O. niloticus) más no a otras especies acompañantes como pacos (Piaractus brachypomus) y gamitanas (Colossoma macropomun).
Los peces afectados exhibieron pérdida del apetito, letargia, erosiones de la piel y muerte (Figura 1). La necropsia mostró hepatomegalia, esplenomegalia y congestión en hígado y cerebro, signos clínicos similares a los descritos en la literatura científica (Ferguson et al., 2014; Dong et al., 2017a, Nicholson et al., 2017) donde ocurrieron mortalidades entre 20 y 90%. El amplio rango en las tasas de mortalidades se debe a factores tales como el sistema de producción, variedades genéticas del TiLV, co-infecciones, y condiciones ambientales como la temperatura. Así, la elevada mortandad observada en el presente estudio pudo deberse principalmente al tipo de sistema de producción (intensivo y semi-intensivo) reflejado en el hacinamiento de los animales y subsecuente estrés, además de las condiciones óptimas de temperatura presentes (estación de verano).

Figura 1 Brote del virus de la tilapia del lago (TiLV) en Piura y San Martín, Perú. (A) Erosiones en la piel a nivel lateral de individuo de O. niloticus. (B) Mortalidades masivas en un centro de cultivo comerci
Los resultados de PCR mostraron bandas definidas con un peso de 250 pb (Figura 2). La metodología utilizada para su identificación fue adaptada de Dong et al. (2017a), quienes describen un ensayo alternativo basado en semi-nested RT-PCR que produce un producto de 415 pb en la primera corrida y otro de 250 pb para la segunda, maximizando la sensibilidad de detección comparado a una PCR convencional, reduciendo así los falsos negativos. Recientemente, Tattiyapong et al. (2018) y Waiyamitra et al. (2018) desarrollaron nuevos métodos de PCR cuantitativo con transcripción reversa (RT-qPCR) basado en SYBR Green y TaqMan, respectivamente, dirigidos al segmento 3 y con una sensibilidad de 2 copias/ìl. Sin embargo, nuevos métodos de detección molecular deberían ser desarrollados, por ejemplo aquellos sistemas basados en amplificación isotérmica como LAMP (amplificación isotérmica mediada por bucles) permitiendo el diagnóstico in situ, reduciendo costos y tiempo.
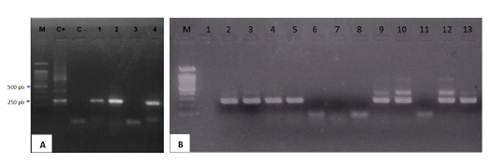
Figura 2 Productos amplificados para la identificación del virus de la tilapia del lago (TiLV) por semi-nested RT-PCR. (A) M: marcador molecular (100 pb); C+: control positivo (pGEM-415 pb); C-: control negativo; 1, 2, 3, 4: muestras de tejido hepático y cerebral de tilapias de Piura. (B) M: marcador molecular (100 bp); 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12: muestras de tejido hepático y cerebral de tilapias de San Martín
Los resultados de secuenciación y análisis por NCBI-BLAST revelaron que las secuencias de nucleótidos obtenidas fueron homólogas con aquellas pertenecientes al segmento 3 de la cepa de referencia israelí (KU751816.1). Además, al comparar las secuencias de nucleótidos entre los aislados de Piura y San Martín se observó una alta identidad evidenciado en su agrupamiento en un mismo clado (Figura 3), sugiriendo que las mortandades en ambas regiones fueron producidas por la misma cepa; sin embargo, se requiere secuenciar el genoma viral completo de los aislados con el fin de demostrar una homología genética completa.
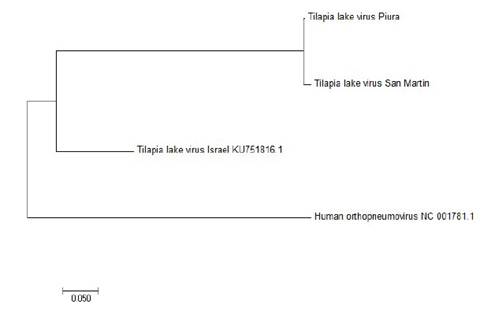
Figura 3 Árbol filogenético que grafica la relación entre las secuencias de nucleótidos de aislados del del virus de la tilapia del lago (TiLV)
La presencia del TiLV en el Perú y su rápida diseminación entre las dos regiones en estudio pudo deberse a su proximidad, así como a la cercanía al Ecuador y Colombia, donde han sido reportados brotes de TiLV, además del ingreso de alevinos y reproductores a los centros de producción. A pesar de que la ruta de transmisión es principalmente horizontal, Dong et al. (2017b) detectaron el virus en huevos embrionados y alevinos en incubadoras de Tailandia sugiriendo su transmisión vertical. La tilapia no es la única especie que puede verse afectada por el TiLV, pues se le ha aislado de Barbonimus schwanenfeldii (Abdullah et al., 2018) y Osheronemus goramy (Jaemwimol et al., 2018), lo cual indica la posibilidad de haber otras especies que actúen como reservorios en sistemas de cultivos mixtos, como es el caso de la amazonia peruana.












 uBio
uBio 


