INTRODUCCIÓN
La técnica de transferencia embrionaria en camélidos sudamericanos tiene diversas limitaciones para su aplicación en forma masiva debido a la variabilidad de la respuesta a los diferentes protocolos de superovulación (Ratto et al., 2015). En dichos protocolos de superovulación se utilizaron hormonas como FSH (hormona folículo estimulante), eCG (gonadotropina coriónica equina) y sus combinaciones, así como diferentes tipos de manejo previo de la onda folicular, habiéndose utilizado hembras en fase lútea natural pos-inducción de ovulación, fase lútea artificial con el uso de dispositivos de liberación de progestágenos y uso de hembras al inicio de la onda folicular determinado mediante ecografía (Bourke et al., 1994; Gamarra et al., 2006).
Las dosis de eCG descritas en investigaciones previas varían desde 1000 UI en dosis única (Bourke et al., 1994; Huanca, 2005), 500 UI diariamente por 3 días, haciendo un total de 1500 UI (Correa et al., 1997), hasta 1200 UI en dosis única (Ratto et al., 2007), lográndose en todos los casos respuestas superovulatorias variables. Asimismo, Huanca et al. (2006) indican que un protocolo superovulatorio utilizando eCG no afecta la tasa de aceptación a la cópula un mes después del tratamiento; sin embargo, no indican la dosis de eCG utilizada.
La ovulación ocurre entre las 26 y 30 horas pos-aplicación de GnRH (Rodríguez et al., 2012), considerando que es necesario iniciar un protocolo de superovulación en ausencia de un folículo dominante (Trasorras et al., 2012). La emergencia de la nueva onda folicular pos-inducción de ovulación en llamas ocurre el día 4.6 en promedio (Andrade, 2007). La eCG ha sido usada como hormona superovulatoria en camélidos sudamericanos, siendo efectiva mediante la aplicación de una sola inyección (Trasorras et al., 2012). El cuerpo lúteo formado luego de una ovulación no presenta capacidad de respuesta ante la aplicación de prostaglandina F2á en los primeros 4 días de la inducción de la ovulación, el día 5 presenta una leve sensibilidad y recién entre los días 6-8 se puede inducir luteólisis mediante la administración de PGF2α o su análogo, el cloprostenol, en llamas (Bianchi et al., 2012). Luego de aplicar un protocolo de superovulación, se ha utilizado la hCG para inducir ovulaciones sincrónicas de los múltiples folículos formados (Bourke, 1995); auque también se ha utilizado una dosis de GnRH para mejorar la tasa ovulatoria (Ratto et al., 2013; Sumar, 2013), además de realizar una o dos montas sucesivas.
En marranas, el uso de altas dosis de eCG produce la aparición de quistes foliculares de manera dosis-dependiente cuando es combinada con hCG (Manjarin et al., 2015). La respuesta superovulatoria en camélidos sudamericanos es muy variable entre individuos además de causar alteraciones luego del tratamiento (Von Baer et al., 2003), tales como quistes foliculares (Bravo et al., 1995). Sin embargo, cuerpos lúteos persistentes, metritis y ovarios acíclicos no han sido reportados en trabajos de superovulación, aunque es un problema latente que origina la desconfianza del productor de utilizar sus mejores animales en protocolos de superovulación. Ante esta situación, el presente trabajo de investigación tuvo como objetivo describir la tasa de superovulación, tasa de recuperación embrionaria y presencia de alteraciones reproductivas possuperovulación en llamas tratadas con 700 y 500 UI de eCG bajo un nuevo protocolo de superovulación.
MATERIALES Y MÉTODOS
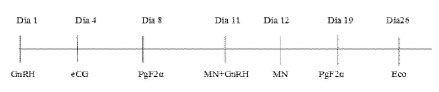
El trabajo de investigación se realizó entre octubre de 2018 y marzo de 2019 en el Centro de Investigación La Raya del Centro de Investigación IVITA, Universidad Nacional Mayor de San Marcos, ubicado en la Región Cusco, Perú, a una altitud de 4400 m. Se utilizaron 36 llamas hembras vacías, adultas con un adecuado historial reproductivo y cría en pie. Los animales presentaban condición corporal promedio de 3 (escala de 1-5), peso promedio de 85 kg y fueron mantenidos sobre pasturas naturales (Gráfico 1).
El nuevo protocolo se inició con la selección de las hembras mediante ecografía (Tringa linear, Esaote(r), Países Bajos), seleccionándose animales con presencia de un folículo preovulatorio con diámetro >7 mm. Los animales fueron distribuidos en dos grupos experimentales: Grupo I (700 UI eCG), n=15, y Grupo II (500 UI de eCG), n=21. El protocolo de superovulación fue el siguiente:
Día 1: Se aplicó 8.4 µg de acetato de buserelina (análogo de GnRH, Conceptase(r)), para inducir ovulación, la cual fue confirmada mediante ecografía.
Día 4: Se aplicó eCG (Novormon(r)), según la dosis establecida para cada grupo, para producir la superovulación cuando está iniciando la nueva onda folicular (Andrade, 2007).
Día 8: Se aplicó 0.26 mg de cloprostenol sódico (análogo de PGF2α; Lutaprost(r)), para causar luteólisis del cuerpo lúteo formado después de la primera inducción de ovulación (Día 1) (Bianchi et al., 2012)
Días 11 y 12: Se realizó la monta natural (MN) utilizando el mismo macho en cada hembra.
Día 11: Se hizo una segunda ecografía para verificar el número y diámetro de los folículos producto de la superovulación. Además, se aplicó 84 µg del análogo de GnRH para mejorar la tasa de ovulación (Ratto et al., 2013).
Día 19: Se hizo el lavado uterino y recuperación de embriones. Se aplicó 0.26 mg de análogo de PGF2α para causar luteólisis de los cuerpos lúteos formados y evitar problemas reproductivos posteriores (como persistencia de cuerpo lúteo o metritis relacionada a un estado de seudo-gestación).
Día 26: Se realizó la evaluación ovárica y uterina mediante ecografía para determinar la presencia de cuerpos lúteos persistentes (cuerpos lúteos o folículos luteinizados), quistes foliculares y metritis, así como iniciar un tratamiento individualizado de ser necesario.
Los datos fueron analizados y presentados utilizando estadística descriptiva (media aritmética y proporciones porcentuales).
RESULTADOS Y DISCUSIÓN
Diez y cinco hembras sometidas al protocolo de superovulación en los grupos I y II no produjeron embriones (Cuadro 1). Es así que se obtuvieron embriones en 5/15 (33.3%) y 16/21 (76.1%) de las hembras, lo cual se traduce en 1.6% (5/8) y 2.6% (42/16) de embriones por hembra que produjo embriones al lavado. Estos resultados son inferiores al reportado por Ratto et al. (2013) y podría corresponder a la variación propia de los individuos. Este hallazgo es consistente con lo descrito por Huanca (2008), quien indica que solo el 53% de las alpacas superovuladas produjeron embriones. Las respuestas obtenidas en este estudio indican una mayor tasa de colección de embriones al utilizar 500 UI de eCG respecto a 700 UI, especialmente considerando que se conoce que a altas dosis de PMSG se disminuye el número de embriones viables colectados (Gonzalez et al., 1994).
El número de embriones colectados por tratamiento fue claramente diferente entre grupos, indicando un efecto dosis-dependiente, tal como ha sido descrito (Bravo et al., 1995; Huanca et al., 2009; Ratto et al., 2013). Huanca et al. (2012) indicaron, asimismo, que obtuvieron 3.5 embriones por llama superovulada al utilizar 800 UI de eCG, resultado superior al presente estudio, y concordante a la mayor cantidad de hormona utilizada.
En las llamas tratadas con 500 UI de eCG se obtuvieron 3.7 folículos en promedio (Cuadro 2), inferior al reporte de Bravo et al. (1995), quienes indican 4.7 folículos en alpacas tratadas con 500 UI de eCG; sin embargo, Trasorras et al. (2009) mencionan que solo tuvieron una respuesta superovulatoria de 17% cuando utilizaron 500 UI de eGC, siendo la dosis óptima de 1000 UI. Esta respuesta altamente variable podría deberse a que en dicho estudio se utilizaron animales con mayor peso (120 kg) mientras que en el presente estudio fueron más livianos (85 kg en promedio). Esto indica que se requiere validar el efecto de la dosis de acuerdo al peso vivo. Además, hay que considerar que el estudio de Trasorras et al. (2009) se hizo con animales en estabulación y a nivel del mar.
La respuesta superovulatoria fue muy variable, encontrándose hembras con 1 a 9 folículos pos-tratamiento, lo cual está ampliamente descrito en camélidos (Ratto et al., 2013). Este resultado podría estar influenciado, además, por la alta variabilidad de la concentración de la hormona eCG en los preparados comerciales (Herrera et al., 2016).
Se pudo observar un efecto dosis-dependiente en el número de folículos por hembra, encontrándose 4.9 folículos cuando se utilizó 700 UI de eCG y 3.7 folículos cuando se utilizó 500 UI, respuesta consistente con lo descrito por Ratto et al. (2007), quienes describen mayor cantidad de folículos cuando utilizaron una alta dosis de eCG (1200 UI). La cantidad de folículos producidos por superovulación es inferior al reporte de Huanca et al. (2009), quienes indican la presencia de 16.6 folículos utilizando 1000 UI de eCG, confirmando el efecto dosis-dependiente de esta hormona.
Cuadro 2 Tasa de superovulación, de recuperación embrionaria y presencia de problemas reproductivos en llamas superovuladas, según la dosis de eCG
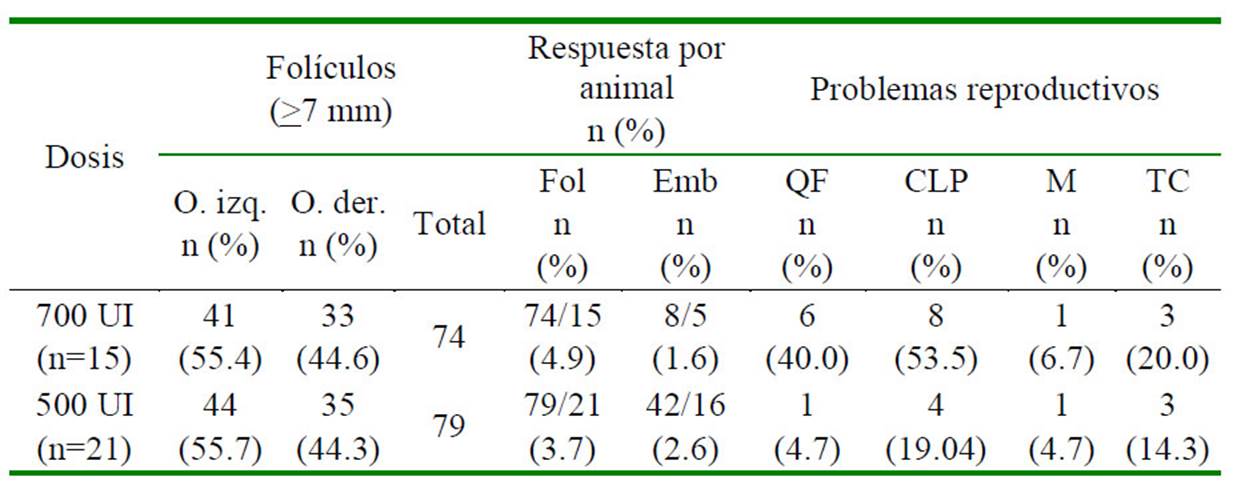
O. izq: Ovario izquierdo; O. der: Ovario derecho; Fol: Folículo; Emb: Embrión; QF: quiste folicular; CLP: cuerpo lúteo persistente; M: metritis; TC: torsión cervical
La mayor proporción de respuesta superovulatoria del ovario izquierdo (OI) respecto al ovario derecho (OD) se presentó en los dos grupos experimentales (Cuadro 2); respuesta similar a lo descrita por Fernández-Baca et al. (1970), quienes indican 59.1 y 40.9 % de cuerpos lúteos en 44 alpacas con gestaciones tempranas luego de ovulaciones naturales en el OI y OD, respectivamente; sin embargo, un reporte posterior de estos autores con mayor número de animales no llegaron a encontrar diferencia estadística de ovulaciones naturales entre los dos ovarios (Fernández-Baca et al., 1973).
El promedio de embriones colectados por hembra fue de 1.6 y 2.6 para los grupos I y II, respectivamente (Cuadro 1 y Cuadro 2), pese a que en el grupo I se presentó un mayor número de folículos producto de la superovulación. Esto podría indicar fallas en la ovulación y una posible luteinización de los folículos, tal como lo indican Vaughan et al. (2013). Otra posible causa de la menor cantidad de embriones colectados respecto a la cantidad de folículos existentes es el mayor tamaño que alcanzan los ovarios superestimulados, toda vez que se desplazan fuera de la bolsa ovárica al presentar un mayor diámetro, causando pérdida de ovocitos hacia la cavidad abdominal (Trasorras et al., 2012, 2017). De otro lado, todos los embriones colectados fueron blastocistos eclosionados, no habiéndose obtenido estructuras embrionarias con zona pelúcida (Huanca et al., 2013; Picha et al., 2013).
Los problemas reproductivos posteriores al tratamiento con eCG son frecuentes en camélidos sudamericanos. Bravo et al. (1995) reportaron presencia de quistes foliculares luego de un protocolo de superovulación utilizando eCG, incrementando su número a medida que se aumenta la dosis de eCG, similar a lo observado en el presente estudio, donde se registró mayor frecuencia de quistes foliculares al utilizar 700 UI de eCG respecto a una dosis menor, evidenciando una respuesta dosis-dependiente, tal como ha sido reportado también en cerdas (Manjarin et al., 2015). La frecuencia de metritis fue mínima en ambos grupos, y pareciera no estar relacionada a la actividad de la hormona superovulatoria; sin embargo, en ambos grupos se registraron casos de torsiones cervicales, posiblemente causada por la evidente alteración en los patrones hormonales de estradiol y progesterona, tal como fue descrito en vacas sometidas a protocolos de superovulación utilizando PMSG (Bevers y Dieleman, 1987) además de encontrarse en fase lútea.
CONCLUSIONES
El uso de un protocolo superovulatorio con una dosis de 500 UI de eCG logra una menor respuesta superovulatoria respecto a la dosis de 700 UI de eCG; sin embargo, la tasa de recuperación de embriones es superior y la frecuencia de problemas reproductivos posteriores (quistes foliculares) fue menor












 uBio
uBio