INTRODUCCIÓN
La Leucosis Bovina Enzoótica (LEB) es una enfermedad de gran importancia económica y sanitaria en la ganadería lechera (Nekouei et al., 2015), además de poseer un importante potencial zoonótico (Buehring et al. 2015, 2019). Varias investigaciones han demostrado que esta enfermedad afecta negativamente la cantidad (Bartlett et al., 2014; Yang et al., 2016) y calidad de la leche producida e incrementa el número de células somáticas (Yang et al., 2016). Asimismo, las vacas seropositivas presentan más problemas reproductivos y tienen mayor riesgo de descarte prematuro en comparación con las negativas (Romero et al., 2015). La LEB amenaza silenciosamente a la respuesta inmune, incrementando los casos de mastitis clínicas, neumonías y otras enfermedades infecciosas en los animales infectados con el virus (Emanuelson et al., 1992; Trainin et al., 1996; Erskine et al., 2011; Frie y Coussens, 2015; Yang et al., 2016).
La LEB es una enfermedad considerada dentro de la lista de enfermedades de declaración obligatoria de la Organización Mundial de Sanidad Animal (OIE, 2012), con alta prevalencia en muchos países, habiéndose logrado eliminar la enfermedad en 22 países (Nuotio et al., 2003; Acaite et al., 2007; Polat et al., 2017). En Perú se han reportado prevalencias entre 12 y 20% (Díaz et al., 1999; Flores y Rivera, 2000; Barrera, 2010); sin embargo, en un estudio más reciente se determinó una prevalencia de 93% en un establo de Lima (Sandoval et al., 2015), posiblemente debido a la falta de medidas de control (Ruiz et al., 2018), dado que la mayoría de los animales infectados son portadores asintomáticos de la enfermedad y no son separados del hato (Kabeya et al., 2001; Juliarena et al., 2007).
El virus de leucosis bovina (VLB) se transmite principalmente a través de sangre, calostro y leche que contienen leucocitos infectados (Burny et al., 1978; Miller y Van Der Maaten, 1979). La transmisión iatrogénica del virus es muy importante, pero la transmisión a través de la leche y el calostro no dejan de serlo. Romero et al. (1983) encontró que el 9 y 27% de los terneros resultaban positivos al ser alimentados con leche de madres negativas y positivas, respectivamente. La alimentación con leche infectada reduce tempranamente la población de terneros seronegativos al virus (Erskine et al., 2012; Juliarena et al., 2017).
Si bien la mejor manera de erradicar la LEB es mediante un programa de detección y descarte, es prácticamente imposible realizarlo en casos de prevalencias elevadas, donde el ganadero no tiene algún tipo de compensación por las pérdidas (Rodríguez et al., 2011). La implementación de tratamientos que permitan la eliminación del VLB presente en la leche y el calostro es necesaria (Foley y Otterby, 1978; McGuirk y Collins, 2004). Se tiene evidencia que los tratamientos de pasteurización y congelación aplicados a la leche materna de mujeres infectadas por citomegalovirus y virus linfotrópico humano (Ando et al., 2004; Forsgren, 2004) reducen las posibilidades de infección de neonatos que consumen la leche de sus madres.
Baumgartener et al. (1976) demostró que leche llevada a altas temperaturas por cortos periodos de tiempo elimina el VLB, en tanto que Johnson et al. (2007) demostró que la pasteurización del calostro permite mantener una adecuada concentración de inmunoglobulinas y mantiene las propiedades nutricionales del calostro. Así mismo, se ha reportado que la congelación del calostro permite la inactivación del VLB (Kanno et al., 2014). Por lo tanto, el objetivo de este trabajo fue evaluar la eficacia de la pasteurización y la congelación sobre la inactivación del virus de la leucosis bovina presente en leche como una posible estrategia de control en terneros lactantes.
MATERIALES Y MÉTODOS
Lugar y Animales
El presente estudio se realizó en la Clínica de Animales Mayores de la Facultad de Medicina Veterinaria de la Universidad Nacional Mayor de San Marcos (Lima, Perú). Se trabajó con 16 ovinos machos criollos, clínicamente sanos, de cuatro meses de edad. Se comprobó que los ovinos fueron seronegativos al VLB mediante el kit comercial INgezim BLV Compac 2.0 (Eurofins Technologies, España). Los animales fueron alimentados ad libitum con una ración completa.
Diseño Experimental
Los ovinos proporcionan un medio alternativo para estudiar la transmisión del VLB (Miller y Van Der Maaten, 1979; Murakami et al., 2011; Kanno et al., 2014), al ser una especie altamente susceptible a la infección experimental por el VLB y sin presentar transmisión horizontal (Kenyon et al., 1981). El tamaño de muestra se determinó utilizando el procedimiento para variables dicotómicas del software PS: Power and Sample Size Calculation 3.1.6 (Duppont y Plummer, 1997). Se calculó un tamaño de muestra de cuatro ovinos por grupo, considerándose que el 100% de los ovinos seroconvierten luego de la inoculación con el VLB (Kenyon et al., 1981) y que los tratamientos (pasteurización y congelación) evitan el 100% de la transmisión del VLB (Baumgartener et al., 1976; Kanno et al., 2014). Se utilizó un poder de prueba del 80% y un error tipo I de 5%.
Los ovinos fueron inoculados por vía intraperitoneal con el inóculo conteniendo 3x108 leucocitos, procedente de muestras de leche con células infectadas por el VLB para evaluar si el procesamiento de la leche lograba la inactivación del VLB presente en leche. Un tratamiento fue considerado como eficaz cuando no existió seroconversión contra el VLB (Ferrer et al., 1981; Kanno et al., 2014).
Cada grupo experimental estuvo conformado por cuatro ovinos. Los grupos fueron:
Grupo Control: Inóculo de leche sin tratamiento previo.
Grupo Pasteurización: Inóculo de leche tratada por pasteurización.
Grupo Congelación 12 horas: Inóculo de leche congelada durante 12 horas.
Grupo Congelación 36 horas: Inóculo de leche congelada durante 36 horas.
Se realizaron cuatro repeticiones. Para esto, se preparó una mezcla de leche contaminada con leucocitos infectados como fue descrito por Roberts et al. (1983). Para cada repetición se trabajó con 4 L de leche proveniente de una vaca seronegativa al VLB y 120 ml de sangre de una vaca seropositiva con linfocitosis persistente. El estado sanitario de las vacas fue identificado empleando el kit comercial INgezim BLV Compac 2.0 y con dos hemogramas a intervalo de 72 días. En cada ensayo fue inoculado un ovino de cada grupo experimental. Para cada tratamiento, la leche y la sangre previamente mezclada fue dividida en cuatro alícuotas de 1 L c/u. Cada litro de leche contaminada contenía al menos 3x108 leucocitos.
El procedimiento de cada grupo experimental consistió en: a) pasteurización: se calentó a 63 °C durante 30 minutos para la inactivación del VLB (Baumgartener et al., 1976), b) congelación 12 horas: la leche fue almacenada a -23 °C durante 12 horas (Kanno et al., 2014) y c) congelación 36 horas: la leche fue almacenada a -23 °C durante 36 horas.
Obtención del Inóculo
Luego de realizar los tratamientos para inactivación del VLB, las alícuotas de leche (1 L) contendiendo las células infectadas fueron centrifugadas a 2800 g durante 15 minutos (distribuido en cuatro envases de 250 ml) para luego proceder a eliminar la grasa de la leche y el sobrenadante. El sedimento (fracción celular) se diluyó en solución buffer fosfato salino (PBS), cantidad suficiente para 5 ml, que fue colocado en jeringas para inocular a los ovinos. Se corroboró que el número de células leucocitarias obtenidas de cada inóculo alcance una concentración mínima 3x108 leucocitos empleando un hemocitómetro (Kanno et al., 2014). Este procedimiento se repitió para cada tratamiento.
Inoculación
Los ovinos fueron inoculados por vía intraperitoneal a través de la fosa paralumbar derecha. Para esto, los animales fueron sedados con xilacina a dosis de 0.3 mg/kg. El inóculo (5 ml) fue introducido empleando un catéter endovenoso (Abbocat) de 16G x 2.5 pulgadas (Kanno et al., 2014). Finalmente, se utilizó yohimbina a una dosis de 0.2 mg/kg, para revertir el efecto de la xilacina.
Se les tomó muestras de sangre semanal durante 10 semanas para determinar la seropositividad al VLB empleando el kit comercial INgezim BLV Compac 2.0, según las indicaciones de la casa comercial. Esta es una prueba de inmunoensayo enzimático de competición basado en la utilización de anticuerpos monoclonales específicos de la gp51 del VLB. El kit diagnóstico tiene una sensibilidad de 100% y especificidad de 100%, requerida por la OIE (2018). Un ovino fue considerado positivo al VLB cuando después de la inoculación se incrementan los títulos se anticuerpos y se mantienen elevados durante las 10 semanas pos-inoculación.
Consideraciones Éticas
La presente investigación fue aprobada por el Comité de Ética y Bienestar Animal (CEBA) de la Universidad Nacional Mayor de San Marcos, según Constancia de Autorización N,º 2019-5. Los ensayos respetaron los principios directrices internacionales para la investigación biomédica que implica el uso de animales aprobado por el Consejo de Organizaciones Internacionales de las Ciencias Médicas, Ginebra, 1985 (CIOMS).
Análisis Estadístico
Para el análisis estadístico se empleó el software IBM SPSS Statistics 22. Se calculó semanalmente el porcentaje de ovinos seropositivos a gp51. Se empleó la prueba exacta de Fisher para determinar si los tratamientos tuvieron un efecto significativo. Todos los análisis fueron realizados con un nivel de significancia del 5%.
RESULTADOS Y DISCUSIÓN
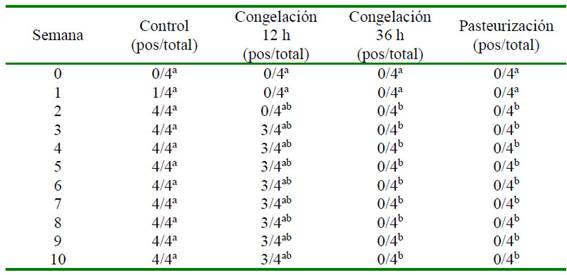
El proceso de pasteurización y el de congelación por 36 horas fueron eficientes para inactivar el virus de leucosis bovina, mientras que el proceso de congelación por 12 horas no logró inactivar el virus. En el Cuadro 1 se puede observar que durante la semana 10 posinoculación todos los animales del grupo control y el 75% de los animales del grupo congelación por 12 horas fueron seropositivos al VLB, mientras que ningún animal fue seropositivo al VLB en el grupo pasteurización y congelación por 36 horas. También se puede observar que los animales del grupo control mostraron positividad a partir de la primera semana pos-inoculación y que los animales del grupo congelación por 12 horas mostraron positividad a partir de la tercera semana de la inoculación.
Las variables críticas para el proceso de pasteurización incluyen la temperatura, el tiempo y la composición del producto (Gröner et al., 2018). Los tratamientos que emplean el calor para inactivar virus desestabilizan térmicamente las interacciones intermole-culares entre las proteínas de la cápside del virus y la integridad de la envoltura del virus. Esta desestabilización térmica produce una pérdida de la integridad estructural de la cápside del virión y, por tanto, la efectividad de los virus (Boschetti et al., 2004). En el presente trabajo las variables consideradas en el proceso de pasteurización fueron una temperatura de 60 °C, durante 30 minutos.
Los resultados demuestran que la pasteurización de la leche es una estrategia factible para la inactivación del VLB, tal como ha sido demostrado por otros autores (Baumgartener et al., 1976; Rubino y Donham, 1984; Lomonaco et al., 2017). Así, Roberts et al. (1983) mostraron que la pasteurización a 50 ° C durante 70 s y Chung et al. (1986) con tratamiento térmico de la leche a 63 °C durante 30 minutos o una pasteurización relámpago a 72-73 °C durante 15-20 s, inactivan los linfocitos infectados con VLB en la leche. Asimismo, la pasteurización relámpago también tiene el beneficio adicional de ayudar a limitar la propagación de la enfermedad de Johne (Stabel y Lambertz, 2004).
La congelación por 36 horas de la leche demostró inactivar las células infectadas con el VLB; resultados que concuerdan con Maschmann et al. (2006), quienes reportan que el proceso de congelación-descongelación de la leche materna evita la transmisión de citomegalovirus en humanos, y con el estudio de Forsgren (2004), quien encontró que la congelación de la leche a -20 °C durante 12 horas sólo redujo la infectividad en un 90%, mientras que la congelación durante 72 horas redujo la infectividad al 100%. Estos resultados se pueden explicar por la formación de hielo intracelular, lo que ocasiona que las células pierdan su potencial de membrana (Shi et al., 2017). Normalmente los virus sobreviven al proceso de congelación; sin embargo, los virus intracelulares, como el VLB, que dependen de la célula que lo alberga, podría verse afectado por el proceso de congelación al destruirse la célula infectada.
En conclusión, los resultados del trabajo indican que la congelación por más de 36 horas y la pasteurización son métodos efectivos para inactivar el VLB y, de esa manera, reducir el riesgo de transmisión de la enfermedad a los terneros lactantes.












 uBio
uBio