INTRODUCCIÓN
Anaplasma phagocytophilum es causante de la Anaplasmosis Granulocítica Canina (AGC) y A. platys es causante de la Trombocitopenia Cíclica Infecciosa Canina (TCIC). Estas enfermedades se presentan de manera subclínica (Brown et al., 2006; Day, 2016) evidenciando mayormente hallazgos hematológicos y, en algunos casos, se presentan signos clínicos como anorexia, fiebre, letargo, mucosas pálidas, hemorragia, esplenomegalia y hepatomegalia a la palpación, poliartritis y en raros casos signos neurológicos (Tateishi et al., 2015; Chirek et al., 2018). Estas enfermedades se transmiten por garrapatas del género Ixodes y por Rhipicephalus sanguineus, respectivamente (Sainz et al., 2015). Estos tipos de garrapatas son las más frecuentes en perros en el norte del Perú (Glenny et al., 2004; Cervantes, 2018).
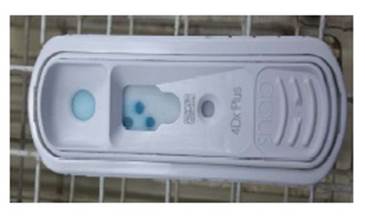
El diagnóstico se basa en los hallazgos hematológicos y serológicos en conjunto de una buena anamnesis. El pronóstico es bueno si es detectado a tiempo (Yancey et al., 2017). En los hallazgos hematológicos se pueden encontrar corpúsculos de inclusión (CI) o mórulas que infectan granulocitos como neutrófilos y eosinófilos (A. phagocytophilum) y plaquetas (A. platys) acompañadas de alteraciones hematológicas (principalmente trombocitopenia, anemia y leucopenia) (Bouzouraa et al., 2016; Chirek et al., 2018); mientras que las pruebas serológicas, como el Test SNAP 4Dx Plus (Idexx), detectan anticuerpos contra Anaplasma spp e incluso de otros patógenos transmitidos por garrapatas.
La información reportada sobre anaplasmosis canina es escasa en el Perú. Existen estudios serológicos con resultados seropositivos frente a Anaplasma spp reportados en Lima, Lambayeque y Piura, incluso con detección de anticuerpos frente a B. burgdorferi y Ehrlichia spp (Rubio et al., 2011; Delgado y Montoya, 2018; Naranjo, 2018), además un estudio hematológico y molecular reportado en Lima Metropolitana donde identificaron A. platys (Tateishi et al., 2015).
El incremento del transporte internacional de animales de compañía, el hacinamiento en perreras como albergues, la crianza con otras especies de animales, el estrecho contacto con el hombre y las coinfecciones con otros patógenos hacen que el diagnóstico se vuelva médicamente más compleja y desafiante; más aún si son animales aparentemente sanos (Sainz et al., 2015). El presente estudio pretende mostrar el panorama actual de la anaplasmosis en perros aparentemente sanos con antecedentes de garrapatas del distrito de Chiclayo (Lambayeque, Perú) mediante hallazgos hematológicos y serológicos.
MATERIALES Y MÉTODOS
Lugar del Estudio
El estudio se realizó en el distrito de Chiclayo, departamento de Lambayeque, Perú, en enero de 2019. La zona se encuentra en la costa norte peruana, presenta un clima subtropical, temperatura máxima de 32 oC, 75% de humedad, condicionando un ambiente favorable para la propagación de los vectores e incidencia de enfermedades rickettsiales. Las muestras fueron procesadas en el Laboratorio Clínico Pet Lab, de Lambayeque, y en el Laboratorio de Patología Clínica Veterinaria de la Facultad de Medicina Veterinaria (FMV) de la Universidad Nacional Mayor de San Marcos (UNMSM), Lima.
Canes
El tamaño muestral (n=88) se determinó mediante la fórmula para estimar poblaciones infinitas utilizando una prevalencia referencial de 6%, reportada por Badillo et al. (2017). Como criterios de inclusión se consideraron perros aparentemente sanos con presencia de garrapatas o de haber estado infestados con estas dentro de los últimos seis meses. No se hizo distinción por raza, sexo o edad. El estudio cumplió con las normas éticas para la investigación establecidas por el Comité de Ética y Bienestar Animal de la FMV-UNMSM.
Muestras
Se colectó sangre de la vena cefálica en en un tubo con EDTA (3 ml) y en otro tubo sin EDTA (5 ml) que posee un gel separador del suero frente al componente celular sanguíneo. Las muestras fueron conservadas en cajas con geles refrigerantes para su traslado al laboratorio.
Hemograma
El hemograma se realizó dentro de las primeras 12 horas en muestras conservadas a 4 °C para evitar falsos valores y alteraciones de la morfología celular producidos por el tiempo de conservación en EDTA. Se hizo el recuento de glóbulos rojos (x106/µl) y glóbulos blancos (x103/µl) con la cámara de Neubauer, hemoglobina (g/dl) mediante el método de la cianometahemoglobina, hematocrito (%) mediante el método del microhematocrito, y el recuento diferencial (%) y plaquetario (x103/µl) a partir del frotis sanguíneo coloreado con tinción Wright. Los valores hematológicos referenciales para perros fueron establecidos por el Laboratorio de Patología Clínica Veterinaria de la FMVUNMSM (Li et al., 2018).
Corpúsculos de Inclusión (CI) o Mórulas
Los frotis sanguíneos teñidos con tinción Wright se evaluaron por duplicado bajo un objetivo de 100X. Cada lámina fue revisada en su totalidad, con énfasis en la monocapa, bordes y cola, buscando CI o mórulas compatibles con A. phagocytophilum y A. platys a nivel intracelular en granulocitos (neutrófilos y eosinófilos) y en plaquetas, respectivamente.
Se consideró como perros positivos aquellos que presentaron trombocitopenias con corpúsculos de inclusión (CI) o mórulas, como sospechosos a aquellos que presentaron solamente CI o mórulas sin trombocitopenia, y como negativos a aquellos que no presentaron trombocitopenia ni CI o mórulas.
Análisis Serológico
Los sueros se conservaron en viales a -20 °C y fueron procesados en el Laboratorio de Patología Clínica Veterinaria de la FMV-UNMSM. Para el análisis se llevaron a temperatura ambiente (15-25 oC) y se utilizó el Test SNAP 4Dx Plus (IDEXX Laboratories, 2018). El kit permitió detectar muestras seropositivas (presencia de anticuerpos) y seronegativas (ausencia de anticuerpos detectables) contra Anaplasma spp.
RESULTADOS Y DISCUSIÓN
Se determinó que el 48.9% (43/88) de los perros con antecedentes de garrapatas presentaron trombocitopenia (<200 x103/µl). Si bien es cierto la trombocitopenia es la alteración hematológica más frecuente en casos de anaplasmosis (Bouzouraa et al., 2016; Chirek et al., 2018), también se presenta en otras enfermedades transmitidas por garrapatas como erliquiosis y babesiosis canina (Santos et al., 2009; Day, 2016), enfermedades prevalentes en la zona.
El 4.5% (4/88) de perros con antecedentes de garrapatas evidenciaron mórulas al interior de plaquetas, siendo compatibles con A. platys (Figura 1), mas no se observaron en granulocitos. Por otro lado, como hallazgo accidental, el 34.1% (30/88) de los perros evidenciaron CI o mórulas en linfocitos siendo compatibles con E. canis, lo cual explicaría la alta frecuencia de animales trombocitopénicos. Cabe mencionar que los cuatro perros que fueron compatibles con A. platys también fueron para E. canis.
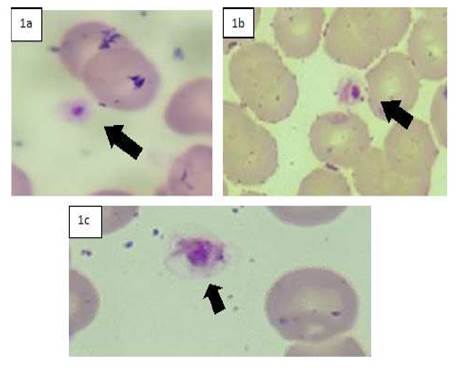
Figura 1 Frotis sanguíneos de perros con antecedentes de garrapatas con mórulas compatibles con A. platys al interior de plaquetas circulantes. Tinción Wright, 1000x
La baja frecuencia de perros con mórulas compatibles con A. platys puede relacionarse con la sensibilidad de la técnica y con los episodios cíclicos que caracteriza la enfermedad. Se sabe que existe mayor sensibilidad de la prueba al inicio o durante la manifestación de los signos clínicos (Greene, 2012; Day, 2016); sin embargo, A. platys se ha reportado en perros aparentemente sanos, siendo confirmado por PCR (Inokuma et al., 2002; Brown et al., 2006). En casos crónicos, la sensibilidad disminuye drásticamente por la baja bacteriemia; no obstante, se han reportado inclusiones ocasionales compatibles con A. platys hasta 21 meses de la inoculación en infecciones experimentales (Kontos et al., 1991). Es por ello por lo que la ausencia de mórulas o corpúsculos de inclusión no descarta la infección, más aún si se evidencia alteraciones compatibles por A. platys.
En infecciones por A. platys generalmente se encuentra involucrado el 1% de las plaquetas (Day, 2016); pero en casos agudos se ha reportado hasta 97% de plaquetas infectadas (Arraga-Alvarado et al., 1997) e incluso en células precursoras de plaquetas (Day, 2016).
No se evidenció CI o mórulas compatibles con A. phagocytophilum en granulocitos; sin embargo, no se puede descartar la infección. Experimentalmente se han encontrado hasta 14 días pos-infección (Greene, 2012). En este sentido, Rubio et al. (2011) y Tateishi et al. (2015) sugieren la presencia de este agente en perros con signos compatibles a anaplasmosis. Por otro lado, en la provincia de Chiclayo (Lambayeque), se hallaron CI o mórulas en neutrófilos compatibles con A. phagocytophilum en 9% (9/100) de caballos aparentemente sanos (Masgo, 2018) demostrando que es posible observarlas a la evaluación del frotis sanguíneo en animales asintomáticos. Cabe mencionar que las mórulas en neutrófilos no pueden diferenciarse de E. ewingii (Day, 2016).
Según Greene (2012), A. phagocytophilum tiene mayor afinidad por los neutrófilos de humanos, caballos y perros; siendo esto motivo de alarma en la provincia de Chiclayo, ya que se ha observado que los haras de caballos tienen usualmente perros guardianes y están en convivencia con el hombre. Se ha detectado anticuerpos contra Anaplasma spp en personas que han estado en contacto con perros infectados (Arraga-Alvarado et al., 2014; Weinborn et al., 2018).
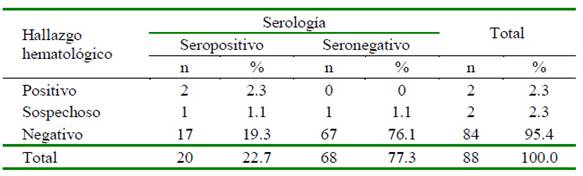
Los CI o mórulas compatibles con Anaplasma spp por sí solas no proporcionan un diagnóstico definitivo; de allí que se requiere complementar el análisis con un hemograma para encontrar alteraciones hematológicas sugerentes de anaplasmosis. Según los resultados obtenidos, se consideró como positivos a dos perros trombocitopénicos con visualización de CI o mórulas compatibles con Anaplasma spp y a 2 perros como sospechosos (no trombocitopénicos con CI o mórulas y a 84 como negativos (no trombocitopénicos ni CI o mórulas) (Cuadro 1). Además, se evidencia la ocurrencia de TCIC mediante el hallazgo hematológico en perros aparentemente sanos con antecedentes de garrapatas en la zona del estudio.
Cuadro 1 Resumen general de los hallazgos hematológicos y serológicos de 88 perros con antecedentes de garrapatas del distrito de Chiclayo (Lambayeque -Perú)
La baja frecuencia de perros (2/88) que resultaron ser sospechosos (solo CI o mórulas sin trombocitopenia) podría explicarse por la trombocitopenia de tipo cíclica que caracteriza a la enfermedad, donde persiste durante entre 7 a 14 días, seguida de un corto periodo de recuperación, durante el cual el recuento plaquetario vuelve a la normalidad (Harvey et al., 1978).
Los dos perros que fueron positivos a los hallazgos hematológicos tenían una moderada trombocitopenia (129 y 139.50 x 103/µl, respectivamente), mas no anemia. En cuanto a la serie leucocítica, uno presentó leucocitosis (20.05 x 103/µl), neutrofilia (14.24 x 103/µl) ylinfocitosis (5.01 x 103/µl); mientras que otro manifestó leucopenia (7.4 x 103/µl) y neutropenia (5.18 x 103/µl). Estos resultados coinciden con los reportados en infecciones causadas por A. platys (Bouzouraa et al., 2016). Por otro lado, los otros dos perros que resultaron ser sospechosos solo presentaron una leve anemia, alteración que es la segunda más reportada en casos de anaplasmosis (Bouzouraa et al., 2016; Chirek et al., 2018).
La presencia de trombocitopenia en infecciones por A. platys se debe a causas tales como fagocitosis plaquetaria, disminución en la producción de plaquetas al verse alterados los megacariocitos, y destrucción inmunomediada (Gaunt et al., 2010). Las hemorragias son poco frecuentes debido a la corta duración de la trombocitopenia (Harvey et al., 1978; Gaunt et al., 2010). Se ha reportado caninos muy trombocitopénicos (<20 x103/ml) que se encuentran aparentemente sanos sin evidencia de hemorragias (Ulutas et al., 2007).
El 22.73% (20/88) de seropositividad mediante el Test SNAP 4Dx Plus fue menor al 34.62% reportado por Delgado y Montoya (2018) utilizando el kit Vet Scan Anaplasma Rapid Test en perros con signos clínicos compatibles con la enfermedad del mismo lugar de estudio. No obstante, estos resultados evidencian una mayor exposición de Anaplasma spp en los perros de Chiclayo que en otras zonas cercanas como Piura donde se ha reportado 4.2% (3/71) en perros con signos clínicos e historial de garrapatas (Naranjo, 2018), a pesar de que en dicha zona se reporta perros con garrapatas Ixodes spp y R. sanguineus (Glenny et al., 2004).
Estudios realizados en países vecinos mediante el test SNAP 4Dx reportan seroprevalencias en perros de 43.7% (35/80) en Chile (Álvarez et al., 2015), de 33% (161/ 498) en Colombia (McCown et al., 2015) y 53.8% (38/80) en perros de barrios rurales en Ecuador (Peñaloza, 2015), siendo en todos los casos mayores a los hallados en el presente estudio. Un resultado serológico para Anaplasma spp depende de muchos factores tales como la etapa de la enfermedad, el sistema inmunológico del perro, la distribución de Anaplasma spp en el territorio y la exposición a garrapatas R. sanguineus e Ixodes spp, entre otros.
La duración de anticuerpos detectables en el perro pos-infección puede ser entre unos pocos meses hasta varios años. En estudios experimentales con A. platys se detectaron títulos de anticuerpos, mediante IFA hasta el día 171 de la inoculación (Kontos et al., 1991) y hasta el día 410 mediante el test SNAP 4Dx (Gaunt et al., 2010) que duraron tales investigaciones. En infecciones naturales con A. phagocytophilum se detectaron anticuerpos hasta los 36 meses (Eberts et al., 2011).
Un resultado seropositivo puede significar que han sido expuestos con anterioridad a la infección y superaron la enfermedad manteniendo los anticuerpos en sangre o que represente una infección activa. Por otro lado, un resultado seronegativo puede indicar que no presentan anticuerpos contra Anaplasma spp ya que nunca estuvieron expuestos al agente, o que los anticuerpos aún no son detectables por la prueba, ya que la infección se encuentra en el periodo de incubación o en una primera etapa de la enfermedad aguda cuando las cargas bacterianas son bajas (en caso de una infección presente) (Sainz et al.., 2015; Day, 2016).
La alteración hematológica de mayor frecuencia en los 20 perros seropositivos a Anaplasma spp fue la trombocitopenia (60%, 12/20), seguido de anemia (55%, 11/20), leucocitosis (30%, 6/20) y leucopenia (15%, 3/20); resultados similares a los reportados por Naranjo (2018) en caninos seropositivos con signos compatibles a la enfermedad con antecedentes de garrapatas.
La única seropositividad múltiple fue Anaplasma spp con Ehrlichia spp (21.59%, 19/88) (Figura 2) siendo menor al 30.1% (150/ 498) hallado en Colombia (McCown et al., 2015). No obstante, seropositividades múltiples menores han sido reportadas por Álvarez et al. (2015) en Chile (3.75%) y por Naranjo (2018) en Piura, Perú (4.2%). En el estudio no se detectaron anticuerpos contra B. burgdorferi.
Al relacionar los hallazgos hematológicos (positivos, sospechosos y negativos) y serológicos para Anaplasma spp en los 88 perros con antecedentes de garrapatas del distrito de Chiclayo se identificaron cinco grupos: 1) perros positivos y seropositivos, 2) perro sospechoso y seropositivo, 3) perro sospechoso y seronegativo, 4) perros negativos y seropositivos y 5) perros negativos y seronegativos (Cuadro 1). La forma de interpretar los exámenes hematológicos y serológicos determinará el paso a seguir en cuanto al tratamiento y seguimiento en un animal aparentemente sano, según el criterio del Médico Veterinario tratante. En el presente trabajo, los perros seopositivos y hematológicamente positivos son indicativos de anaplasmosis subclínica y, por tanto, se debería iniciar el tratamiento de inmediato; más aún en los casos en que se encontró coinfección con E. canis. En este caso, un tratamiento con doxiciclina a 10 mg/kg durante 28 días sería necesario.
CONCLUSIONES
El 2.27% de perros con antecedentes de garrapatas fueron positivos a Anaplasma platys mediante los hallazgos hematológicos.
El 22.73% de perros con antecedentes de garrapatas fueron seropositivos a Anaplasma spp.
Las alteraciones hematológicas más frecuentes en perros seropositivos fueron trombocitopenia, anemia y leucocitosis.
El 21.59% de perros con antecedentes de garrapatas presentó una seropositividad múltiple contra Anaplasma spp y Ehrlichia spp.












 uBio
uBio