INTRODUCCIÓN
La blastocystosis es una zoonosis emergente (Maloney et al., 2019) causada por organismos unicelulares eucarióticos del género Blastocystis, incluidos en el Reino Chromista (Cavalier-Smith et al., 2018), y presentes en anélidos, artrópodos, peces, anfibios, reptiles y un amplio espectro de aves y mamíferos, incluyendo el humano (Yoshikawa et al., 2016a; Valenca-Barbosa et al., 2019). La infección intestinal de trasmisión fecaloral tiene una alta prevalencia en la población humana, siendo más frecuente en países en desarrollo con deficientes condiciones de saneamiento ambiental (Tan, 2008; Andersen y Stensvold, 2016). Su trasmisión se favorece a través del consumo de agua o alimentos contaminados con los estados quísticos del parásito (Tan, 2008).
La prevalencia de blastocystosis en gallinas (Gallus gallus domesticus) ha sido registrada en Australia (Lee y Stenzel, 1999), Brasil (do Bomfim y Machado do Couto et al., 2013), Malasia (Farah Hazigah et al., 2014; Termizi et al., 2018; Mohammad et al., 2018), Indonesia (Yoshikawa et al., 2016b), Polonia (Lewicki et al., 2016), China (Wang et al., 2018) y Líbano (Greige et al., 2018).
La diversidad y especialmente la prevalencia de parásitos eucarióticos en gallinas en Chile ha sido escasamente estudiada, documentándose alrededor de 34 especies entre protozoos, platelmintos, nematodos y artrópodos (Alcaino y Gorman, 1999), sin registrarse Blastocystis sp. Sin embargo, la prevalencia de blastocystosis en población humana, de distinta edad y sectores rurales del sur de Chile fluctúa entre 27.2 y 64.3% (Torres et al., 1990, 1997; Navarrete y Torres, 1994; Barra et al., 2016) y en cerdos criados libremente alcanza un 22.2% (Torres et al., 1992).
La patogenicidad de B. hominis es controvertida, sugiriéndose que es dependiente de nueve subtipos (ST1-ST9), basados en la filogenia del gen de la subunidad rRNA (SSUrDNA) (Yoshikawa et al., 2016b). De estos, ocho han sido identificados en pollos, vacunos, ovinos, roedores, cerdos o primates no humanos (Ramirez et al., 2014; ValencaBarbosa et al., 2019; Oliveira-Arbex et al., 2018). Los subtipos ST1-ST2, ST4-ST8 pueden encontrarse en aves (Stensvold y Clark, 2016; Valenca-Barbosa et al., 2019), siendo ST6-ST7 los más frecuentes (Stensvold y Clark, 2016). Sin embargo, la correlación entre subtipos zoonóticos y patogenicidad aún se encuentra en debate (Deng et al., 2019) y en Chile el único estudio sobre subtipos de Blastocystis determinó ST1-ST2 y ST4 en 37 pacientes en la ciudad de Santiago (Peña et al., 2018). En los casos sintomáticos, la infección humana ha sido asociada a diarrea, náuseas, constipación y dolor abdominal, asociándose también al síndrome de colon irritable y urticaria (Stensvold y Clark, 2016).
En el diagnóstico de Blastocystis se han utilizado métodos basados en el estudio de la morfología del parásito (microscopía) a través del examen de heces fijadas y teñidas, métodos de cultivo, detección de ADN (PCR), antígenos del parásito o anticuerpos (Stensvold y Clark, 2016). La identificación morfológica de Blastocystis sp es mediante el hallazgo de la forma vacuolada que se encuentra frecuentemente en las heces (García, 2007). Desde un punto de vista clínico, los métodos de microscopía no son tan sensibles en la detección de Blastocystis; sin embargo, hay situaciones en que pueden ayudar cuando el propósito es verificar su presencia en varios tipos de muestras no humanas, incluidas las de origen ambiental y animal (Stensvold y Clark, 2016).
Por la elevada prevalencia de blastocystosis humana en el sur de Chile, en especial en zonas rurales donde la población suele vivir en contacto con aves y otros animales domésticos, se planteó el presente estudio cuyos objetivos fueron: 1) determinar si la infección por Blastocystis sp está presente en gallinas en localidades del sur de Chile, 2) determinar la prevalencia en humanos y en gallinas de su tenencia al menos en una de las localidades y, 3) determinar otras infecciones por parásitos intestinales en las aves.
MATERIALES Y MÉTODOS
Entre 2016 y 2019 se colectaron 176 muestras de heces frescas de gallinas criadas libres, en domicilios distribuidos en dos localidades urbanas: Valdivia (n=40) y Niebla (n=36) y en tres localidades rurales: Ñancul (n=50), Quilquico (n=22) y Teupa (n=28), las dos últimas situadas en la Isla Grande de Chiloé. Adicionalmente, en la localidad de Ñancul se colectaron 16 muestras de heces humanas en siete de los ocho domicilios donde se obtuvo las muestras de aves.
Las muestras (3-5 g de heces) fueron colocadas en frascos de plástico con 15 ml del fijador PAF (phenol-alcohol-formalin) (Burrows, 1967), homogenizándose con una varilla de madera. Las muestras fueron procesadas mediante el método de sedimentación propuesto por Burrows (1967) y adaptado por Torres y Navarrete (1972). De cada muestra procesada, se observaron dos preparaciones microscópicas utilizando cubreobjetos de 22 x 22 mm: una en la fase A del método (centrifugación de la muestra tamizada con NaCl 0.15M a 540 g durante 3 min, permitiendo mayor concentración de trofozoítos), y otra en la fase B (centrifugación del sedimento remanente de la fase A, con NaCl 015 M + 2 ml de acetato de etilo, que favorece la mayor concentración de quistes y huevos). Ambas preparaciones fueron teñidas con tionina de 0.1% y examinadas a 100 y 400x.
Adicionalmente, al sedimento remanente en el tubo de la fase B se agregó una solución de sulfato de zinc (70 g de sulfato de zinc en 100 ml de agua destilada), centrifugado durante 5 min a 540 g, para incrementar la recuperación de huevos de helmintos y coccidias (Torres et al., 1972). Posteriormente, al tubo se le agregó solución de sulfato de zinc hasta formar un menisco sobre el cual se depositó un cubreobjetos de 22 x 22 mm durante 30 min y luego colocado sobre un portaobjetos, examinándose a 100 y 400x.
La identificación de los parásitos se realizó con la literatura pertinente (Levine, 1961; Mehlhorn et al., 1993; Tan, 2008). En el caso de los huevos de Ascaridia galli y Heterakis gallinarum, por ser morfológicamente similares, se registraron como A. galli /H. gallinarum.
El análisis de prevalencia para cada parásito entre distintas localidades incluyó la prueba de Chi cuadrado de Pearson, con corrección de Yates en el caso de dos muestras. Cuando hubo frecuencias esperadas inferiores a cinco, se utilizó la prueba exacta de Fisher para pares de muestras. Para la aplicación de las pruebas estadísticas se empleó el software EPI DAT 3.1TM. Para todas las pruebas, p<0.05 fue considerada estadísticamente significativa, utilizando ensayos de dos colas.
RESULTADOS
Las formas vacuoladas de Blastocystis sp en las muestras de aves midieron 12.1 ± 3.2 µm de diámetro (5-25 µm; n=84), con una vacuola central y un delgado citoplasma periférico que incluyó un número variable de núcleos (Figura 1A-C). La forma vacuolada fue similar en las muestras humanas, midiendo 10.1 ± 2.3 µm (7.5-15 µm; n=26). En la mitad de los domicilios se encontraron gallinas infectadas con Blastocystis sp, siendo la prevalencia promedio de 14.2%, siendo mayor (p<0.05) en la zona rural y, particularmente, en la localidad de Teupa (Cuadro 1). En la localidad de Ñancul, la prevalencia de infección en humanos fue mayor respecto a las aves (p<0.05); además, la infección afectó simultáneamente a gallinas y humanos en 4 de los 7 domicilios, pero en los restantes solo estuvo presente en uno de los hospederos (Cuadro 2).
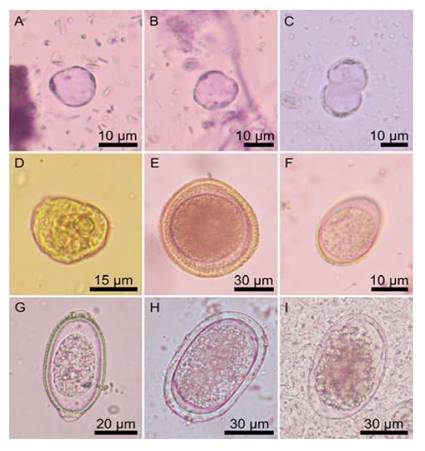
Figura 1 Parásitos intestinales de Gallus gallus domesticus en localidades del sur de Chile. (A-B) Formas vacuoladas de Blastocystis sp; (C) Forma vacuolada de Blastocystis sp en división; (D) Trofozoito de Entamoeba gallinarum; (E) Huevo de Toxocara sp; (F) Ooquiste de Eimeria sp; (G) Huevo de Capillariidae gen. sp.; (H) Huevo de Ascaridia galli/Heterakis gallinarum; (I) huevo de Trichostrongylidae gen. sp
Cuadro 1 Prevalencia de infección por Blastocystis sp en Gallus gallus domesticus en domicilios del sector urbano y rural en el sur de Chile
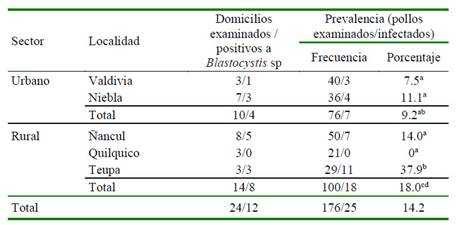
Superíndices con letras diferentes en la columna dentro de sectores y localidades indican diferencia estadística (p<0.05)
Cuadro 2 Hospederos de Blastocystis sp y su prevalencia en domicilios de la localidad de Ñancul, Chile
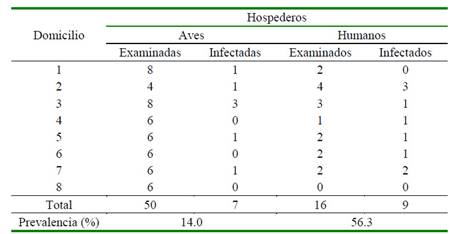
Prueba de Fisher (p<0.02)
La prevalencia de infección por Entamoeba gallinarum (Figura 1D) y la presencia de huevos de Toxocara sp (Figura 1E) no mostró diferencias significativas (p>0.05) entre localidades (Cuadro 3). La prevalencia de Eimeria spp (Figura 1F) fue similar al comparar la mayoría de las localidades (p>0.05), excepto en Ñancul donde fue inferior (p<0.05) a Valdivia y Quilquico (Cuadro 3). Las prevalencias de infección por Capillariidae gen. spp (Figura 1G) y H. gallinarum /A. galli (Figura 1H) fueron superiores (p<0.05) en Valdivia y Teupa, respecto a las demás localidades (Cuadro 3). Solo en Valdivia se registraron muestras con huevos de Trichostrongylidae gen. spp (Figura 1I; Cuadro 3).
Cuadro 3 Otros parásitos eucarióticos en heces de Gallus gallus domesticus en localidades del sur de Chile
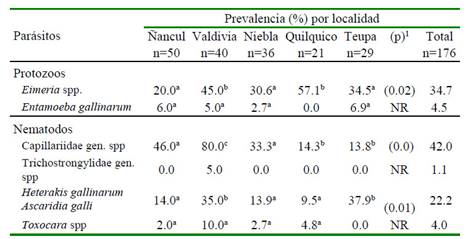
1 Comparación entre todas las localidades para cada parásito
NR: no realizada por haber frecuencias esperadas <5 o presencia del parásito en una sola localidad
Superíndices diferentes dentro de las filas indican diferencia estadística (p<0.05) entre pares de localidades, mediante las pruebas de Chi cuadrado o de Fisher
DISCUSIÓN
En el presente estudio se registra por primera vez la presencia y prevalencia por Blastocystis sp y E. gallinarum en gallinas de Chile y además se aportan datos de prevalencia para otros parásitos intestinales en distintas localidades del sur de este país. Las formas vacuoladas de Blastocystis fueron morfológicamente similares a las descritas por otros autores con tamaños entre 3-120 µm (Lee y Stenzel (1999), 10.9-32.1 µm (do Bomfim y Machado do Couto, 2013) y 10-30 µm (Farah Haziqah et al., 2014).
La prevalencia promedio de infección por Blastocystis sp en gallinas fue mayor en la zona rural (p<0.05); sin embargo, la prevalencia de infección humana fue cuatro veces mayor a la encontrada en las gallinas de la localidad de Ñancul, donde además se observó la presencia simultánea de blastocystosis en aves y humanos en cuatro de los siete domicilios donde se presentó la infección, sugiriendo la posibilidad de trasmisión entre ambos hospederos. Estudios previos de la prevalencia de blastocystosis humana en las localidades de Panguipulli y Choshuenco (56%) (Torres et al., 1982), ambas cercanas a Ñancul, en Valdivia (50%) (Torres et al. 1997), en Niebla (64%) (Navarrete y Torres, 1994) y en Natri y Huillinco (27%-41%), próximas a Teupa (Torres et al., 1990); también sugieren ser comparativamente mayores que las prevalencias de blastocystosis determinadas en el presente estudio, en gallinas de la mayoría de las localidades; no obstante, se debe considerar el que muchos de estos trabajos son de años atrás.
Se requiere profundizar la determinación de los subtipos de Blastocystis en aves y humanos que comparten domicilios, ya que si bien existe la infección en ambos hospederos, esta podría ser causada por diferentes subtipos (Yoshikawa et al., 2016b; Mohammad et al., 2018). No obstante, también podría deberse a subtipos comunes indicando una situación zoonótica (Lewicki et al., 2016; Greige et al., 2018). El mayor porcentaje de infección en humanos podría, en parte, estar en relación con el mayor espectro de subtipos de Blastocystis que pueden vivir en su intestino respecto a aquellos que se establecen en pollos (Stensvold y Clark, 2016; Valenca-Barbosa et al., 2019).
Respecto a la prevalencia de blastocystosis en aves de otros países, do Bomfim y Machado do Couto (2013) reportaron prevalencias de 22.9 y 42.8% en dos mercados de Brasil; Farah Haziqah et al. (2014) y Termizi et al. (2018) reportaron mayores prevalencias en pollos criados libremente respecto a otros sistemas de crianza. Con relación a los subtipos, Mohammad et al. (2018) detectaron ST1-ST3 en grupos humanos y solo ST6 en pollos, mientras que Lewicki et al. (2016) en dos granjas de Polonia encontraron prevalencias de 31% para ST6 y 24% para ST7 en aves criadas libremente, donde la infección humana es frecuente y ocasionalmente causada por ST6. De otra parte, Oliveira-Arbex et al. (2018) detectaron tres casos de infección con ST7 en niños de 1, 5, y 6 años, que vivían en contacto con gallinas criadas libres en los patios de sus casas.
Respecto a otros parásitos, Entamoeba gallinarum, considerada una ameba no patógena (Hooshyar et al., 2015), se presentó con baja prevalencia en los sectores donde fue identificada alcanzando un máximo de 6.9% en Teupa. En el caso de infecciones por Eimeria spp, en Chile se han reportado E. tenella, E. necatrix, E. acerbulina, E. mitis y E. maxima (Alcaino y Gorman, 1999), pero no hay registros publicados sobre su prevalencia en el país. En este estudio, la eimeriosis fue mayor (p<0.05) en gallinas de las localidades de Valdivia y Quilquico.
La mayor prevalencia de Capillariidae gen. spp. correspondió a Valdivia, donde se han identificado Eucoleus contortus (=Capillaria contorta), Baruscapillaria obsignata (=Capillaria obsignata) y Pterothominx caudinflata (Capillaria caudinflata) con prevalencias de 15 a 25% (Torres et al., 1974). La infección por H. gallinarum /A. galli alcanzó su mayor prevalencia (p<0.05) en las localidades de Valdivia y Teupa. Ascaridia galli puede causar enteritis, diarrea, disminución en la producción de huevos, obstrucción y hemorragia intestinal en infecciones intensas (Soulsby, 1968). Heterakis gallinarum habitualmente produce una patología leve que no afecta significativamente al rendimiento de las aves (Schwarz et al., 2011). Sin embargo, H. gallinarum es económicamente importante para la industria avícola debido a que sus huevos sirven como vector para el protozoo Histomonas meleagridis, causante de lesiones severas en el tracto digestivo e hígado, provocando elevada mortalidad en las aves (Schwarz et al., 2011; Cupo y Beckstead, 2019). Por otro lado, en la localidad de Valdivia se registraron huevos de la familia Trichostrongylidae que probablemente correspondan a Trichostrongylus tenuis, única especie de Strongylida registrada en gallinas de Chile (Alcaino y Gorman, 1999).
En la mayoría de las localidades las aves presentaron infecciones espurias al encontrarse huevos de Toxocara spp en sus heces, los que probablemente ingresaron a su tracto digestivo por ingestión de agua o alimentos contaminados. En todos los sitios de muestreo hubo presencia de perros que por ser hospederos definitivos de T. canis contribuyen a la contaminación del suelo con sus heces. Experimentalmente, se ha determinado que los huevos no infectantes de T. canis al pasar por el tracto digestivo de las aves y ser eliminados con las heces mantienen su viabilidad (Merigueti et al., 2018), lo cual aumenta las probabilidades de contaminación de alimento o agua de bebida y a la vez facilita la infección humana. Al menos, Vargas et al. (2016) en la localidad de Niebla determinaron 25% de seroprevalencia de toxocariosis en la población humana, cuyos principales factores de riesgo fueron la edad, ruralidad y carencia de agua potable.
CONCLUSIONES
Blastocystis sp fue registrada por primera vez en gallinas en 4 de 5 de localidades del sur de Chile con prevalencia promedio de 14.2%, siendo más elevada en la zona rural y en la localidad de Teupa (p<0.05).
En la localidad de Ñancul, el examen de heces humanas y de gallinas reveló infección simultánea en cuatro domicilios.
En las heces de las gallinas también se registrarontrofozoítosyquistesdeEntamoeba gallinarum, ooquistes de Eimeria spp, huevos de H. gallinarum /A. galli, Capillariidae gen.spp, Trichostrongylidae gen. spp y Toxocara spp.
Financiado parcialmente por el Programa de Diversidad de Parásitos y Zoonosis Trasmitidas por Organismos Acuáticos. Dirección de Investigación y Desarrollo (DID N° 12010-02). Universidad Austral de Chile












 uBio
uBio 

