INTRODUCCIÓN
La diarrea asociada a Escherichia coli es una enfermedad de importancia en crías de alpacas y llamas, cuya presentación está frecuentemente acompañada con septicemia. Las crías afectadas presentan profusa diarrea acuosa, letargia, deshidratación e incluso distención abdominal (Whitehead y Anderson, 2006). En alpacas y llamas se han desarrollado diversos estudios para la identificación de factores de virulencia asociados a los patotipos de E. coli presentes. Así, se han descrito los patotipos EPEC, ETEC y EHEC como los más frecuentes a partir de aislados de crías y adultos, tanto en casos de animales con diarreas (enfermos) y sin diarrea (Cid et al., 2012; Luna et al., 2012; Mori et al., 2014; Rosadio et al., 2012). A la vez, se han descrito algunos serotipos fimbriales y su asociación con rotavirus en crías de alpacas con diarreas y en alpacas clínicamente sanas (Morales y Paredes, 2007).
Uno de los primeros factores de virulencia en la patogénesis de E. coli son las adhesinas, que le permite a la bacteria asentarse y colonizar las células blanco y, posteriormente, eliminar toxinas o proteínas efectoras que alteran el funcionamiento normal de las células de la mucosa intestinal. Entre las adhesinas más representativas son las de tipo fimbrial, principalmente las fimbrias F4, F5, F6, F17, F41, F18, que están asociadas a los patotipos Enteropatogénicos (EPEC), y con mucha más frecuencia a los enterotoxigénicos (ETEC). En porcinos, la fimbria F18 está asociada a las E. coli productoras de Shiga toxina (STEC) (Nagy y Fekete, 1999). Sin embargo, estos patrones han mostrado variaciones particulares, tanto en aves como en bovinos, teniendo bacterias con combinaciones de factores de virulencia, tanto adhesinas como fimbrias de diferentes patotipos. Así, se ha reportado que la fimbria F17 es una familia de fimbrias y que sus variedades están asociados como principal adhesina de muchos patotipos, inclusive los necrotoxigénicos (NTEC) de reciente clasificación y los enterohemorrágicos (EHEC), cuya estructura fimbrial se compone de una base que es la proteína estructural mayor «A», mientras que la proteína estructural menor que tiene función de interacción o adhesión es la «G» (Bihannic et al., 2014). Por ello, las fimbrias han servido como candidato vacunal contra E coli para la inmunización de diferentes especies (Francis y Willgohs, 1991; Luna-Pineda et al., 2016; Tiels et al., 2008; Zhang et al., 2018).
La vacunación sigue siendo una de las principales estrategias para la prevención de diarreas. Se han desarrollado diferentes tipos de vacunas contra E. coli para diferentes especies, con base a células muertas o bacterinas de determinado serotipo fimbrial o somático, toxoides, así como algunas vacunas recombinantes contra determinados antígenos estructurales, hallándose diferente grado de protección (Cox et al., 2014). Entre las más difundidas y con mejores resultados en bovinos y porcinos son las orientadas contra determinados serotipos fimbriales (Hur et al., 2012). Por ello, el presente estudio buscó determinar la capacidad inmunogénica de la proteína recombinante de la adhesina fimbrial F17 de E. coli, mediante la medición de citoquinas relacionadas a Th1 y Th2, paso importante en la evaluación de un candidato vacunal para la prevención de diarreas en alpacas asociadas a E. coli.
MATERIALES Y MÉTODOS
Lugar del Estudio
El desarrollo y caracterización de la proteína F17 se llevó a cabo en las instalaciones de la Facultad de Microbiología, Inmunología y Bioquímica de The University of Tennessee Health Science Center, Memphis, USA, mientras que la evaluación in vitro de citoquinas se realizó en el Laboratorio de Biología y Genética Molecular de la Facultad de Medicina Veterinaria (FMV) de la Universidad Nacional Mayor de San Marcos (UNMSM), Lima, Perú. Los protocolos utilizados fueron aprobados por el Comité de Ética y Bienestar Animal de la FMVUNMSM, mediante Autorización de Ética N.° 2017-003.
Proteína Recombinante F17 (rF17)
Los protocolos para la elaboración y producción de la proteína recombinante F17 (rF17) fueron adaptados de Gomes-Solecki et al. (2006), utilizándose el péptido señal de OspA de Borrelia burgdorferi.
Se utilizó la secuencia optimizada, acompañada del péptido señal del gen de la fimbria F17 N.° de Acceso NC_012944.1 (pVir_11 F17) del banco de genes (Escherichia coli Vir68); secuencia conformada por 1032 pares de bases, el cual fue insertado en el plásmido pET-28a (Novagen). El plásmido posee genes de resistencia a la kanamicina y una secuencia de residuos de histidina, para la purificación proteica.
Se utilizó a la E. coli competente BL21 (Biolab) para la transformación y expresión proteica de rF17 insertado el plásmido pET28a para la purificación proteica, siguiendo las instrucciones del fabricante.
Vector y Expresión de rF17
BL21 conteniendo pET-28ª, plásmido codificante de rF17 (BL21+F17), fue cultivado en el medio TBY (caldo triptona y levadura) con kanamicina a una concentración final de 50 mg/ml, durante más de 12 h a 37 p C, con agitación a 200 rpm. Una vez que el cultivo alcanzó 0.7-0.9 de densidad óptica, se añadió 0.5 mM del inductor de expresión, isopropil-β-D-1-tiogalactopiranósido (IPTG) y se incubó durante 3 h con las condiciones previas. Luego, se centrifugó el cultivo a 4000 rpm durante 8 min, se descartó el sobrenadante y se añadió 5 ml de glicerol al 20% por litro de cultivo, y se almacenó a -80 °C. Se utilizó un método estándar para la caracterización proteica (Gomes-Solecki et al., 2006).
Purificación de rF17
Se estandarizó un protocolo para la purificación del antígeno vacunal recombinante rF17: utilizando tres soluciones: Solución de Unión: fosfato de sodio 0.1M pH 7.5. Urea 6 M; Solución de lavado: fosfato de sodio 0.1M pH 6.5. Urea 6 M; Solución de elución: fosfato de sodio 0.1 M pH 4.5. Urea 6 M. Asimismo, se utilizó una columna de purificación de proteínas, y con 500 µl de resina de cobalto.
Cuadro 1 Secuencias y características de los cebadores utilizados para las evaluaciones de citoquinas
| Genes | Secuencias | Productos pares de bases (bp) | Temperatura de alineamiento (°C) |
| IFN γ | 5′-ATTGTCTCCTTCTACTTCAA-3′ 5′-AGCGGAAGAGAAGTCAGAAT -3′ | 258 | 45 |
| TNFα | 5′-CTACTCCCAGGTCCTCCTGA-3′ 5′-GGTAGTTGGGCATGTTGATC-3′ | 251 | 60 |
| IL-2 | 5′-AAACTCTCCAGGATGCTCAC-3′ 5′-GGAACTGAAGGGATCTGAAA-3′ | 202 | 49 |
| IL-4 | 5′-CAAAGAACACAACTGAGAAG-3′ 5′-GGCTAAAGAAGATTATGAAG-3′ | 203 | 46 |
| IL-10 | 5′-AAGCCTTGTCGGAGATGAC-3′ 5′-AGCCATGAGTGAGTTCGACA-3′ | 246 | 55 |
| GAPDH | 5′-GTGAAGGTCGGAGTGAACG-3′ 5′-GAGATGATGACCCTCTTGGC-3′ 5′-CTCAAGTTGGGGGACAAAAA-3′ | 356 | 60 |
Finalmente se realizó una electroforesis para proteínas (SDS-PAGE) para la verificación de la expresión y la purificación de rF17. Además, se comprobó mediante Western Blot usando anticuerpos monoclonales contra los residuos de histidina (ThermoFisher) de las proteínas purificadas de la solución de elución.
Inmunogenicidad
Para evaluar la respuesta inmune a través de la respuesta por citoquinas se utilizó un método in vitro, en el cual se cuantifica el ARN mensajero producido por los leucocitos de sangre periférica de alpaca frente al estímulo antigénico de la proteína vacunal, el cual consta de los siguientes pasos:
Obtención de leucocitos circulantes
Para obtener células mononucleares sanguíneas periféricas (PBMC) se obtuvo sangre venosa de alpaca en un tubo de ensayo de 15 ml conteniendo EDTA como anticoagulante. Se utilizó una solución salina (PBS 1X con pH 7.4) que se mezcló con un mismo volumen de sangre (proporción 1:1).
Se utilizó el método de centrifugación en gradiente de densidad. Para ello, 03 volúmenes del reactivo Ficoll®-Paque (Sigma, USA) fue mezclado con 04 volúmenes de sangre con PBS. Se realizaron 2-3 lavados de las células con PBS 1X pH 7.4. Finalmente se suspendieron en medio de cultivo RPMI 1640 con L-Glutamina (Sigma, USA).
Para determinar la concentración celular se uniformizó cada cultivo a una concentración de células por ml (cel/ml). Se tomaron 5 µl del paquete celular y se mezclaron con 5 µl azul de tripán diluido al décimo con PBS (1:10). La concentración y evaluación de la viabilidad celular de determinó en una cámara de Neubauer (400X). Las células se diluyeron en RPMI 1640 con L-glutamina, adicionando 100 IU/ml de penicilina (Sigma, USA) y 10% de Suero Fetal Bovino (SFB) (Sigma, USA) inactivado por calor. Los homogenizados se colocaron en una placa de poliestireno para cultivo celular de 24 pocillos unos 1200 µl de cultivo celular con una concentración final de células 1x106 células/ml.
Evaluación de la respuesta inmune
La respuesta de los leucocitos frente al estímulo del antígeno vacunal recombinante rF17 se evaluó con el siguiente esquema experimental:
Pocillo 1: Control celular (leucocitos circulantes).
Pocillo 2: Antígeno fimbrial rF17 (10 ng)
Pocillo 3: BL21 (10 ng) sin antígeno fimbrial (sin plásmido)
Pocillo 4: BL21 (10 ng) + antígeno fimbrial rF17 (plásmido) (20 ng)
Las placas fueron incubadas a 37 °C. La evaluación de la expresión de ARN mensajero de las citoquinas de la respuesta inmune celular y humoral se realizó a las 48 y 72 horas, mediante un RT-PCR y la cuantificación relativa delta delta Ct (ΔΔCt). Para la evaluación de citoquinas de la respuesta inmune Th1 y Th2 de alpacas (Odbileg et al., 2005) se utilizaron los cebadores respectivos (Cuadro 1).
El RT-PCR fue realizado en un termociclador PikoReal 96 (Thermo Scientific), usando como fluoróforo Maxima SYBR Green. Se utilizó el ADNc (4 ng, aproximadamente) sintetizado a partir del ARNm obtenido durante la extracción de los cultivos celulares incubados en diferentes tiempos. Para la prueba de PCR en tiempo real se utilizaron un Maxima SYBR Green/ ROX qPCR Master Mix (2X) a concentración 1X. En la qPCR se llevó a 50 °C durante 2 min (TDG), luego una temperatura de desnaturalización (TD) inicial de 95 °C durante 10 min, luego 40 ciclos de desnaturalización (TD) a 95 °C durante 35 s, hibridación (TA) a la temperatura que corresponde a cada cebador durante 30 s y una extensión (TE) de 72 °C durante 35 s (40 en caso de GAPDH). Finalmente, una evaluación de la temperatura de disociación (TMELT), que va desde «X» 95 °C, donde «X» corresponde a la TA de cada gen evaluado.
RESULTADOS
Expresión y Purificación Proteica
La caracterización de la proteína recombinante rF17 mediante la determinación de la naturaleza y ubicación de expresión del antígeno vacunal en el vector recombinante pET-28a, con base a la secuencia de nucleótidos de 35 Kda en promedio, determinó a rF17 en la fase detergente, tal como se observa en la Figura 1.
Se observó un producto aproximado de 35 Kda correspondiente a la purificación del antígeno vacunal, rF17, como se observa en la Figura 2. La evaluación de especificidad del purificado mediante la técnica de Western Blot muestra un producto único (Figura 3).
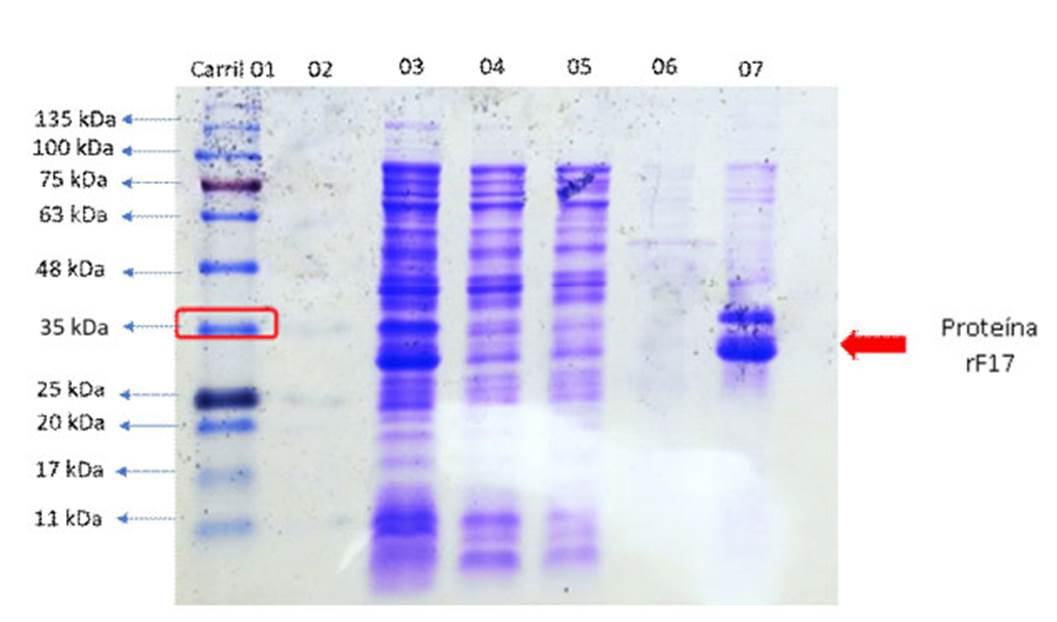
Figura 1 SDS-PAGE de la caracterización de la proteína recombinante rF17 usando el plásmido pET-28a. Carril 01: Marcador de peso molecular; Carril 02: blanco; Carril 03: célula completa; Carril 04: Citosol; Carril 05: Envoltura celular; Carril 06: Fracción acuosa, Carril 07: Fracción detergente. La flecha roja indica la proteína recombinante
Evaluación de la Inmunogenicidad
La cuantificación relativa de la producción de ARNm de las citoquinas Interferón gamma (IFN), Factor de Necrosis Tumoral á, IL-2, IL-4 e IL-10, estimulada por la proteína recombinante purificada rF17 en leucocitos de sangre periférica de alpaca (PBMC) mostraron los siguientes resultados: la mayor expresión de interferón gamma (IFN-γ) por leucocitos de sangre periférica de alpaca a las 48 h posterior a la exposición se evidenció en el grupo Vector (3.87 ± 0.57), el cual mostró niveles significativamente mayores en relación al control (2.13 ± 0.58), mientras que a las 72 h, tanto el Vector (5.00 ± 0.90) como la combinación Vector + rF17 (4.10 ± 0.59) mostraron niveles significativamente mayores que los controles (Figura 4).
La producción de TNF-γ a las 48 y 72 h mostraron niveles relativamente similares comparado con el control frente a la proteína rF17, vector y la combinación, sin hallase diferencias significativas (Figura 5).
La expresión de la interleucina 2 (IL-2) a las 48 horas de la exposición de las proteínas rF17, vector y la combinación mostraron niveles significativamente mayores en relación al control, siendo el vector (6.54 ± 1.44) el de mayor expresión. Sin embargo, a las 72 horas, solo el vector (5.32 ± 1.77) presentó niveles significativamente mayores (Figura 6).
En la expresión de la interleucina 4 (IL-4) a las 48 h de la exposición, solo los grupos Vector (5.62 ± 1.12) y la combinación Vector+ rF17 (4.67 ± 0.42) mostraron niveles significativamente mayores con relación al control, mientras que a las 72 h solo la combinación Vector + rF17 (5.12 ± 0.93) expresaron niveles significativamente mayores (Figura 7).
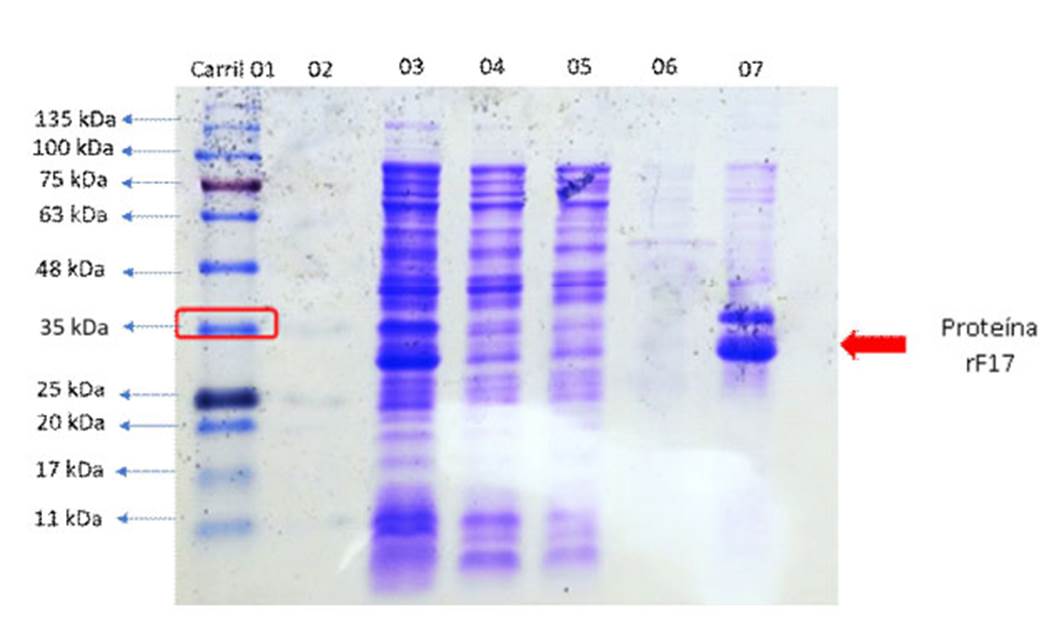
Figura 2 SDS-PAGE de la purificación de la proteína recombinante rF17. Carril 01: Marcador de peso molecular; Carril 02: blanco; Carril 03: Filtrado; Carril 04: Lavado A; Carril 05: Lavado B; Carril 06: Elusión 01, Carril 07: Elusión 02

Figura 3 Western Blot usando un marcador de residuos de histidina. Carril 01: Marcador de peso molecular; Carril 02: blanco; Carril 03: Elusión 1; Carril 04: Elusión 2; Carril 05: Elusión 3; Carril 06: Elusión 4; Carril 07: Elusión 5. La flecha roja indica la proteína recombinante
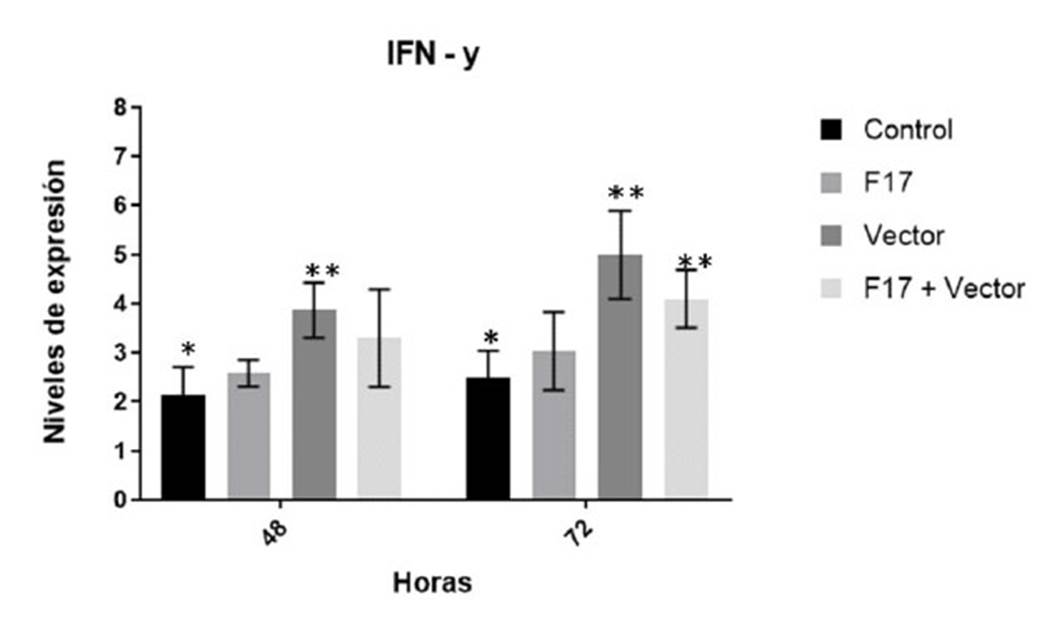
Figura 4 Niveles de expresión relativa de INF-γ producidos por células mononucleares sanguíneas periféricas estimulados por la proteína purificada rF17 y componentes estructurales del vector inactivado. Las barras representan la media ± SEM
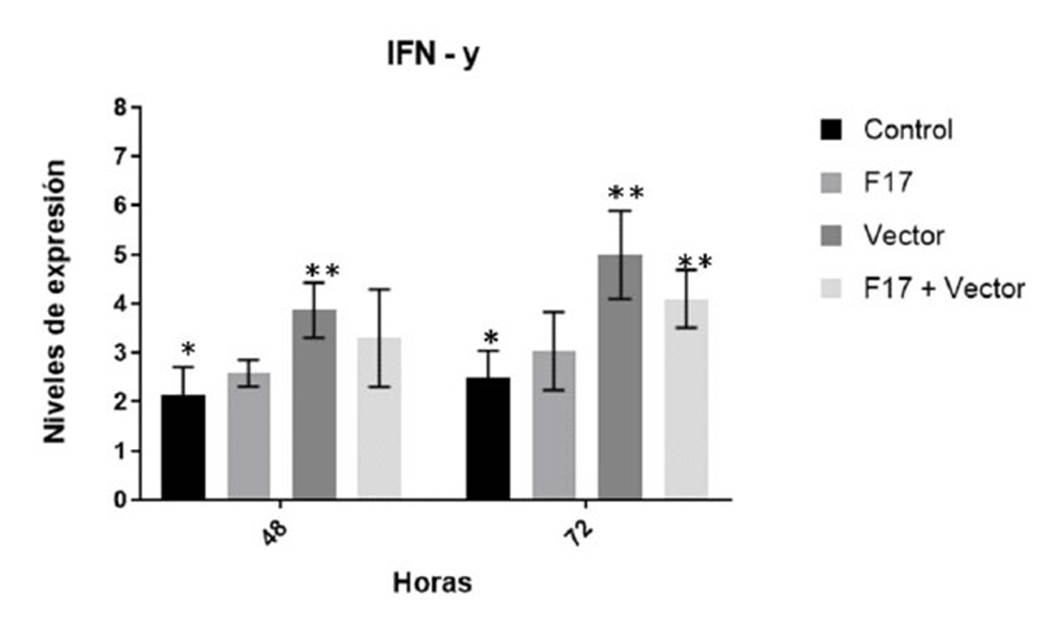
Figura 5.Niveles de expresión relativa de TNF-α producidos por células mononucleares sanguíneas periféricas estimulados por la proteína purificada rF17 y componentes estructurales del vector inactivado. Las barras representan la media ± SEM

Figura 6 Niveles de expresión relativa de IL-2 producidos por células mononucleares sanguíneas periféricas estimulados por la proteína purificada F17 y componentes estructurales del vector inactivado. Las barras representan la media ± SEM
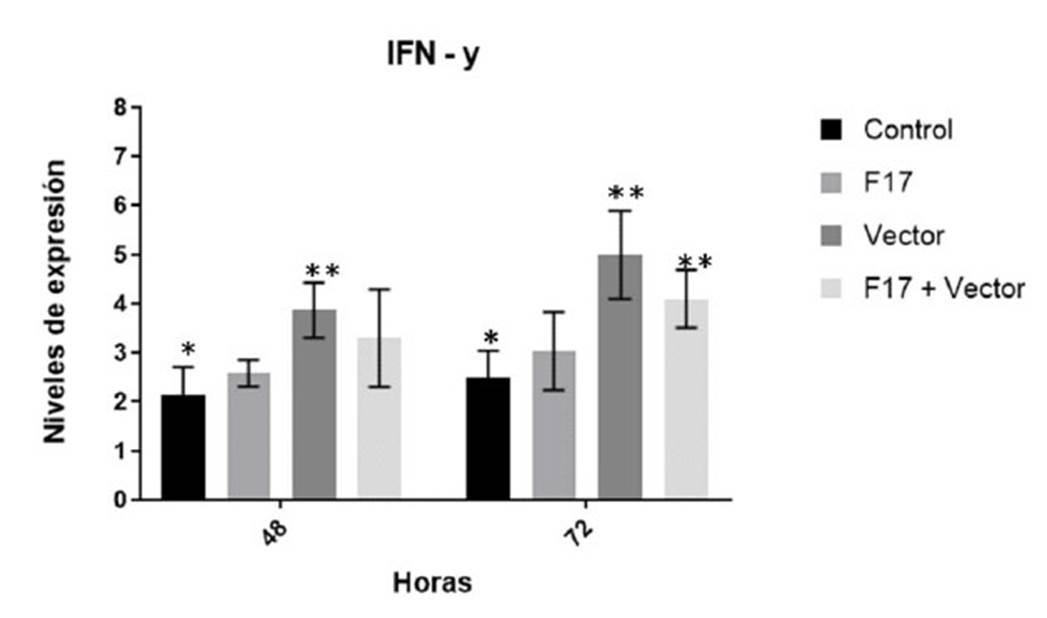
Figura 7 Niveles de expresión relativa de IL-4 producidos por células mononucleares sanguíneas periféricas estimulados por la proteína purificada rF17 y componentes estructurales del vector inactivado. Las barras representan la media ± SEM
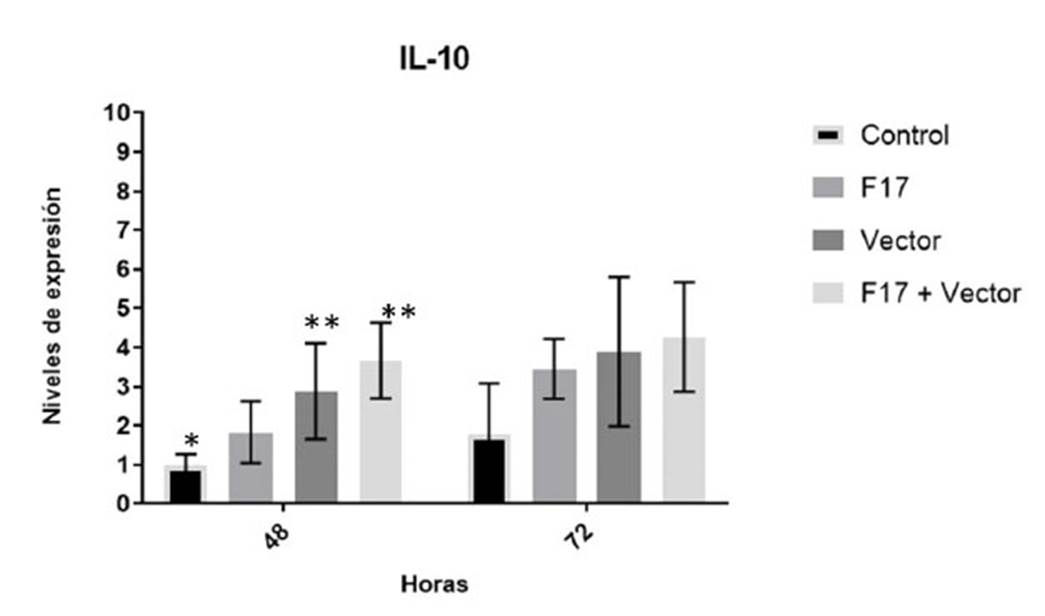
Figura 8 Niveles de expresión relativa de IL-10 producidos por células mononucleares sanguíneas periféricas estimulados por la proteína purificada rF17 y componentes estructurales del vector inactivado. Las barras representan la media ± SEM
La expresión de la interleucina 10 (IL-10) evidenció a las 48 h de la exposición que solo los grupos Vector (2.88 ± 1.23) y la combinación Vector + rF17 (3.67 ± 0.97) alcanzaron niveles significativamente mayores con relación al grupo control, mientras que a las 72 h no hubo diferencias significativas entre grupos (Figura 8).
DISCUSIÓN
Se llevó a cabo la expresión de la proteína recombinante F17 (rF17) utilizando el vector BL21, el cual es uno de los más usados para la síntesis de proteínas recombinantes (Rosano y Ceccarelli, 2014). La producción de la proteína fimbrial rF17 se obtuvo utilizando el vector pET-28a, obteniéndose un producto de 35 Kda en promedio (Figura 1). Utilizando las colas de histidina se pudo purificar la proteína (Figura 2), y para corroborar la purificación se realizó un Western Blot obteniéndose bandas únicas de 35 Kda en todas las eluciones (Figura 3), como resultado de procedimientos estandarizados que han sido utilizados para la expresión y purificación de otras proteínas fimbriales de E. coli, como son las fimbrias de ETEC, CFA/I y CS4 (Curtis et al., 2016), F9 de EHEC del serotipo O157:H7 (Mohawk et al., 2010), e inclusive hasta la expresión de varias adhesinas fusionadas, dímeros y trímeros en E. coli uropatogénica (UPEC) (Luna-Pineda et al., 2016).
La evaluación de citoquinas y su producción frente a estímulos es una de las herramientas para la evaluación del sistema inmune, siendo una de las alternativas la medición directa en suero. Sin embargo, el suero posee gran cantidad de inhibidores (proteínas dianas o receptores antagonistas y anticuerpos) (Heney y Whicher, 1995). Así, la evaluación en células mononucleares de sangre periférica (PBMC), es un método que ofrece ventajas para la evaluación de la inmunocompetencia o el estado de respuesta específica (Friberg et al., 1994; Whiteside, 1994). Este método ha sido utilizado en la evaluación de la respuesta inmune en camellos y alpacas, tanto para la evaluación de la respuesta inmune frente a inmunógenos bacterianos o proteínas simples como para la evaluación de vacunas (More et al., 2013; Tambillo et al., 2014; Watanabe et al., 2014; Sulabh et al., 2019). En bovinos, utilizando la misma metodología se ha evaluado la capacidad de resistencia y/o susceptibilidad a enfermedades de algunas razas (Sulabh et al., 2019).
En el presente estudio, la expresión de IFN-ã a las 48 h de la exposición el grupo Vector (3.87 ± 0.57) fue el único que presentó niveles significativamente mayores con relación al grupo control (2.13 ± 0.58); respuesta que podría estar relacionada al lipopolisacárido (LPS) que recubre la pared externa del vector (E. coli), el cual ha mostrado ser un componente que estimula la respuesta de esta citoquina (Tizard, 2013; Kleiveland, 2015). Si bien, la proteína recombinante rF17, por sí sola, no mostró tener la capacidad suficiente para estimular la producción de IFN-γ, al menos, hasta las 72 h, tanto el Vector como la combinación Vector + rF17, mostraron niveles mayores que los controles. Estas respuestas podrían explicarse a la naturaleza de respuesta de los linfocitos, los cuales producen una mejor respuesta frente a moléculas complejas (la combinación proteína purificada con el LPS del vector). Similares respuestas de incremento de la expresión de IFN-γ in vitro en alpacas se ha reportado usando proteínas purificadas P6 like de Pasteurella y antígenos clostridiales (More et al., 2013: Maximiliano et al., 2018).
La producción de TNF-α a las 48 y 72 h presentaron niveles relativamente similares al control frente a la proteína rF17, vector y su combinación; y aumentando a las 72 h por encima del control, aunque sin llegar a mostrar diferencias significativas. Si bien, TNF-α es una citoquina proinflamatoria, es una citoquina producida principalmente por células de la inmunidad innata, como son los polimorfonucleares (Tizard, 2013). Sin embargo, se debe considerar que en células de PBMC, utilizadas en este tipo de evaluaciones, se han separado a los granulocitos, siendo la respuesta obtenida por Linfocitos T y B, que son células que expresan otro perfil de citoquinas (Tizard, 2013; Kleiveland, 2015). Además, su expresión puede ser inhibida por la IL-10 (Schandené et al., 1994), citoquina que fue expresada en niveles significativamente mayores en el presente estudio. Patrones similares fueron observados utilizando la proteína P6 like (Maximiliano et al., 2018) y frente a antígenos clostridiales (Tambillo et al., 2014).
La expresión de la interleucina 2 (IL-2) a las 48 h de la exposición de las proteínas rF17, vector y su combinación mostraron niveles significativamente mayores con relación al control, siendo el vector (6.54 ± 1.44) el de mayor expresión por encima de rF17 (3.42 ± 0.96) y la combinación Vector +rF17 (3.71 ± 0.94). Sin embargo, a las 72 h, solo el vector (5.32 ± 1.77) presentó niveles significativamente mayores. Esta respuesta podría ser explicada debido a que IL-2 es el principal activador de Linfocitos T, los cuales expresan el receptor de IL-2. El PBMC está compuesto hasta por 85% por linfocitos, lo que generaría los niveles observados (Malek, 2003; Tizard, 2013; Kleiveland, 2015). Los niveles obtenidos son comparables a los expresados utilizando antígenos clostridiales y de pasteurelas frente a la evaluación de la expresión in vitro (More et al., 2013; Watanabe et al., 2014; Maximiliano et al., 2018).
Con relación a la respuesta Th2, la expresión de la interleucina 4 (IL-4) a las 48 h de la exposición, solo los grupos Vector (5.62 ± 1.12) y la combinación Vector + rF17 (4.67 ± 0.42), mostraron niveles significativamente mayores con relación al control (2.82 ± 0.54), mientras que a las 72 h solo la combinación Vector + rF17 (5.12 ± 0.93) expresó niveles significativamente mayores. Estos niveles fueron similares a los obtenidos por Maximiliano et al. (2018), quienes entre las 24 y 48 h obtienen niveles de hasta ocho veces la expresión. No obstante, la proteína rF17 no mostró niveles significativamente mayores, resultado similar al obtenido con el estímulo de antígenos clostridiales (More et al., 2013). IL-4 tiene como función la polarización de linfocitos T vírgenes hacia Th2, lo cual estimula su expansión y activación, siendo producida por Linfocitos T, principalmente (Tizard, 2013). Liu et al. (2009), utilizando un sistema in vivo, obtuvieron niveles de IL-4 predominantes sobre IFN-γ, expresados en bazo y placas de Peyer al inmunizar ratones BALB/c, utilizando Lactobacillus casei expresando F41 de E. coli enterotoxigénica (ETEC).
La expresión de la interleucina 10 (IL10), en PBMC de alpaca, a las 48 h de la exposición evidenció que los grupos Vector (2.88 ± 1.23) y la combinación Vector + rF17 (3.67 ± 0.97) mostraron niveles significativamente mayores con relación al control (0.98 ± 0.28), mientras que a las 72 h no hubo expresiones significativas. Esta expresión podría explicarse debido a que esta citoquina tiene como función principal la inmunoregulación, y permite la inhibición demacrófagos y células asesinas naturales o NK, disminuyendo la respuesta Th1, actuando frente a niveles altos de IFN-γ (Schandené et al., 1994; Tizard, 2013). Se ha demostrado tendencias similares utilizando antígenos clostridiales (More et al., 2013; Tambillo et al, 2014), así como con P6-like de Pasteurella (Maximiliano et al., 2018).












 uBio
uBio 

