INTRODUCCIÓN
La industria avícola en Colombia ha tenido un gran auge en los últimos años gracias a la innovación tecnológica en manejo y mejoramiento genético de las aves, aumentando la contención de patógenos mediante el uso de antibióticos como una alternativa para la prevención y tratamiento de infecciones y mediante el uso de promotores de crecimiento en las dietas (Stockwell y Duffy, 2012), logrando mayores índices de productividad (Bueno et al., 2016). Sin embargo, diversos estudios en aves han identificado la circulación de bacterias resistentes a diferentes clases de antibióticos (Mellata et al., 2018), incluyendo a bacterias con posible potencial zoonótico (Mitchell et al., 2015; Stromberg et al., 2017). Asimismo, se han encontrado determinantes genéticos implicados en la resistencia a los antimicrobianos en Escherichia coli patogénica aviar (APEC) aislados de granjas de pollos de engorde (Awad et al., 2016; Staji et al., 2018; Subedi, 2018).
Se conocen diferentes mecanismos de resistencia que pueden ser adoptados por E. coli, tales como modificación del sitio blanco, cambios de permeabilidad (Fábrega et al., 2008), producción de enzimas modificadoras de aminoglucósidos e incremento en la expresión de las bombas de expulsión (Tafur et al., 2008). Las β-lactamasas de espectro extendido (ESBLs) son un grupo de enzimas transportadas en plásmidos que hidrolizan penicilinas, cefalosporinas y monobactámicos. Entre ellas están las β-lactamasas sulfhidrilo variable (SHV), temoneira (TEM), cefotaximasa (CTX-M) (Sadat et al., 2016) y β-lactamasas AmpC plasmídicas (pAmpC) (Huijbers et al., 2015; Madec et al., 2017). Las enzimas que confieren resistencia a fluoroquinolonas son también mediadas por plásmidos e incluyen las proteínas Qnr, la enzima aac(6´)-Ib-cr y la bomba de eflujo QepA (Vetting et al., 2011). Se ha evidenciado asociación de la resistencia a las quinolonas con la producción de β-lactamasas de espectro extendido (ESBL) o de AmpC âlactamasas mediadas por plásmidos (Mendonça et al., 2016; Salgado et al., 2016) y de la incidencia de los integrones como responsables del paso de determinantes de resistencia entre microorganismos Gram negativos (Berglund, 2015).
Por otra parte, E. coli se comporta como un patógeno oportunista en situaciones de estrés y de deficiente manejo (LeStrange, 2017; Perello, 2009), donde los patotipos APEC, responsables de infección primaria en aves de corral, causan grandes pérdidas económicas a la industria avícola (Dziva y Stevens, 2008; Guabiraba y Schouler, 2015). En el humano, E. coli patógena extraintestinal (ExPEC) representa un patógeno emergente, con cepas implicadas en casos de infecciones del tracto urinario (ITU), bacteriemia y meningitis (Manges, 2016). Varios estudios han revelado características superpuestas entre APEC y ExPEC humano (Maluta, 2014; Xiangkai, 2014), lo que lleva a la hipótesis de un potencial zoonótico de las cepas de aves de corral (Cunha et al., 2017). Así mismo, la Organización Mundial de Sanidad Animal (OIE) estima que cerca del 60% de los patógenos humanos y del 75% de las enfermedades de reciente aparición son de curso zoonótico (Labro y Bryskier, 2014).
El uso excesivo e indebido de los agentes antimicrobianos en aves para consumo humano, además de las hipótesis de los linajes o raíces evolutivas comunes entre E. coli aviar y humana (Manges, 2016), contribuyen al desarrollo y la propagación de la resistencia a antibióticos (Hussain et al., 2017), lo que lleva a la aparición de patógenos multirresistentes, los cuales pueden presentar la transmisión cruzada al humano (Moulin-Schouleur et al., 2016), convirtiéndose en un grave e importante problema de salud pública. Esta situación obliga a mejorar las prácticas al margen de las recomendaciones de producción, control de calidad e inocuidad alimentaria (FAO, 2011). El presente estudio tuvo como objetivo determinar la resistencia a antibióticos β-lactámicos y quinolonas y establecer la presencia de genes involucrados en aislamientos de E. coli obtenidos de pollos broiler provenientes de granjas de producción avícola de Santander, Colombia.
MATERIALES Y MÉTODOS
Se realizó un estudio descriptivo de corte transversal, recolectando 400 muestras de varios órganos (tráquea, intestinos, sacos aéreos abdominales y claviculares, pericardio, bolsa de Fabricio y páncreas) en necropsias de 200 pollos de engorde sanos de cinco edades (12, 18, 21, 36 y 42 días). Todos los especímenes provinieron de granjas avícolas del departamento de Santander, Colombia.
Las muestras fueron inoculadas en caldo Infusión Cerebro Corazón (BHI) para posterior siembra en agar MacConkey. Las colonias fermentadoras de lactosa en agar MacConkey se identificaron bioquímicamente (Borie et al., 1997), con el kit BBLTM CrystalTM E/NF y se corroboraron mediante PCR para detectar el gen uidA que codifica la enzima 1glucuronidasa (Molina et al., 2015), la cual es específica para E. coli, utilizando cebadores propuestos por Hessain et al. (2015).
Susceptibilidad a Antibióticos
A los aislados identificados como E. coli se les realizó la prueba de Kirby Bauer (CLSI, 2017) con antibióticos pertenecientes a grupos de las quinolonas y β-lactámicos. Cada cepa se expuso frente a sensidiscos impregnados con los siguientes antibióticos: ampicilina 10 µm, amoxacilina/ácido clavulánico 20/10 µm, piperacilina 100 µm, piperacilina/ tazobactam 100/10 µm, cefalotina 30 µm, cefuroxime 30 µm, cefoxitin 30 µm, cefotaxime 30 µm, ceftazidime 30 µm, ceftriaxona 30 µm, cefepime 30 µm, ácido nalidíxico 30 µm, norfloxacina 10 µm y ciprofloxacino 5 µm. Luego se evaluó la susceptibilidad de las cepas siguiendo las recomendaciones del CLSI (2017) (Cuadro 1).
Cuadro 1 Condiciones de PCR para amplificación de los genes de resistencia en cepas de Escherichia coli fenotipo ESLB
| Gen | Secuencia 53’ | Tamaño (pb | Desnaturalización inicial | Ciclos | Alineamiento | Extensión | Extensión final |
| blaTEM | 5´-AAACGCTGGTGAAA GTA 3´ 5´-AGCGATCTGTCTAT 3´ | 239 | 94 °C, 30 s | 35 | 49 °C, 1 min | 72 °C, 1 min | 72 °C, 10 min |
| blaSHV | 5´ATGCGTTATATTCGCCTG TG 3´ 5´-TGCTTTGTTATTCGGG CCAA 3´ | 241 | 94 °C, 30 s | 35 | 56 °C | 72 °C, 1 min | 72 °C, 10 min |
| blaCTX-M1 | 5´-GACGATGTCACTGGC TGAGC 3´ 5´-AGCCGCCGACGCTA ATACA 3´ | 499 | 94 °C, 30 s | 35 | 58 °C | 72 °C, 1 min | 72 °C, 10 min |
| Amp-C | 5’-ATCAAAACTGGCAG CCG-3’ 5’-GAGCCCGTTTTATGC ACCCA-3’ | 170 | 94 °C, 30 s | 35 | 56.9 °C | 72 °C, 1 min | 72 °C, 10 min |
Fuente: Protocolo de estandarización de Paterson et al. (2003), modificado por Velandia et al. (2016)
Genes de Resistencia blaTEM, blaSHV, blaCTX-M1, Amp-C
Mediante PCR convencional se realizó la amplificación a las cepas de E. coli. Se utilizó la cepa Klebsiella pneumoniae ATCC 700603 control positivo y la cepa E. coli ATCC 25922 como control negativo. La Figura 1 presenta las condiciones del PCR.
La caracterización de los genes qnrA, qnrB y qnrS en cada una de las cepas de E. coli se realizó de acuerdo con el protocolo estandarizado por Aguilar et al. (2015). Los resultados de PCR se visualizaron en gel de agarosa al 1% con tinción de Safeview classic. Se utilizó un transiluminador UltraSlim Led Illuminator (ABM). La presencia de los genes en evaluación se determinó en las cepas resultantes (Figura 1).
Bienestar Animal
Se siguieron todas las pautas internacionales, nacionales e institucionales para el cuidado y uso de los animales. Se tuvieron en cuenta todas las normas de bienestar animal de acuerdo con la Ley 1774 del 6 de enero de 2016, Art. 339B, Párrafo 1 de la Republica de Colombia (2016). El estudio contó, además, con el aval del comité de ética de la Unversidad de Boyacá. El manuscrito no contiene estudios clínicos ni datos de pacientes.
RESULTADOS
Se obtuvieron 176 aislados de E. coli de las 400 muestras colectadas. La resistencia de los aislados a antibióticos betalactámicos fue del 97.7% y a quinolonas del 86.7%. Los antibióticos del grupo de betalactámicos probados y el porcentaje de resistencia para cada uno de ellos fueron: ampicilina 100%, cefuroxime 98.9%, amoxacilina ácido clavulánico 98.9%, cefalotina 97.7%, piperacilina tazobactam 97%, cefoxitina 96.6%, cefotaxime 96.6%, piperacilina: 95.5%, ceftazidime 93.2%, ceftriaxona 92.0%, y cefepime 83.0%. Frente a las quinolonas se obtuvo resistencia para ácido nalidíxico en el 100% de los aislados, a la ciprofloxacina en el 83% y a la norfloxacina en el 77.3% (Figura 2).
Los resultados de la prueba confirmatoria evidencian resultado positivo para el 71.6% de los aislamientos, los cuales expresaron fenotípicamente ESLB (Figura 3).
Los datos de PCR para genes que codifican la resistencia tipo ESLB revelaron que el gen AmpC (74%) fue el más frecuente en los aislados de E. coli, seguido de los genes blaSHV y blaCTXM (65%) y el gen blaTEM (50%). El 34.9% de las cepas amplificaron los cuatro genes, 25.6% tres, 20.9% dos y 4.7% un gen, y el restante 13.9% no mostró amplificación. Por otra parte, los datos de PCR para genes que codifican resistencia a las quinolonas mostró al gen qnrB con el 86.4% y al qnrS con el 11.9% de los aislados de E. coli, mientras que no se evidenció la presencia del gen qnrA (Figura 4).
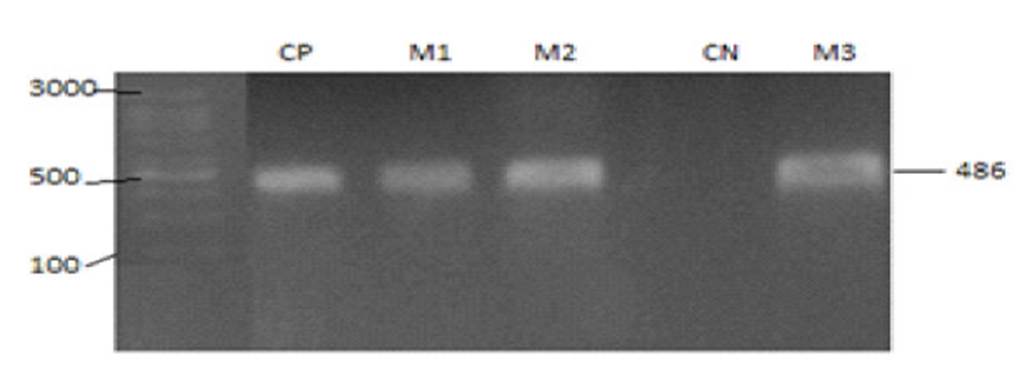
Se obtuvo las amplificaciones de los genes con el protocolo establecido revelando bandas de 700, 700, 500 y 550 pb para los genes blaTEM, blaSHV, blaCTX-M1 y AmpC, respectivamente (Figura 5 y Figura 6).
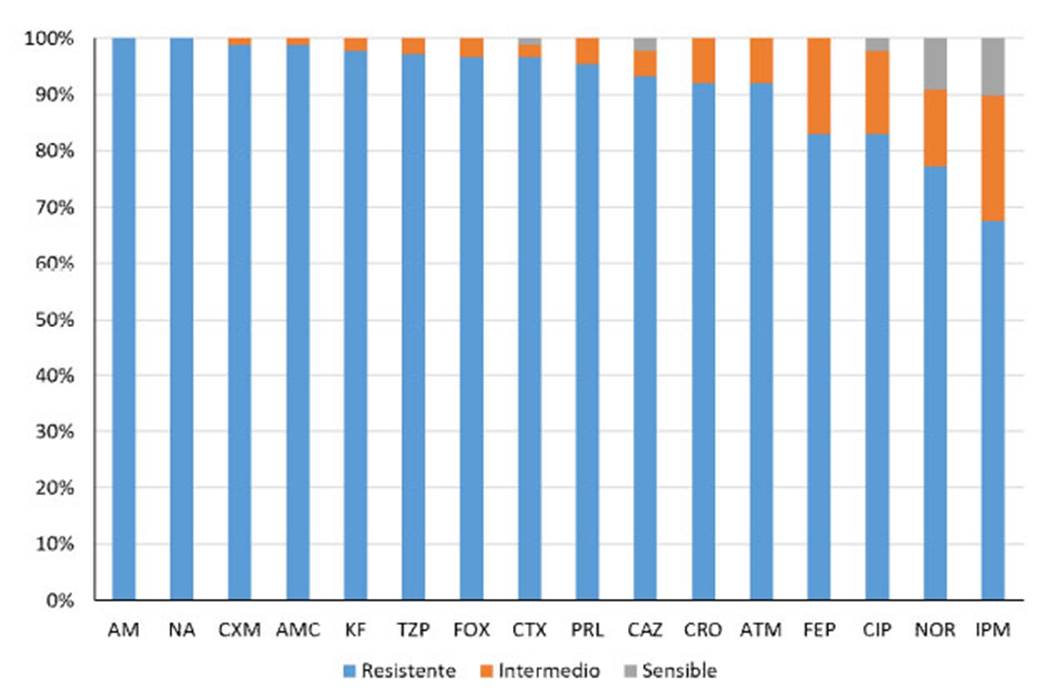
Figura 2 Patrón de resistencia de 176 aislamientos de E. coli a 16 agentes antimicrobianos: AM: ampicilina; NA: ácido nalidíxico; CXM: cefuroxima; AMC: amoxicilina/ácido clavulánico; KF: cefalotina; TZP: piperacilina/tazobactam; FOX: cefoxitina; CTX: cefotaxime; PRL: piperacilina; CAZ: ceftazidima; CRO: ceftriaxona; ATM: aztreonam; FEP: cefepime; CIP: ciprofloxacina, NOR: norfloxacina
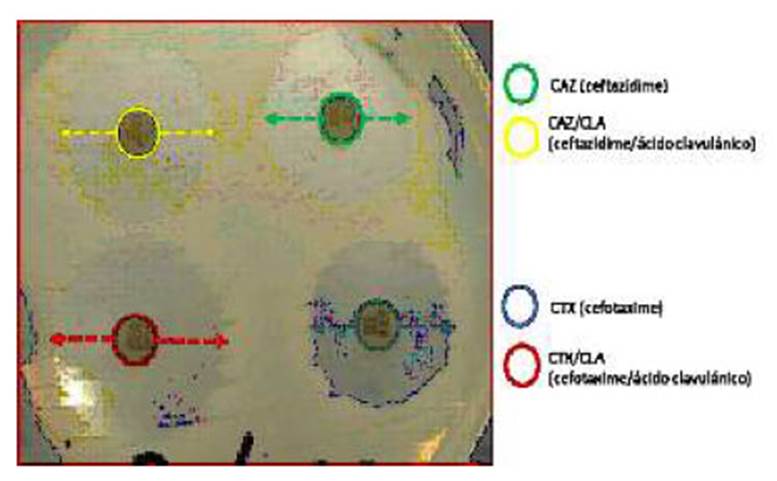
Figura 3 Prueba confirmatoria fenotipo ESLB: método del doble disco. Se observa el aumento del halo en más de 5 mm con los sensidiscos de mezcla de cefalosporina y ácido clavulánico, con relación al disco de cefalosporina sola (CLSI, 2017)
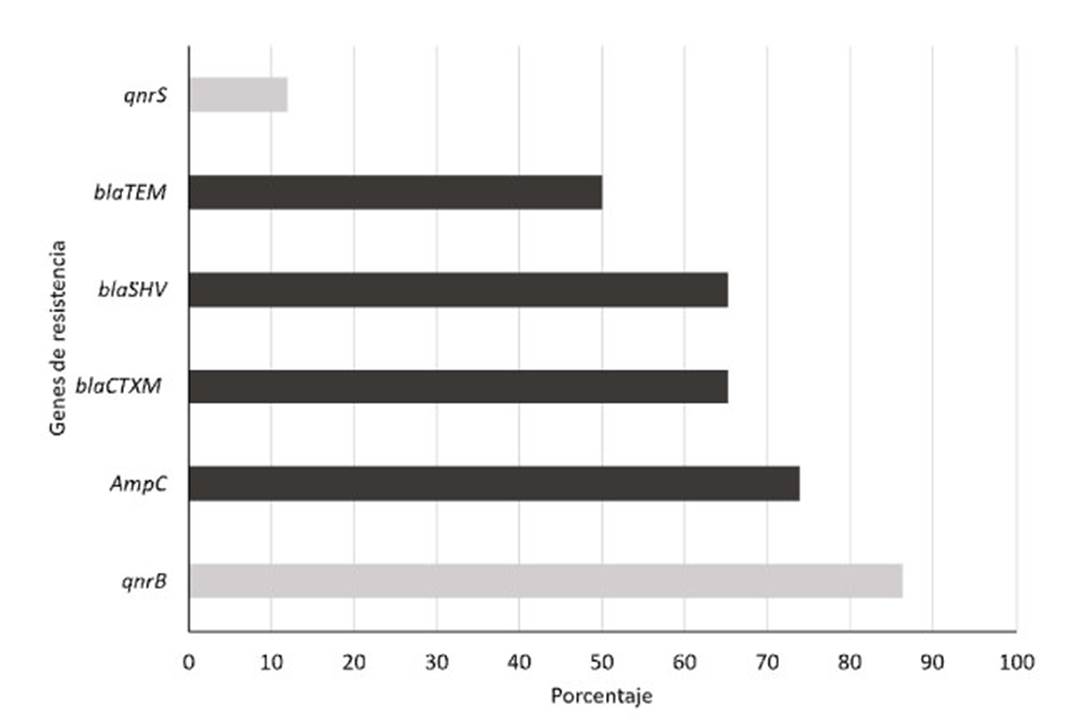
Figura 4 Porcentaje de genes de resistencia de los aislados de E. coli a antibióticos betalactámicos: genes AmpC; blaSHV; blaCTXM y blaTEM y quinolonas: genes qnrS y qnrB
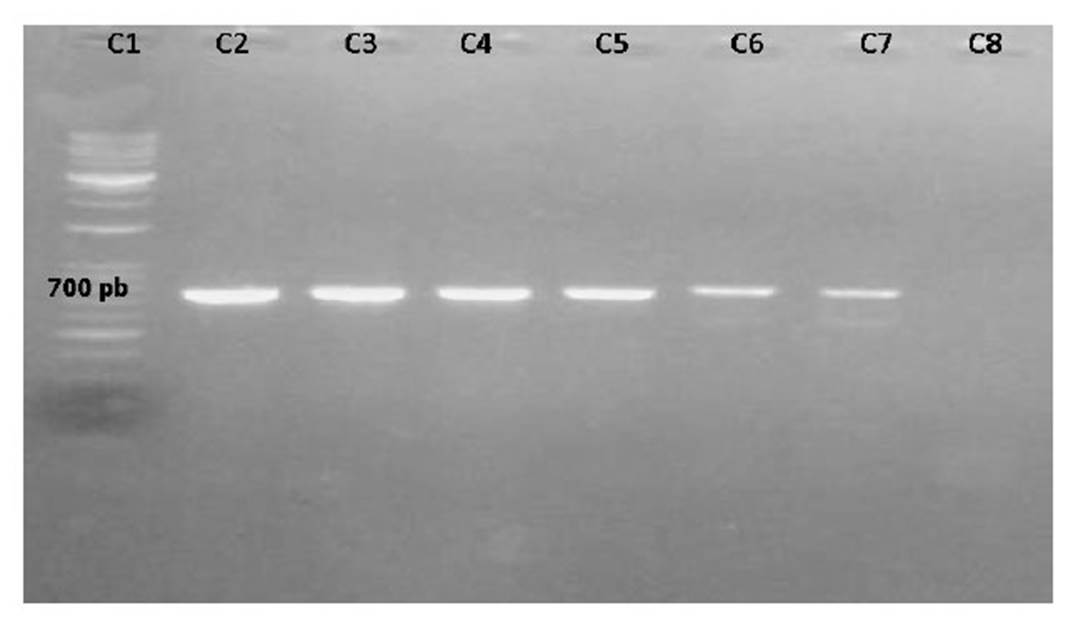
Figura 5 Gel de electroforesis del gen blaSHV: C1: 1.5 Kb; C2: Control positivo; C3: Mx1; C4: Mx2; C5: Mx3; C6: Mx4; C7: Mx5; C8: control negativo
DISCUSIÓN
El estudio evidenció la multirresistencia de las cepas de E. coli a los antibióticos evaluados por el método de difusión en disco. Todas las cepas presentaron resistencia a la ampicilina y el 95% a todos los betalactámicos enfrentados, resaltando la producción de ESBL en el 71% de las cepas. En este sentido, diversos estudios muestran la presencia de bacterias portadoras de genes que codifican resistencia a antibióticos betalactámicos (Cuadro 2).
Se observó una elevada prevalencia del gen AmpC, que codifica para la resistencia a las cefamicinas (cefoxitina y cefotetan), oximinocefalosporinas (ceftazidima, cefotaxime y ceftriaxona), monobactámicos (aztreonam) y aminopenicilinas combinadas con inhibidores de betalactamasas (amoxicilina-ácido clavulánico, ampicilina-sulbactam). Este gen se ha caracterizado por estar presente en especies y géneros bacterianos como Enterobacter, Providencia, Morganella morganii, Serratia marcescens y Citrobacter freundii; sin embargo, en E. coli puede identificarse aunque con una expresión baja (Lopez et al. , 2016). Muzo (2017) comprobó el fenotipo de cepas ESLB (80%) y AmpC (20%), lo cual evidencia la amplia difusión de bacterias resistentes a antibióticos betalactámicos en pollos broiler de Galápagos destinados para el consumo humano. Los hallazgos de Castellanos (2017) en aves de corral en Colombia indican una 100% de prevalencia del gen bla TEM, así como resistencia causada por genes como bla CMY-2 y bla SHV-12. La diseminación de estas cepas resistentes está dada por plásmidos IncI1/ST12 homogéneos, los que sugiere que la propagación de la resistencia está mediada principalmente por la transferencia horizontal de genes (Castellanos et al., 2017).
Cuadro 2 Estudios de genes de resistencia a antibióticos betalactámicos
| Aislamientos E. coli ESLB | CTX-M (%) | SHV (%) | TEM (%) | AmpC (%) | Referencia |
| 196 | 59.1 | Abreu et al. (2014) | |||
| 134 | 8.9 CTX-M-1 17.2 CTX-M-2 7.5 CTXM-9 | 67.7 | 77.6 | 11.2 | Ghodousiet al. (2015) |
| 78 | 47.0 | 27.0 | 12.0 | Reich et al. (2013) | |
| 176 | 65.2 | 50.0 | 73.9 | Este estudio |
En la resistencia de 100% encontrada para las cepas al NA y 83% a la CIP, el gen qnrB amplificó en el 86.4% de las cepas aisladas y el qnrS en el 11.9%, sin evidenciarse el gen qnrA. Todas las cepas con resistencia presentaban 1 o 2 genes, similares a los resultados de Cota-Rubio (2014) con E. coli aislada de pollos enfermos, quienes obtuvieron un porcentaje similar de resistencia al NA y de 79% a CIP. De igual forma, el 9% de los aislamientos portadores del gen qnr presentaron sensibilidad intermedia a la ciprofloxacina y a la norfloxacina en las pruebas de difusión en disco.
Aguilar et al. (2015) encontraron en aislados de E. coli provenientes de canales de bovinos, resistencia al ácido nalidíxico (64%), seguida de ampicilina (32%), ciprofloxacino (10%), ceftazidima y cefotaxima (ambos con 1.3%), porcentajes de resistencia menores a los obtenidos en este trabajo. La alta circulación de bacterias resistentes en la producción avícola se manifiesta; así Bezerra et al. (2016) reporta resistencia a más de tres grupos de antibióticos, Hernández et al. (2017) encontraron 93.3% de multirresistencia y Mainali et al. (2013) identificaron 79.2% de resistencia a uno o más de los antibióticos evaluados, donde el 54.3% fueron resistentes a tres o más antimicrobianos y el 10.8% a cinco o más antimicrobianos.
CONCLUSIONES
Los aislados de E. coli de muestras de órganos de pollos broiler de granjas avícolas de Santander, Colombia, portan genes de resistencia a antibióticos betalactámicos como Amp-C (74%), blaCTX-M (65%), blaSHV (65%) y blaTEM (50%), y a quinolonas qnrB (86.4%) y qnrS (11.9%), pero sin evidenciar el gen qnrA












 uBio
uBio