INTRODUCCIÓN
Los agentes fúngicos como hongos filamentosos y algunas levaduras han sido considerados como una causa poco probable de infección dermatológica en especies animales; sin embargo, a lo largo del tiempo se han identificado muchos de estos como agentes etiológicos de patologías como la dermatitis, los cuales pueden transmitirse de manera zoonótica afectando al ser humano (Prats, 2012; Galvis y Borda, 2016).
La dermatitis se define como una enfermedad inflamatoria de la piel, originada generalmente por procesos alérgicos, intoxicaciones y por agentes infecciosos que ocasionan una respuesta inflamatoria en la epidermis, evidenciada por prurito, edema, irritación, alopecia e incluso hipo o hiperpigmentación de la zona afectada (Ashbee, 2007; Hossain et al., 2007; Torres et al., 2008). La dermatofitosis es una de las dermatitis causadas por agentes fúngicos, producida por hongos de los géneros Trichophyton, Microsporum y Epidermophyton, más conocidos como dermatofitos, siendo los dos primeros patógenos tanto para animales como humanos (Silva et al., 2003; Frymus et al., 2013; Murmu et al., 2015; Murray et al., 2015). Adicionalmente, se reportan las dermatomicosis y otomicosis causadas por levaduras del género Malassezia, que, aunque son parte de la microbiota normal de los mamíferos, puede dejar de ser un microorganismo comensal y convertirse en patógeno para el hospedero al presentarse factores predisponentes, como cambios en el microambiente de la piel o en la concentración lipídica (Hernández, 2005; Copetti et al., 2006).
Las dermatofitosis y las dermatomicosis representan las micosis superficiales de mayor importancia en la salud de los animales de compañía y de granja. Se han reportado dermatofitos como M. canis y levaduras como Malassezia spp, especialmente M. pachydermatis como los principales agentes etiológicos asociados con enfermedades dermatológicas en animales domésticos (Crespo et al., 2002; Copetti et al., 2006; Prado et al, 2008; Rodrígues y Kozusny, 2008). Estas patologías afectan el bienestar animal en todas las especies y generan pérdidas económicas en los sistemas de producción y los animales de granja; además, de representar un riesgo potencial para la salud pública, dada las características zoonóticas de estos microorganismos (Bond, 2010; Moretti et al., 2013).
En Bogotá, Colombia, se ha determinado que cerca del 20% de las consultas veterinarias en caninos son debidas a procesos dermatológicos y óticos (Pulido-Villamarín et al., 2010). Las características clínicas de las lesiones en la piel de los caninos se pueden asociar con dermatofitos (86.9%) y los procesos óticos con Malassezia spp (86.5%) (Pulido-Villamarín et al., 2011). Por tal motivo, el objetivo de este estudio fue determinar la presencia de patógenos fúngicos en lesiones dermatológicas de grandes y pequeñas especies animales, en instituciones de cuidado y atención veterinaria de Bogotá.
MATERIALES Y MÉTODOS
Se evaluaron 30 caninos, 15 felinos y 2 equinos, cuyos propietarios consultaron por problemas dermatológicos u óticos en tres clínicas veterinarias para pequeños animales y en una clínica para grandes animales de la ciudad de Bogotá, o que se encontraban en el Instituto Distrital de Protección y Bienestar Animal (IDPYBA). Según criterio médico, por compatibilidad clínica de las lesiones dermatológicas con sospecha de presencia de agentes fúngicos, se obtuvieron muestras de las lesiones dérmicas.
El muestreo se realizó mediante raspado de piel profundo, colectando escamas y costras de la zona alopécica. Adicionalmente, se obtuvo pelo completo con raíz y se realizaron hisopados en las lesiones exudativas e inflamatorias (Corell, 2006.). En forma similar, se obtuvieron muestras de hisopado ótico. Las muestras de raspado de piel se colectaron en recipientes plásticos estériles y los hisopos fueron introducidos en tubos estériles con Tween 20 al 0.05% (Pulido-Villamarín et al., 2010). Las muestras fueron transportadas al laboratorio de la Pontificia Universidad Javeriana.
Se realizó análisis directo con hidróxido de potasio KOH (Tricograma) a partir de muestras de raspados de piel para determinar la presencia de estructuras fúngicas (lesión endotrix y ectotrix) y presencia de ectoparásitos (Curtis, 2001; Pulido-Villamarín et al., 2016). A partir de los hisopados se realizó tinción de Gram para determinar la presencia de levaduras, bacterias y otras estructuras, reportando los resultados mediante la escala semicuantitativa por cruces (Pulido-Villamarín et al., 2010). A todas las muestras obtenidas se les hicieron cultivos y aislamientos primarios en agar Dixon, incubando durante 5 días a 32 °C para la obtención de levaduras lípido-dependientes y agar Sabouraud con cloranfenicol (Sab+Clo) para determinar la presencia de dermatofitos u otras levaduras, incubando durante máximo 30 días a 25 °C. Una vez obtenidos los aislamientos, se les realizó caracterización macroscópica, microscópica y bioquímica.
En la evaluación de las características macroscópicas de los dermatofitos se tuvo en cuenta el color anverso y reverso de la colonia del hongo, textura, aspecto y presencia de pigmentos difusibles al medio. En las levaduras se consideraron la forma, tamaño, borde, elevación, textura y color de las colonias. La caracterización microscópica se realizó mediante la tinción de Gram y tinción de azul de lactofenol con el fin de evaluar la presencia de estructuras levaduriformes, blastoconidias y/o estructuras fúngicas como hifas y macro-microconidios, respectivamente. Los aislamientos de morfologías compatibles con hongos (n=27) ingresaron al proceso de identificación de especie, utilizando las claves taxonómicas de Barnett y Hunter, 1998 y Guy y Summerbell, 1996.
Para la identificación preliminar de levaduras se realizó la prueba de la ureasa, con la que se determinó si el aislamiento pertenecía al phyllum Basidiomycota o Ascomycota (Batra et al., 2005; Guého-Kellermann et al., 2010). La definición de especie para los aislamientos de Malassezia se realizó a partir de pruebas bioquímicas como catalasa, betaglucosidasa, asimilación de tween, cremophor y crecimiento en Sabouraud; para los aislamientos compatibles con Candida spp y otras levaduras se utilizó el medio InTray™ Colorex™ Yeast ®.
RESULTADOS
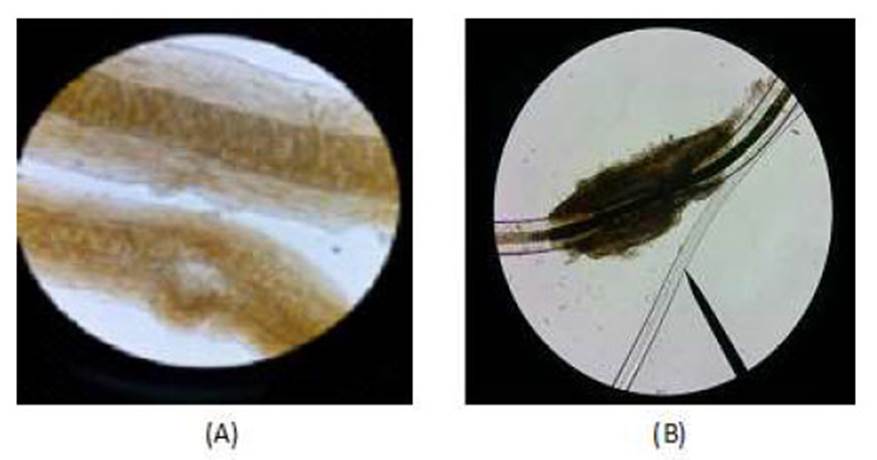
De los 47 pacientes con sintomatología dermatológica, se obtuvieron entre 2 a 3 muestras por animal, siendo 44 hisopados de piel, 31 raspados de piel y 26 hisopados óticos, para un total de 101 muestras analizadas. A partir de los tricogramas en las muestras de raspado de piel se evidenció que 16.1% (5/31) presentaban lesión endotrix, 22.6% (7/31) lesión ectotrix y 29.0% (9/31) los dos tipos de lesión (Figura 1), mientras que las demás muestras no presentaron lesión en el pelo. Adicionalmente, se evidenció la presencia de ectoparásitos como Demodex spp (1 muestra) y Trichodectes canis (3 muestras).
La presencia de levaduras en hisopados de piel fue en el 11.4% (5/44) de las muestras y en óticos del 57.7% (15/26), mayormente con dos a tres cruces. Además, se detectó la presencia de bacterias (predominio de cocos Gram positivos) en hisopados óticos (50.0%; 13/26) y células epiteliales en hisopados de piel (4.5%; 2/44) y ótico (38.5%; 10/26).
Se obtuvieron 27 aislamientos compatibles con hongos entre filamentosos y levaduriformes. Los hongos filamentosos compatibles con Microsporum canis, presentaron colonias blancas a amarillas y al reverso presentaron color de amarillo a naranja, aspecto radiado y sin pigmento difusible, con macroconidios septados, gruesos, con pared rugosa, ligeramente curvos. Por otro lado, Fusarium spp también es un hongo hialino con macroconidios largos en forma de canoa con presencia de microconidios. El 25.9% (7/de los aislamientos se identificó como M. canis y el 3.7% (1/27) como Fusarium spp.
Adicionalmente, se logró identificar 13 aislamientos compatibles con Malassezia spp, con colonias circulares, color beige, borde entero o rizoide, textura cremosa seca y elevadas. La tinción de Gram evidenció levaduras gemantes, que fueron confirmadas mediante la prueba de ureasa positiva, además del panel bioquímico donde se evaluaron los requerimientos para su desarrollo y crecimiento. Se encontró que el 37.0% (10/27) correspondió a Malassezia pachydermatis, ya que poseen la capacidad de asimilar todos los tweenes y de crecer en agar Sabouraud con cloranfenicol (Sab+Clo) a 32 °C, en tanto que 11.1% (3/27) de los aislamientos no presentaron un perfil bioquímico concluyente y fueron designadas como Malassezia spp. De otra parte, seis aislamientos, con morfología macroscópica (colonias con forma circular, color blanco, borde entero, textura cremosa brillante y elevadas) y microscópica compatibles con levaduras, evidenciaron una reacción negativa para ureasa y fueron consideradas como compatibles con Candida spp. Para la identificación a nivel de especie de estos últimos se utilizó el estuche InTray™ Colorex™ Yeast, determinando que un aislamiento correspondía a C. krusei, cuatro a Candida spp y uno fue Trichosporon spp.
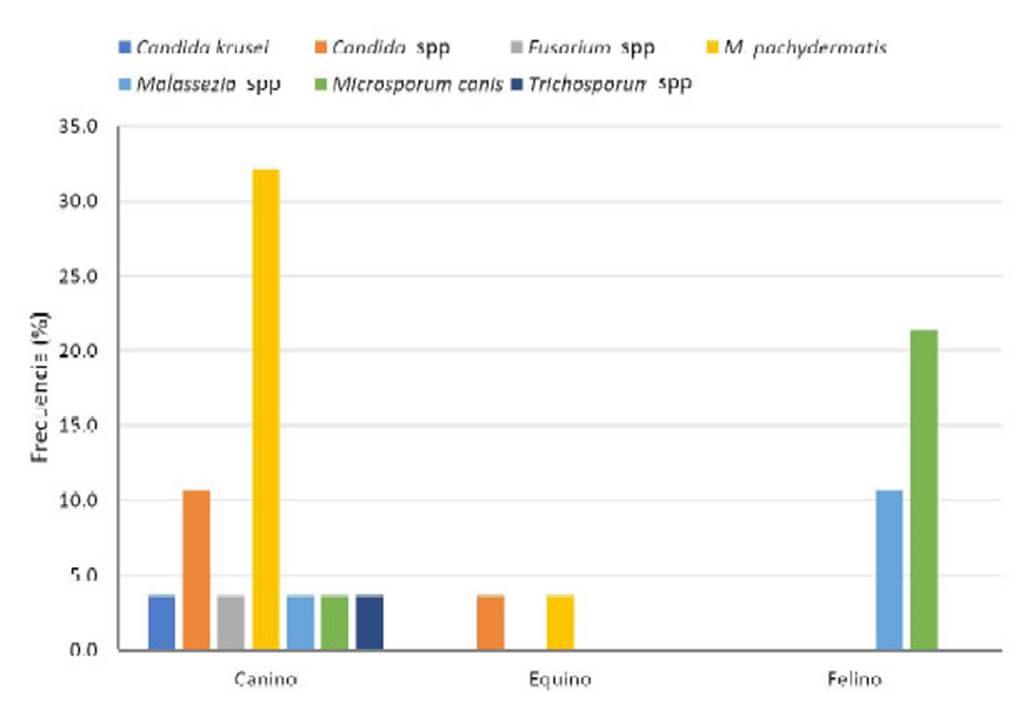
Figura 2 Frecuencia porcentual de agentes fúngicos hallados en lesiones dérmicas de 47 pacientes según especie animal
En el análisis de los aislamientos compatibles con hongos, según la especie animal, partiendo del total de pacientes (n=47) y teniendo en cuenta que se obtuvieron dos tipos de aislamientos a partir de un mismo animal en un canino, un equino y un felino, se determinó la presencia de M. canis con predominio en felinos (21.4%), siendo este el único dermatofito identificado y Malassezia pachydermatis (32.1%), principalmente en caninos. En equinos se identificó en un paciente a dos agentes etiológicos: M. pachydermatis (3.6%) y levaduras del género Candida spp (3.6%). Además, se aislaron otros microorganismos como Trichosporon spp y Fusarium spp en caninos. De otra parte, no se determinó etiología fúngica asociada con el motivo de consulta en el resto de los pacientes (n=22) (Figura 2).
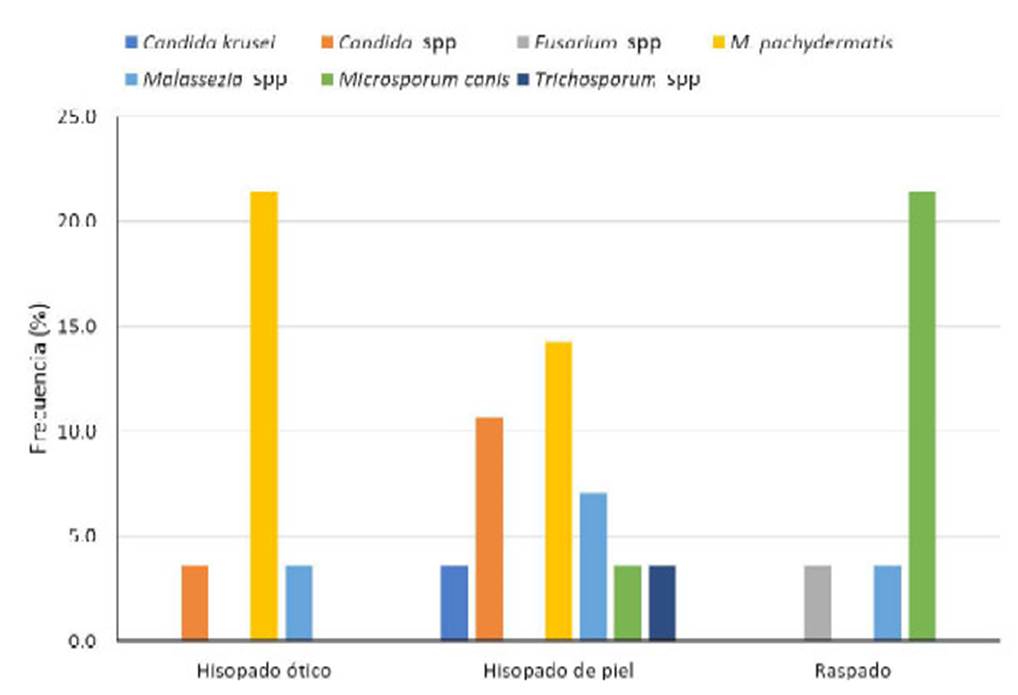
Figura 3 Frecuencia porcentual de hongos hallados en lesiones dérmicas de 47 pacientes según tipo de muestra
En el análisis de los aislamientos de acuerdo con el tipo de muestra se encontró que a partir de 8 hisopados óticos, 12 hisopados de piel y 8 raspados de piel, hubo una mayor frecuencia fúngica en raspado de piel (M. canis [21.4%]) y de hisopado ótico (Malassezia spp [21.4%]) (Figura 3).
Únicamente 23.8% (5/21) de los tricogramas positivos con lesión endotrix y ectorix resultaron positivos al cultivo micótico con morfología compatible con M. canis, mientras las 16 muestras restantes no presentaron crecimiento microbiológico. Por otra parte, en las muestras de hisopado (ótico y de piel) se pudo observar una relación entre la positividad citológica y el crecimiento en cultivo, ya que en 17.1% (12/70) de las citologías positivas para levaduras hubo crecimiento en Agar Dixon, donde se aisló Malassezia spp.
DISCUSIÓN
Los microorganismos generalmente implicados como agentes etiológicos en dermatitis infecciosas son hongos dermatofitos y levaduras del género Malassezia (Prado et al., 2008), como se pudo evidenciar en el presente estudio, donde los agentes fúngicos de mayor frecuencia fueron dermatofitos en felinos y Malassezia spp en caninos. López et al. (2012) afirman que M. canis puede estar presente en la piel de los animales sin causar lesiones, especialmente en felinos; sin embargo, otros autores indican que su presencia está relacionada con procesos dermatológicos en diversas especies animales (Brilhante et al., 2003; Segundo et al., 2004), tal y como se evidenció en este estudio donde se identificó M. canis. Este resultado también concuerda con otros estudios donde se identifica con mayor prevalencia en felinos a M. canis (Cabañes, 2000; Moriello, 2014; Murmu et al., 2015; Guerrero et al., 2016).
Malassezia spp (3.67%) y M. pachydermatys (32.2%) se identificaron con mayor proporción en caninos con respeto a los felinos (Malassezia spp [10.7%]), resultado que concuerda con otras investigaciones (Prado et al., 2008; Kagueyama et al., 2016; Luján-Roca et al., 2016).
En equinos, White (2005) reportó que la presencia de Trichophyton equinum, T. mentagrophytes, T. verrucosum y M. equinum en lesiones dérmicas. Asimismo, se reporta especies del género Malassezia (Crespo et al., 2000, Cabañes et al., 2007, Cafarchia et al., 2013; Aldrovandi et al., 2016); sin embargo, en este estudio solamente se determinó la presencia de levaduras (M. pachydermatis) en hisopados óticos. Este resultado, no obstante, coincide con otros estudios (White, 2005; White et al., 2006; Castañeda-Salazar et al., 2020) quienes reportan varias especies de Malassezia (M. equi, M. slooffiae, M. restricta, M. furfur, M. pachydermatis, M. globosa), aunque M. pachydermatis es usualmente la más frecuente (Shokri, 2016).
Las levaduras del género Candida aisladas a partir de piel de equino e hisopados óticos y piel de caninos están descritas como microbiota comensal en animales (PulidoVillamarín et al., 2017), incluyendo equinos (Castañeda-Salazar et al., 2020). No obstante, también se ha reportado la presencia de este género de levaduras en caninos con dermatitis, principalmente Candida parapsilosis (Yurayart et al., 2011, 2013; Bumroongthai et al., 2016); sin embargo, en Colombia no se ha reportado la presencia de esta especie como agente involucrado en procesos dermatológicos en animales.
Los resultados obtenidos en este estudio, de acuerdo con el tipo de muestra, evidenciaron que en las lesiones dermatológicas se identificó tanto Malassezia spp como M. canis; mientras a nivel ótico el principal microorganismo identificado fue Malassezia spp; resultados que concuerdan con los reportes de Pulido-Villamarín et al. (2011) y por Copetti et al. (2006). Adicionalmente, en el presente estudio se aisló Fusarium spp, considerado como un hongo ambiental, habitante natural del suelo, patógeno para plantas y humanos (Lainhart, 2018). Sin embargo, se ha reportado su potencial infeccioso en lesiones superficiales en animales (Forero-Reyes et al., 2016).
Los agentes etiológicos identificados en este estudio pueden representar un riesgo de transmisión al ser humano por su carácter zoonótico (Pérez, 2005; Bond, 2010), debido a que no solo se transmiten cuando el animal presenta lesiones, sino que también pueden permanecer en estos hospederos sin generar alteración y pueden ser transmitidos a otros animales y humanos susceptibles de adquirir la infección (Silva et al., 2003; Bond, 2010).
CONCLUSIONES
Los principales agentes micóticos asociados con las lesiones dermatológicas en la población estudiada fueron hongos dermatofitos como M. canis y levaduras del género Malassezia.
Los dermatofitos, principalmente M. canis, se aislaron con mayor frecuencia en felinos, mientras las levaduras del género Malassezia spp fueron los agentes predominantes en caninos.
Los hongos dermatofitos se aislaron con mayor frecuencia en muestras de raspado de piel (21.4%), mientras Malassezia spp se aisló principalmente de hisopado ótico (21.4%)












 uBio
uBio