INTRODUCCIÓN
El principal estado productor de mango en México es Guerrero, al generar 21% de la producción nacional con 385 125 t (SIAP, 2018). Las empresas industrializadoras de esta fruta generan volúmenes importantes de desechos o residuos como cáscaras, huesos, frutas dañadas o con problemas de madurez y calidad, todos los cuales representan una importante fuente de contaminación. Los desechos de la agroindustria se encuentran entre 28 y 43% del total del mango procesado (Guzmán et al., 2010; Sumaya-Martínez et al., 2012). Los desechos frutales almacenados sin tratamiento presentan inestabilidad y se fermentan rápidamente por efecto de la temperatura generando productos contaminantes (Cañeque y Sancha, 1998). Por otra parte, la estacionalidad de la producción del mango y los desechos generados por la agroindustria surgen como una opción de aprovecharlos en la alimentación de rumiantes en forma ensilada (Guzmán et al., 2010).
El ensilado es la conservación de forrajes frescos u otros alimentos con elevado contenido de humedad (Cañeque y Sancha, 1998), cuyo objetivo es la conservación del valor nutritivo del alimento durante el almacenamiento (Garcés et al., 2004). Las características del proceso de ensilado permiten conservar desechos agroindustriales (Valencia et al., 2011), incluyendo los del mango (Guzmán et al., 2010; Cavallini et al., 2015; Sánchez-Santillán et al., 2019). Una alternativa de ensilados con desechos frutales es la elaboración de silos en bolsa; los cuales deben hacerse rápidamente para conservar el máximo de los azucares para asegurar una fermentación láctica. Un ensilado con desechos frutales debe tener valores de 3.8±0.2 de pH, un contenido de ácido láctico promedio de 30 g kg-1 de MS, presencia nula de ácido butírico y menos de 25 g kg-1 de materia seca (MS) de ácido acético (Cañeque y Sancha, 1998).
Hernández-Rodríguez (2017) evaluó la composición química y características fermentativas de ensilados elaborados en bolsa con mango maduro molido y heno de pasto pangola (Digitaria decumbens) como absorbente de humedad; mientras Sánchez-Santillán et al. (2019) publicaron las variables de calidad de ensilado, análisis bromatológico, producción de biogás, metano y características fermentativas in vitro de ensilados elaborados en bolsa con mango maduro y heno de pasto pangola, en ambos casos realizando la apertura de los silos con 21 d de fermentación. Por tanto, el objetivo del presente estudio fue evaluar las características de calidad, químicas y fermentativas in vitro de ensilados de mango maduro molido conservados mediante una fermentación láctica hasta por 168 días para establecer los cambios que ocurren durante la fermentación láctica.
MATERIALES Y MÉTODOS
Lugar de Estudio
El estudio se realizó en el Laboratorio de Nutrición Animal de la Facultad de Medicina Veterinaria y Zootecnia No. 2 de la Universidad Autónoma de Guerrero, ubicado en el municipio de Cuajinicuilapa, Guerrero, México.
Elaboración de Silos
El desecho del mango maduro se recolectó de la empacadora del municipio de Cuajinicuilapa, Guerrero. El ensilado estuvo compuesto por este desecho (80.64%), además de heno de pasto pangola (11.38%) con 120 d de rebrote, rastrojo de maíz (4.55%), melaza de caña de azúcar (2.04%) y urea (1.36%). El mango maduro, el rastrojo de maíz y el heno se molieron en una trituradora de forraje (M.A.GRO® TR-3500) con una criba de 2.54 cm. Se utilizaron bolsas de propileno (80 x 90 cm) para preparar silos, en unidades Lorenzo-Hernández et al. (2019). Los silos se dejaron fermentar por 28 días a temperatura ambiente en una galera.
La evaluación de los silos (3 repeticiones por tiempo de fermentación) se llevó a cabo en ocho tiempos de fermentación láctica, los cuales constituyeron los tratamientos en estudio: T1 = 28 d, T2 = 44 d, T3 = 97 d, T4 = 113 d, T5 = 126 d, T6 = 140 d, T7 = 154 y T8 = 168 d.
Indicadores de Calidad
En cada tratamiento se realizaron análisis para determinar la calidad de los ensilados. Para determinar el pH se utilizó la metodología descrita por Lorenzo-Hernández et al. (2019). El contenido de MS (método 930.15) se estimó según lo descrito por la AOAC (2005). El ácido láctico se determinó con la metodología de Kimberley y Taylor (1996) modificado por Lorenzo-Hernández et al. (2019).
Análisis Bromatológico
Las muestras de los ensilados se deshidrataron en una estufa (Riossa® HCF-41, México) a 60 ºC por 72 h y fueron molidas en un molino Thomas-Wiley Mill (Thomas Scientific®, USA) con criba de 1 mm de diámetro. Se determinó el contenido de proteína cruda (PC; método 920.105), cenizas (Ce) y materia orgánica (MO; método 942.05) con los procedimientos descritos por la AOAC (2005). La fibra detergente neutro (FDN) y la fibra detergente ácido (FDA) se determinaron con el método descrito por van Soest et al. (1991). La hemicelulosa se calculó por diferencia entre FDN y FDA.
Medio de Cultivo
Se utilizó 30 ml de líquido ruminal bovino fresco centrifugado durante 10 min a 12 857 x g, 5 ml de solución mineral I [6 g K2HPO4 (Sigma-Aldrich) en 1000 ml de agua destilada], 5 ml de solución mineral II [6 g KH2PO4 (Sigma-Aldrich) + 6 g (NH4)2SO4 (Merck) + 12 g NaCl (Sigma-Aldrich) + 2.45 g MgSO4 (Sigma-Aldrich) + 1.6 g CaCl-2H2O (Sigma-Aldrich®) en 1 L de agua destilada], 0.1 ml de resarzurina a 0.1 % (Sigma-Aldrich), 0.2 g de peptona de soya (Merck), 0.1 g de extracto de levadura (Sigma-Aldrich), 4 ml de solución cisteína-sulfido [2.5 g Lcisteína (Sigma-Aldrich) en 15 mL de 2N NaOH (Meyer) + 2.5 g de Na2S-9H2O (Merck) aforado en 100 ml de agua destilada], 5 ml de solución a 8% de Na2CO3(Merck) y 52.6 ml de agua destilada.
El medio se esterilizó durante 15 min en autoclave a 121 °C y 15 psi (Sánchez-Santillán et al., 2016; Herrera-Pérez et al., 2018). El bovino se manejó de acuerdo con el reglamento interno de bioética y bienestar de la UAGro con fundamento en las normas oficiales (NOM062-ZOO-1999 y NOM-051-ZOO-1995).
Biodigestores
Los biodigestores se prepararon usando la metodología descrita por Torres-Salado et al. (2019), en la cual se cambió la fuente de carbono del biodigestor por uno de los tratamientos del presente estudio.
Producción de Biogás y Metano (CH4)
La producción de biogás a las 24, 48 y 72 h de incubación se midió mediante el desplazamiento del émbolo de una jeringa de vidrio (50 ml; BD Yale®, Brasil), según lo descrito por Hernández-Morales et al. (2018). La producción de CH4 a las 24, 48 y 72 h de incubación se midió con la metodología de Stolaroff et al. (2008) modificada por TorresSalado et al. (2018) y Herrera-Pérez et al. (2018).
Características Fermentativas
A las 72 de fermentación se determinaron las características fermentativas in vitro. Para nitrógeno amoniacal (N-NH3) se siguió la metodología de McCullough (1967) modificado por Herrera-Pérez et al. (2018). El pH del medio se midió según lo descrito por Torres-Salado et al. (2019). La cantidad de bacterias totales se calculó según la metodología descrita por Sánchez-Santillán et al. (2016). La degradación de la materia seca (DMS) se calculó con la metodología descrita por Hernández-Morales et al. (2018) y Torres-Salado et al. (2019); mientras la degradación de la FDN (DFDN) fue según lo descrito por Hernández-Morales et al. (2018).
Análisis Estadístico
Las variables de PC, MS, Ce, pH silo, MO, FDN, FDA, Hemicelulosa (3 repeticiones independientes), ácido láctico (6 repeticiones independientes), producción de biogás, CH , pH del biodigestor, DMS, DFDN (5 repeticiones independientes), N-NH3 , y conteo de bacterias (3 repeticiones independientes) se analizaron en un diseño completamente al azar usando el procedimiento GLM (SAS, 2011). La diferencia entre promedios fue con la prueba de Tukey (p<0.05).
Cuadro 1 Características de calidad y bromatológicos de ensilados de mango maduro con diferentes tiempos de fermentación láctica
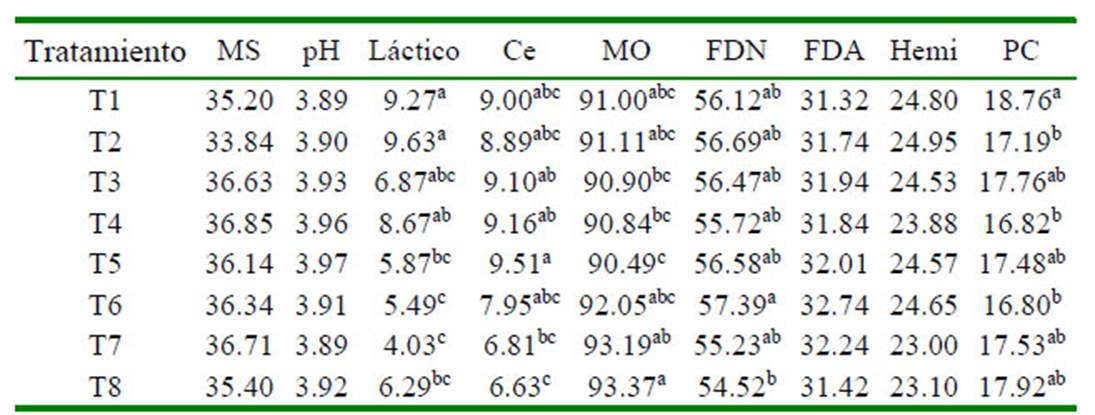
a,b,c Valores promedio con distinta letra en una misma columna son diferentes (p< 0.05)
MS = materia seca, %; pH = potencial de hidrógeno; Láctico = porcentaje de ácido láctico con respecto a la MS; Ce = cenizas, %; MO = materia orgánica, %; FDN = fibra detergente neutro, %; FDA = fibra detergente ácido, %; Hemi = hemicelulosa, %; PC = proteína cruda, %
T1 = 28 d, T2 = 44 d, T3 = 97 d, T4 = 113 d, T5 = 126 d, T6 = 140 d, T7 = 154, T8 = 168 d
RESULTADOS
Las características fisicoquímicas de ensilados de mango maduro con diferentes tiempos de fermentación láctica se presentan en el Cuadro 1. El contenido de MS, pH, FDA y hemicelulosa no mostró diferencias significativas por el tiempo de conservación de los ensilados, obteniendo en promedio 35.89% de MS, pH de 3.92, 31.91% de FDA y 24.18% de hemicelulosa. T2 presentó el mayor contenido de ácido láctico (p<0.05), sin diferencias con T1, T3 y T4 (p>0.05). Los tratamientos T1, T2, T3, T4, T5 y T6 no presentaron diferencias en el contenido de Ce (p>0.05), indicando que de los 28 a 140 días de fermentación láctica no se afectó el contenido de cenizas de los ensilados de mango maduro. El contenido de MO en T1, T2, T6, T7 y T8 fue relativamente mayor, aunque sin diferencias significativas (p>0.05), lo cual indicó que los ensilados durante los primeros 44 días de fermentación láctica mostraron el mismo contenido de MO que los ensilados que tenían de 140 a 168 d. El contenido de FDN de los ensilados presentaron diferencias entre los 140 (T6) y 168 (T8) d de fermentación láctica (p<0.05), pero sin diferencias significativas con los demás tratamientos (p>0.05). Los ensilados con 28 d (T1) de fermentación láctica mostraron mayor contenido de PC que los ensilados con 44 (T2), 113 (T4) y 140 d (T6) (p<0.05).
La producción acumulada de biogás y metano se presenta en el Cuadro 2. T7 y T8 mostraron la mayor producción de biogás a las 24 h de fermentación (p<0.05), del cual 20.78% corresponde a CH . A las 48 h de fermentación, los ensilados de 97 a 126 d (T3, T4 y T5) de fermentación láctica mostraron la menor producción de biogás, respecto a T7 y T8 (p<0.05). En estos tratamientos, la fracción de CH4 promedió 18.70%. A las 72 h de incubación, se observó que la producción de biogás acumulado no se afectó con el tiempo de fermentación láctica del ensilado, toda vez que los promedios fueron estadísticamente similares a T1 (p>0.05); mientras que la producción de CH4 a las 72 h de incubación fue menor para los ensilados de T4 (p<0.05), aunque sin diferencias con T1, T3 y T5 (p>0.05; Cuadro 2).
La mayor DMS se mostró en los tratamientos T1, T2, T3, T7 y T8 (p<0.05) con un promedio de 71.55% DMS, indicando que los ensilados de 28 a 97 d y de 154 a 168 d de fermentación láctica mostraron mayor DMS que el resto de los ensilados. En contraste, la menor DFDN fue para T4 y T5 (p<0.05) al promediar 45.87%; por lo que los ensilados con 113 y 126 d de fermentación láctica mostraron la menor DFDN, respecto al resto de los ensilados. Los ensilados con 113 d (T4) de fermentación láctica mostraron el mayor valor de pH del medio de cultivo a las 72 h (p<0.05), en tanto que el mayor contenido de N-NH3 del medio de cultivo después de 72 h de fermentación fue para los ensilados con 28 (T1) y 44 d (T2) de fermentación láctica (p<0.05). El mayor conteo total de bacterias ruminales a las 72 h fue cuando se usó como sustrato ensilados con 28 (T1), 44 (T2) y 97 d (T3) de fermentación láctica (p<0.05; Cuadro 3).
Cuadro 2 Producción acumulada de biogás y metano a las 72 h en ensilados de mango maduro con diferentes tiempos de fermentación láctica
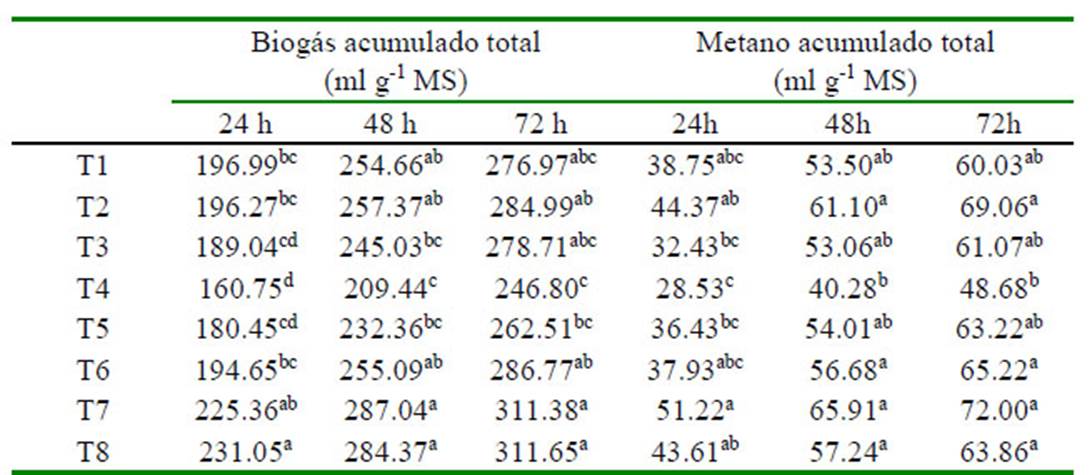
a,b,c Valores promedio con distinta letra en una misma columna son diferentes (p<0.05)
T1 = 28 d, T2 = 44 d, T3 = 97 d, T4 = 113 d, T5 = 126 d, T6 = 140 d, T7 = 154 y T8 = 168 d
DISCUSIÓN
Las características de calidad de un ensilado condicionan el proceso de fermentación, por lo que se requiere un pH de 3.5 (Garcés et al, 2004), MS de 30 a 40% (SAGARPA, 2017) y de 8 a 12% de carbohidratos fermentables como sustrato para las bacterias acido lácticas homofermentativas y heterofermentativas (Anaya-Reza y LópezArenas, 2018). En este sentido, los valores de MS, pH y ácido láctico encontrados en el presente estudio de ensilados de mango maduro fermentados hasta por 168 días indican que sus características de calidad no se vieron afectadas.
Los contenidos de FDN y FDA en el presente estudio se deben a la inclusión de heno de pasto pangola y rastrojo de maíz, los cuales contienen hasta 70% de FDN (de la Roza-Delgado, 2005). Estos elementos fueron incluidos porque el mango contiene de 79 a 94% de humedad (Yahía et al., 2006; Sánchez-Santillán et al., 2019) y se requería de ingredientes que contrarrestaran dicha humedad. Las diferencias en el contenido de PC con lo reportado para ensilado de maíz (Ruiz et al., 2009) se debe a la inclusión de 1.36% de urea en este trabajo; dado que la urea contiene 286% de PC (NRC, 2007).
El contenido de MS y PC, así como el valor de pH fueron de 77.78, 10.11 y 84.52% mayores, además el contenido de ácido láctico, MO, FDN y FDA fueron 52.42, 0.96, 16.59 y 30.40% menores que lo reportado en ensilados de maíz (Ruiz et al., 2009). De otra parte, valores inferiores al presente estudio fueron reportados por Hernández-Rodríguez (2017) en MS, FDN, FDA, PC, Ce, ácido láctico y pH en ensilados elaborados con 60% de mango maduro, 35% de heno de pasto pangola, 3% de melaza de caña y 2% de urea.
Cuadro 3 Características fermentativas in vitro a las 72 h de incubación en ensilados de mango maduro con diferentes tiempos de fermentación láctica
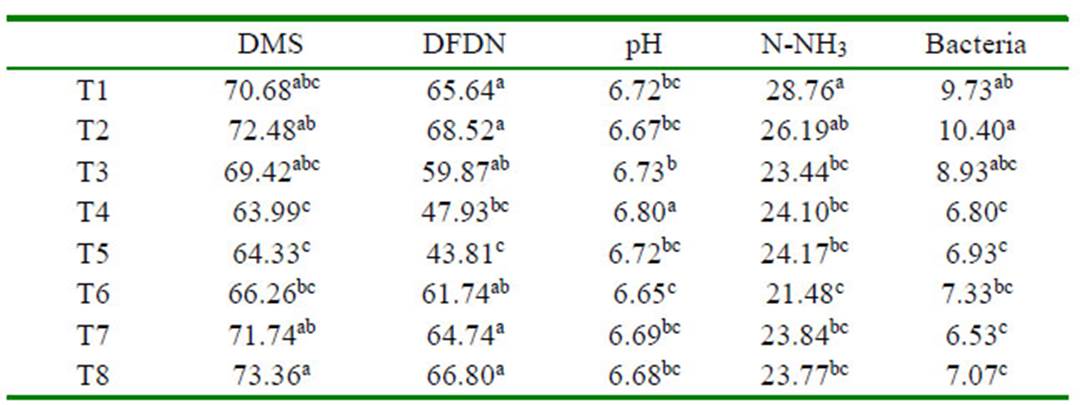
a,b,c Valores promedio con distinta letra en una misma columna son diferentes (p<0.05)
T1 = 28 d, T2 = 44 d, T3 = 97 d, T4 = 113 d, T5 = 126 d, T6 = 140 d, T7 = 154 y T8 = 168 d
DMS = degradación de materia seca, %; DFDN = degradación de fibra detergente neutro, %; pH = potencial de hidrogeno; N-NH3 = nitrógeno amoniacal, mg dL-1; Bacteria = 108 células mL-1
La producción de biogás sirve como un indicador indirecto de la cantidad de carbohidratos disponibles para la fermentación. La producción de biogás de los ensilados se puede asumir a la disponibilidad de nutrientes para los microorganismos ruminales durante la fermentación y que la digestión de los carbohidratos produce CO2 y CH4 como producto de la fermentación (Elghandour et al., 2016; Posada et al., 2006); no obstante, resultados inferiores han sido publicados. Así, Lorenzo-Hernández (2017) reportó 69.77 ml de biogás g-1 de MS en ensilados elaborados con 72.5% de residuos de calabaza, 22.5% de heno pangola, 3% de melaza y 2% de urea, lo que representó una producción de biogás acumulada a las 72 h de 304.86% menor al valor observado en el presente estudio. Cavallini et al. (2015) reportaron 191 ml g-1 de MS en ensilados elaborados con mango maduro con 48 h de incubación, lo que representó 75.44% de lo producido en promedio por los ensilados evaluados. Aragadvay-Yung et al. (2015), por otra parte, obtuvieron 240 ml g-1 MS en ensilados elaborados con maíz, siendo 71.65 ml g-1 MS menos que el ensilado de mango maduro con 168 días de fermentación láctica (T8).
El CH4 es un gas de efecto invernadero y representa una pérdida de energía para el animal. Los ensilados en el presente estudio contenían grandes cantidades de carbohidratos estructurales (pasto pangola y rastrojo de maíz), los cuales durante su fermentación producen ácido acético, CO2 e H2 como productos finales. Estos productos son utilizados por arqueas metanogénicas como sustratos para producir energía y producen CH como producto de dicha fermentación (Torres-Salado et al., 2018). Por consiguiente, es importante identificar cuanto CH4 corresponde del total de biogás producido, dado que a menor porcentaje sería menor la perdida de energía contenida en los ensilados (Araujo et al., 2011). Así, el ensilado con 113 días (T4) de fermentación láctica mostró que CH4 representó 17.74, 19.23 y 19.72% del total de biogás a las 24, 48 y 72 h de incubación.
La degradación de la MS permite establecer la cantidad de nutrientes disponibles para los microorganismos, de modo que degradaciones superiores a 60% se relacionan con bajas concentraciones de fibras detergentes o alta digestibilidad de estas (Hernández-Morales et al., 2018); por lo que los ensilados con 168 días de fermentación láctica contienen fibras detergentes que no reducirían el consumo en el animal. Además, la degradación de la FDN permitió predecir que no se afectaría el consumo potencial de la materia seca, ya que se requieren degradaciones de FDN menores a 40% para estimar una afectación (Hoffman et al., 2007; Torres-Salado et al., 2019).
En los biodigestores del presente estudio se estimó en promedio una población de 108 células ml-1 a las 72 h de incubación, valores inferiores a lo reportado por HerreraPérez et al. (2018), Almaraz-Buendía et al. (2019) y Torres-Salado et al. (2019), quienes reportaron concentraciones de 109 células ml-1 a las 72 h de incubación en biodigestores inoculados con bacterias ruminales usando como sustratos rastrojo de maíz (Herrera-Pérez et al., 2018), pastos tropicales con 56 d de rebrote (Almaraz-Buendía et al., 2019) y heno de pasto cobra (Brachiaria hibrido CV. CIAT BR02/1794) con 56 d de rebrote (Torres-Salado et al., 2019). Así mismo, los valores de pH del presente estudio fueron mayores a 6, por lo que no se afectó la adherencia de las bacterias celulolíticas al material celulósico (Nag-Jin et al., 2005; SánchezSantillán et al., 2016) ni se inhibió su crecimiento (Sánchez-Santillán y Cobos-Peralta, 2016). La concentración de N-NH3 en los biodigestores se asumen al contenido y la degradabilidad de la PC que contiene el ensilado (Herrera-Pérez et al., 2018), por lo que los valores reportados en el presente estudio se ubican dentro del rango reportado por Mehrez et al. (1977), quienes estimaron una concentración entre 20 y 27 mg dl-1 para alcanzar la máxima tasa de digestibilidad de la materia seca. Esto permite asumir que la población bacteriana probablemente se vea afectada por el tipo de sustrato usado en el biodigestor.
CONCLUSIONES
Los valores reportados de materia seca, pH, ácido láctico, fibras detergentes, proteína cruda, cenizas y materia orgánica indicaron que los ensilados de mango maduro con una fermentación láctica hasta de 168 días no afectan sus características de calidad.
El ensayo in vitro indicó que los ensilados de mango maduro tienen buena disponibilidad de carbohidratos estructurales y no estructurales












 uBio
uBio 

