INTRODUCCIÓN
El Melophagus ovinus (M. ovinus) también llamado oveja ked es un díptero hematófago sin alas de la familia Hippoboscidae que se ubica en la lana de las ovejas. Es un parásito que puede llegar a causar anemia en casos de alta carga parasitaria, afectar la conducta de pastoreo por la irritación y el prurito, pérdidas en la ganancia de peso diaria y en la producción de lana y piel (Antonelli y Sandoval, 2010; Larroza et al., 2012; Larroza, 2013; Duan et al., 2017).
El tratamiento contra esta parasitosis se realiza con productos inyectables como lactonas macrocíclicas, así como con baños de inmersión y aspersión con cipermetrinas (Álvarez, 2007); sin embargo, el uso de tratamientos de control alternos con hongos, diatomeas y nemátodos entomopatógenos ha sido considerado (Gómez et al., 2012).
Los hongos entomopatógenos son enemigos naturales de los insectos; y pueden llegar a exterminar poblaciones de plagas sin generar efectos perjudiciales para la salud humana o el medio ambiente (Khan et al., 2012). Se conoce que hongos del género Beauveria son eficaces para el control de varios insectos por su alta patogenicidad al penetrar en el hemocele de su hospedero y causarle la muerte tras la producción de toxinas (Mejía et al., 2016; Rao y Narladkar, 2018)..Las esporas del hongo entran en contacto con la superficie quitinosa del insecto, donde inicia el mecanismo entomopatógeno de adhesión, germinación y penetración por medio de enzimas proteasas, quitinasas y lipasas (Monzón, 2001; Pedrini et al., 2007; Wang y Leger, 2007) y dentro del huésped contrarresta los mecanismos inmunes del insecto propiciando efectos nocivos y la muerte (Téllez et al., 2009).
El presente trabajo tuvo como objetivo evaluar el efecto in vivo del hongo entomopatógeno B. bassiana en el parásito ovinus de ovejas naturalmente infestadas provenientes del municipio de Güicán de la Sierra, Boyacá, Colombia.
MATERIALES Y MÉTODOS
Lugar del Estudio
El estudio se realizó en la finca La Cabaña, ubicada en el municipio de Güicán de la Sierra, departamento de Boyacá, Colombi. La región se encuentra a una altitud de 2895 msnm, y presenta una temperatura media de 13 °C y humedad relativa de 80% (Alcaldía Guicán de la Sierra, 2019).
Animales
Se utilizaron 15 ovejas adultas Hampshire Down cruzadas que se encontraban naturalmente infestadas por M. ovinus. Los animales tenían un peso promedio de 40 kg, edades de 2.5 a 3 años y eran parte del rebaño comercial de la finca. Las ovejas se distribuyeron en tres grupos en corrales de 12 m2, con periodos de pastoreo de 4 horas al día en praderas de pasto kikuyo (Pennisetum clandestinum) y agua a voluntad.
Hongo Entomopatógeno
Se usó la cepa comercial del hongo Beuveria bassiana ADRAL®wp de BioCrop (Colombia), en la presentación líquida en agua destilada con Tween 80 al 0.1%. Se tomó 1 ml en una cámara de Neubauer y se calculó el número total de conidios por mililitro usando la fórmula (Cañedo y Ames, 2004) Conidias (ml) = N.° conidias contadas x 25 000 x factor de dilución, obteniéndose una concentración de 2x108 conidios/ml de B. bassiana.
Adicionalmente se cultivó el hongo en caja Petri con agar Sabouraud usando la técnica de estría por agotamiento en incubación a 30 °C y 80% HR durante 72 h. La identificación del hongo se hizo con tinción de lactofenol a interpretación microscópica de las características morfológicas según el Manual de Hongos Entomopatógenos (Cañedo y Ames, 2004).
Tratamientos
Se trabajó con tres tratamientos:
T1: 8.3 ml de la cepa comercial en 500 ml de agua destilada (3.2 x 106 conidias/ml)
T2: 8.3 ml de la cepa comercial en 500 ml de agua destilada y azucara al 5% como coadyuvante (3.2 x 106 conidias/ml)
T(Control): 500 ml de agua destilada
Cuadro 1 Tablas de frecuencia de grados de densidad poblacional
| Grado | Parásitos (n) |
| 0 1 2 3 4 | 0 1-12 13-24 25-36 37-50 |
Los tratamientos fueron aplicados una vez por aspersión con bomba de espalda a cada animal cubriendo toda la superficie corporal del animal. La aplicación se hizo en horas de la tarde con los animales dentro del aprisco para evitar efectos de la luz solar sobre la cepa fúngica.
Identificación de Parásitos
El conteo de los parásitos se realizó cada 24 horas a la misma hora en la mañana de forma directa y durante tres semanas. Se observó cada canal formado naturalmente por el vellón desde cuello, pecho, brazo y antebrazo de la región lateral izquierda, repitiendo la observación en la región contralateral (Becerra y Otrando, 2020; Small, 2005). Los datos se organizaron en tablas de frecuencia con intervalos, a los que para efectos de este estudio se les denominaron grado de densidad poblacional (Cuadro 1).
Para determinar el efecto del hongo se realizó conteo diario de los parásitos presentes en área corporal establecida. El valor fue expresado en porcentaje con el número de melófagos vivos en cada repetición y tratamiento. Los valores se reemplazaron con las siguientes fórmulas de eficacia de ectoparasiticidas (Abbott, 1925; Holdsworth et al., 2006):
% Supervivencia = (Número de melógagos vivos / número total de melófagos) * 100
% Mortalidad (%) = 100 Supervivencia (%)
% Eficacia = [(% Supervivencia del Control % Supervivencia del tratamiento) / (% Supervivencia del Control] * 100
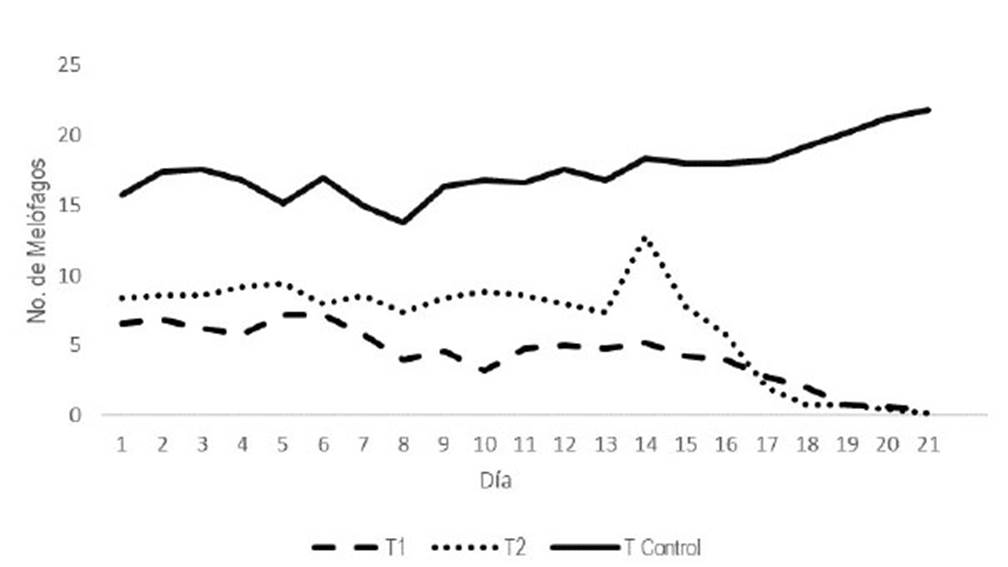
Figura 1 Número de Melophagus ovinus en cuello, pecho, brazo y antebrazo de la región lateral izquierda y derecha de ovinos tratados con Beuveria bassiana. T1: 3.2 x 106 conidias/ml de agua destilada; T2; como T1 pero con agua destilada azucarada al 5%; T Control: agua destilada
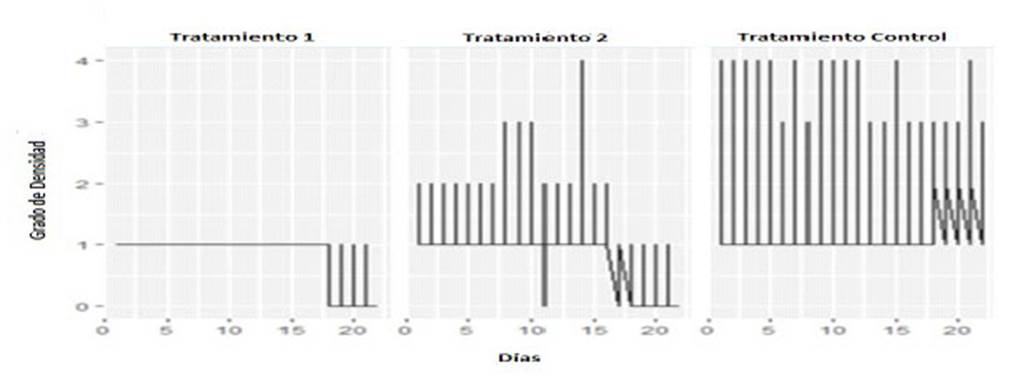
Figura 2 Densidad poblacional de Melophagus ovinus tratados con Beuveria bassiana (LSD de Fisher). T1: 3.2 x 106 conidias/ml de agua destilada; T2; como T1 pero con agua destilada azucarada al 5%; T Control: agua destilada
Los resultados fueron analizados mediante análisis de varianza y las diferencias entre medias mediante la prueba de Fisher (p<0.05).
RESULTADOS
El número promedio de melófagos al inicio del estudio fue de 4.3 ± 2.1, 6.6 ± 3.5 y de 17.5 ± 1.9 para T1, T2 y T(Control), respectivamente. La variabilidad en el número de M. ovinos en cada conteo pudo asociarse al desplazamiento de parásitos dentro del área de conteo (Figura 1).
La población tratada con B. bassiana se redujo en 50% a partir del día 16 del estudio (Figura 1). Los ovinos de T1 presentaron valores de control más favorables, que fueron igualados por los ovinos de T2 a los 21 días llegando a un promedio de 0.5 parásitos por conteo, valor significativamente menor que en el grupo control (p<0.05).
Los tratamientos con B. bassiana tuvieron densidad «0» a partir de la segunda semana, mientras que la densidad en el grupo control fue de «4» (p<005) (Figura 2). La mortalidad fue determinada a partir de la relación de supervivencia, ya que el conteo de los insectos muertos que caen del vellón del animal fue imperceptible. En los parásitos muertos o moribundos que fueron colectados se evidenció una coloración más oscura, nulas (o poca) respuesta al estímulo y algunos de ellos con micelios en la cutícula (Figura 3).
Los porcentajes de mortalidad de M. ovinus en los días 7, 14 y 21 del estudio se muestran en el Cuadro 2. La mortalidad se incrementó notoriamente en T1 y T2, llegando a ser de 90% en el día 21, en tanto que en el grupo control fue de 5.9% (p<0.05). La eficacia en el control de M. ovinus fue de 89.3% (p<0.05), indicando la conveniencia de los tratamientos con hongos (Holdsworth et al., 2006).
Cuadro 2 Porcentaje de mortalidad en el día 7, 14 y 21 de Melophagus ovinus en ovinos tratados con Beuveria bassiana
| Día | Mortalidad (%) | ||
| T1 | T2 | T control | |
| 7 | 18.3a | 6.0b | 7.4b |
| 14 | 18.8a | 11.0b | 5.9c |
| 21 | 90.0a | 90.0a | 5.9b |
a,b,c Valores promedios de filas con diferentes letra son diferentes (p<0.05)
T1: 3.2 x 106 conidias/ml de agua destilada; T2; como T1 pero con agua destilada azucarada al 5%; T Control: agua destilada
DISCUSIÓN
Las características biológicas de M. ovinus y su notable necesidad de realizar todo su ciclo biológico en la oveja, su hospedero natural, contribuyen a que su cultivo in vitro se dificulte, ya que solo sobrevive una media de 24 horas fuera del hospedero (Manosalva et al., 2013).
A pesar de que los tratamientos se unificaron por peso y edad, se encontraron diferencias en la densidad poblacional inicial, lo cual puede atribuirse a factores de susceptibilidad intrínsecos como condición corporal, densidad de la lana, edad, gestación, y sexo que permiten una mayor o menor colonización de los melófagos (Olaechea et al., 2006; Olaechea, 2009; Scasta y Koepke, 2016). La población de melófagos se mantuvo muy activa durante el estudio, desplazándose en el vellón, próximos o alejados de la piel, comportamiento motivado por variaciones de temperatura corporal y ambiental (Olaechea, 2009).
Existen diversas causas naturales que generan bajas en la población del melófago, como adaptabilidad y resistencia propia del hospedador (Nelson y Bainborough, 1963; Nelson y Kozub, 1980), aunque ha sido sugerido que los parásitos ubicados en la superficie del vellón tienen mayor riesgo de mortalidad por caer al suelo, por depredación e incluso por ingestión por parte de la oveja (Becerra y Otrando, 2020); sin embargo, la densidad poblacional «0» obtenida en los tratamientos con B bassiana indican un efecto controlador del hongo para M. ovinus al comparar las densidades con la del grupo no tratado.
La mortalidad obtenida en T1 y T2 de 90% fue superior a la reportada por Gómez et al. (2012) con mortalidades de 64.1% en ovejas con vellón largo y de 79.4% en ovinos esquilados, donde estos grupos fueron tratados con formulación líquida de 109 conidios/ml de bassiana por 30 días. De otra parte, el
89% de eficacia de los tratamientos con B. bassiana, se acercan a la eficacia reportada por Tofiño et al. (2018) de 96.8%, al aplicar aspersiones del hongo a una concentración de 106conidias/ml para el control de garrapatas R. microplus. Las diferencias pueden sugerir que los datos de mortalidad varían en virtud de la concentración, el potencial patógeno de la cepa fúngica y las condiciones de humedad y temperatura adecuadas para el crecimiento de B. bassiana.
Los M. ovinos de los grupos tratados presentaron disminución de movimiento hasta parálisis y cambio en la coloración tornándose a un café oscuro. Los cambios de color pueden estar asociados a la melanización, proceso que es descrito en los insectos como una respuesta del sistema inmune humoral a la llegada de cualquier agente externo, y se conoce bajo el nombre de sistema profenoloxidasa (Vargas y Ortega, 1994; Chase et al., 2000; Chávez et al., 2014; Jiang et al., 2019).
El efecto del hongo entomopatógeno fue comprobado. La muerte de los parásitos contrasta con su capacidad patógena, que se resume en ingresar a la hemolinfa ocasionando disrupción en la homeodinamia parasitaria y con ello la muerte (Kirkland et al., 2005; Pucheta et al., 2006; Harrison y Bonning, 2010; Ortiz y Nemat, 2013). La muerte del parásito y el tiempo de presentación del hongo influenciada por la actividad enzimática y la cantidad de sustrato establece que entre 3 a 7 días de la muerte del parásito ocurre la esporulación fuera del esqueleto (Angelo et al., 2010). La esporulación puede ocurrir interna y externamente, dependiendo de la humedad, que cuando es baja se dificulta la esporulación externa pudiendo ser el caso de los tratamientos (Delgado y Murcia, 2011); sin embargo, este comportamiento justifica que una baja germinación puede igual generar la muerte de los parásitos (Feijó et al., 2007), pueslos conidios pudieron producir toxinas que generaron la patogenicidad. La muerte de los parásitos no se encontró asociada a la presentación de micelios de B. bassiana. La producción de micelios no está asociada a mayor virulencia y a la patogenicidad (Obando y Bustillo, 2011).
La aplicación de azúcar como coadyudante del B. bassiana en el presente estudio no alteró la eficacia entre los tratamientos, no evidenció el objetivo de su aplicación para mejorar la eficacia en campo del producto, la estabilidad durante su aplicación, ni la adhesión y penetración del hongo en el parásito (Bastidas et al 2009), datos que difieren a Arrubla et al. (2008), quienes mezclaron B. bassiana con azúcar al 5% para el control de la broca, demostrando un mejor resultado.












 uBio
uBio 


