INTRODUCCIÓN
El término microplástico (MP) (<5 mm de diámetro) abarca una amplia variedad de materiales plásticos, cada uno con características físicas y químicas únicas. El término plástico es bastante amplio y generalmente se refiere a cualquier polímero sintético insoluble en agua (típicamente de origen petroquímico) que se puede moldear al calentar y manipular en varias formas diseñadas para mantenerse durante el uso (Crooks et al., 2019; Miller et al., 2021).
Los alimentos marinos son altamente susceptibles a xenobióticos y a contaminantes emergentes, producto de la actividad humana con una industria facilista con el uso de materiales «prácticos» y «fáciles de manejar» (Andrady, 2011; Reinoso et al., 2017; Thompson y Darwish, 2019). Es posible que los microplásticos (MP) puedan estar presentes en alimentos de importancia hidrobiológica en el ámbito de la gastronomía, con implicaciones en la salud pública y en la seguridad alimentaria (Barboza et al., 2018; Mc Carthy et al., 2018; Smith et al., 2018; De-la-Torre, 2019). Se ha señalado que los MP ingeridos por el humano pudieran estar asociados con inflamación de los tejidos, proliferación celular y necrosis, así como comprometer a las células inmunes (De-la-Torre, 2019).
El consumo de productos hidrobiológicos representa una vía importante para la exposición a MP a los humanos. Varias investigaciones han mostrado contaminación por MP en recursos alimenticios comerciales; es decir, en aquellos que se expenden en los mercados, conservas de pescado, agua potable, sal de mesa, miel y azúcar, etc. (Liebezeit G y Liebezeit E, 2013; GESAMP, 2015; Karami et al., 2018; Li et al., 2018a; Schymanski et al., 2018; Renzi y Blaskovic, 2018; Cho et al., 2019; De-la-Torre, 2019). La ingesta mundial de estos productos hidrobiológicos representa el 6.7% de todas las proteínas consumidas y, aproximadamente, el 17% del consumo de proteínas de origen animal (Smith et al., 2018).
Los MP presentes en la biota acuática están bien documentados (Bravo et al., 2013; Kumar et al., 2018; Li et al., 2018c; Pegado et al., 2018; Su et al., 2018; Castañeta et al., 2020; Donoso y Rios-Touma, 2020; Rani- Borges et al., 2021). Los MP en especies marinas comerciales obtenidas de los mercados y usadas en la gastronomía debe considerarse como una vía potencial para el impacto en el ser humano (Halden, 2010; Lithner et al., 2011; Rochman et al., 2014, 2015; Brennecke et al., 2016; Camacho et al., 2019; Akhbarizadeh et al., 2018; Li et al., 2018b; Carbery et al., 2018; De-la-Torre, 2019). Los MP pueden interactuar con otros contaminantes tóxicos (Araujo et al., 2002; Rochman et al., 2014; Brennecke et al., 2016; Li et al., 2018b; Camacho et al., 2019) y con microorganismos patógenos que se les pueden adherir (Virsek et al., 2017).
En el Perú, existen escasas publicaciones científicas que abordan la problemática de los MP, las cuales tienen generalmente un enfoque ecológico (Purca y Henostroza, 2017; De-la-Torre et al., 2019a,b; Gavilán et al., 2019; Iannacone et al., 2019, 2021; Santillán et al., 2020; Valencia-Velasco et al., 2020; Molina-Castro et al., 2021).
El orden Decapoda, el más diverso dentro de la clase Malacostraca, incluye alrededor de 15 000 especies que desempeñan un papel importante en la red trófica acuática (Ferreira et al., 2020). Existe información que aborda la problemática de los MP en crustáceos decápodos marinos y de agua dulce (Farrell y Nelson, 2013; Brennecke et al., 2015; Smith et al., 2018; Piarulli et al., 2020). En el Perú no hay estudios con MP en crustáceos decápodos marinos, a pesar de que este grupo es uno de los recursos principales de invertebrados marinos que forman parte de la productividad terciaria que sustenta la pesquería, principalmente artesanal, y son ampliamente usados en la alimentación humana y en diversos potajes gastronómicos marinos. Entre las especies de crustáceos decápodos marinos más importantes para el consumo humano tenemos al «cangrejo peludo» Romaleon setosum (Molina, 1782) (Cancridae), a la «jaiva» Cancer porteri Rathbun, 1930 (Cancridae) y al «cangrejo violáceo» Platyxanthus orbignyi (H. Milne Edwards & Lucas, 1843) (Platyxanthidae) (Gutiérrez-Ramos y González-Campos, 2016; Carbajal-Enzian y Santamaría, 2017; Musrri et al., 2019).
Se han realizado varias investigaciones en R. setosum, como la evaluación de los efectos reproductivos por acción de la temperatura (Fischer et al., 2009), su identidad taxonómica (Retamal et al., 2014), la composición y distribución de las capturas en el ambiente marino (Muñoz et al., 2006), el comportamiento reproductivo de las hembras (Baeza y Fernández, 2002), la estructura espermática (Goldstein y Dupré, 2011) y el riesgo del consumo humano por presencia metales pesados (Loaiza et al., 2018); sin embargo, no se tiene información con su relación con los MP. El objetivo de la presente investigación fue caracterizar los MP en el «cangrejo peludo» R. setosum usado en la gastronomía peruana.
MATERIALES Y MÉTADOS
Muestra
Se evaluaron 15 individuos de «cangrejo peludo» R. setosum, adquiridos en diciembre de 2020 y enero 2021 en el Mercado Mayorista Pesquero de Ventanilla, Callao, Perú, un punto principal a nivel de Lima y Callao para la adquisición de recursos de invertebrados bentónicos de consumo gastronómico. Se determinaron las medidas biométricas de cada espécimen como marco referencial: ancho del cefalotórax (AC en mm), longitud del cefalotórax (LC en mm) con un calibrador vernier, y peso húmedo (P en g) (Espinoza et al., 2016). Este material biológico fue evaluado para la búsqueda de MP en sus diferentes formas y colores asociados al músculo, branquias y tracto digestivo del cangrejo. La unidad de análisis fue cada cangrejo. La identificación de la especie de cangrejo fue con base al protocolo de Carbajal y Santamaría (2017). Ninguno de los individuos seleccionados de R. setosum fueron hembras ovígeras (con huevos) según la Resolución Ministerial N.º 159-2009- PRODUCE (PRODUCE, 2009a).
Procedimiento
El lugar para la evaluación del material biológico fue desinfectado con alcohol etílico al 70%, previamente filtrado con un papel filtro de 5 µm. Se usaron guantes de nitrilo durante todo el proceso evaluativo. Los materiales usados durante todo el protocolo fueron de vidrio o de metal. El agua empleada para el lavado del material biológico fue filtrada a 0.22 µm (Iannacone et al., 2021). También se utilizó el método descrito por Torre et al. (2016) para minimizar alguna contaminación en el aire, reduciendo la posibilidad de sesgo en el análisis.
Para el manejo de los cangrejos se siguió el protocolo establecido por Piarulli et al. (2020). Los cangrejos fueron lavados con agua filtrada con un papel filtro de 2.5 µm. El agua fue almacenada en una congeladora a -20 °C para luego ser empleada para la caracterización de los MP. Cada individuo fue evaluado integralmente a nivel del músculo, branquias y tracto digestivo, separando cada componente en placas de Petri y mantenidos en congelación a -20 °C y finalmente se realizó la búsqueda de los MP (Iannacone et al., 2021).
Se preparó una solución de hidróxido de potasio (KOH) al 10% (100 g de KOH en 1 L de agua destilada) (Dehaut et al., 2016). La cantidad de la solución se ajustó en relación a cada muestra. El KOH fue mezclado con el agua con un agitador magnético hasta que los «pellets» se disolvieron, se dejó enfriar por al menos 15 min y se filtró (2.5 µm) empleando una bomba de vacío. Para la digestión de las muestras se empleó el KOH en una proporción de 4:1 (KOH: muestra). Se incubó dicho material a 60 °C por 24 h con agitación permanente a 45 rpm y luego se procedió a filtrar (6 µm) con la ayuda de una bomba de vacío.
Para la caracterización visual de los MP se utilizó un microscopio binocular con cámara adaptada para buscar las partículas en el papel de filtro y hacer los registros fotográficos. La caracterización se hizo siguiendo criterios preestablecidos. Para la forma se consideraron tres categorías: fibra «plástico delgado, fibroso y recto» que puede provenir de textiles, artes de pesca y filtros de cigarrillos, fragmento «partícula de MP duro e irregular» que puede provenir de la descomposición de desechos plásticos más grandes, y film «plástico endeble, plano e irregular» como bolsas de plástico y envoltorios (Lusher, 2015; Sruthy y Ramasamy, 2017; Miller et al., 2021), en tanto que se consideraron seis colores (negro, azul, rojo, verde, blanco y amarillo). Se excluyeron aquellas partículas de MP con un color no uniforme o con estructuras naturales como células. Se verificó que las fibras presentaran un grosor homogéneo y que estuvieran deshilachadas en los bordes apicales. También se usaron agujillas calientes durante la evaluación óptica para completar la identificación de las partículas de MP que reaccionan a altas temperaturas mediante un doblez o fusión.
Para cada una de las tres variables biométricas (AC, LC y P), y para el número de partículas de MP por ubicación en el cuerpo de R. setosum, así como para la forma y el color se determinaron los estadísticos de nor- malidad con la prueba de Shapiro-Wilk y para la homocesticidad de varianzas fue usada la prueba de Levene (Morales y Pino, 2009).
En los casos que no se cumplieron estos requisitos se emplearon sus equivalentes no paramétricos. Se empleó la prueba de Kruskall-Wallis (H) con el fin de compa- rar el número de partículas de MP entre las tres partes del cuerpo (músculo, branquias y tracto digestivo), entre las tres formas y entre los seis colores. Luego se realizó la prueba a posteriori de Tukey.
Se empleó la prueba de Chi-cuadrado para determinar la relación entre las tres formas y entre los seis colores de MP con base a la frecuencia de ocurrencia (FO) de los MP.
Se empleó la prueba de U de Mann- Whitney para comparar entre machos y hembras de R. setosum el AC, LC, P, el número de partículas de MP total, del músculo, de las branquias y del tracto digestivo, de las tres formas y de los seis colores.
La data obtenida con relación al AC, LC y P fue asociada con el número de partí- culas de MP totales, en músculo, branquias y tracto digestivo usando el coeficiente de correlación de Spearman (rs).
De igual forma se correlacionó el AC, LC y P con el número de partículas de MP por ubicación en el cuerpo de R. setosum, por la forma y por el color.
Con el fin de determinar el estado actual del conocimiento sobre los MP en crustáceos acuáticos a nivel mundial se realizó una búsqueda de artículos científicos publicados en revistas arbitradas e indizadas en tres bases de datos: Google Académico, Scielo, y Scopus. Se hizo la pesquisa con las palabras o frases: «microplásticos», «cangrejo», «biota acuática» y «crustáceos», tanto en español, inglés y portugués, publicados hasta diciembre de 2020. No fueron consideradas las tesis ni resúmenes de congreso. Se clasificaron los artículos científicos encontrados por orden de antigüedad a partir de 2013. Se elaboraron cuadros de resumen que incluyeron año, país, especie de crustáceo, cantidad de muestra, tamaño, peso, sexo y parte del organismo evaluado. De igual forma se incorporó en la base de datos con relación a los MP en crustáceos acuáticos, la cantidad, forma, tamaño, color y medio. Posteriormente, la información fue consolidada en cuadros dinámicos.
Aspectos Éticos
Se siguió la Resolución Ministerial N.º 159-2009-PRODUCE (PRODUCE, 2009a) y el «Reglamento de Ordenamiento Pesquero de Recursos Invertebrados Marinos Bentónicos» con la Resolución Ministerial N.° 501- 2019-PRODUCE (2019b) para la selección y empleo adecuado de los especímenes de R. setosum en el presente estudio.
RESULTADOS
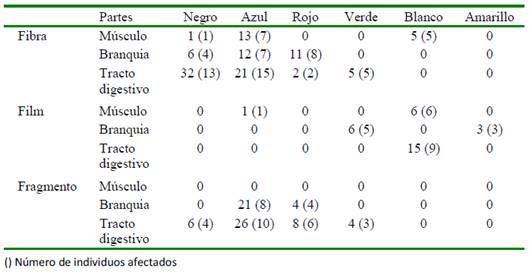
Las fibras azules de MP fueron más abundantes en el músculo, las fibras azules y rojas en las branquias, y las de color negro y azul en el tracto digestivo de R. setosum (Cuadro 1). En el caso del MP tipo film, el color blanco fue el dominante en el músculo y en el tracto digestivo, mientras que el MP verde dominó en las branquias. El tipo fragmento no se encontró en músculo. Asimismo, los fragmentos de color azul fueron más abundantes en las branquias y en el tracto digestivo.
Cuadro 1 Número de partículas de microplásticos (MP) encontradas en el músculo, branquias y tracto digestivo del “cangrejo peludo” Romaleon setosum (n=15) procedentes del Mercado Mayorista Pesquero de Ventanilla, Callao, Perú
Se encontró un total de 208 partículas de MP en R. setosum, observándose la siguiente secuencia de mayor a menor: tracto digestivo > branquias > músculo (Figura 1a), con diferencias significativas entre el tracto digestivo (7.93±4.68a), branquias (4.20±2.88b) y músculo (1.73±2.12c) (H=21.93; p<0.05). En las formas de MP se observó el siguiente orden: fibra > fragmento > film (Figura 1b) con diferencias significativas entre fibra (7.20±2.81a), fragmento (4.60±3.07b) y film (2.07±1.39c) (H=19.02, p<0.05). Asimismo, se notó que el color azul y negro fueron los dominantes con relación al número de partí- culas de MP (Figura 1c), habiendo diferencias significativas entre el azul (6.27±3.83a), negro (3.00±1.96b), blanco (1.73±1.10bc), rojo (1.67±1.07bc), verde (1.00±1.07c) y amarillo (0.20±0.41d) (H=46.56, p<0.05).
Todos los R. setosum presentaron MP en músculo, branquias y tracto digestivo basándose en la FO (Figura 2a). En las formas de MP con base a la FO se observó el siguiente orden: fibra > fragmento > film (Fi- gura 2b), aunque sin diferencias significativas entre las tres formas (X2= 2.14, p>0.05). Por otro lado, los colores de MP azul, blanco, rojo y negro fueron los más frecuentes según la FO de MP (X2= 37.82, p<0.05) (Figura 2c).
Se encontró una correlación negativa entre la LC y el AC de R. setosum (rs=-0.64; p<0.05). La LC presentó una correlación significativa con el número de partículas de MP en los cangrejos in toto (rs=0.52; p<0.05), con el músculo (rs=0.53; p<0.05) y con el color azul (rs=0.51; p<0.05), pero no para el resto de variables (rs=-0.43-0.45; p>0.05).
En el caso de machos y hembras de R. setosum no se observaron diferencias significativas al comparar la LC, el número de partículas de MP total, del músculo, de las branquias y del tracto digestivo, entre las formas y entre los seis colores (U=14.5-23.5; p<0.05).
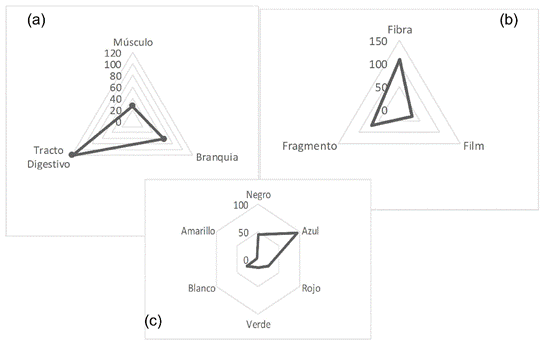
Figura 1 Gráfico radial del número de partículas de MP en: (a) Parte del cuerpo; (b) Forma: (c) Color
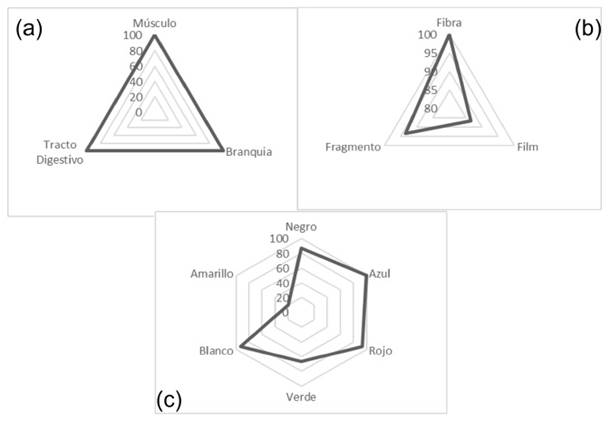
Figura 2 Gráfico radial de la Frecuencia de ocurrencia (FO) de partículas de MP en: (a) Parte del cuerpo; (b) Forma: (c) Color
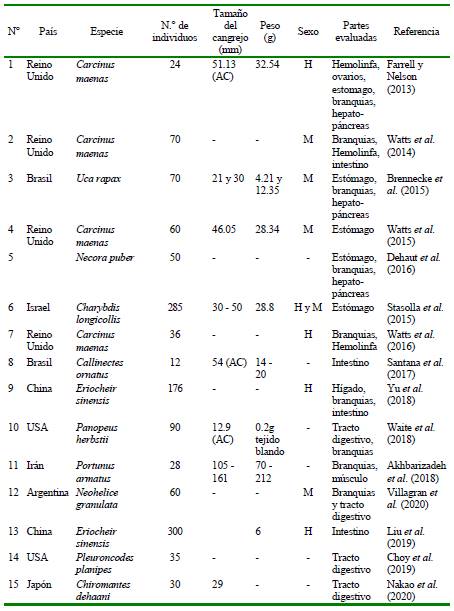
Cuadro 2 Resumen bibliográfico de 15 artículos científicos a nivel mundial que señalan año, país, especie de crustáceo, cantidad de muestra, tamaño, peso, sexo y parte del organismo evaluada para microplásticos (MP). AC= Ancho del cefalotórax. H=Hembra. M=Macho (Parte 1)
Cuadro 3 Resumen bibliográfico de seis artículos científicos a nivel mundial que señalan año, país, especie de crustáceo, cantidad de muestra, tamaño, peso, sexo y parte del organismo evaluada para microplásticos (MP). AC= Ancho del cefalotórax. H=Hembra. M=Macho (Parte 2)
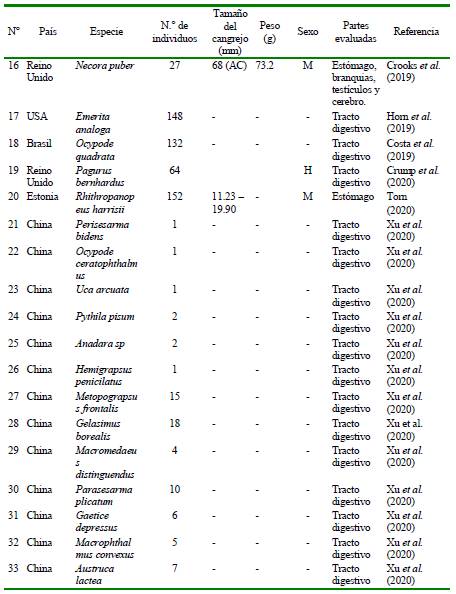
Cuadro 4 Resumen bibliográfico de ocho artículos científicos a nivel mundial que señalan año, país, especie de crustáceo, cantidad de muestra, tamaño, peso, sexo y parte del organismo evaluada para microplásticos (MP). AC=Ancho del cefalotótax. H=Hembra. M=Macho (Parte 3)
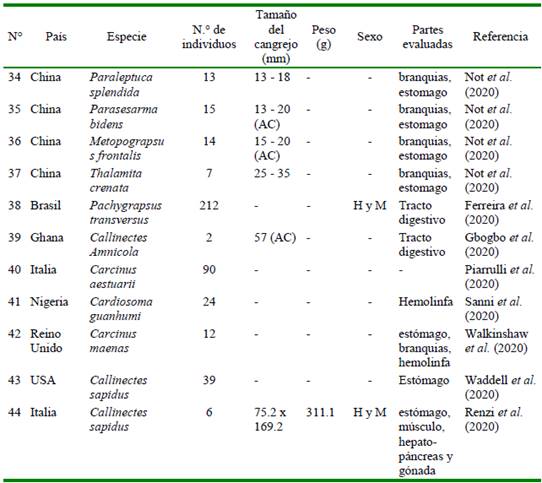
Los cuadros 2, 3 y 4 presentan un resumen bibliográfico de 29 artículos que evalúan MP en diferentes especies de crustáceos a nivel mundial. Estos cuadros muestran que durante 2013 a 2020 se evaluaron MP en 44 especies de crustáceos decápodos. China (43.18%) y Reino Unido (15.90%) fueron los países que evaluaron más especies de crustáceos. El género Carcinus Leach, 1814 fue el que presentó el mayor número de estudios con MP. El tamaño de la muestra varió entre 1 a 300 individuos analizados. El tamaño varió para la LC entre 11.23 a 169.2 mm, y para el AC entre 13 a 68 mm. El P se encontró entre 4.21 a 311.1 g. Con relación al sexo de los cangrejos, cinco fueron hembras, seis machos, tres de ambos sexos, y 30 no señalaron el sexo de los especímenes. El tracto digestivo de los crustáceos fue la parte corporal más estudiada.
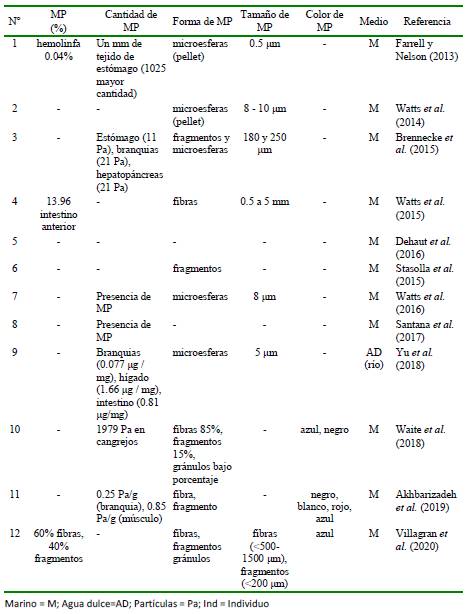
Cuadro 5 Resumen bibliográfico de 12 artículos científicos a nivel mundial que señalan en los crustáceos la cantidad, forma, tamaño y color y medio para microplásticos (MP) (Parte 1)
Cuadro 6 Resumen bibliográfico de nueve artículos científicos a nivel mundial que señalan en los crustáceos la cantidad, forma, tamaño y color y medio para microplásticos (MP) (Parte 2)
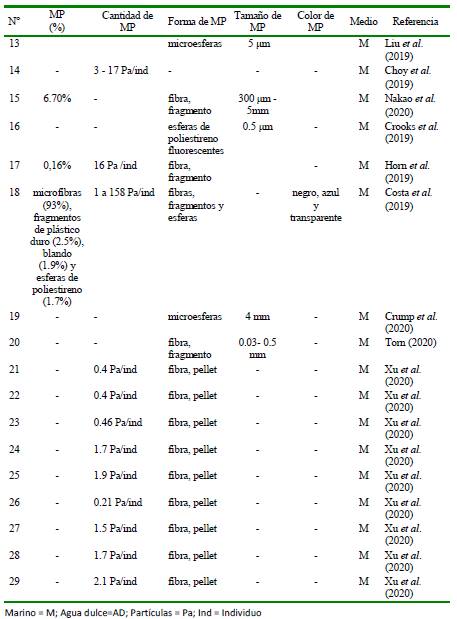
Cuadro 7 Resumen bibliográfico de nueve artículos científicos a nivel mundial que señalan en los crustáceos la cantidad, forma, tamaño y color y medio para microplásticos (MP) (Parte 3)
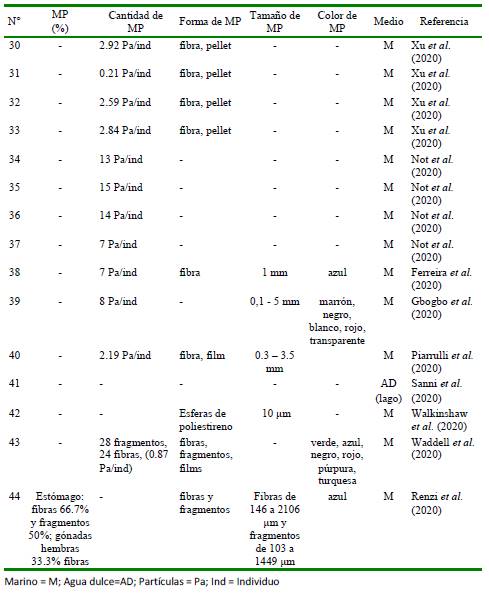
Los cuadros 5, 6 y 7 señalan que las formas tipo fibras y los pellets de los MP fueron los dominantes en los estudios con crustáceos. Con relación a la cuantificación de MP estos son presentados en el animal in toto de cangrejo, por parte corporal o solo presencia de MP. Con relación al tamaño, 17 estudios (38.6%) señalaron el tamaño y 27 (61.4%) no lo presentaron. Los dos colores de MP más dominantes fueron el azul y el negro. El medio más estudiado para el estudio de los MP en crustáceos en el medio marino (95.5%).
DISCUSIÓN
Todos los cangrejos presentaron MP en el animal in toto, en el músculo, branquias y tracto digestivo. Por otro lado, Renzi et al. (2020) detectaron 83.3% de MP en el crustáceo Callinectes sapidus Rathbun, 1896, y Xu et al. (2020) encontraron 70% de MP en 13 especies de crustáceos en el sur de China, en tanto que en el cangrejo Rhithropanopeus harrisii (Gould, 1841) se observó 5% de ocurrencia de MP (Torn, 2020). Muchos trabajos no realizan evaluaciones individualizadas de MP por espécimen, sino, por el contrario, realizan evaluaciones tipo «pool» (Villagran et al., 2020).
Es muy probable que la vía principal de ingestión de plástico por el crustáceo béntico R. setosum sea indirecta, a través del consumo de bivalvos (Ferreira et al., 2020). Sin embargo, las vías de entrada de los MP a los depredadores en el ambiente marino como es el cangrejo peludo R. setosum puede involucrar tanto a sus presas como al medio ambiente. Los MP no solo se transfieren de depredadores de orden inferior a depredadores de orden superior a través de las redes alimentarias (Nakao et al., 2020). Los hallazgos sugieren que R. setosum pueden ingerir los MP a través de la ingestión directa, la alimentación por filtración, la alimentación en suspensión y la transmisión de la cadena alimentaria, tal y como ocurre en otras especies de crustáceos decápodos (Yu et al., 2018).
Por cada individuo de R. setosum se observaron 13.87 ± 6.02 (5-27) partículas de MP/cangrejo y en el tracto digestivo/cangrejo de 7.93 ± 4.68 (3-18). Los reportes de MP/cangrejo en la literatura son variables; así, se encontraron entre 3 a 17 partícu- las de MP/individuo para el tracto digestivo del crustáceo Pleuroncodes planipes (Stimpson, 1860) (Choy et al., 2019), de 16 partículas de MP/individuo en el tracto digestivo de Emerita analoga (Stimpson, 1857) y de 1 a 158 partículas/individuo en Ocypode quadrata Fabricius, 1787 (Costa et al., 2019; Horn et al., 2019).
En el presente estudio se observó la secuencia de tracto digestivo > branquias > músculo en relación al número de partículas de MP. El número de MP extraídos de la bran- quia fue 2.42 veces mayor que el músculo. En el crustáceo Eriocheir sinensis H. Milne Edwards, 1853, se observaron valores superiores de MP en el tracto digestivo que en las branquias (Yu et al., 2018). Los resultados concuerdan con Akhbarizadeh et al. (2018), quienes encontraron que había más MP en las branquias que en el músculo del cangrejo Portunus armatus (A. Milne-Edwards, 1861), posiblemente debido a la mayor exposición de las branquias al agua y al medio circundante, que las convierten en un órgano importante para la acumulación de MP, así como el tipo de alimentación del cangrejo. Otra posible hipótesis podría ser que las fibras lleguen primero al músculo del crustáceo decápodo a través de las branquias, los ojos, la circulación sanguínea y el epitelio intestinal en el tracto digestivo (Akhbarizadeh et al., 2018). Los MP llegan primero al tracto digestivo y posteriormente las micropartículas más pequeñas se trasladan más fácilmente a otros tejidos, como el tejido muscular (Crump et al., 2020).
Las fibras, entre las formas de MP, fueron las más frecuentes en R. setosum, lo cual coincide con diversos autores para varias especies de cangrejos decápodos (Watts et al., 2015; Waite et al., 2018; Akhbarizadeh et al., 2018; Horn et al., 2019; Ferreira et al., 2020; Xu et al., 2020). Así, Costa et al. (2019) encontraron mayores valores porcentuales de fibras (93%) de MP en O. quadrata en Brasil. Renzi et al. (2020) observaron mayores porcentajes de fibras de MP en el cangrejo marino C. sapidus, siendo 67% en el estómago y 33% en las gónadas. Torn (2020) encontraron la presencia de fibras de MP en R. harrisii. Es posible que la alta frecuencia de fibras de MP presente en R. setosum se deba a que sean más abundantes, se suspenden más fácilmente por la acción de las olas y son más «pegajosas» a la biota (Horn et al., 2019).
El segundo grupo de MP fueron los fragmentos (4.60±3.07). Brennecke et al. (2015) mostraron la ocurrencia de fragmentos de MP entre 180 y 250 ìm de tamaño en el estómago, branquias y hepatopáncreas del crustáceo marino Uca rapax (Smith, 1870), Stasolla et al. (2015) señalaron la presencia de fragmentos de MP en el estómago de Charybdis longicollis Leene, 1938, y Akhbarizadeh et al. (2018) evidenciaron la presencia de fragmentos en las branquias y el músculo de Portunus armatus (A. Milne-Edwards, 1861). El impacto de los fragmentos en los organismos acuáticos incluye daño tisular, crecimiento reducido, baja condición corporal e incluso mortalidad.
Los films «películas» se presentaron con 2.07±1.39 partículas de MP / R. setosum. Se ha observado la presencia de films de MP en Carcinus aestuarii Nardo, 1847 y C. sapidus (Piarrulli et al., 2020; Waddell et al., 2020). Sin embargo, Renzi et al. (2020) no encontraron la presencia de películas «films» en el crustáceo marino C. sapidus.
Con relación a los colores de MP de R. setosum, las fibras azules de MP fueron más abundantes en el músculo, las azules y rojas de MP en las branquias, y las negras y azules en el tracto digestivo. En el caso del MP tipo film, el color blanco fue el dominante en el músculo y en el tracto digestivo, en tanto que el verde dominó en las branquias, mientras que en el caso de los fragmentos, el color azul fue el más abundante en las branquias y en el tracto digestivo, no habiendo fragmentos en el músculo. Estos resultados son concordantes con otros reportes en otras especies de cangrejos decápodos que indican que las fibras con colores negro y azul fueron los más frecuentes (Waite et al., 2018). Las fibras de estos dos colores se originan a partir del nailon de las actividades de pesca, de las cuerdas de los barcos y de las fibras de la ropa en las aguas residuales (Costa et al., 2019).
Una posible fuente de MP son las aguas de los ríos Rímac, Chillón y Lurín, cercanos a la zona de donde provienen los crustáceos de la presente investigación. Por ejemplo, a lo largo del río Chillón se encuentran industrias que usan plásticos como envases y que vierten los residuos sólidos al río, las cuales final- mente llegan al mar. Las cuencas bajas de estos ríos están sufriendo un proceso de deterioro ambiental como resultado de una falta de tratamiento y manejo de los residuos líquidos y sólidos, y por la inexistencia de condiciones sanitarias básicas en gran parte de esta cuenca (Gallarday y Bedia, 2021).
La LC de R. setosum se observó correlacionada con el número de partículas de MP, con el músculo y con el color azul. Opuestamente, otros estudios señalaron que los tamaños más pequeños del crustáceo decápodo Nephrops norvegicus (Linnaeus, 1758) presentaron mayores niveles de MP, lo cual podría ser el resultado de su morfología intestinal, que presenta un molino gástrico, con un conjunto de placas quitinosas que se encuentran en el intestino anterior (Welden y Cowie, 2016).
En la evaluación por sexo no se observó diferencia significativa por el número de partículas de MP total. Otros estudios señalan que las hembras de N. norvegicus presentan mayor cantidad de MP en el tracto digestivo (Welden y Cowie, 2016, 2018).
Los MP detectados en el crustáceo marino como los cangrejos R. setosum son motivo de preocupación por su potencial efecto negativo en la seguridad alimentaria, ya que estos crustáceos forman parte de la dieta del humano. Los impactos dependerán de las tasas y patrones de consumo (por ejemplo, especies y partes anatómicas consumidas de los crustáceos). Los registros sobre la contaminación por MP de los productos del mar, en particular los tejidos comestibles, son muy limitados, por lo que se desconoce el riesgo de consumo de MP para la salud humana (Wright y Kelly, 2017; Prata et al., 2021). Se consideran tres posibles impactos: 1) la toxicidad de las partículas de plástico más pequeñas al interactuar o translocar a tejidos y células; 2) la toxicidad química debido a la lixiviación de aditivos añadidos a los MP durante su fabricación o la liberación de contaminantes como metales pesados que se han acumulado en los plásticos en el ambiente marino y 3) los riesgos de enfermedades debido a la contaminación bacteriana de los MP (Sana et al., 2020).
La toxicidad dependerá de la concentración de MP en el alimento marino, pero, por otro lado, se carece de una base sólida de pruebas de los niveles de exposición (Wright y Kelly, 2017). Se ha estimado que un coreano promedio ingiere 212 partículas al año a través del consumo de productos marinos, mientras que los consumidores europeos de mariscos ingieren entre 1800 a 11000 MP anualmente, en tanto que los consumidores chinos podrían alcanzar una mayor exposición alimentaria (Li et al., 2015; Cho et al., 2019). De hecho, la exposición humana a los MP varía significativamente en cada región del mundo (De-la-Torre, 2019). Por otro lado, las investigaciones de MP en crustáceos acuáticos señalan que las concentraciones de exposición son relativamente bajas, posiblemente debido a las limitaciones técnicas en el muestreo y en la identificación de MP (Wright y Kelly, 2017).
CONCLUSIONES
Todos los individuos (n=15) de Romaleon setosum presentaron microplásticos (MP) en músculo, branquias y tracto digestivo.
Las fibras azules de MP fueron más abundantes en el músculo, las azules y rojas en branquias, y el negro y azul en el tracto digestivo.
En las MP de tipo film, el color blanco fue el dominante en el músculo y en el tracto digestivo, y el verde en la branquia.
En fragmentos de PM, el color azul fue el más abundante en la branquia y en el tracto digestivo, y no se encontró en el músculo.
El número de partículas de MP presentó la siguiente secuencia: tracto digestivo > branquia > músculo, así como el siguiente orden con relación a su forma: fibra > fragmento > film, con dominancia del color azul y negro.
La longitud del cefalotórax de R. setosum presentó una correlación significativa con el número de partículas de MP in toto del cangrejo, con el músculo y con el color azul.












 uBio
uBio 

