INTRODUCCIÓN
Los cestodos del orden Cyclophyllidea son helmintos endoparásitos obligados, los cuales incluyen los cestodos más importantes involucrados en la salud humana y animal (Schmidt, 1986). El cuerpo de los ciclofilideos es largo, parenquimatoso, acelomado y consta de segmentos llamados proglótides. Además, tienen un escólex con cuatro ventosas musculares posicionadas radialmente y pueden presentar un róstelo (Wardle y McLeod, 1952).
Diversos estudios han demostrado la ocurrencia de anomalías anatómicas en diferentes especies de ciclofilideos (Koubek, 1986; Lyons et al., 1997; Yanagida et al., 2010). Estas anomalías incluyen un mayor número de ventosas, escólex y róstelo, así como anomalías morfológicas de los ganchos rostelares (Schiller, 1973). Las anomalías internas generalmente implican una variación en el número y la posición de los ovarios, testículos, poros y glándulas genitales (Cho et al., 1967; Fan et al., 2001). Asimismo, la distribución polirradiada, pentaradiada, tetraradiada y trirradiada de los estróbilos y proglótides son incluidas en las anomalías anatómicas (Foster, 1915).
Un cestodo trirradiado, término aceptado por muchos parasitólogos, se caracteriza por tener un estróbilo conformado por tres alas en el mismo eje (Foster, 1915; Schiller, 1973; Lyons et al., 1997). Esta anomalía se ha informado en muchas especies de cestodos, las cuales incluyen a Anoplo- cephala perfoliata, Dipylidium caninum, Hydatigera taeniaeformis, Taenia solium, Taenia saginata, Taenia hydatigena, Taenia pisiformis y Taenia multiceps, principalmente (Yoshida, 1913; Foster, 1915; Lyons et al., 1997).
Estas anomalías anatómicas pueden causar confusión y dificultad en el diagnóstico morfológico de los cestodos (Rao y Ayvar, 1932), por lo que es necesario desarrollar métodos analíticos moleculares para ayudar en la identificación de parásitos (Yanagida et al., 2010). Este informe presenta un hallazgo novedoso de T. multiceps trirradiado recolectado de un perro doméstico en la sierra peruana. Se estudia la caracterización morfológica y molecular de los parásitos y su comparación con cestodos normales.
MATERIALES Y MÉTODOS
En febrero de 2014, una perra fue atropellada y murió en la carretera entre Cuzco y Puno en el distrito de Maranganí, provincia de Melgar, región de Cusco, Perú (3700 msnm). El animal fue sometido a necropsia en el Centro de Investigación IVITA, sede Maranganí, de la Universidad Nacional Mayor de San Marcos. Se colectaron 327 cestodos del intestino delgado, se lavaron en solución salina al 0.8%, se fijaron en formaldehído caliente al 4% y se conservaron en etanol al 70%. Algunas proglótides grávidas se conservaron en etanol absoluto antes de la fijación para estudios moleculares.
Para el diagnóstico morfológico, los cestodos se tiñeron con carmín-clorhídrico y se deshidrataron en una serie ascendente de alcohol hasta etanol absoluto. Los cestodos se aclararon en aceite de clavo y se montaron en láminas portaobjetos usando bálsamo de Canadá. El escólex y algunas proglótides grávidas se montaron en medio de Berlese para facilitar la observación de los ganchos rostelares y los huevos. Las fotografías se tomaron usando un microscopio Carl Zeiss, Axioskop 40. Las medidas se tomaron usando el programa Leica IM50 v. 4.0 R117. Las medidas están expresadas en micrómetros, a menos que se indique lo contrario, y se expresan en rango con el valor promedio entre paréntesis. La nomenclatura taxonómica utilizada en este estudio está de acuerdo con Loos-Frank (2000) y Rausch (1994).
El ADN fue extraído de proglótides grávidas conservadas en etanol, utilizando un kit comercial (DNeasy Blood & Tissue Kit, QIAGEN, Alemania). Se amplificó un fragmento de aproximadamente 400 pares de bases (pb) del gen mitocondrial citocromo c oxidasa subunidad 1 (cox1) utilizando un protocolo de reacción en cadena de la polimerasa (PCR), adoptado de Liu et al. (2011), utilizando los cebadores JB3 y JB4.5 (Bowles y McManus, 1994). Los amplicones se analizaron mediante electroforesis en gel de agarosa al 1.5% y posteriormente se visualizaron con tinción con bromuro de etidio. Los productos positivos de PCR se secuenciaron utilizando un secuenciador automático ABI 3100 (Applied Biosystems). Todas las secuencias se compararon consecuencias de referencia en el GenBank utilizando ClustalX (http://www.clustal.org/). Se utilizó el software MEGA-X (http:// www.megasoftware.net/) para crear un árbol filogenético mediante el método de unión de vecinos (neighbour-joining method) con la distancia de 2-parámetros de Kimura. Las secuencias de nucleótidos se registraron en la base de datos GenBank. Los especímenes fueron depositados en la Colección de Parásitos del Laboratorio de Epidemiología y Economía Veterinaria de la FMV-UNMSM (Resolución de la Dirección General N.° 023- 2018-MINAGRI-SERFOR-DGGSPFFS) ubicada en Lima, Perú (número de registro FMV-599).
RESULTADOS
Todos los cestodos recolectados (n=327) fueron identificados como T. multiceps mediante diagnóstico morfológico y mediciones de los ganchos rostelares. Algunos especímenes fueron confirmados mediante el diagnóstico molecular. Tres cestodos mostraron anomalías morfológicas que fueron clasificadas como cestodos trirradiados según la nomenclatura propuesta por Foster (1915), mientras que los otros cestodos tuvieron apariencia normal. Todos los cestodos trirradiados se confirmaron molecularmente como T. multiceps.
Descripción de Cestodos Trirradiados (n = 3)
El estróbilo de estos cestodos anormales estaba formado por tres alas que irradiaban desde un eje común creando una forma trirradiada o prismática. Las alas de cada cestodo eran de tamaño similar y estaban dispuestas en el mismo ángulo produciendo una forma trirradiada uniforme (Figura 1A). Todos los cestodos estaban grávidos con longitudes de 30.10-38.70 (33.80) cm con 168- 183 (174) proglótides craspedotes. Se midió un ancho máximo de 3.84-4.82 (4.31) mm en proglótides grávidos justo después de la línea media. El escólex fue globular, de 1095-1184 (1140) µm de ancho, tenía seis ventosas que medían 311-334 (325) µm de ancho máximo (Figura 1C). El róstelo midió 324-340 (330) µm de diámetro, estaba armado con dos filas de ganchos (grandes n=3-4 y pequeños n=15- 18). Los ganchos grandes medían 130-164
(152) µm de largo y los pequeños 116-124 (120) µm de largo. Algunos de los ganchos grandes tenían una morfología anormal.
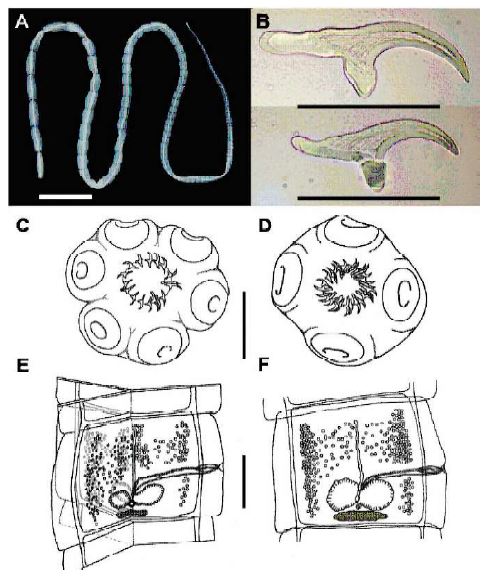
Figura 1 (A) Ejemplar completo de Taenia multiceps trirradiado. Escala = 2.0 cm. (B) Características de los ganchos rostelares de T. multiceps normal. Escala = 100 µm. (C y E) Morfología del escólex y proglótide maduro de T. multiceps trirradiado. (D y F) Morfología del escólex y proglótide maduro de T. multiceps normal. Escala en C y D = 500 µm. Escala en E y F = 1000 µm
Las proglótides maduras medían 1.98- 2.14 (2.08) mm de largo y 2.75-3.70 (2.93) mm de ancho máximo. El ancho máximo se midió entre los bordes de dos alas adyacentes. Las proglótides contenían un poro genital que se alternaba irregularmente en el medio del margen lateral. El poro genital estaba ubicado en una de las tres alas de la proglótide (Figura 2). El atrio genital medía 121-225 (151) µm de largo por 188-588 (432) µm de ancho. Cada proglótide madura tenía entre 273 y 348 (306) testículos, los cuales se dis- tribuyeron en las tres alas y se distribuyeron en la zona anterior y lateral a los ovarios, entre los canales osmorreguladores longitudinales. Los testículos ocuparon principalmente toda la parte lateral de la proglótide con excepto de la región poral. Los testículos eran morfológicamente ovalados a subesféricos y medían 35-106 (76) µm de largo por 28-76 (63) µm de ancho. El saco del cirro medía 189-398 (345) µm de largo y 112-165 (142) µm de ancho, fue alargado y se extendió a lo largo del canal ventral longitudinal. Los conductos deferentes distales estaban enroscados (por lo general con 1 a 2 asas) dentro del saco cirro. Los conductos deferentes proximales estaban ondulados (Figura 1E).
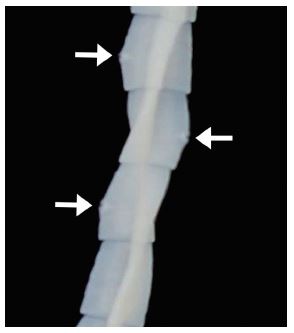
Figura 2 Morfología de las proglótides maduras de Taenia multiceps trirradiado. Nótese que el poro genital está ubicado en el margen de las tres alas
El ovario midió 375-502 (432) µm de largo y 986-1138 (1045) µm de ancho, tenía forma trilobulada y se distribuía medialmente a la cara posterior de la proglótide. El ancho máximo se midió entre los bordes de los dos lóbulos adyacentes. Los lóbulos antiporal y poral eran morfológicamente similares en tamaño. La glándula vitelógena midió 680-874 (774) µm de largo y 144-172 (157) µm de ancho, era trilobulado y se situaba debajo del ovario. El poro vaginal se abrió debajo del saco cirro. La glándula de Mehlis midió 152- 217 (188) µm de largo y 152-170 (164) µm de ancho, tenía forma ovalada o subesférica (Figura 1E).
Las proglótides grávidas tenían un útero ramificado con su tronco principal atravesando el centro de la proglótide trirradiada, con ramas laterales hacia cada ala. Los huevos tenían apariencia normal con seis ganchos cada uno.
Descripción de Cestodos Normales (n = 10)
Todos los cestodos eran de tamaño mediano y estaban grávidos. La longitud de los estróbilos fue de 29.30-48.00 (39.46) cm y 4.30-5.23 (4.85) mm de ancho máximo cerca de la línea media de las proglótides grávidas. El escólex era globular y medía 988-1042 (1004) µm de diámetro. Cada escólex tenía cuatro ventosas musculares que medían 284- 315 (298) µm de diámetro (Figura 1D). El róstelo midió 265 a 366 (328) µm de diámetro, estuvo armado con dos filas de 14 a 16 ganchos cada uno. Los ganchos grandes medían 152-165 (158) µm de largo y los pequeños 120-148 (132) µm (Figura 1B, Cuadro 1).
Las proglótides maduras medían 2.14- 2.71 (2.34) mm de largo y 2.19-3.26 (2.73)
mm de ancho (Figura 1F). Los poros genitales de las proglótides se alternaban irregularmente y se ubicaban en el medio de los márgenes laterales de cada proglótide. El atrio genital midió 118-229 (158) µm de largo por 191-600 (437) µm de ancho. El número de testículos varió entre 264 y 374 (302) y se distribuyeron anterior y lateralmente al ovario entre los canales osmorreguladores longitudinales. Los testículos se distribuyeron a lo largo de las zonas laterales de cada proglótide, excepto en la región poral. Los testículos tenían una morfología ovalada a subesférica con medidas de 32-104 (72) µm de largo y 25-85 (62) µm de ancho. El saco del cirro se extendía a lo largo del canal ventral longitudinal, era alargado y medía 192-412 (334) µm de largo y 101-168 (150) µm de ancho. Los conductos deferentes distales estaban enroscados dentro del saco cirro. El conducto deferente proximal estaba enrollado. El ovario midió 416-502 (549) µm de largo y 949-1350 (1151) µm de ancho, estaba bilobulado y se distribuía medial y posterior de la proglótide. Los lóbulos del ovario antiporal y poral eran morfológicamente similares. La glándula vitelógena medía 817-1091 (969) µm de largo y 138-221 (168) µm de ancho y estaba situada debajo del ovario. El poro vaginal se abrió debajo del saco cirro y los conductos deferentes. La glándula de Mehlis era ovalada o subesférica y medía 150-221 (185) µm de largo y 151-182 (163) µm de ancho. Las proglótides grávidas tenían un útero ramificado con su tronco principal con ramas laterales hacia cada lado. Los huevos tenían apariencia normal con seis ganchos cada uno.
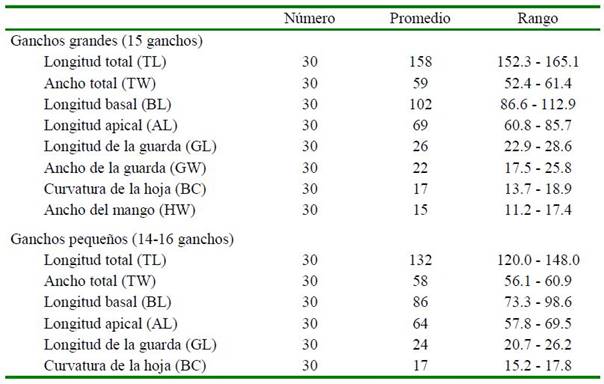
Cuadro 1 Medidas del gancho (en µm) de la Taenia multiceps normal aislada de un perro doméstico. Los parámetros seleccionados (y abreviaciones) se basaron en el sistema utilizado por Haukisalmi et al. (2011)
Diagnóstico Molecular
Las secuencias de nucleótidos del gen cox1 fueron generados a partir de muestras PCR- positivas de los tres cestodos trirradiados (aislamientos 1, 2 y 3) y dos cestodos normales (aislamientos 7 y 8). Las secuen cias del cestodo trirradiado (GenBank No. KX511888, KX511889 y KX511890) y de los cestodos normales (GenBank No. KX511891 y KX511892) eran idénticas entre sí y tenían más de 99% de similitud con otras secuencias publicadas y registradas anteriormente en el GenBank para T. multiceps (Figura 3).
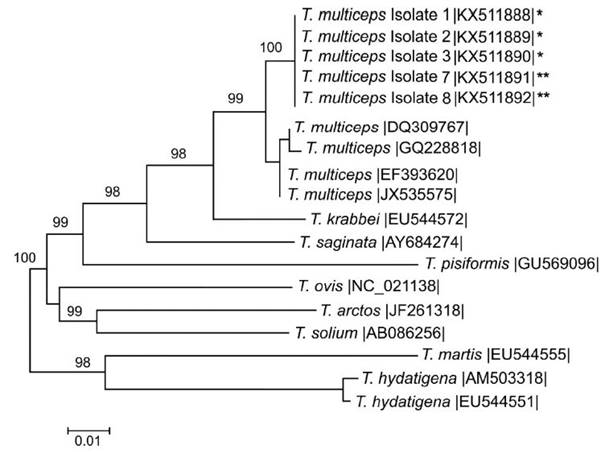
Figura 3 Relación filogenética de Taenia multiceps colectados de un perro de Cusco, Perú, y otras secuencias de T. multiceps inferidas por el método de unión de vecinos (neighbour-joining method) de las secuencias parciales del gen cox1. El número de acceso a la secuencia está entre las barras verticales (|). La secuencia marcada con un asterisco (*) es de T. multiceps trirradiado y con dos asteriscos (**) es de T. multiceps normal. La barra de escala indica 1 sustitución por cada 100 posiciones de nucleótidos
DISCUSIÓN
Estudios previos han demostrado la ocurrencia de anomalías en diversas especies de cestodos, siendo los estróbilos polirradiados los más comunes registrados en el género Taenia (Foster, 1915; Faust, 1925; Thatcher, 1972). El diagnóstico de una Taenia polirradiada es difícil, debido a que los especímenes pueden tener alteraciones morfológicas en sus ganchos rostelares, una estructura anatómica principal para el diagnóstico de la especie del género Taenia (Rao y Ayvar, 1932; Loos-Frank, 2000). En este estudio, tres cestodos trirradiados recolectados de un perro presentaron alteraciones en el número de ganchos rostelares y una morfología anormal, por lo que fue necesario el uso de análisis moleculares para identificar la especie. El análisis de códigos de barras de ADN del gen cox1, un gen capaz de distinguir especies de la familia Taeniidae (Zhang et al., 2014), confirmó que las muestras correspondían a T. multiceps.
En este estudio, los especímenes de T. multiceps trirradiados tenían un escólex con seis ventosas, una característica similar a todos los casos reportados previamente sobre cestodos trirradiados. Asimismo, los estróbilos de los especímenes trirradiados de T. multiceps estaban completamente desarrollados. Los proglótides maduros y grávidos mostraron órganos internos. El desarrollo de los testículos, ovario, glándula vitelógena y útero ramificado fue homogéneo en las tres alas de cada proglótide. Como ocurre con las proglótides maduras normales, el ovario, la glándula vitelógena y la glándula de Mehlis ocuparon la porción central de cada proglótide. Los huevos tenían morfología normal y embriones hexacantos normales. Estas características anatómicas también se observaron en otros casos de cestodos trirradiados (Yoshida, 1913; Foster, 1915; Rao y Ayvar, 1932).
Las medidas del cuerpo y de los órganos internos del T. multiceps normal y trirradiado fueron muy similares entre ellos. Solo el tamaño del escólex fue ligeramente mayor en T. multiceps trirradiado, debido a la presencia de seis ventosas. Un hallazgo interesante fue el número y tamaño de los testículos, ya que las muestras de T. multiceps normales y trirradiadas tenían un número similar de testículos (264-374 y 273-348, respectivamente), así como órganos sexuales de tamaño similar.
Las causas de las anomalías morfológicas en los cestodos son desconocidas. Estudios previos han mencionado anomalías en los huevos de cestodos (Foster, 1915). La principal anomalía descrita fue el aumento del número de ganchos de las oncosferas (Lubinsky, 1958, 1959). Por ejemplo, Yoshino (1933) describió oncósferas de T. solium que tenían entre 8 y 18 ganchos. En algún momento se pensó que las anomalías polirradiadas en cestodos comenzaban en las oncósferas; sin embargo, se han encontrado metacestodos anormales en algunas especies de cestodos Taeniidae, los cuales tenían un número mayor de ventosas en el escólex; es decir, más de cuatro ventosas (Lubinsky, 1959; Tiðin, 1971; Sakamoto, 1978). Esta anomalía también se ha encontrado en metacestodos de T. multiceps, comúnmente llamado cenuro (Tiðin, 1971; Chervy, 2002). Tiðin (1971) describió un cenuro que tenía protoescólices normales y anormales, donde estos últimos tenían seis ventosas. Como se sabe, un cenuro se origina a partir de un huevo y consiste en un quiste donde se desarrollan muchos escólices; por lo tanto, es probable suponer que un cestodo polirradiado se origina en un metacestodo y no en una oncósfera.
Aún no se sabe si estas anomalías en los cestodos pueden tener algún impacto en los hospederos. Recientemente se ha documentado cestodiasis maligna causada por algunas especies de cestodos Taeniidae en humanos y animales (Olson et al., 2003; Muehlenbachs et al., 2015). Estos informes mencionan la invasión del tejido humano por células de cestodos anormales y en proliferación alterada (Goldberg et al., 2014; Muehlenbachs et al., 2015). Sin embargo, en ambos casos no se evaluó la estructura anatómica de los cestodos adultos. Es necesario realizar futuros estudios para evaluar si estas anomalías en los cestodos tienen algún efecto en los hospederos.












 uBio
uBio 

