Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Ecología Aplicada
versión impresa ISSN 1726-2216
Ecol. apl. vol.12 no.2 Lima ago./dic. 2013
ARTÍCULOS ORIGINALES
Patogenicidad de Beauveria bassiana (Bals) Vuill., sobre el gusano defoliador del maracuyá Dione juno (Cramer) (Lepidoptera: Nymphalidae) en laboratorio
Pathogenicity of Beauveria bassiana (Bals) Vuill against the "passion fruit butterfly Dione juno (Cramer) (Lepidoptera: Nymphalidae) in the laboratory
Jenny Malpartida-Zevallos1, Mónica Narrea-Cango2 y William Dale-Larraburre3
1 Museo de Entomología Klaus Raven Büller – Universidad Nacional Agraria La Molina. Apartado 456, Lima 100, Perú. E-mail: jmalpartida@lamolina.edu.pe.
2 Departamento de Entomología. Facultad de Agronomía. Universidad Nacional Agraria La Molina. E-mail: mnarrea@lamolina.edu.pe.
3 Departamento de Entomología. Facultad de Agronomía. Universidad Nacional Agraria La Molina. E-mail: wdale@lamolina.edu.pe.
Resumen
Los hongos entomopatógenos constituyen una alternativa en el manejo integrado de muchas plagas. En el presente trabajo se determinó la patogenicidad del hongo Beauveria bassiana (Bals.) Vuill., para uso potencial como agente de control biológico contra larvas de tercer estadío del "defoliador del maracuyá" Dione juno (Lepidoptera: Nymphalidae), una plaga importante del maracuyá. El aislamiento evaluado mediante aplicación directa de suspensiones de 106, 107 y 108 conidias mL-1 pertenece a la colección comercial del Servicio Nacional de Sanidad Agraria SENASA y registró una mortalidad en las larvas de D. juno, entre 20% y 84% al cuarto día. La CL50 y la CL95 fueron de 9.39 x 106conidias mL-1, y 1.42 x 108conidia mL-1respectivamente, por lo que se concluye que la cepa CCB-LE 262 de Beauveria bassiana (Bb SENASA) tiene un gran potencial como controlador biológico de D. juno.
Palabras clave: Control Biológico, Beauveria bassiana, Dione juno, maracuyá.
Abstract
Entomopathogenic fungi are a real alternative in insect pest integrated management. In the present study, pathogenicity of the Beauveria bassiana fungus and its potential use as a biological control agent against white grub third instar larvae of the"passion fruit butterfly" Dione juno, (Lepidoptera: Nymphalidae) a very important pest of passion fruit, was determined. Isolation evaluated by direct application of conidia suspensions of 106, 107 y 108 mL-1 belongs to the commercial collection of Servicio Nacional de Sanidad Agraria (SENASA), and mortality registered on larvae ranged from 20 to 84 %. The LD50 and LD95 were de 9.39 x 106conidia mL-1 y 1.42 x 108 conidia mL-1, respectively in the fourth day. The Beauveria bassiana isolate CCB-LE 262 (Bb SENASA) was found to be efficient in the control of D. juno, hence showing a high potential as a biological control agent.
Key words: Biological control, Beauveria bassiana, Dione juno, yellow passion fruit.
Introducción.
El maracuyá (Passiflora edulis Sims) es una planta trepadora y originaria de la Amazonía brasileña, que se cultiva ampliamente en países tropicales y subtropicales. Esta planta tiene problemas en la polinización, dependiendo de insectos como abejas y abejorros para polinizarse. Otro factor adverso son las plagas entre las que se mencionan: moscas de la fruta, Anastrepha spp. y Ceratitis capitata (Wied.); pulgones Myzus persicae (Sulzer) y Aphis gossypii Glover; al ácaro Tetranychus y a los lepidópteros Dione juno (Cramer) y Agraulis vanillae (L.). De todos ellos D. juno llamado "gusano defoliador del maracuyá" es la más importante, defolia parcial o totalmente la planta y en consecuencia ocasiona pérdidas en la producción. Esta plaga se distribuye en EEUU, Las Antillas, Guyana, Surinam y en América del Sur, desde Colombia hasta Argentina (Toledo, 1991). Las larvas de D. juno son negras con grandes verrucas que le dan una apariencia espinosa y desagradable, tiene 5 estadíos y en todos ellos mantiene un comportamiento gregario. Cada estadío dura en promedio 4 días, por lo que completa su desarrollo larval entre 19 a 27 días, a una temperatura promedio de 25ºC; los adultos son mariposas de alas anaranjadas con márgenes oscuros que oviponen en promedio unos 70-150 huevos por postura, completándose su ciclo biológico en aproximadamente 38 a 42 días (Gallo et al,. 2002; Molina-Moreira & Arias De López, 2006).
En el control químico a esta plaga, se recomienda Malathion 57% (400cc/cilindro de agua) el cual es efectivo pero afecta seriamente a los polinizadores y con ello la producción de frutos. Dentro del control biológico, se recomienda a Bacillus thuringiensis (300g/h), y VPN-Dione (2LE/l de agua), pero no se menciona ninguna especie de hongo entomopatógeno, lo cual llama la atención, considerando que estos bioplagucidas son responsables de muchos éxitos en el control biológico, como lo es Beauveria bassiana, una especie que es producida en muchos países y que está asociada precisamente al control de lepidópteros y coleópteros.
B. bassiana, al igual que otros hongos entomopatógenos, antes de matar a su hospedero le causa síntomas importantes como son: pérdida de sensibilidad, falta de coordinación, letargo, inapetencia, melanización y parálisis. Con la muerte del insecto, el beneficio se incrementa pues la esporulación y posterior dispersión del hongo, permite un control más allá de la aplicación (Estrada et al., 1997; Vargas, 2003; Malpartida, 2004).
Teniendo en cuenta todos estos aspectos, se realizó el presente ensayo, con el fin de estudiar una cepa comercial de B. bassiana en el control de larvas de D. juno, evaluando su patogenicidad, sintomatología, efecto en la alimentación y caracterización morfológica, además de determinar la CL50 y CL95. Estableciendo de esta manera si constituye o no, una alternativa eficiente de control biológico del "gusano defoliador del maracuyá".
Materiales y métodos.
Insecto –Plaga. Se colectaron larvas del 3er estadío de D. juno de una planta de maracuyá ubicada en los alrededores de la Facultad de Agronomía de la Universidad Nacional Agraria La Molina. Esta planta de naturaleza ornamental, no registraba ninguna aplicación de bioplaguicidas ni ningún otro plaguicida. Las larvas colectadas fueron colocadas en tapers ventilados y llevadas al laboratorio de Sanidad de la Municipalidad de Miraflores, donde fueron evaluadas, siendo seleccionadas para el ensayo aquellas que mostraron mayor actividad y capacidad de alimentación (Figura 1). El laboratorio en mención, durante todo el ensayo registró una temperatura promedio de 22+/-1ºC y una humedad entre 60-70% de humedad relativa.

Cepa de B. bassiana. La cepa seleccionada (código CCB-LE 262) fue proporcionada por el Servicio Nacional de Sanidad Agraria del Perú (SENASA) a partir de su producción comercial, que utiliza arroz como sustrato de crecimiento, identificándose por lo tanto a la cepa como Bb-SENASA.
Pruebas de Patogenicidad, evaluación de la sintomatología y alimentación. Se siguió el siguiente procedimiento tomado de González et al., 1993 y Bustillo & Marín, 2002, con algunas modificaciones:
-
Las larvas colectadas se desinfectaron con hipoclorito de sodio al 0.5% y luego se enjuagaron 3 veces con agua destilada estéril, antes de secarlas en papel toalla estéril. Se escogieron 125 larvas activas y se colocaron en grupos de 25 individuos en placas estériles de 50 mL.
-
De la presentación comercial de B. bassiana, se preparó una solución madre del 109 conidias mL-1 adicionado a la misma 1 gota del tween al 0.1% como agente dispersante. A partir de esta solución se prepararon 3 concentraciones seriadas con un factor de dilución 0.1, para obtener: 106, 107 y 108 conidias mL-1 a las que se identificó como T1, T2 y T3, respectivamente.
-
Las larvas desinfectadas se inocularon por inmersión durante 2 minutos en 10 mL., de cada una de las concentraciones preparadas (T1, T2 y T3). Luego las larvas fueron colocadas sobre papel toalla, para eliminar el exceso de humedad y trasferidas en grupos de 5 individuos a placas petri, acondicionadas con un disco de papel filtro e identificadas con el código de la concentración. (25 larvas por tratamiento)
-
Para el testigo se emplearon larvas a las que se le aplico la misma metodología, pero usando una solución de agua destilada estéril con 1 gota de tween al 0.1%.
-
Como alimento, se colocó en cada placa, discos de 2cm. de diámetro de hojas de maracuyá de la planta hospedera, previamente lavadas y desinfectadas. El recambio se hizo en forma diaria o antes si eran totalmente consumidas.
-
Las observaciones fueron 2 veces al día y a la misma hora, evaluándose los síntomas como el color y alimentación de la larva. Este último parámetro, se determinó midiendo el área foliar consumida, mediante cálculo diferencial entre el área foliar inicial y el área foliar remanente después del consumo. El consumo diario promedio por larva fue determinado dividiendo el consumo total diario entre el número de individuos vivos.
-
La mortalidad se determinó por la ausencia de movimiento de la larva al ser tocada, con un hisopo estéril. Para confirmar el agente causal, los insectos muertos se colocaron en placas petri con papel húmedo con 5 gotas de agua estéril y dejadas en cámara oscura hasta la emergencia del hongo.
El diseño experimental utilizado fue completamente al azar, empleándose 25 insectos por tratamiento, con 5 repeticiones. Los tratamientos fueron las 3 concentraciones y 1 testigo sin aplicación. La mortalidad de las larvas de D. juno se expresó como porcentaje de mortalidad y con los resultados de cada repetición se calculó la mortalidad total y se corrigió con arcoseno para cumplir con los supuestos de normalidad y homogenidad de la varianza (Little & Jackson, 1989). Posteriormente estos datos fueron sometidos a un análisis de varianza (ANOVA) y prueba de Duncan (P < 0.05) (SAS Institute, 1989). Finalmente se realizó el análisis Probit (CIPSTAT, 2006), para calcular la CL50 y CL95 de la población a través de la ecuación de regresión.
Caracterización fisiológica de la cepa Bb-SENASA. Es una indicación primordial realizar controles sobre las propiedades de los hongos entomopatógenos comerciales, que aseguren un producto de máxima eficacia en condiciones de campo (Vélez et al.,1997; Carballo, 1998). Por ello, como parte del ensayo y para comprobar las propiedades de la cepa, se evaluaron 2 características fisiológicas: crecimiento radial y porcentaje de germinación, empleando el medio Agar Sabouraud Dextrosa (SDA) y siguiendo la metodología de Varela & Morales (1996) y Vélez et al. (2000):
-
Crecimiento Radial.
Porcentaje de Germinación
Resultados y discusión.
Patogenicidad, Sintomatología y Alimentación. El ensayo fue evaluado hasta el 6to día (Figura 2), sin embargo para la obtención de la CL50 y demás análisis estadístico, los tratamientos fueron comparados al 4to día de la inoculación (antes del llegar al 100% de mortalidad). En la Tabla 1, se presentan, los porcentajes de mortalidad obtenidos en el ensayo, para el testigo y los demás tratamientos, así como el análisis estadístico que establece la separación entre medias y que señala diferencias significativas (P< 0.05) entre los tratamientos.
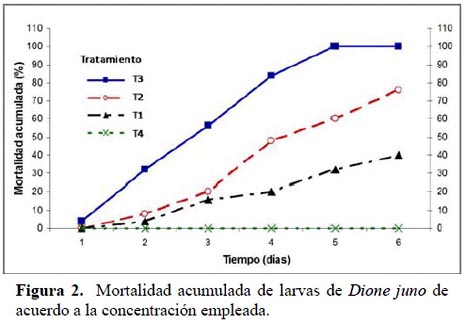
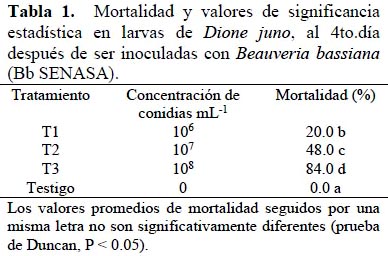
De acuerdo a los resultados, se observa que entre todos los tratamientos hubo diferencias entre sí y con el testigo, además de que este último no registró ninguna mortalidad mientras duró el ensayo. Observamos también que la mortalidad en los 3 tratamientos fue directamente proporcional a la concentración de conidias, siendo que al 4to día, el T3 fue el más efectivo, con un 84% de mortalidad que llegó al 100% un día después. La curva de mortalidad a través del tiempo, originada a dicha concentración fue diferente a las producidas por las concentraciones de 107 y 106 conidias mL-1, con las que se alcanzó el 48 y 20 % de mortalidad respectivamente al 4to día y 60 y 32% % en el 5to día posterior a la inoculación. Estos resultados son cercanos a los obtenidos por otros autores, en otros lepidópteros, bajo similares condiciones de laboratorio; así Solis-Soto et al. (2006) a una concentración de 2.4 x 108 conidias mL-1, obtuvieron una mortalidad del 93% en larvas de Cydia pomonella L (Tortricidae), mientras que Quintana (2000), con 108 conidias mL-1, logró un 100% de mortalidad en larvas de Rhyacionia buoliana Denis & Schiff (Tortricidae). Por su parte Rodríguez et al. (2006) con la misma concentración obtuvieron al 4to día de inoculación, cerca del 60% de mortalidad en larvas del 3er estadío de Tuta absoluta Meyrick (Gelechiidae), logrando en el 7mo día, una mortalidad del 80%.
Luego de la transformación dosis mortalidad y usando Probit se determinó que la CL50 fue de 9.39 x 106conidias mL-1y la CL95 de 1.42 x 108conidias mL-1, con la ecuación de la recta para Bb-SENASA, de y = 0.916 x – 1.387 (Figura 3). Estos valores también se encuentran dentro de los obtenidos en trabajos similares con otros lepidópteros, así González et al. (1996), reportaron que una cepa de B. bassiana, tuvo una CL50 de 2.44 x 106 conidias mL-1 sobre larvas del 3er. estadío de Ecdytolopha torticornis (Tortricidae). Fuentes & Carballo (1999) encontraron que para Plutella xylostella (Plutellidae), la CL50 y CL95 fue de 2.2 x 105 y 5.1 x 107conidias mL-1 respectivamente, mientras que Solis-Soto et al. (2006), señalan una CL50 de 8.82 x 106 conidias mL-1 para C. pomonella y Rodríguez et al. (2006) para T. absoluta obtuvieron valores de 1.0 x 104,4 y 1.0 x 107,6 conidias mL-1 para la CL50 y CL95 respectivamente.
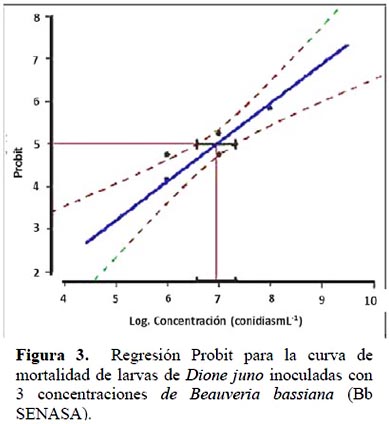
Estos resultados demuestran la efectividad del hongo B. bassiana sobre larvas de lepidópteros y señalan a la concentración de 108 conidias mL-1, como la de mayor efectividad para obtener resultados certeros en la lucha biológica de plagas. Sin embargo se debe tomar en cuenta que, la alta mortalidad observada y los valores de CL50 y CL95 obtenidos en condiciones de laboratorio, no siempre son los que se obtienen bajo condiciones de campo, donde la cantidad de conidias que logran llegar al insecto es generalmente menor; por lo que para su aplicación en campo debe determinarse previamente su concentración.
En cuanto a la sintomatología mostrada en nuestro ensayo, no fue posible determinar la melanización ni el letargo, que caracterizan a las larvas infestadas con B. bassiana y que son reportadas por otros autores en diferentes hospederos (Alves, 1998); debido principalmente a que las larvas sanas de D. juno tienen el tegumento muy oscuro y son evidentemente muy lentas en sus movimientos.
En cuanto al efecto del hongo sobre la alimentación, si fue evidente observar la acción sobre las larvas de D. juno, que a partir del 2do día disminuyeron considerable su apetito (Figura 4). De tal manera que se observa una relación inversamente proporcional entre la concentración empleada y el consumo de hojas (Tabla 2). El testigo a diferencia de los tratamientos, mantuvo una tendencia creciente, en el consumo foliar, excepto en el 4to día, en que disminuyó, muy posiblemente debido, al envejecimiento de las larvas.
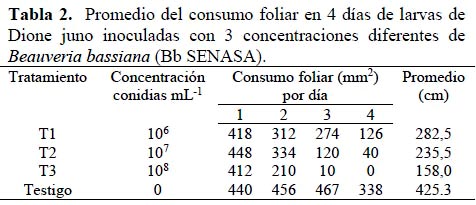

Tomando como patrón el consumo foliar del testigo en un 100%, en la Figura 5, se visualiza la tendencia lineal decreciente en los tres tratamientos. Así se puede observar que al siguiente día de la inoculación, el consumo es casi el mismo, en todas las larvas del ensayo; pero a partir del 2do se observa que las larvas expuestas al tratamiento T3 presentan una reducción significativa del consumo foliar, hasta en un 50% con respecto al testigo, mientras que al 4to día, ya no se registra alimentación. Con respecto a las demás concentraciones, también se observa un marcado efecto del hongo, lo que ocasiona una disminución alimentaría que llega al 4to día hasta 63% y 82% en los tratamientos T1 y T2 respectivamente. Esto demuestra que a mayor concentración, mayor efecto del hongo, lo que origina consecuentemente mayor mortalidad.
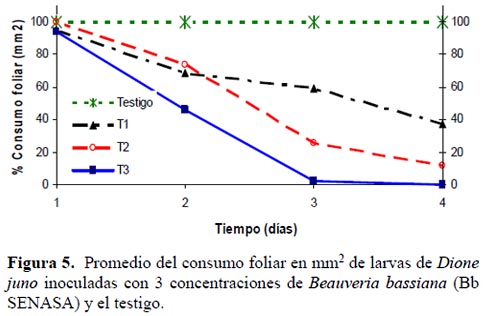
Los resultados obtenidos son superiores a los reportados por Tefera & Pringle (2003) quienes reportaron que a una concentración de 1x108 conidias mL-1 de B. bassiana en larvas del segundo estadío de Chilo partellus (Pyralidae), el consumo de alimentos se redujo en un 70-85%, los mismos autores, señalan que esta reducción es importante pues compensa la acción lenta de los hongos en su efecto mortal sobre el insecto. Además según Alves, 1998, este menor consumo de alimento, puede deberse a la producción de beauvericinas, que actúan como inhibidoras de las reacciones de defensa del hospedero, destruyen la hemolinfa y núcleos de las células.
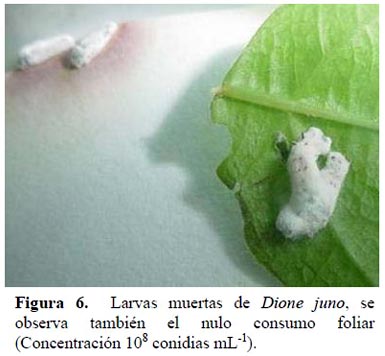
Todas las larvas muertas y mantenidas en cámara húmeda, presentaron micelio entre el segundo y tercer día después de muertas, confirmando a la cepa Bb-SENASA, como el agente causal. Luego del cuarto día se observó la aparición de conidios, que cubrieron totalmente el cuerpo de cada larva (Figura 6). Estas mismas características han sido reportadas para otros insectos por Alves (1998); De la Rosa et al. (1997); Malpartida 2004 y Rodríguez et al. (2006).
Caracterización fisiológica de la cepa Bb SENASA: El crecimiento de las colonias de Bb-SENASA, en la mayoría de las placas, fue expansivo y muy homogéneo; en la Figura 7, se muestra el crecimiento radial promedio hasta el día 10, con una esperada tendencia lineal conforme avanzan los días. En promedio, se registra 35 mm de desarrollo radial, con 80 una TDCR de 3.45 mm.día-1.
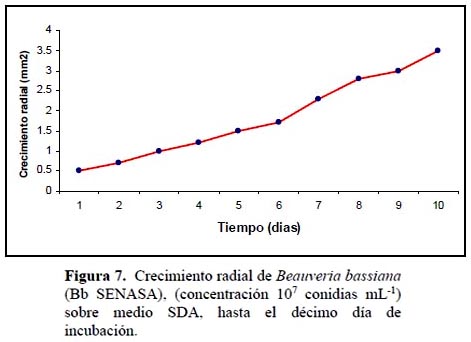
Estos datos son mayores a los reportados 60 por Elósegui & Elizondo (2010), quienes en Agar Papa Dextrosa (PDA) 40 encontraron que una cepa de B. bassiana, hasta el décimo día registró un crecimiento radial, menor a 25 mm., sin embargo hay que considerar que estos autores utilizaron una concentración de sólo 106 conidias mL-1. Por su parte Luna Rodríguez & Leucona (2002), en medio Agar Papa Glucosa reportan que la cepa Bb 142 de B. bassiana tuvo un crecimiento radial de 36,8 mm., a los nueve días; estos autores, si emplearon la misma concentración de este ensayo, pero la alícuota de siembra fue de 3 mL.
La cepa Bb-SENASA, demostró un alto porcentaje de germinación, con un promedio de 94,5%, lo que demuestra la alta viabilidad de sus conidias. Este valor cumple con lo expresado por Velez et al. (1997), quienes señalan que una formulación comercial debe tener una germinación superior al 85% en un tiempo de incubación de 24 horas, ya que al asperjar en campo, el hongo debe tener un rápido efecto sobre la población del insecto que está atacando y un corto periodo de exposición a condiciones ambientales.
Nuestros resultados también demostraron alta similitud con los reportados por otros autores, para diferentes medios de cultivo, superando todos ellos, el 90% de germinación (Elósegui & Elizondo, 2010; Echevarría, 2006).
Conclusiones.
En condiciones de laboratorio la cepa comercial Bb-SENASA de Beauveria bassiana fue patogénica para larvas de Dione juno en el 3er estadío, alcanzando mortalidades del 100% con la concentración 108 conidias ml.L-1, además presenta alta capacidad para disminuir drásticamente el consumo de alimentos al segundo día de aplicación. La CL50 obtenida para esta cepa, fue de 9,39 x 106 conidias ml.L-1 y La CL95 fue de 1,42 x 108 conidias ml.L-1. Estos valores son similares a los reportados para el control de otros insectos, e indican que Dione juno es susceptible de ser controlado por Beauveria bassiana.
La caracterización fisiológica de la cepa Bb-SENASA, indica que esta es una cepa de buena calidad biológica, ya que presenta una germinación cercana al 100% además de tener un buen crecimiento en medios de cultivos artificiales.
Los resultados de esta evaluación, indican que B. bassiana, es una agente de control biológico, que debe ser considerado en un programa de manejo integrado de D. juno, sobre todo si se tiene en cuenta las características del tegumento, y el comportamiento lento y gregario de esta plaga, que sin duda son condiciones que favorecen el desarrollo y efecto del hongo, en el campo. Sin embargo es recomendable hacer ensayos previos, bajo condiciones de campo, para determinar la concentración más óptima, así como las condiciones ambientales más favorables.
Agradecimientos.
Al Dr. Pedro Polo Peinado y al personal de la Gerencia de Salud de la Municipalidad de Miraflores, por las facilidades prestadas en la ejecución de este trabajo.
Literatura citada.
Alves S. 1998. Fungos entomopatogenicos. p. 289-370. In S.B. Alves (ed.). Controle microbiano de insetos. 2nd ed. Fundación de Estudios Agrarios Luiz de Queiroz, Piracicaba, Brasil. 350 p. [ Links ]
Carballo M. 1998. Formulación de hongos entomopatógenos. Revista Manejo Integrado de Plagas Ed. CATIE No 47: 1-4.
CIPSTAT 2006. Programa de determinación Probit. © Centro Internacional de la Papa [ Links ]
De la Rosa W., Godínez J., Alatorre R. & Trujillo J. 1997. Susceptibilidad del parasitoide Cephalonomia stephanoderis a diferentes cepas de Beauveria bassiana y Metarhizium anisopliae. Southwest Entomol 22: 233-242. [ Links ]
Echevarría F. 2006. Caracterización biológica y molecular de aislamientos del hongo entomopatógeno Beauveria bassiana (Bálsamo) Vuillemin. Tesis de Bachiller en Ingeniería en Biotecnología. Escuela de Biología. Instituto Tecnológico de Costa Rica. 105 p. [ Links ]
Elósegui O. & Elizondo A. 2010. Evaluación microbiológica in vitro de mezclas de especies de hongos entomopatógenos ingredientes activos de bioplaguicidas cubanos. Revista Fitosanidad (14) Nº 2, 102-109.
Estrada M. Romero M. & Snowball M. 1997. Aplicación de Beauveria bassiana en la Lucha biológica contra Diatraea saccharalis. Revista Caña de Azúcar, Vol. 15 (1): 39-43. Instituto Nacional de Investigaciones de la caña de Azúcar. La Habana Cuba.
Fuentes M. & Carballo M. 1999. Evaluación de Aislamientos de B. bassiana para el control de larvas de la palomilla. Plutella xylostella. Informe de Investigación. CATIE, 1998. [ Links ]
Gallo D., Nakano O., Silveira Neto S., Carvalho R., Batista G., Berti Filho E., Parra J., Zucchi R., Alves S., Vendramim J., Marchini L., Lopes J. & Omoto C. 2002. Entomología agrícola. Piracicaba: FEALQ. p. 682. (920 p). [ Links ]
González M. Posada F. & Bustillo A. 1993. Desarrollo de un bioensayo para evaluar la patogenicidad de Beauveria bassiana sobre Hypothenemus hampei. Revista Cenicafé (Colombia) 44 (3): 93-102. [ Links ]
González H. Carballo M. & Blanco H. 1996. Efecto de cepas deBeauveria bassiana sobre la mortalidad de Ecdytolopha torticornis (Lep.: Tortricidae) en macadamia. En Revista de Manejo Integrado de Plagas 40:17-23.
Little T. & Jackson H.1989. Métodos estadísticos para la investigación en la agricultura. Edit. Trillas. México, D. [ Links ]
Luna Rodríguez J. & Lecuona R. 2002. Selección de cepas de hongos entomopatógenos nativos para el control de la tucura Rhammatocerus pictus (Bruner) (Orthoptera: Acrididae) RIA. Revista de Investigaciones Agropecuarias 31: 67-83. [ Links ]
Malpartida J. 2004. Patogenicidad de Beauveria brongniartii en Premnotrypes suturicallus. Tesis para optar el grado de Biólogo. Universidad Nacional Federico Villarreal. [ Links ]
Molina-Moreira, N. & Arias De Lopez, M. 2006. Bioetología de Dione juno andicola (Bates, 1864) (Lep.: Nymphalidae: Heliconiinae). Revista Nicaragüense de Entomología (66) 9-18. [ Links ]
Quintana D. 2000. Beauveria spp. nativas para control de Rhyacionia buoliana Denis & Schiff. (Lep.: Tortricidae). 30 p. Tesis de Ingeniero Agrónomo. Universidad de Concepción, Facultad de Agronomía, Chillán, Chile. [ Links ]
Rodríguez M. Gerding M. & France A. 2006. Efectividad de aislamientos de hongos entomopatógenos sobre larvas de Polilla del Tomate Tuta absoluta Meyrick (Lep.: Gelechiidae). Agricultura Técnica (Chile) 66(2):159-165. [ Links ]
SAS Institute Inc. 1989. SAS/STAT © User´s Guide. Version 6. Fourth Edition, Volumen 2. Cary, Nc: SAS Institute Inc.
Solis-Soto A., García-Gutiérrez C., González-Maldonado M., Medrano-Roldán H. & Galán-Wong L. 2006. Toxicidad de Blastosporas de Beauveria bassiana contra palomilla del Manzano Cydia pomonella (Lepidoptera: Tortricidae). Folia Entomol. Mex., 45(2): 195-200. [ Links ]
Tefera T. & Pringle K. 2003. Food consumption by Chilo partellus (Lepidoptera: Pyralidae) larvae infected with Beauveria bassiana and Metarhizium anisopliae and effects of feeding natural versus artificial diets on mortality and mycosis. J. Invertebr. Pathol. 84:220-225. [ Links ]
Toledo D. 1991. Fauna del noroeste argentino. Contribución al conocimiento de los lepidópteros argentinos. IX. Dione juno (Cramer) (Lepidóptera, Rhopalocera, Heliconiidae) - Acta zoologica Lilloana 40(1), pp. 109-117.
Varela A. & Morales E. 1996. Characterization of some Beauveria bassiana isolates and their virulence toward the coffee berry borer Hypothenemus hampei. Journal of Invertebrate Pathology 67:147-152. [ Links ]
Vargas M. 2003. Caracterización De tres cepas de Beauveria brongniartii y su efecto en larvas de Phthorimaea opercullella. Tesis de Biólogo.UNMSM. [ Links ]
Vélez P., Posada F., Marín P., Bustillo A., González M. & Osorio, E. 1997. Técnicas para el control de calidad de formulaciones de hongos entomopatógenos. Chinchiná, Revista Cenicafé (Boletín Téc. N° 17). 37 p.
Vélez P., González G., Valderrama F., Estrada V., Bustillo A. & Montoya R. 2000. Caracterización morfológica, fisiológica y molecular de aislamientos de Beauveria bassiana. Revista Cenicafé. (Colombia) 51 (3): 196-206. [ Links ]
Presentado: 11/09/2012
Aceptado: 06/09/2013













